Изоэлектрическая точка
Изоэлектрическая точка ( pI , pH(I) , IEP ) — это уровень pH , при котором молекула не несет чистого электрического заряда или является электрически нейтральной в среднестатистическом значении . Стандартная номенклатура для обозначения изоэлектрической точки — pH(I). [1] Однако pI также используется. [2] Для краткости в этой статье используется pI. На суммарный заряд молекулы влияет pH окружающей среды, и она может стать более положительно или отрицательно заряженной из-за присоединения или потери соответственно протонов (H + ).
Поверхности естественным образом заряжаются, образуя двойной слой . В обычном случае, когда поверхностными ионами, определяющими заряд, являются H + /ХО − На чистый поверхностный заряд влияет pH жидкости, в которую погружено твердое вещество.
Значение pI может влиять на растворимость молекулы при данном pH. Такие молекулы имеют минимальную растворимость в воде или растворах солей при pH, соответствующем их pI , и часто выпадают в осадок из раствора . Биологические амфотерные молекулы, такие как белки, содержат как кислотные, так и основные функциональные группы . Аминокислоты, входящие в состав белков, могут быть положительными, отрицательными, нейтральными или полярными по своей природе и вместе придают белку общий заряд. При pH ниже их pI белки несут суммарный положительный заряд; выше своего PI они несут чистый отрицательный заряд. Таким образом, белки можно разделить по суммарному заряду в полиакриламидном геле , используя либо препаративный нативный PAGE , в котором для разделения белков используется постоянный pH, либо изоэлектрическое фокусирование , в котором для разделения белков используется градиент pH. Изоэлектрическое фокусирование также является первым этапом двумерного электрофореза в полиакриламидном геле .
В биомолекулах белки можно разделить с помощью ионообменной хроматографии . Биологические белки состоят из цвиттерионных аминокислотных соединений; суммарный заряд этих белков может быть положительным или отрицательным в зависимости от pH среды. Специфический pI целевого белка можно использовать для моделирования процесса, а затем соединение можно очистить от остальной смеси. В этом процессе очистки можно использовать буферы с различным pH для изменения pH окружающей среды. При загрузке в ионообменник смеси, содержащей целевой белок, неподвижная матрица может быть как положительно заряженной (для подвижных анионов), так и отрицательно заряженной (для подвижных катионов). При низких значениях pH суммарный заряд большинства белков в смеси положительный – в катионообменниках эти положительно заряженные белки связываются с отрицательно заряженным матриксом. При высоких значениях pH суммарный заряд большинства белков отрицательный, поскольку они связываются с положительно заряженной матрицей анионообменников. Когда значение pH среды равно pI белка, суммарный заряд равен нулю, и белок не связан ни с каким обменником и, следовательно, может быть элюирован. [3]
Расчет значений пи
[ редактировать ]Для аминокислоты , содержащей только одну аминогруппу и одну карбоксильную группу, pI можно рассчитать по среднему значению pKas этой молекулы. [4]
pH для электрофоретического геля определяется буфером, используемым этого геля. Если pH буфера выше pI обрабатываемого белка, белок будет мигрировать к положительному полюсу (отрицательный заряд притягивается к положительному полюсу). Если pH буфера ниже pI белка обрабатываемого , белок будет мигрировать к отрицательному полюсу геля (положительный заряд притягивается к отрицательному полюсу). Если белок работает с буферным pH, равным pI, он вообще не будет мигрировать. Это справедливо и для отдельных аминокислот.
Примеры
[ редактировать ]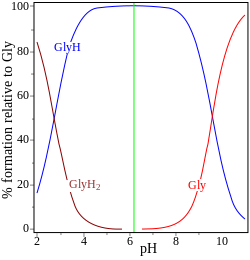 | 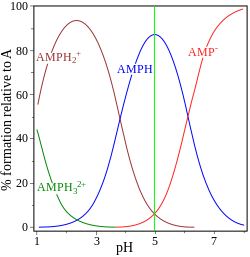 |
| глицин рК = 2,72, 9,60 | аденозинмонофосфат рК = 0,9, 3,8, 6,1 |
В двух примерах (справа) изоэлектрическая точка показана зеленой вертикальной линией. В глицине значения pK разделены почти на 7 единиц. Таким образом, в газовой фазе концентрация нейтрального вещества, глицина (GlyH), фактически составляет 100% от аналитической концентрации глицина. [5] Глицин может существовать в виде цвиттер-иона в изоэлектрической точке, но константа равновесия реакции изомеризации в растворе
не известно.
Другой пример, аденозинмонофосфат , иллюстрирует тот факт, что в принципе может быть задействован третий вид. Фактически концентрация (AMP)H 2+ 3 в этом случае в изоэлектрической точке пренебрежимо мал.Если pI больше pH, молекула будет иметь положительный заряд.
Пептиды и белки
[ редактировать ]ряд алгоритмов оценки изоэлектрических точек пептидов и белков Разработан . Большинство из них используют уравнение Хендерсона-Хассельбаха с разными значениями pK. Например, в рамках модели, предложенной Бьеллквистом и его коллегами, pK определялись между близкородственными иммобилинами путем фокусировки одного и того же образца в перекрывающихся градиентах pH. [6] Также были предложены некоторые улучшения методологии (особенно в определении значений pK для модифицированных аминокислот). [7] [8] Более продвинутые методы учитывают влияние соседних аминокислот на расстоянии ±3 остатка от заряженной аспарагиновой или глутаминовой кислоты , влияние на свободный С-конец, а также применяют корректирующий член к соответствующим значениям pK с использованием генетического алгоритма . [9] Другие недавние подходы основаны на алгоритме машины опорных векторов. [10] и оптимизация pKa относительно экспериментально известных изоэлектрических точек белка/пептида. [11]
Кроме того, экспериментально измеренные изоэлектрические точки белков были агрегированы в базы данных. [12] [13] Недавно также была разработана база данных изоэлектрических точек для всех белков, предсказанных с использованием большинства доступных методов. [14]
На практике белок с избытком основных аминокислот (аргинин, лизин и/или гистидин) будет иметь изоэлектрическую точку примерно выше 7 (основная), тогда как белок с избытком кислых аминокислот (аспарагиновая кислота и/или глутаминовая кислота) ) часто имеет изоэлектрическую точку ниже 7 (кислая).Электрофоретическое линейное (горизонтальное) разделение белков с помощью Ip по градиенту pH в полиакриламидном геле (также известное как изоэлектрофокусирование ) с последующим линейным (вертикальным) разделением по стандартной молекулярной массе во втором полиакриламидном геле ( SDS-PAGE ) представляет собой так называемый двумерный гель-электрофорез или PAGE 2D. Этот метод позволяет тщательно разделить белки на отдельные «пятна», при этом белки с высокой молекулярной массой и низким Ip мигрируют в верхнюю левую часть двумерного геля, а белки с низкой молекулярной массой и высоким Ip располагаются в правом нижнем углу. область того же геля.
Керамические материалы
[ редактировать ]Изоэлектрические точки (ИЭТ) металлооксидной керамики широко используются в материаловедении на различных этапах обработки воды (синтез, модификация и т. д.). В отсутствие хемосорбированных или физисорбированных частиц поверхности частиц в водной суспензии обычно считаются покрытыми поверхностными гидроксильными частицами M-OH (где M представляет собой металл, такой как Al, Si и т. д.). [15] При значениях pH выше IEP преобладающими поверхностными частицами являются МО. − , а при значениях pH ниже IEP M-OH 2 + виды преобладают. Некоторые приблизительные значения обычной керамики указаны ниже: [16] [17]
| Материал | ИЭП |
|---|---|
| WOWO3 [18] | 0.2–0.5 |
| Sb2OСб2О5 [18] | <0,4–1,9 |
| V2OV2O5 [18] [19] | 1–2 (3) |
| δ-MnO 2 | 1.5 |
| SiO 2 [18] | 1.7–3.5 |
| Карбид кремния [20] | 2–3.5 |
| Ta2OТа2О5 [18] | 2.7–3.0 |
| ТиО 2 [21] | 2.8–3.8 |
| в- Fe 2 O 3 [18] | 3.3–6.7 |
| SnO 2 [22] | 4–5.5 (7.3) |
| ЗрО 2 [18] | 4–11 |
| ЭТОТ [23] | 6 |
| Cr2OCr2O3 [18] [19] | 6.2–8.1 (7) |
| Fe 3 О 4 [18] | 6.5–6.8 |
| СеО 2 [18] | 6.7–8.6 |
| Y2OY2O3 [18] | 7.15–8.95 |
| в- Al 2 O 3 | 7–8 |
| β-MnO 2 [19] | 7.3 |
| Тл 2 О [24] | 8 |
| а- Al 2 O 3 | 8–9 |
| α-Fe 2 O 3 [18] | 8.4–8.5 |
| ZnO [18] | 8.7–10.3 |
| Si3NСи3Н4 [22] | 9 |
| CuO [22] | 9.5 |
| La2OLa2O3 | 10 |
| Девять [22] | 10–11 |
| PbO [18] | 10.7–11.6 |
| MgO [18] | 12–13 (9.8·12.7) |
Примечание. В следующем списке указана изоэлектрическая точка при 25 ° C для некоторых материалов в воде. Точное значение может широко варьироваться в зависимости от материальных факторов, таких как чистота и фаза, а также физических параметров, таких как температура. Более того, точное измерение изоэлектрических точек может быть затруднено, поэтому многие источники часто приводят разные значения изоэлектрических точек этих материалов.
Смешанные оксиды могут иметь значения изоэлектрической точки, промежуточные по сравнению со значениями соответствующих чистых оксидов. Например, первоначально измеренный синтетически полученный аморфный алюмосиликат (Al 2 O 3 -SiO 2 ) имел IEP 4,5 (в электрокинетическом поведении поверхности преобладали поверхностные частицы Si-OH, что объясняет относительно низкое значение IEP). [25] сообщили о значительно более высоких значениях IEP (pH от 6 до 8) для 3Al 2 O 3 -2SiO 2 . Другие [22] Аналогично, IEP титаната бария BaTiO 3 находился в диапазоне 5–6 [22] в то время как другие получили значение 3. [26] Были изучены смеси титана (TiO 2 ) и диоксида циркония (ZrO 2 ), и было обнаружено, что их изоэлектрическая точка находится в диапазоне 5,3–6,9, нелинейно изменяясь в зависимости от % (ZrO 2 ). [27] Поверхностный заряд смешанных оксидов коррелировал с кислотностью. Повышенное содержание диоксида титана приводило к повышению кислотности Льюиса, тогда как оксиды с высоким содержанием циркония проявляли кислотность Br::onsted. Различные типы кислотности вызывают различия в скорости и емкости адсорбции ионов.
Против точки нулевого заряда
[ редактировать ]Термины изоэлектрическая точка (IEP) и точка нулевого заряда (PZC) часто используются как взаимозаменяемые, хотя при определенных обстоятельствах может быть полезно провести различие.
В системах, в которых H + /ОЙ − – интерфейсные потенциалопределяющие ионы, точка нулевого заряда выражается через pH. Уровень pH, при котором поверхность демонстрирует нейтральный суммарный электрический заряд, является точкой нулевого заряда на поверхности. Электрокинетические явления обычно измеряют дзета-потенциал , а нулевой дзета-потенциал интерпретируется как точка нулевого суммарного заряда в плоскости сдвига . Это называется изоэлектрической точкой. [28] Таким образом, изоэлектрическая точка — это значение pH, при котором коллоидная частица остается неподвижной в электрическом поле. Ожидается, что изоэлектрическая точка будет несколько отличаться от точки нулевого заряда на поверхности частицы, но на практике это различие часто игнорируется для так называемых первичных поверхностей, т. е. поверхностей без специально адсорбированных положительных или отрицательных зарядов. [15] В данном контексте под специфической адсорбцией понимают адсорбцию, происходящую в слое Штерна , или хемосорбцию . Таким образом, точка нулевого заряда на поверхности принимается равной изоэлектрической точке при отсутствии специфической адсорбции на этой поверхности.
По словам Жоливе, [19] в отсутствие положительных или отрицательных зарядов поверхность лучше всего описывается точкой нулевого заряда. Если положительные и отрицательные заряды присутствуют в равных количествах, то это изоэлектрическая точка. Таким образом, PZC относится к отсутствию любого типа поверхностного заряда, тогда как IEP относится к состоянию нейтрального суммарного поверхностного заряда. Таким образом, разница между ними заключается в количестве заряженных участков в точке чистого нулевого заряда. Жоливе использует константы внутреннего равновесия поверхности p K − и п К + определить два условия с точки зрения относительного количества платных сайтов:
Для больших Δp K (>4 по Жоливе) преобладающей разновидностью является MOH, тогда как заряженных частиц относительно мало, поэтому PZC уместен. При малых значениях Δp K имеется много заряженных частиц примерно в равном количестве, поэтому говорят об ИЭП.
См. также
[ редактировать ]- Электрофоретическое осаждение
- Уравнение Хендерсона-Хассельбаха
- Изоэлектрическая фокусировка
- Изионная точка
- Константа диссоциации pK кислоты
- Препаративная нативная СТРАНИЦА
- Дзета-потенциал
Ссылки
[ редактировать ]- ^ Приемлемые варианты pH(I) включают pH I , pH IEP и т. д .; Суть в том, что нельзя измерить «силу» I, а измерить pH при заданных условиях.
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн исправленная версия: (2006–) « Изоэлектрическая точка в электрофорезе ». дои : 10.1351/goldbook.I03275
- ^ Дейтон, WR (1983). «Методы разделения белков» (PDF) . Материалы взаимной мясной конференции . 36 : 98–102.
- ^ Для получения этого выражения см. константу диссоциации кислоты.
- ^ Дженсен, Ян Х.; Гордон, Марк С. (август 1995 г.). «О количестве молекул воды, необходимом для стабилизации глицина цвиттериона» . Журнал Американского химического общества . 117 (31): 8159–8170. дои : 10.1021/ja00136a013 . ISSN 0002-7863 .
- ^ Бьеллквист, Б.; Хьюз, Дж.Дж.; Паскуали, К.; Паке, Н.; Равье, Ф.; Санчес, Дж.К.; Фрутигер, С.; Хохштрассер, Д. (1 октября 1993 г.). «Фокусирующие положения полипептидов в иммобилизованных градиентах pH можно предсказать по их аминокислотным последовательностям». Электрофорез . 14 (10): 1023–1031. дои : 10.1002/elps.11501401163 . ISSN 0173-0835 . ПМИД 8125050 . S2CID 38041111 .
- ^ Гаучи, Шарон; ван Брекелен, Бас; Лемер, Симона М.; Крийгсвельд, Йерун; Черт возьми, Альберт-младший (1 декабря 2008 г.). «Универсальный пептидный калькулятор pI для фосфорилированных и N-концевых ацетилированных пептидов, экспериментально протестированный с использованием изоэлектрического фокусирования пептидов». Протеомика . 8 (23–24): 4898–4906. дои : 10.1002/pmic.200800295 . ISSN 1615-9861 . ПМИД 19003858 . S2CID 21527631 .
- ^ Гастайгер, Элизабет; Гаттикер, Александр; Хугланд, Кристина; Иваний, Иван; Аппель, Рон Д.; Байрох, Амос (1 июля 2003 г.). «ExPASy: сервер протеомики для углубленных знаний и анализа белков» . Исследования нуклеиновых кислот . 31 (13): 3784–3788. дои : 10.1093/нар/gkg563 . ISSN 0305-1048 . ПМК 168970 . ПМИД 12824418 .
- ^ Каргайл, Бенджамин Дж.; Севински, Джоэл Р.; Эссадер, Амаль С.; Ю, Джерри П.; Стивенсон, Джеймс Л. (1 июля 2008 г.). «Расчет изоэлектрической точки триптических пептидов в диапазоне pH 3,5–4,5 на основе эффектов соседних аминокислот» . Электрофорез . 29 (13): 2768–2778. дои : 10.1002/elps.200700701 . ISSN 0173-0835 . ПМИД 18615785 .
- ^ Перес-Ривероль, Яссет; Оден, Энрике; Миллан, Алели; Рамос, Ясель; Санчес, Аниэль; Вискайно, Хуан Антонио; Ван, Руй; Мюллер, Маркус; Мачадо, Йоан Дж. (3 апреля 2012 г.). «Оптимизация изоэлектрической точки с использованием пептидных дескрипторов и машин опорных векторов». Журнал протеомики . 75 (7): 2269–2274. дои : 10.1016/j.jprot.2012.01.029 . ISSN 1876-7737 . ПМИД 22326964 .
- ^ Козловский, ЛП. (2016). «IPC — Калькулятор изоэлектрической точки» . Биол Директ . 11 (1): 55. дои : 10.1186/s13062-016-0159-9 . ПМК 5075173 . ПМИД 27769290 .
- ^ Хугланд, К.; Мостагир, К.; Санчес, Дж. К.; Хохштрассер, Германия; Аппель, РД. (2004). «SWISS-2DPAGE, десять лет спустя». Протеомика . 4 (8): 2352–6. дои : 10.1002/pmic.200300830 . ПМИД 15274128 . S2CID 31933242 .
- ^ Бункутэ, Э.; Камминс, К.; Крофтс, ФДж.; Банс, Г.; Набни, IT.; Флауэр, ДР. (2015). «PIP-DB: база данных изоэлектрических точек белков» . Биоинформатика . 31 (2): 295–6. doi : 10.1093/биоинформатика/btu637 . ПМИД 25252779 .
- ^ Козловский, ЛП. (2016). «Протеом-pI: база данных изоэлектрических точек протеома» . Нуклеиновые кислоты Рез . 45 (Д1): Д1112–Д1116. дои : 10.1093/nar/gkw978 . ПМК 5210655 . ПМИД 27789699 .
- ^ Перейти обратно: а б Ханаор, ДАХ; Микелацци, М.; Леонелли, К.; Соррелл, CC (2012). «Влияние карбоновых кислот на водную дисперсию и электрофоретическое осаждение ZrO 2 ». Журнал Европейского керамического общества . 32 (1): 235–244. arXiv : 1303.2754 . doi : 10.1016/j.jeurceramsoc.2011.08.015 . S2CID 98812224 .
- ^ Харута, М. (2004). «Наночастичные золотые катализаторы низкотемпературного окисления CO». Журнал новых материалов для электрохимических систем . 7 : 163–172.
- ^ Брюнель JP (1978). «Приготовление катализаторов адсорбцией металлических комплексов на минеральных оксидах». Чистая и прикладная химия, том. 50, стр. 1211–1229.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот Марек Космульски, «Химические свойства поверхностей материалов», Марсель Деккер, 2001.
- ^ Перейти обратно: а б с д Жоливет Дж. П., Химия и синтез оксидов металлов. От решения к твердотельному телу , John Wiley & Sons Ltd., 2000 г., ISBN 0-471-97056-5 (английский перевод оригинального французского текста, De la Solution à l'Oxyde , InterEditions и CNRS Editions, Париж, 1994).
- ^ Патент США 5 165 996.
- ^ Анодное водное электрофоретическое осаждение диоксида титана с использованием карбоновых кислот в качестве диспергирующих агентов. Журнал Европейского керамического общества, 31 (6), 1041-1047, 2011.
- ^ Перейти обратно: а б с д и ж Льюис, Дж. А. (2000). «Коллоидная обработка керамики». Журнал Американского керамического общества . 83 (10): 2341–2359. CiteSeerX 10.1.1.514.1543 . дои : 10.1111/j.1151-2916.2000.tb01560.x . S2CID 9513223 .
- ^ Дайдо, Т; Акаике, Т (1993). «Электрохимия цитохрома с: влияние кулоновского притяжения с электродом из оксида индия и олова». Журнал электроаналитической химии . 344 (1–2): 91–106. дои : 10.1016/0022-0728(93)80048-м .
- ^ Космульский, М; Санелута, К. (2004). «Точка нулевого заряда/изоэлектрическая точка экзотических оксидов: Tl2O3». Журнал коллоидной и интерфейсной науки . 280 (2): 544–545. Бибкод : 2004JCIS..280..544K . doi : 10.1016/j.jcis.2004.08.079 . ПМИД 15533430 .
- ^ Хара, А.А.; Гольдберг, С.; Мора, МЛ (2005). «Исследование поверхностного заряда аморфных алюмосиликатов с использованием моделей поверхностного комплексообразования». Журнал коллоидной и интерфейсной науки . 292 (1): 160–170. Бибкод : 2005JCIS..292..160J . doi : 10.1016/j.jcis.2005.05.083 . hdl : 10533/176403 . ПМИД 16051258 .
- ^ Вамвакаки, Мария; Биллингем, Норман К.; Армс, Стивен П.; Уоттс, Джон Ф.; Гривз, Стивен Дж. (2001). «Сополимеры с контролируемой структурой для диспергирования высокоэффективной керамики в водных средах». Журнал химии материалов . 11 (10): 2437–2444. дои : 10.1039/b101728o . ISSN 0959-9428 .
- ^ Дриско, Гленна Л; Лука, Витторио; Сизгек, Эрден; Весы, Николас Ф.; Карузо, Рэйчел А. (2009). «Шаблонный синтез и адсорбционные свойства иерархически пористых оксидов циркония и титана». Ленгмюр . 25 (9): 5286–5293. дои : 10.1021/la804030h . ISSN 0743-7463 . ПМИД 19397363 .
- ^ AW Adamson, AP Gast, «Физическая химия поверхностей», John Wiley and Sons, 1997.
Дальнейшее чтение
[ редактировать ]- Нельсон Д.Л., Кокс М.М. (2004). Ленингерские принципы биохимии . WH Фриман; 4-е издание (в твердом переплете). ISBN 0-7167-4339-6
- Космульский М. (2009). Поверхностный заряд и точки нулевого заряда . ЦРК Пресс; 1-е издание (в твердом переплете). ISBN 978-1-4200-5188-9
Внешние ссылки
[ редактировать ]- IPC — Калькулятор изоэлектрической точки — рассчитайте изоэлектрическую точку белка, используя более 15 методов.
- prot pi – изоэлектрическая точка белка — онлайн-программа для расчета pI белков (включает несколько субъединиц и посттрансляционные модификации)
- CurTiPot — набор электронных таблиц для расчета кислотно-щелочного равновесия (график зависимости заряда от pH амфотерных молекул, например аминокислот)
- pICalculax — предиктор изоэлектрической точки (pI) для химически модифицированных пептидов и белков.
- SWISS-2DPAGE — база данных изоэлектрических точек, полученных в результате двумерного электрофореза в полиакриламидном геле (~ 2000 белков)
- PIP-DB — база данных изоэлектрических точек белков (~ 5000 белков)
- Proteome-pI — база данных изоэлектрических точек протеома (прогнозируемая изоэлектрическая точка для всех белков)


![{\displaystyle \mathrm {p} K^{-}-\mathrm {p} K^{+}=\Delta \mathrm {p} K=\log {\frac {\left[\mathrm {MOH} \right ]^{2}}{\left[\mathrm {MOH} {_{2}^{+}}\right]\left[\mathrm {MO} ^{-}\right]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1e3191d7ab56090ff3c419b53868c6c52134d80a)