Винная кислота
 | |
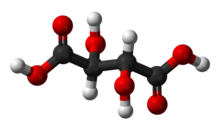 Шаровидная модель L -(+)-винной кислоты. | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 2,3-Дигидроксибутандиовая кислота | |
| Другие имена Винная кислота 2,3-Дигидроксиянтарная кислота Треариновая кислота Рацемическая кислота Увиковая кислота Паравинная кислота Уайнстоун | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.121.903 |
| номер Е | Е334 (антиоксиданты, ...) |
| КЕГГ | |
| МеШ | винная+кислота |
ПабХим CID |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| C 4 H 6 O 6 (основная формула) HO 2 CCH(OH)CH(OH)CO 2 H (структурная формула) | |
| Молярная масса | 150,087 г/моль |
| Появление | Белый порошок |
| Плотность | 1,737 г/см 3 (R,R- и S,S-) 1,79 г/см 3 (рацемат) 1,886 г/см 3 (мясо) |
| Температура плавления | 169, 172 °C (R,R- и S,S-) 206 °С (рацемат) 165-6 °С (мезо) |
| |
| Кислотность ( pKa ) | Л(+) 25 °С: рК а1 = 2,89, рК а2 = 4,40 мезо 25 °С: рК а1 = 3,22, рК а2 = 4,85 |
| Сопряженная база | битартрат |
| −67.5·10 −6 см 3 /моль | |
| Опасности | |
| СГС Маркировка : [3] | |
 | |
| Опасность | |
| H318 | |
| П280 , П305+П351+П338+П310 | |
| Родственные соединения | |
Другие катионы | Тартрат натрия Тартрат динатрия Монокалий тартрат Дикалий тартрат |
Родственные карбоновые кислоты | Масляная кислота Янтарная кислота Димеркаптоянтарная кислота Яблочная кислота Малеиновая кислота Фумаровая кислота |
Родственные соединения | 2,3-бутандиол Цикоровая кислота |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Винная кислота — это белая кристаллическая органическая кислота , которая в природе содержится во многих фруктах, особенно в винограде , а также в тамариндах , бананах , авокадо и цитрусовых . [1] Его соль , битартрат калия , широко известный как винный камень, образуется естественным путем в процессе ферментации . Битартрат калия обычно смешивают с бикарбонатом натрия и продают в виде разрыхлителя, используемого в качестве разрыхлителя при приготовлении пищи. Сама кислота добавляется в пищу в качестве антиоксиданта Е334 и для придания ей характерного кисловатого вкуса. Природная винная кислота является полезным сырьем в органическом химическом синтезе . Винная кислота, альфа-гидроксикарбоновая кислота , имеет дипротонные и альдаровые кислотные характеристики и является дигидроксильным производным янтарной кислоты .
История
[ редактировать ]Винная кислота известна виноделам на протяжении веков. Однако химический процесс экстракции был разработан в 1769 году шведским химиком Карлом Вильгельмом Шееле . [4]
Винная кислота сыграла важную роль в открытии химической хиральности . Это свойство винной кислоты было впервые обнаружено в 1832 году Жаном Батистом Био , который наблюдал ее способность вращать поляризованный свет . [5] [6] Луи Пастер продолжил это исследование в 1847 году, исследуя форму кристаллов тартрата натрия-аммония , которые, как он обнаружил, были хиральными. Сортируя вручную кристаллы разной формы, Пастер первым получил чистый образец левовинной кислоты. [7] [8] [9] [10] [11]
Стереохимия
[ редактировать ]
Природной формой кислоты является декстровинная кислота или L -(+)-винная кислота (устаревшее название d -винная кислота). Поскольку он доступен в природе, он дешевле, чем его энантиомер и мезоизомер . Префиксы dextro и levo являются архаичными терминами. [12] В современных учебниках природная форма упоминается как (2R , 3R ) -винная кислота ( L -(+)-винная кислота) , а ее энантиомер - как (2S , 3S ) -винная кислота ( D -(-)- винная кислота) . Мезодиастереомер 3S называют (2R , ) , -винной кислотой или (2S 3R ) -винной кислотой.
- Декстро и лево образуют моноклинные клиновидные кристаллы. [13] и орторомбические кристаллы.
- Рацемическая винная кислота образует моноклинную [14] и триклинные кристаллы ( пространственная группа P 1 ). [15] [16]
- Безводная мезовинная кислота образует две безводные полиморфные модификации : триклинную и ромбическую.
- Моногидратная мезовинная кислота кристаллизуется в виде моноклинного и триклинного полиморфизма в зависимости от температуры, при которой происходит кристаллизация из водного раствора. [17]
Винная кислота в растворе Фелинга связывается с ионами меди(II), предотвращая образование нерастворимых гидроксидных солей.
| DL -винная кислота ( рацемическая кислота ) (в соотношении 1:1) | мезовинная кислота | |
|---|---|---|
| декстровинная кислота (L-(+)-винная кислота) | левовинная кислота (D-(-)-винная кислота) | |
 |  |  |
| Общее имя | Винная кислота | Левовинная кислота | Декстровинная кислота | Мезовинная кислота | Рацемическая кислота |
|---|---|---|---|---|---|
| Синонимы | (2S , 3S ) -винная кислота ( S , S )-винная кислота (-)-винная кислота л -винная кислота (устар.) левовинная кислота D -винная кислота D- треариновая кислота («неестественный изомер») [18] | (2R , 3R ) -винная кислота ( R , R )-винная кислота (+)-винная кислота d -винная кислота (устарело) L -винная кислота L- треариновая кислота («природный изомер») [19] | (2R , 3S ) -винная кислота мезо -винная кислота эритрариновая кислота | рац- (2R , 3S ) -винная кислота (2 RS ,3 SR )-винная кислота (±)-винная кислота DL -винная кислота dl -винная кислота (устарело) паравинная кислота увиковая кислота | |
| PubChem | CID 875 от PubChem | CID 439655 от PubChem | CID 444305 от PubChem | CID 78956 от PubChem | CID 5851 от PubChem |
| Номер EINECS | |||||
| Номер CAS | 526-83-0 | 147-71-7 | 87-69-4 | 147-73-9 | 133-37-9 |
Производство
[ редактировать ]L -(+)-Винная кислота
[ редактировать ]L -( + )-винная кислота Изомер винной кислоты промышленно производится в наибольших количествах. Его получают из осадка , твердого побочного продукта брожения. Первые побочные продукты в основном состоят из битартрата калия (KHC 4 H 4 O 6 ). Эта калиевая соль превращается в тартрат кальция (CaC 4 H 4 O 6 ) при обработке гидроксидом кальция «известковым молоком» (Ca(OH) 2 ): [20]
На практике более высокие выходы тартрата кальция получают при добавлении сульфата кальция . Тартрат кальция затем превращают в винную кислоту путем обработки соли водным раствором серной кислоты:
Рацемическая винная кислота
[ редактировать ]Рацемическую винную кислоту можно получить многостадийной реакцией из малеиновой кислоты . На первом этапе малеиновую кислоту эпоксидируют перекисью водорода с использованием вольфрамата калия в качестве катализатора. [20]
- HO 2 CC 2 H 2 CO 2 H + H 2 O 2 → OC 2 H 2 (CO 2 H) 2
На следующем этапе эпоксид гидролизуется.
- OC 2 H 2 (CO 2 H) 2 + H 2 O → (ВЫСОКИЙ) 2 (CO 2 H) 2
мезо -Винная кислота
[ редактировать ]Смесь рацемической и мезовинной кислот образуется при . нагревании декстровинной кислоты в воде при температуре 165°C в течение примерно 2 дней мезо -Винная кислота также может быть получена из дибромянтарной кислоты с использованием гидроксида серебра: [21]
- HO 2 CCHBrCHBrCO 2 H + 2 AgOH → HO 2 CCH(OH)CH(OH)CO 2 H + 2 AgBr
мезо -винную кислоту можно отделить от остаточной рацемической кислоты кристаллизацией, при этом рацемат менее растворим.
Реактивность
[ редактировать ]L-(+)-винная кислота может участвовать в нескольких реакциях. Как показано на схеме реакции ниже, дигидроксималеиновая кислота получается при обработке L-(+)-винной кислоты перекисью водорода в присутствии соли двухвалентного железа .
- HO 2 CCH(OH)CH(OH)CO 2 H + H 2 O 2 → HO 2 CC(OH)C(OH)CO 2 H + 2 H 2 O
Дигидроксималеиновую кислоту затем можно окислить до тартроновой кислоты азотной кислотой. [22]
Производные
[ редактировать ]

Важные производные винной кислоты включают:
- Тартрат натрия-аммония , первое вещество, разделенное на энантиомеры.
- винный камень ( битартрат калия ), используемый в кулинарии.
- Сепельная соль (тартрат калия-натрия), обладающая необычными пьезоэлектрическими свойствами.
- рвотное средство для зубного камня (тартрат сурьмы и калия), рассасывающее средство . [23] [24] [25] Диизопропилтартрат используется в качестве сокатализатора в асимметрическом синтезе.
Винная кислота — это мышечный токсин , который подавляет выработку яблочной кислоты и в высоких дозах вызывает паралич и смерть. [26] Средняя смертельная доза (LD 50 ) составляет около 7,5 грамм/кг для человека, 5,3 грамм/кг для кроликов и 4,4 грамм/кг для мышей. [27] Учитывая эту цифру, для того чтобы убить человека весом 70 кг (150 фунтов) с вероятностью 50% потребуется более 500 г (18 унций), поэтому его можно безопасно включать во многие продукты, особенно в сладости с кислым вкусом . В качестве пищевой добавки винная кислота используется как антиоксидант с номером Е E334 ; тартраты – это другие добавки, служащие антиоксидантами или эмульгаторами .
Когда в воду добавляют винный камень, образуется суспензия, которая очень хорошо очищает медные монеты , поскольку раствор винного камня может растворить слой оксида меди (II), присутствующий на поверхности монеты. Образующийся комплекс меди(II)-тартрата легко растворим в воде.
Винная кислота в вине
[ редактировать ]Эта статья нуждается в дополнительных цитатах для проверки . ( ноябрь 2023 г. ) |

Винная кислота может быть сразу узнаваема любителями вина как источник «винных алмазов», маленьких кристаллов битартрата калия , которые иногда спонтанно образуются на пробке или дне бутылки. Эти «тартраты» безвредны, хотя иногда их принимают за битое стекло, и во многих винах их можно предотвратить за счет холодной стабилизации (которая не всегда предпочтительна, поскольку может изменить профиль вина). Тартраты, оставшиеся внутри бочек для выдержки, когда-то были основным промышленным источником битартрата калия.
Винная кислота играет важную химическую роль, снижая pH бродящего «сусла» до уровня, при котором многие нежелательные бактерии, вызывающие порчу, не могут жить, и действует как консервант после брожения . Во рту винная кислота придает вину некоторую терпкость, хотя лимонная и яблочная кислоты также играют определенную роль.
Винная кислота во фруктах
[ редактировать ]Виноград и тамаринды имеют самый высокий уровень концентрации винной кислоты. Другими фруктами, содержащими винную кислоту, являются бананы , авокадо , опунция , яблоки , вишня , папайя , персики , груши , ананасы , клубника , манго и цитрусовые . [1] [28]
Следовые количества винной кислоты были обнаружены в клюкве и других ягодах . [29]
Винная кислота также присутствует в листьях и стручках растений пеларгонии и бобах .
Приложения
[ редактировать ]Винная кислота и ее производные имеют множество применений в области фармацевтики. Например, его использовали при производстве шипучих солей в сочетании с лимонной кислотой для улучшения вкуса пероральных препаратов. [22] Антимониловое производное калия кислоты, известное как рвотный камень, включается в небольших дозах в сироп от кашля в качестве отхаркивающего средства .
Винная кислота также имеет несколько применений в промышленности. Было обнаружено, что кислота хелатирует ионы металлов, таких как кальций и магний. Поэтому кислота используется в сельском хозяйстве и металлургической промышленности в качестве хелатирующего агента для комплексообразования микроэлементов в почвенных удобрениях и для очистки металлических поверхностей, состоящих из алюминия, меди, железа и сплавов этих металлов соответственно. [20]
Токсичность у собак
[ редактировать ]Хотя винная кислота хорошо переносится людьми и лабораторными животными, в письме редактору JAVMA от апреля 2021 года высказано предположение, что винная кислота в винограде может быть причиной токсичности винограда и изюма у собак . [30]
У собак винная кислота тамаринда вызывает острое повреждение почек , которое часто может привести к летальному исходу. [31]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Винная кислота – Обзор соединений , PubChem .
- ^ Доусон, RMC и др., Данные для биохимических исследований , Оксфорд, Clarendon Press, 1959.
- ^ GHS: Запись в базе данных веществ GESTIS Института охраны труда.
- ^ Ретциус, Андерс Джахан (1770) «Эксперименты с винным камнем и его кислотой», академии наук Труды Королевской , 31 : 207–213. Со стр. 209: «§. 6. Я упоминаю об этих опытах от имени г-на Карла Вильгельма Шееле (быстрого и прилежного студента фармакологии)… )
- ^ Био (1835) «Мемуары о круговой поляризации и о ее приложениях к органической химии» , Мемуары Академии наук Института , 2-я серия, 13 : 39–175. То, что винная кислота ( кристаллизованная винная кислота ) вращает плоскополяризованный свет, показано в таблице G, следующей за стр. 168. (Примечание: эта статья была зачитана Французской королевской академии наук 5 ноября 1832 г.)
- ^ Био (1838) «Чтобы различить определенные или неопределенные смеси и химические комбинации, которые действуют на поляризованный свет; с последующими применениями к комбинациям винной кислоты с водой, спиртом и спиртом буа» (Чтобы различить смеси и химические соединения, определенные или неопределенные, действующие на поляризованный свет, с последующим применением сочетаний винной кислоты с водой, спиртом [т. е. этанолом] и древесным спиртом [т. е. метанолом]), Мемуары Академии наук СССР ; Институт , 2-я серия, 15 : 93–279.
- ^ Пастер, Л. (1848). «Мемуары о связи, которая может существовать между кристаллической формой и химическим составом, и о причине вращательной поляризации» . Труды Парижской академии наук (на французском языке). 26 :535–538.
- ^ Л. Пастер (1848) и химическим составом, а также смыслом вращающейся поляризации» ( «О связях, которые могут существовать между кристаллической формой поляризация), Annales de Chimie et de Physique , 3-я серия, 24 : 442–459.
- ^ Пастер, Луи (1850) «Исследования специфических свойств двух кислот, составляющих рацемовую кислоту» [Исследования специфических свойств двух кислот, составляющих рацемовую кислоту], Annales de Chimie et de Physique , 3-я серия, 28 ( 3): 56–99. См. также Таблицу II. (См. также отчет комиссии, назначенной для проверки выводов Пастера, стр. 99–117.) [на французском языке]
- ^ Джордж Б. Кауфман; Робин Д. Майерс (1998). «Решение Пастера о рацемической кислоте: полуторавековая ретроспектива и новый перевод» (PDF) . Химический педагог . 3 (6): 1–4. дои : 10.1007/s00897980257a . S2CID 95862598 . Архивировано из оригинала (PDF) 17 января 2006 г.
- ^ Флэк, HD (2009). «Открытие Луи Пастером молекулярной хиральности и спонтанного разрешения в 1848 году, а также полный обзор его кристаллографических и химических работ» (PDF) . Акта Кристаллографика А. 65 (5): 371–389. Бибкод : 2009AcCrA..65..371F . дои : 10.1107/S0108767309024088 . ПМИД 19687573 . Архивировано из оригинала (PDF) 6 сентября 2012 г.
- ^ «Лекция 28: Стереохимическая номенклатура; Рацемизация и разрешение | Химия CosmoLearning» . КосмоОбучение .
- ^ W, T, Эстбери (февраль 1923 г.). «Кристаллическая структура и свойства винной кислоты» . Учеб. Р. Сок. А. 102 (718): 506–528. Бибкод : 1923RSPSA.102..506A . дои : 10.1098/rspa.1923.0010 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) , на основе «Химической кристаллографии» П. Грота. - ^ Справочник CRC по химии и физике, 49-е издание.
- ^ Саманта Каллир и Майкл Херстхаус (2008). «D-Винная кислота» . Открытая база данных кристаллографии .
- ^ Пол Лунер; и др. (июль 2002 г.). «(+-)-Винная кислота» . Acta Crystallographica Раздел C. 58 (6): о333–о335. Бибкод : 2002AcCrC..58O.333L . дои : 10.1107/S0108270102006650 . ПМИД 12050433 . , «(±)-Винная кислота» . Открытая база данных кристаллографии . 2002.
- ^ Г. А. Бутсма и Дж. К. Шун (1967). «Кристаллические структуры мезовинной кислоты» . Акта Кристаллогр . 22 (4): 522–532. Бибкод : 1967AcCry..22..522B . дои : 10.1107/S0365110X67001070 .
- ^ «Д-Винная кислота» . ПабХим .
- ^ «L-(+)-Винная кислота» . ПабХим . Архивировано из оригинала 16 мая 2015 года.
- ^ Перейти обратно: а б с Ж.-М. Кассаян «Винная кислота» в Энциклопедии промышленной химии Ульмана; VCH: Вайнхайм, Германия, 2002, 35, 671–678. два : 10.1002/14356007.a26_163
- ^ Огастес Прайс Вест. Экспериментальная органическая химия. Всемирная книжная компания: Нью-Йорк, 1920, 232–237.
- ^ Перейти обратно: а б Блэр, GT; ДеФратис, Джей-Джей (2000). «Гидроксидикарбоновые кислоты». Энциклопедия химической технологии Кирка Отмера . стр. 1–19. дои : 10.1002/0471238961.0825041802120109.a01 . ISBN 0471238961 .
- ^ Залкин, Аллан; Темплтон, Дэвид Х.; Уэки, Тацуо (1973). «Кристаллическая структура l-трис (1,10-фенатролин) железа (II) бис (сурьмы (III) d-тартрат) октагидрата». Неорганическая химия . 12 (7): 1641–1646. дои : 10.1021/ic50125a033 .
- ^ Хак, я; Хан, К. (1982). «Вред традиционной косметики для глаз - СУРМА». Журнал Пакистанской медицинской ассоциации . 32 (1): 7–8. ПМИД 6804665 .
- ^ МакКаллум, Род-Айленд (1977). «Обращение президента. Замечания по сурьме» . Труды Королевского медицинского общества . 70 (11): 756–63. дои : 10.1177/003591577707001103 . ПМК 1543508 . ПМИД 341167 .
- ^ Альфред Суэйн Тейлор, Эдвард Хартшорн (1861). Медицинская юриспруденция . Бланшар и Леа. п. 61 .
- ^ Джозеф А. Мага, Энтони Т. Ту (1995). Токсикология пищевых добавок . ЦРК Пресс. стр. 137–138. ISBN 0-8247-9245-9 .
- ^ Дж. Б. Гуртлер, Т. Л. Май, в Энциклопедии пищевой микробиологии (второе издание), 2014. КОНСЕРВАНТЫ | Традиционные консерванты – органические кислоты: винная кислота.
- ^ Фитохимические вещества клюквы и продуктов из клюквы: характеристика, потенциальное воздействие на здоровье и стабильность обработки https://www.researchgate.net/publication/44573816_Phytochemicals_of_Cranberry_and_Cranberry_Products_Characterization_Potential_Health_Effects_and_Processing_Stability .
- ^ Макрейнольдс, Тони (1 апреля 2021 г.). «Что вызывает токсичность винограда у собак? Playdough мог бы привести к прорыву» . Американская ассоциация больниц для животных .
- ^ Вегенаст, Калифорния (2022 г.). «Острое повреждение почек у собак после приема винного камня и тамаринда и связь с винной кислотой как предполагаемым токсичным компонентом винограда и изюма». J Ветеринарная неотложная помощь при критических ситуациях . 32 (6): 812–816. дои : 10.1111/vec.13234 . PMID 35869755 . S2CID 250989489 .
Внешние ссылки
[ редактировать ]- PDB-файл для MSE. Архивировано 20 сентября 2018 г. на Wayback Machine.

