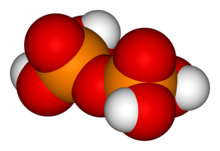
Пирофосфорная кислота
 | |
 | |
| Имена | |
|---|---|
| ИЮПАК имена Дифосфорная кислота μ-оксидо-бис(дигидроксидооксидофосфор) | |
| Другие имена Пирофосфорная кислота Фосфонофосфорная кислота Фосфонодигидрофосфат | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.017.795 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| H4P2OH4P2O7 | |
| Молярная масса | 177.97 g/mol |
| Температура плавления | 71,5 ° C (160,7 ° F; 344,6 К) |
| Чрезвычайно растворим | |
| Растворимость | Хорошо растворим в спирте , эфире |
| Сопряженная база | Пирофосфат |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Пирофосфорная кислота , также известная как дифосфорная кислота , представляет собой неорганическое соединение с формулой H 4 P 2 O 7 или, более описательно, [(HO) 2 P(O)] 2 O. Бесцветно и без запаха, растворимо в воде . диэтиловый эфир и этиловый спирт . Безводная кислота кристаллизуется в двух полиморфных формах , которые плавятся при 54,3 и 71,5 °C. Соединение является компонентом полифосфорной кислоты, важного источника фосфорной кислоты. [1] Анионы , соли и эфиры пирофосфорной кислоты называются пирофосфатами .
Подготовка
[ редактировать ]Его можно получить реакцией фосфорной кислоты с хлористым фосфорилом : [2]
- 5 H 3 PO 4 + POCl 3 → 3 H 4 P 2 O 7 + 3 HCl
Его также можно получить путем ионного обмена из пирофосфата натрия или обработкой пирофосфата свинца сероводородом . [1]
Кипячение воды из ортофосфорной кислоты смесь орто-, пиро- и полифосфорной кислот , максимальная концентрация пирофосфорной кислоты остается ниже 50% и возникает немного раньше, чем в противном случае была бы чистая пирофосфорная кислота. не приводит к обезвоживанию ее до чистой пирофосфорной кислоты, вместо этого образуется [3]
Реакции
[ редактировать ]Пирофосфорная кислота представляет собой тетрапротонную кислоту с четырьмя различными pKa: [4]
- H 4 P 2 O 7 ⇌ [H 3 P 2 O 7 ] − + Ч + , рКа = 0,85
- [Н 3 Р 2 О 7 ] − ⇌ [H 2 P 2 O 7 ] 2− + Ч + , рКа = 1,96
- [Н 2 Р 2 О 7 ] 2− ⇌ [HP 2 O 7 ] 3− + Ч + , рКа = 6,60
- [ХП 2 О 7 ] 3− ⇌ [П 2 О 7 ] 4− + Ч + , рКа = 9,41
рКа встречаются в двух различных диапазонах, поскольку депротонирование происходит на отдельных фосфатных группах. Для сравнения: рКа фосфорной кислоты составляют 2,14, 7,20 и 12,37.
При физиологических значениях pH пирофосфат существует в виде смеси дважды и одинарно протонированных форм.
При плавлении пирофосфорная кислота быстро превращается в равновесную смесь фосфорной кислоты, пирофосфорной кислоты и полифосфорных кислот. Массовое содержание пирофосфорной кислоты составляет около 40%, и ее трудно перекристаллизовать из расплава.
Даже в холодной воде пирофосфорная кислота гидролизуется до фосфорной кислоты. Все полифосфорные кислоты ведут себя одинаково. [5]
- Н 4 Р 2 О 7 + Н 2 О → 2 Н 3 ПО 4
Безопасность
[ редактировать ]Хотя пирофосфорная кислота вызывает коррозию, в других отношениях она не токсична. [6]
История
[ редактировать ]Название пирофосфорная кислота было дано «мистером Кларком из Глазго» в 1827 году, которому приписывают ее открытие после нагревания до красного каления соли фосфата натрия . Было обнаружено, что фосфорная кислота при нагревании до красного каления образует пирофосфорную кислоту, которая легко превращается в фосфорную кислоту горячей водой. [7]
См. также
[ редактировать ]- Дисерная кислота
- Пирофосфат натрия
- Болезнь отложения дигидрата пирофосфата кальция
- Диметилаллилпирофосфат
- АДП
- СПС
- Ортокислоты
- трифосфорная кислота
Ссылки
[ редактировать ]- ^ Jump up to: а б Авеланж, Себастьян; Лиерде, Николас; Жермо, Ален; Мартинс, Эммануэль; Тейс, Тибо; Сонво, Марк; Туссен, Клаудия; Шрёдтер, Клаус; Беттерманн, Герхард; Стаффель, Томас; Валь, Фридрих; Кляйн, Томас; Хофманн, Томас (2022). «Фосфорная кислота и фосфаты». Энциклопедия промышленной химии Ульмана . стр. 1–55. дои : 10.1002/14356007.a19_465.pub4 . ISBN 9783527303854 . S2CID 246266565 .
- ^ Р. Клемент (1963). «Конденсированные ортофосфаты». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 2. Нью-Йорк, Нью-Йорк: Академик Пресс. п. 546.
- ^ Корте, Карстен; Конти, Фоска; Вакерль, Юрген; Ленерт, Вернер (2016), Ли, Цинфэн; Айли, Дэвид; Хьюлер, Ханс Оге; Йенсен, Йенс Олуф (ред.), «Фосфорная кислота и ее взаимодействие с полимерами типа полибензимидазола» , Высокотемпературные топливные элементы с мембраной из полимерного электролита , Cham: Springer International Publishing, стр. 169–194, номер документа : 10.1007/978-3- 319-17082-4_8 , ISBN 978-3-319-17081-7 , получено 11 февраля 2023 г.
- ^ Ядав, Прерна; Блак, Оливье; Рудт, Андреас; Зельдер, Феликс (2021). «Индуцированное зондирование, основанное на активности: механистическое исследование обнаружения пирофосфата с помощью «гибкого» комплекса Fe-сален» . Границы неорганической химии . 8 (19): 4313–4323. дои : 10.1039/d1qi00209k . ПМЦ 8477187 . ПМИД 34603734 .
- ^ Корбридж, Д. (1995). «Глава 3: Фосфаты». Исследования по неорганической химии, том. 20 . Elsevier Science BV, стр. 169–305. дои : 10.1016/B978-0-444-89307-9.50008-8 . ISBN 0-444-89307-5 .
- ^ Паспорт безопасности материала: MSDS пирофосфорной кислоты www.sciencelab.com
- ^ Бек, Льюис Калеб (1834). Руководство по химии: краткий обзор современного состояния науки с многочисленными ссылками на более обширные трактаты, оригинальные статьи и т . д . РЭБ и С Скиннер. п. 160 . Проверено 30 января 2015 г.