Четверная облигация
Четверная связь — это тип химической связи между двумя атомами с участием восьми электронов . Эта связь является продолжением более известных типов ковалентных связей : двойных и тройных связей . [1] Стабильные четверные связи наиболее распространены среди переходных металлов в середине d-блока , таких как рений , вольфрам , технеций , молибден и хром . Обычно лиганды , поддерживающие четверные связи, являются π-донорами , а не π-акцепторами . Четверные связи редки по сравнению с двойными и тройными связями , но были получены сотни соединений с такими связями. [2]

История [ править ]
Ацетат хрома(II) Cr 2 ( μ -O 2 CCH 3 ) 4 (H 2 O) 2 был первым химическим соединением, синтезированным содержащим четверную связь. Он был описан в 1844 году Э. Пелиго , хотя его отличительная связь не была признана более столетия. [3]
Первое кристаллографическое исследование соединения с четверной связью было проведено советскими химиками для солей Re.
2 кл. 2−
8 . [4] Было отмечено очень короткое расстояние Re–Re. Это короткое расстояние (и диамагнетизм соли) указывает на связь Re – Re. Однако эти исследователи неверно сформулировали анион как производное Re(II), т.е. Re
2 кл. 4−
8 .
Вскоре после этого Ф. Альберт Коттон и К. Б. Харрис сообщили о кристаллической структуре октахлордирената калия или K 2 [Re 2 Cl 8 ]·2H 2 O. [5] Этот структурный анализ показал, что предыдущая характеристика была ошибочной. Коттон и Харрис сформулировали молекулярно-орбитальное обоснование связи, которое явно указывает на четверную связь. [3] рений-ренией Длина связи в этом соединении составляет всего 224 пм . В теории молекулярных орбиталей связь описывается как σ 2 п 4 д 2 с одной сигма-связью , двумя пи-связями и одной дельта-связью .
Структура и связь [ править ]
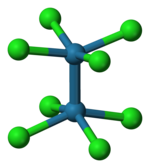

[Re 2 Cl 8 ] 2− ион принимает затменную конформацию, как показано слева. Дельта-связывающая орбиталь затем образуется в результате перекрытия d-орбиталей на каждом атоме рения, которые перпендикулярны оси Re-Re и лежат между связями Re-Cl. d-орбитали, направленные вдоль связей Re–Cl, стабилизируются за счет взаимодействия с орбиталями хлорлиганда и не вносят вклада в связывание Re–Re. [6] Напротив, [Os 2 Cl 8 ] 2− ион с еще двумя электронами (σ 2 п 4 д 2 д* 2 Os–Os ) имеет тройную связь и шахматную геометрию . [6]
Многие другие соединения с четверными связями между атомами переходных металлов были описаны, часто Коттоном и его коллегами. Изоэлектронным соединению дирения является соль K 4 [Mo 2 Cl 8 ] ( октахлордимолибдат калия ). [7] Примером соединения дивольфрама с четверной связью является тетравольфрам (hpp) .
Четверные связи между атомами элементов основной группы неизвестны. Для молекулы диуглерода (C 2 ), в качестве примера, теория молекулярных орбиталей показывает, что существует два набора спаренных электронов в сигма-системе (один связывающий, один разрыхляющий) и два набора спаренных электронов в вырожденном наборе π-связывающих орбитали. В сумме это дает порядок связи 2, что означает, что между двумя атомами углерода существует двойная связь . Диаграмма молекулярных орбиталей двухатомного углерода показала бы, что существует две пи-связи и нет сигма-связей. Недавняя статья С. Шайка и др. предположил, что в диуглероде существует четверная связь. [8] но это оспаривается. [9]
См. также [ править ]
Ссылки [ править ]
- ^ Радиус, У.; Бреер, Ф. (2006). « Смело преодолеть четверную связь металл-металл». Энджью. хим. Межд. Эд. 45 (19): 3006–3010. дои : 10.1002/anie.200504322 .
- ^ Коттон, Ф. Альберт; Уилкинсон, Джеффри (1988). «23. Связи металл-металл и кластеры атомов металлов». Продвинутая неорганическая химия (5-е изд.). Джон Уайли и сыновья. п. 1089. ИСБН 0-471-84997-9 .
- ↑ Перейти обратно: Перейти обратно: а б Коттон, ФА; Уолтон, РА (1993). Множественные связи между атомами металлов . Оксфорд: Издательство Оксфордского университета . ISBN 0-19-855649-7 .
- ^ Kuznetsov, V. G.; Koz'min, P. A. "The structure of (pyH)HReCl4" Zhurnal Strukturnoi Khimii 1963, 4, 55-62.
- ^ Коттон, Флорида ; Харрис, CB (1965). «Кристаллическая и молекулярная структура дигидрата дигидрата октахлордирената (III) дикалия, K 2 [Re 2 Cl 8 ] · 2H 2 O». Неорг. хим. 4 (3): 330–333. дои : 10.1021/ic50025a015 .
- ↑ Перейти обратно: Перейти обратно: а б Мисслер, Г.Л.; Тарр, Д.А. (1999). Неорганическая химия (2-е изд.). Прентис-Холл. п. 531. ИСБН 0-13-841891-8 .
- ^ Джиролами, Г.С.; Раухфус, ТБ; Анжеличи, Р.Дж. (1999). Синтез и техника в неорганической химии . Милл-Вэлли, Калифорния: Университетские научные книги. ISBN 0935702482 .
- ^ Шайк, Сасон; Данович, Дэвид; Ву, Вэй; Су, Пейфэн; Рзепа, Генри С.; Хиберти, Филипп К. (2012). «Четверная связь в C 2 и аналогичные восьмивалентные электроны». Природная химия . 4 : 195–200. Бибкод : 2012НатЧ...4..195С . дои : 10.1038/nchem.1263 .
- ^ Груненберг, Йорг (2012). «Квантовая химия: углерод с четверной связью». Природная химия . 4 (3): 154–155. Бибкод : 2012НатЧ...4..154Г . дои : 10.1038/nchem.1274 . ПМИД 22354425 .
Дальнейшее чтение [ править ]
- Коттон, ФА; Харрис, CB (1965). «Кристаллическая и молекулярная структура дигидрата дигидрата октахлордирената (III) дикалия, K 2 [Re 2 Cl 8 ] · 2H 2 O». Неорг. хим. 4 (3): 330–333. дои : 10.1021/ic50025a015 .