Молибдат


В химии молибдат — это соединение, содержащее в высшей оксианион молибдена степени окисления 6: ТО − −Мо(=О) 2 −О − . Молибден может образовывать очень широкий спектр таких оксианионов, которые могут представлять собой дискретные структуры или полимерные протяженные структуры, хотя последние встречаются только в твердом состоянии. Более крупные оксианионы являются членами группы соединений, называемых полиоксометаллатами , и, поскольку они содержат только один тип атома металла, их часто называют изополиметаллатами . [1] Размер дискретных оксианионов молибдена варьируется от простейшего MoO до 2−
4 , обнаружены в молибдате калия вплоть до чрезвычайно крупных структур, обнаруженных в изополимолибденовом синем цвете , которые содержат, например, 154 атома Мо. Поведение молибдена отличается от других элементов группы 6 . Хром образует только хроматы , CrO 2−
4 , Кр
22О 2−
7 , Кр
33О 2−
10 и Кр
4 Ох 2−
13 ионов, все из которых основаны на тетраэдрическом хроме. Вольфрам подобен молибдену и образует множество вольфраматов, содержащих 6-координатный вольфрам. [2]
Примеры молибдат-анионов
[ редактировать ]Примерами молибдатных оксианионов являются:
- МО 2−
4 , например, в Na 2 MoO 4 и минерале повеллите CaMoO 4 ; - Мо
22О 2−
7 , в виде гидратированного димолибдата аммония . Безводная тетрабутиламмониевая соль Mo
22О 2−
7 ; также известно [3] - Мо
33О 2−
10 в соли этилендиамина ; [4] - Мо
4 Ох 2−
13 в калиевой соли; [5] - Мо
5 О 2−
16 в анилинии ( C
66Ч
5 НХ +
3 ) соль; [6] - Мо
6 Ох 2−
19 (гексамолибдат) в тетраметиламмониевой соли; [7] - Мо
77О 6−
24 в гептамолибдате аммония , (NH 4 ) 6 Mo 7 O 24 ·4H 2 O; [8] - Мо
8 О 4−
26 в триметиламмониевой соли. [1]
В названии молибдатов обычно используется префикс, указывающий количество присутствующих атомов Мо. Например, димолибдат на 2 атома молибдена; тримолибдат для 3 атомов молибдена и т. д. Иногда степень окисления добавляется в виде суффикса, например, в пентамолибдате (VI) . Гептамолибдат-ион Mo
77О 6−
24 , часто называют «парамолибдатом».
Структура молибдат-анионов
[ редактировать ]Меньшие анионы MoO 2−
4 и Мо
22О 2−
7 имеют тетраэдрические центры. В МО 2−
4 четыре атома кислорода эквивалентны, как в сульфате и хромате , с одинаковыми длинами связей и углами. Мо
22О 2−
7 можно рассматривать как два тетраэдра, имеющие общий угол, т.е. с одним мостиковым атомом О. [1] В более крупных анионах молибден обычно, но не исключительно, 6 координируется с ребрами или вершинами MoO 6 общих октаэдров . Октаэдры искажены, типичные длины связей МО составляют:
- в терминальном немостиковом M–O примерно 1,7 Å.
- в мостиковых единицах М–О–М примерно 1,9 Å.
Мо
8 О 4−
Анион 26 содержит как октаэдрический, так и тетраэдрический молибден и может быть выделен в двух изомерных формах: альфа и бета. [2]
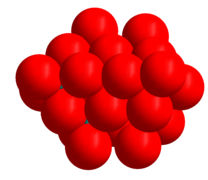
На изображении гексамолибдата ниже показаны координационные многогранники. Модель заполнения пространства изображения гептамолибдата показывает плотноупакованную природу атомов кислорода в структуре. Оксид-ион имеет ионный радиус 1,40 Å, молибден(VI) значительно меньше — 0,59 Å. [1] Существует большое сходство между структурами молибдатов и оксидов молибдена ( MoO 3 , MoO 2 и оксидов « кристаллографического сдвига » Mo 9 O 26 и Mo 10 O 29 ), все структуры которых содержат плотноупакованные оксидные ионы. [9]
- (а) Гексамолибдат [Mo 6 O 19 ] 2− (б) Гептамолибдат [Mo 7 O 24 ] 6−
- Шариковая модель гептамолибдата.
- Гептамолибдат с заполнением пространства атомами кислорода.
Равновесие в водном растворе
[ редактировать ]Когда МоО 3 , триоксид молибдена растворяют в растворе щелочи простым Анион MoO 2− 4 образуется:
При понижении pH происходит конденсация с потерей воды и образованием связей Mo–O–Mo. Показана стехиометрия, приводящая к образованию гекса-, гепта- и октамолибдатов: [1] [10]
Пероксомолибдаты
[ редактировать ]Известно множество пероксомолибдатов. Они имеют тенденцию образовываться при обработке солей молибдата перекисью водорода. Примечательно равновесие мономер-димер:
Также известен, но нестабилен [Мо(О 2 ) 4 ] 2− (см. тетрапероксохромат калия (V) ). Некоторые родственные соединения находят применение в качестве окислителей в органическом синтезе . [11]
Тетратиомолибдат
[ редактировать ]Красный тетратиомолибдат- анион образуется при обработке растворов молибдата сероводородом :
Как и сам молибдат, MoS 2−4 . подвергается конденсации в присутствии кислот, но эта конденсация сопровождается окислительно-восстановительными процессами
Промышленное использование
[ редактировать ]Катализ
[ редактировать ]Молибдаты широко используются в катализе . С точки зрения масштабов, крупнейшим потребителем молибдата является предшественник катализаторов гидрообессеривания — процесса удаления серы из нефти. состава Bi 9 PMo 12 O 52 катализирует аммоксидирование пропилена акрилонитрила до . Молибдаты висмута номинально Молибдаты железа используются в промышленности для катализа окисления метанола в формальдегид . [12]
Ингибиторы коррозии
[ редактировать ]Молибдат натрия используется в промышленной очистке воды в качестве ингибитора коррозии . Первоначально считалось, что он станет хорошей заменой хромату, когда хромат был запрещен из-за токсичности. Однако молибдат требует высоких концентраций при использовании отдельно, поэтому обычно добавляются дополнительные ингибиторы коррозии. [13] и в основном используется в высокотемпературных замкнутых контурах охлаждения. [14] Согласно экспериментальному исследованию, молибдат считается эффективным биоцидом против микробиологической коррозии (MIC), где добавление 1,5 мМ молибдата в день приводило к снижению скорости коррозии на 50%. [15]
Суперконденсаторы
[ редактировать ]Молибдаты (особенно FeMoO 4 , Fe 2 (MoO 4 ) 3 , NiMoO 4 , CoMoO 4 и MnMoO 4 ) использовались в качестве анодных или катодных материалов в водных конденсаторах. [16] [17] [18] [19] За счет псевдоемкостного накопления заряда удельная емкость до 1500 Ф г. −1 наблюдалось. [17]
Лекарство
[ редактировать ]Радиоактивный молибден-99 в форме молибдата используется в качестве исходного изотопа в генераторах технеция-99m для визуализации в ядерной медицине . [20]
Другой
[ редактировать ]Для фиксации азота необходимы молибдоферменты бобовых (например, сои, акации и т. д.). По этой причине удобрения часто содержат небольшое количество солей молибдата. Расход обычно составляет менее килограмма на акр. [12]
Молибдатные хромовые пигменты являются специальными, но коммерчески доступными пигментами. [12] Молибдат (обычно в форме молибдата калия) также используется в аналитическом колориметрическом тестировании концентрации кремнезема в растворе, называемом методом молибденового синего. [21] Кроме того, он используется при колориметрическом определении количества фосфатов в сочетании с красителем малахитовым зеленым.
Коллекционный молибдат
[ редактировать ]Кристаллы молибдата, собранные энтузиастами драгоценных камней, с лучшими в мире образцами кристаллизованного молибдата, добываемыми на шахте Мадаваска . [22]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Перейти обратно: а б с д Коттон, Ф. Альберт ; Уилкинсон, Джеффри ; Мурильо, Карлос А.; Бохманн, Манфред (1999), Передовая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ День Фольксвагена; М. Ф. Фредрих; В.Г. Клемперер ; В. Шум (1977). «Синтез и характеристика димолибдат-иона Mo
22О 2−
7 ". Журнал Американского химического общества . 99 (18): 6146. doi : 10.1021/ja00460a074 . - ^ Гийу Н.; Ферей Г. (август 1997 г.). «Гидротермальный синтез и кристаллическая структура безводного тримолибдата этилендиамина (C
22Ч
10 Н
2 ) [Мо
33О
10 ] ». Журнал «Химия твердого тела» . 132 (1): 224–227(4). Bibcode : 1997JSSCh.132..224G . doi : 10.1006/jssc.1997.7502 . - ^ БМ Сторожка; П. Леверетт (1971). «Кристаллическая структура тетрамолибдата калия, К
2 я
4 Ох
13 , и его связь со структурами других полимолибдатов одновалентных металлов». J. Chem. Soc. A : 2107–2112. doi : 10.1039/J19710002107 . - ^ В. Ласоча; Х. Шенк (1997). «Кристаллическая структура пентамолибдата анилиния по данным порошковой дифракции. Решение кристаллической структуры пакетом прямых методов POWSIM». Дж. Прил. Кристаллогр . 30 (6): 909–913. дои : 10.1107/S0021889897003105 .
- ^ С. Гаммами (2003). «Кристаллическая и молекулярная структура гексамолибдата (VI) бис (тетраметиламмония)». Кристаллические исследования и технологии . 38 (913): 913–917. дои : 10.1002/crat.200310112 . S2CID 95078211 .
- ^ Ховард Т. Эванс младший; Брайан М. Гейтхаус; Питер Леверетт (1975). «Кристаллическая структура иона гептамолибдата(VI)(парамолибдата), [Mo 7 O 24 ] 6− , в солях тетрагидрата аммония и калия». J. Chem. Soc., Dalton Trans. (6): 505–514. doi : 10.1039/DT9750000505 .
- ^ «Оксиды: химия твердого тела» WH McCarroll, Энциклопедия неорганической химии Ed. Р. Брюс Кинг, Джон Уайли и сыновья (1994) ISBN 0-471-93620-0
- ^ Клемперер, WG (1990). «Изополиоксометаллаты тетрабутиламмония». Неорганические синтезы . Неорганические синтезы. Том. 27. С. 74–85. дои : 10.1002/9780470132586.ch15 . ISBN 9780470132586 .
- ^ Дикман, Майкл Х.; Поуп, Майкл Т. (1994). «Пероксо- и супероксокомплексы хрома, молибдена и вольфрама». хим. Преподобный . 94 (3): 569–584. дои : 10.1021/cr00027a002 .
- ^ Перейти обратно: а б с Роджер Ф. Себеник и др. «Молибден и соединения молибдена» в Энциклопедии химической технологии Ульмана, 2005 г.; Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a16_655
- ^ «Открытые рециркуляционные системы охлаждения — GE Water» . gewater.com .
- ^ «Закрытые рециркуляционные системы охлаждения — GE Water» . gewater.com .
- ^ «Микробиологическая коррозия в нефтедобывающей и газовой промышленности» .
- ^ Пурушотаман, КК; Куба, М.; Муралидхаран, Г. (1 ноября 2012 г.). «Суперконденсаторное поведение наностержней α-MnMoO4 на разных электролитах». Бюллетень исследования материалов . 47 (11): 3348–3351. doi : 10.1016/j.materresbull.2012.07.027 .
- ^ Перейти обратно: а б Сентилкумар, Баскар; Санкар, Калимуту Виджая; Сельван, Рамакришнан Калаи; Даниэль, Мейрик; Маникам, Минакши (5 декабря 2012 г.). «Нано α-NiMoO4 как новый электрод для электрохимических суперконденсаторов». РСК Адв . 3 (2): 352–357. дои : 10.1039/c2ra22743f . ISSN 2046-2069 .
- ^ Цай, Даопин; Ван, Дандан; Лю, Бин; Ван, Янжун; Лю, Юань; Ван, Линлинг; Ли, Хан; Хуан, Хуэй; Ли, Цюхун (26 декабря 2013 г.). «Сравнение электрохимических характеристик наностержней NiMoO4 и иерархических наносфер для применения в суперконденсаторах». Прикладные материалы и интерфейсы ACS . 5 (24): 12905–12910. дои : 10.1021/am403444v . ISSN 1944-8244 . ПМИД 24274769 .
- ^ Ся, Сифэн; Лей, Ву; Хао, Цинли; Ван, Вэньцзюань; Ван, Синь (01 июня 2013 г.). «Одностадийный синтез композитов CoMoO4/графен с улучшенными электрохимическими свойствами для суперконденсаторов». Электрохимика Акта . 99 : 253–261. дои : 10.1016/j.electacta.2013.03.131 .
- ^ Комитет Национального исследовательского совета (США) по производству медицинских изотопов без высокообогащенного урана. (2009). «Производство и применение молибдена-99/технеция-99м» . Производство медицинских изотопов без высокообогащенного урана . Вашингтон, округ Колумбия: Издательство национальных академий.
- ^ «ASTM D7126-15 Стандартный метод испытаний для колориметрического измерения кремнезема в режиме реального времени» . astm.org .
- ^ Макдугалл, Рэймонд (3 сентября 2019 г.). «Основные полезные ископаемые из района Бэнкрофт, Онтарио, Канада» . Камни и минералы . 94 (5): 408–419. дои : 10.1080/00357529.2019.1619134 . ISSN 0035-7529 . S2CID 201298402 .
![(а) Гексамолибдат [Mo6O19]2- (б) Гептамолибдат [Mo7O24]6-](http://upload.wikimedia.org/wikipedia/commons/thumb/9/9c/Polyederstrukturen_Molybd%C3%A4n.png/417px-Polyederstrukturen_Molybd%C3%A4n.png)


![{\displaystyle {\ce {6 [MoO4]^2- + 10 HCl -> [Mo6O19]^2- + 10 Cl- + 5 H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6c7e460523b6c3300811b23faa0595a372be2c04)


![{\displaystyle {\ce {[Mo2O3(O2)2(H2O)2]^2- <=> [Mo2O3(O2)4(H2O)2]^2-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/75670ef6b00c8c1655975c07b5436ee08ec092fe)
![{\displaystyle {\ce {[NH4]2[MoO4] + 4 H2S -> [NH4]2[MoS4] + 4 H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9249a8f52bb6630839661353c724fc6650781ae4)