Псевдоемкость
Было предложено Псевдоконденсатор» объединить тему « в эту статью. ( Обсудить ) Предлагается с января 2024 г. |

Псевдоемкость — это электрохимическое хранение электричества в электрохимическом конденсаторе, известном как псевдоконденсатор . Этот фарадеевский перенос заряда возникает в результате очень быстрой последовательности обратимых фарадеевских окислительно-восстановительных процессов , электросорбции или интеркаляции на поверхности подходящих электродов . [1] [2] [3] Псевдоемкость сопровождается переносом электронного заряда между электролитом и электродом, происходящим от десольватированного и адсорбированного иона . На единицу заряда приходится один электрон. Адсорбированный ион не вступает в химическую реакцию с атомами электрода ( химические связи не возникают) . [4] ), поскольку происходит только перенос заряда.
Фарадеевская псевдоемкость возникает только вместе со статической емкостью двойного слоя . Псевдоемкость и емкость двойного слоя неразрывно влияют на общее значение емкости.
Величина псевдоемкости зависит от площади поверхности, материала и структуры электродов. Псевдоемкость может увеличивать емкость в 100 раз, чем емкость двойного слоя для той же площади поверхности. [1]
Количество электрического заряда, хранящегося в псевдоемкости, линейно пропорционально приложенному напряжению . Единицей псевдоемкости является фарад .
История
[ редактировать ]- Разработка модели двойного слоя и псевдоемкости см. Двойной слой (межфазный).
- Разработка электрохимических компонентов см. Суперконденсаторы.
Окислительно-восстановительные реакции
[ редактировать ]Различия
[ редактировать ]Аккумуляторные батареи
[ редактировать ]Окислительно-восстановительные реакции в батареях с фарадеевским переносом заряда между электролитом и поверхностью электрода были охарактеризованы десятилетия назад. Эти химические процессы связаны с химическими реакциями материалов электродов, обычно с сопутствующими фазовыми переходами . Хотя эти химические процессы относительно обратимы, циклы зарядки/разрядки аккумулятора часто необратимо приводят к необратимым продуктам химических реакций реагентов. Соответственно, срок службы аккумуляторных батарей обычно ограничен. Кроме того, продукты реакции снижают удельную мощность . Кроме того, химические процессы протекают относительно медленно, что увеличивает время зарядки/разрядки.
Электрохимические конденсаторы
[ редактировать ]
Принципиальное отличие окислительно-восстановительных реакций в аккумуляторах от электрохимических конденсаторов (суперконденсаторов) состоит в том, что в последних реакции представляют собой очень быструю последовательность обратимых процессов с переносом электрона без каких-либо фазовых изменений молекул электрода. Они не связаны с созданием или разрывом химических связей . атомы Десольватированные или ионы, вносящие вклад в псевдоемкость, просто прилипают. [4] атомной структуре электрода и заряды распределяются по поверхности за счет процессов физической адсорбции . По сравнению с батареями, фарадеевские процессы в суперконденсаторах происходят гораздо быстрее и стабильнее во времени, поскольку оставляют лишь следы продуктов реакции. Несмотря на уменьшенное количество этих продуктов, они вызывают деградацию емкости. Такое поведение является сутью псевдоемкости.
Псевдоемкостные процессы приводят к линейному емкостному поведению, зависящему от заряда, а также к созданию нефарадеевской емкости двойного слоя в отличие от батарей, поведение которых практически не зависит от заряда. Величина псевдоемкости зависит от площади поверхности, материала и структуры электродов. Псевдоемкость может превышать значение емкости двойного слоя для той же площади поверхности в 100 раз. [1]
Функциональность емкости
[ редактировать ]
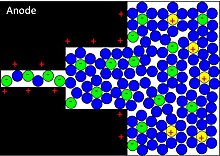
Приложение напряжения к клеммам конденсатора перемещает поляризованные ионы или заряженные атомы электролита к противоположно поляризованному электроду. Между поверхностями электродов и прилегающим электролитом образуется двойной электрический слой . Один слой ионов на поверхности электрода и второй слой соседних поляризованных и сольватированных ионов в электролите перемещаются к противоположно поляризованному электроду. Два ионных слоя разделены одним слоем молекул электролита. Между двумя слоями образуется статическое электрическое поле , в результате чего возникает емкость двойного слоя . В сопровождении двойного электрического слоя некоторые десольватированные ионы электролита проникают в разделяющий слой растворителя и адсорбируются атомами поверхности электрода. Они специфически адсорбируются и доставляют свой заряд к электроду. Другими словами, ионы в электролите внутри двойного слоя Гельмгольца также действуют как доноры электронов и переносят электроны атомам электрода, что приводит к фарадеевскому току. . Этот фарадеевский перенос заряда , возникающий в результате быстрой последовательности обратимых окислительно-восстановительных реакций, электросорбции или процессов интеркаляции между электролитом и поверхностью электрода, называется псевдоемкостью. [5]
В зависимости от структуры электрода или материала поверхности псевдоемкость может возникнуть, когда специфически адсорбированные ионы проникают в двойной слой, протекая в несколько одноэлектронных стадий . ) электрода или из них Электроны, участвующие в фарадеевских процессах, переходят в валентно-электронные состояния ( орбитали и перетекают через внешнюю цепь к противоположному электроду, где образуется второй двойной слой с равным количеством противоположно заряженных ионов. Электроны остаются в сильно ионизированных и «электроножадных» ионах переходных металлов на поверхности электрода и не передаются адсорбированным ионам. Такого рода псевдоемкость имеет линейную функцию в узких пределах и определяется зависящей от потенциала степенью покрытия поверхности адсорбированными анионами. Емкость псевдоемкости ограничена конечным количеством реагента или доступной поверхностью.
Системы, в которых возникает псевдоемкость: [5]
- Редокс- система: Ox + ze‾ ⇌ Красный.
- интеркаляции Система : Li +
в « Ма
2 " - Электросорбция , гипопотенциальное осаждение адатомов металлов или H: M +
+ ze‾ + S ⇌ SM или H +
+ e‾ + S ⇌ SH (S = узлы поверхностной решетки)
В суперконденсаторах проявились все три типа электрохимических процессов. [5] [6]
При разряде псевдоемкости перенос заряда меняется на обратный, ионы или атомы покидают двойной слой и распространяются по электролиту.
Материалы
[ редактировать ]Способность электродов создавать псевдоемкость сильно зависит от химического сродства материалов электродов к ионам, адсорбированным на поверхности электрода, а также от структуры и размеров пор электрода. Материалы, демонстрирующие окислительно-восстановительное поведение для использования в качестве электродов псевдоконденсатора, представляют собой оксиды переходных металлов , введенные путем легирования в проводящий материал электрода, такой как активный уголь, а также проводящие полимеры, такие как полианилин или производные политиофена, покрывающие материал электрода.
Оксиды/сульфиды переходных металлов
[ редактировать ]Эти материалы обеспечивают высокую псевдоемкость и были тщательно изучены Конвеем. [1] [7] Многие оксиды переходных металлов, таких как рутений ( RuO
2 ), иридий ( IrO
2 ), железо ( Fe
33О
4 ), марганец ( MnO
2 ) или сульфиды, такие как сульфид титана ( TiS
2 ) или их комбинации генерируют фарадеевские реакции переноса электрона с низким проводящим сопротивлением. [ нужна ссылка ]
Диоксид рутения ( RuO
2 ) в сочетании с серной кислотой ( H
2 ТАК
4 ) электролит представляет собой один из лучших примеров псевдоемкости с зарядом/разрядом в окне около 1,2 В на электрод. Кроме того, обратимость этих электродов из переходных металлов превосходна: срок службы превышает несколько сотен тысяч циклов. Псевдоемкость возникает в результате сопряженной обратимой окислительно-восстановительной реакции с несколькими стадиями окисления с перекрывающимся потенциалом. электрода Электроны в основном приходят с валентных орбиталей . Реакция переноса электрона протекает очень быстро и может сопровождаться большими токами.
Реакция переноса электрона протекает по схеме:
- где [8]
Во время зарядки и разрядки H +
( протоны ) включаются в RuO или удаляются из него.
2 кристаллическая решетка , которая генерирует накопление электрической энергии без химического превращения. ОН-группы осаждаются в виде молекулярного слоя на поверхности электрода и остаются в области слоя Гельмгольца. Поскольку измеримое напряжение окислительно-восстановительной реакции пропорционально заряженному состоянию, реакция ведет себя как конденсатор, а не батарея, напряжение которой в значительной степени не зависит от состояния заряда.
Проводящие полимеры
[ редактировать ]Другим типом материалов с высокой псевдоемкостью являются электронопроводящие полимеры. Проводящие полимеры, такие как полианилин , политиофен , полипиррол и полиацетилен, имеют меньшую обратимость окислительно-восстановительных процессов, включающих фарадеевский перенос заряда, чем оксиды переходных металлов, и страдают от ограниченной стабильности во время циклирования. [ нужна ссылка ] В таких электродах используется электрохимическое легирование или дедопирование полимеров анионами и катионами. Наивысшая емкость и плотность мощности достигаются при использовании полимерной конфигурации p-типа с одним отрицательно заряженным (n-легированным) и одним положительно заряженным (p-легированным) электродом.
Структура
[ редактировать ]Псевдоемкость может возникать из-за структуры электрода, особенно из-за размера пор материала. Использование карбидного углерода (CDC) или углеродных нанотрубок (УНТ) в качестве электродов обеспечивает сеть мелких пор, образующихся в результате переплетения нанотрубок. Эти нанопористые материалы имеют диаметр в диапазоне <2 нм, и их можно назвать интеркалированными порами. Сольватированные ионы в электролите не могут проникнуть в эти маленькие поры, но десольватированные ионы, размеры которых уменьшились, могут проникнуть, что приводит к большей плотности ионной упаковки и увеличению накопления заряда. Специально подобранные размеры пор в наноструктурированных углеродных электродах могут максимизировать удержание ионов, увеличивая удельную емкость за счет фарадеева H.
2 адсорбционная обработка. Заселение этих пор десольватированными ионами из раствора электролита происходит по принципу (фарадеевской) интеркаляции. [9] [10] [11]
Проверка
[ редактировать ]
Свойства псевдоемкости можно выразить в виде циклической вольтамперограммы . В идеальном двухслойном конденсаторе ток меняется на противоположный сразу же после изменения направления потенциала, что дает вольтамперограмму прямоугольной формы с током, не зависящим от потенциала электрода. У двухслойных конденсаторов с резистивными потерями форма меняется на параллелограмм . В фарадеевских электродах запасаемый в конденсаторе электрический заряд сильно зависит от потенциала, поэтому вольтамперометрические характеристики отклоняются от параллелограмма из-за задержки при изменении направления потенциала, в конечном итоге обусловленной кинетическими процессами заряда. [12] [13]
Приложения
[ редактировать ]Псевдоемкость — важное свойство суперконденсаторов .
Литература
[ редактировать ]- Эктор Д. Абрунья ; Ясуюки Кия; Джей К. Хендерсон (2008), «Батареи и электрохимические конденсаторы» (PDF) , Physics Today , вып. 12, стр. 43–47.
- Беген, Франсуа; Раймундо-Пиньеро, Э.; Фраковяк, Эльжбета (18 ноября 2009 г.). «8 электрических двухслойных конденсаторов и псевдоконденсаторов» . Углероды для электрохимических систем хранения и преобразования энергии . ЦРК Пресс. стр. 329–375. дои : 10.1201/9781420055405 . ISBN 978-1-4200-5540-5 .
- Мюллер, Клаус; Бокрис, Дж. О'М.; Деванатан, МАВ (1965). «О структуре заряженных интерфейсов» . Труды Лондонского королевского общества. Серия А, Математические и физические науки . 274 (1356): 55–79. Бибкод : 1963РСПСА.274...55Б . дои : 10.1098/rspa.1963.0114 . S2CID 94958336 .
- Б. Е. Конвей (1999), Электрохимические суперконденсаторы: научные основы и технологические применения (на немецком языке), Берлин: Springer, ISBN 978-0306457364
- Лейтнер, К.В.; Зима, М.; Безенхард, Дж. О. (декабрь 2003 г.). «Композитные электроды суперконденсатора». Журнал электрохимии твердого тела . 8 (1): 15–16. дои : 10.1007/s10008-003-0412-x . ISSN 1432-8488 . S2CID 95416761 .
- Ю М., Вольфкович; Сердюк Т.М. (сентябрь 2002 г.). «Электрохимические конденсаторы». Российский журнал электрохимии . 38 (9): 935–959. дои : 10.1023/А:1020220425954 . ISSN 1608-3342 .
- Айпин Юй; Аарон Дэвис; Чжунвэй Чен (2011). «8 – Электрохимические суперконденсаторы» . В Цзюцзюнь Чжан; Лей Чжан; Хансан Лю; Энди Сан; Ру-Ши Лю (ред.). Электрохимические технологии хранения и преобразования энергии, диапазон 1 . Вайнхайм: Wiley-VCH. стр. 317–376. ISBN 978-3-527-32869-7 .
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д Б. Е. Конвей (1999), Электрохимические суперконденсаторы: научные основы и технологические применения (на немецком языке), Берлин: Springer, стр. 1–8, ISBN. 978-0306457364 см. также Брайана Э. Конвея в Энциклопедии электрохимии: ЭЛЕКТРОХИМИЧЕСКИЕ КОНДЕНСАТОРЫ. Их природа, функции и применение. Архивировано 30 апреля 2012 г. на Wayback Machine.
- ^ Марин С. Халпер, Джеймс К. Элленбоген (март 2006 г.). Суперконденсаторы: краткий обзор (PDF) (Технический отчет). Группа компаний МИТЕР Наносистемы. Архивировано из оригинала (PDF) 1 февраля 2014 г. Проверено 20 января 2014 г.
- ^ Э. Фраковяк , Ф. Бегин: Углеродные материалы для электрохимического хранения энергии в конденсаторах. В: УГЛЕРОД. 39, 2001, с. 937–950 ( PDF [ постоянная мертвая ссылка ] ) Э. Фраковяк , К. Юревич, С. Дельпе, Ф. Беген: Нанотрубчатые материалы для суперконденсаторов. В: Журнал источников энергии. Тома 97–98, июль 2001 г., с. 822–825, дои : 10.1016/S0378-7753(01)00736-4 .
- ^ Перейти обратно: а б Гартуэйт, Джози (12 июля 2011 г.). «Как работают ультраконденсаторы (и почему они терпят неудачу)» . Земля2Тех . Сеть ГигаОМ. Архивировано из оригинала 22 ноября 2012 года . Проверено 23 апреля 2013 г.
- ^ Перейти обратно: а б с Б. Е. Конвей, У. Г. Пелл, Двухслойные и псевдоемкостные типы электрохимических конденсаторов и их применение для разработки гибридных компонентов.
- ^ Б. Е. Конвей, В. Бирсс , Дж. Войтович, Роль и использование псевдоемкости для хранения энергии суперконденсаторами , Журнал источников питания, том 66, выпуски 1–2, май – июнь 1997 г., страницы 1–14
- ^ Конвей, Бельгия (май 1991 г.). «Переход от поведения «суперконденсатора» к поведению «батареи» при электрохимическом хранении энергии» . Дж. Электрохим. Соц . 138 (6): 1539–1548. Бибкод : 1991JElS..138.1539C . дои : 10.1149/1.2085829 .
- ^ П. Саймон, Ю. Гогоци, Материалы для электрохимических конденсаторов, природные материалы , ТОМ 7, НОЯБРЬ 2008 г.
- ^ А.Г. Пандольфо, А.Ф. Холленкамп, Свойства углерода и их роль в суперконденсаторах. Архивировано 2 января 2014 г. в Wayback Machine , Journal of Power Sources 157 (2006) 11–27.
- ^ Б.П. Бахматюк, Б.Я. Венгринь, И.И. Григорчак, М.М. Мицов, С.И. Мудрый, ИНТЕРКАЛЯЦИОННАЯ ПСЕВДОЕМКОСТЬ В УГЛЕРОДНЫХ СИСТЕМАХ ХРАНЕНИЯ ЭНЕРГИИ
- ^ П. Саймон, А. Берк, Наноструктурированный углерод: двухслойная емкость и многое другое. Архивировано 14 декабря 2018 г. на Wayback Machine.
- ^ Эльжбета Фронковяк , Франсуа Беген, PERGAMON, Carbon 39 (2001) 937–950, Углеродные материалы для электрохимического хранения энергии в конденсаторах.
- ^ Почему идеальный конденсатор дает прямоугольную циклическую вольтамперограмму

