Трифторид брома
 | |
 | |
| Идентификаторы | |
|---|---|
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.211 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
| Число | 1746 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| BrFБрФ3 | |
| Молярная масса | 136.90 g/mol |
| Появление | жидкость соломенного цвета гигроскопичен |
| Запах | Удушающий, острый [1] |
| Плотность | 2,803 г/см 3 [2] |
| Температура плавления | 8,77 ° С (47,79 ° F; 281,92 К) |
| Точка кипения | 125,72 ° С (258,30 ° F; 398,87 К) |
| Реагирует с водой [3] | |
| Структура | |
| Т-образный (С 2в ) | |
| 1,19 Д | |
| Опасности [4] | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Бурно реагирует с водой с выделением HF , высокотоксичного, коррозионного, мощного окислителя. |
| СГС Маркировка : | |
    | |
| Опасность | |
| Х271 , Х300+Х310+Х330 , Х314 , Х373 | |
| P102 , P103 , P210 , P220 , P221 , P260 , P264 , P271 , P280 , P283 , P284 , P301+P310 , P301+P330+P331 , P303+P361+P353 , P304+P312 , P30 5+П351+П338+П310 , П306+П360 , П308+П313 , П340 , П363 , П370+П380 | |
| NFPA 704 (огненный алмаз) | |
| Паспорт безопасности (SDS) | http://www.chammascutters.com/en/downloads/Bromine-Trifluoride-MSDS.pdf |
| Родственные соединения | |
Другие анионы | Бром монохлорид |
Другие катионы | Трифторид хлора Трифторид йода |
Родственные соединения | монофторид брома Пентафторид брома |
| Страница дополнительных данных | |
| Трифторид брома (страница данных) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Трифторид брома представляет собой межгалогенное соединение формулы BrF 3 . При комнатной температуре представляет собой жидкость соломенного цвета с резким запахом. [5] который бурно разлагается при контакте с водой и органическими соединениями . Это мощный фторирующий агент и ионизирующий неорганический растворитель. Его используют для получения гексафторида урана (UF 6 ) при переработке и переработке ядерного топлива. [6]
Синтез
[ редактировать ]Трифторид брома был впервые описан Полем Лебо в 1906 году, который получил этот материал реакцией брома с фтором при 20 °C: [7]
- Бр2 3Ф2 2БрФ3 → +
Диспропорционирование : монофторида брома дает также трифторид брома [5]
- 3 БрФ → БрФ 3 + Бр 2
Структура
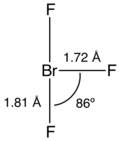
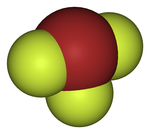
[ редактировать ]Подобно ClF 3 и IF 3 BrF 3 , молекула имеет Т-образную форму и плоскую. В формализме VSEPR бромному центру соответствуют две пары электронов . Расстояние от брома до каждого аксиального фтора составляет 1,81 Å , а до экваториального фтора - 1,72 Å. Угол между осевым фтором и экваториальным фтором немного меньше 90 ° - наблюдаемый угол 86,2 ° обусловлен тем, что отталкивание, создаваемое парами электронов, больше, чем отталкивание связей Br-F. [8] [9]
Химические свойства
[ редактировать ]В сильно экзотермической реакции BrF 3 реагирует с водой с образованием бромистоводородной и плавиковой кислот :
- BrF 3 + 2 H 2 O → 3 HF + HBr + O 2
BrF 3 является фторирующим агентом, но менее реакционноспособен, чем ClF 3 . [10] Уже при -196°С он реагирует с ацетонитрилом с образованием 1,1,1-трифторэтана. [11]
- БрФ 3 + СН 3 CN → СН 3 CF 3 + 1 ⁄ 2 Бр 2 + 1 ⁄ 2 Н 2
Жидкость проводит за счет автоионизации : [6]
- 2 БрФ 3 ⇌ БрФ + 2 + БрФ − 4
Фторидные соли легко растворяются в BrF 3 с образованием тетрафторбромата: [6]
- КФ + БрФ 3 → КБрФ 4
Он реагирует как донор фтора: [12]
- БрФ 3 + СбФ 5 → [БрФ + 2 ][СбФ − 6 ]
Ссылки
[ редактировать ]- ^ «Паспорт безопасности: трифторид брома» (PDF) . Chamascutters.com . Проверено 17 марта 2022 г.
- ^ Лиде, Дэвид Р., изд. (2006). Справочник CRC по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 0-8493-0487-3 .
- ^ «Архивная копия» (PDF) . Архивировано из оригинала (PDF) 13 мая 2012 г. Проверено 25 ноября 2012 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ) - ^ «Паспорт безопасности трифторида брома» (PDF) . Аэрогаз . Проверено 16 января 2020 г. .
- ^ Jump up to: а б Саймонс Дж. Х. (1950). «Фторид брома (III) (трифторид брома)». Фторид брома (III) – трифторид брома . Неорганические синтезы. Том. 3. С. 184–186. дои : 10.1002/9780470132340.ch48 . ISBN 978-0-470-13234-0 .
- ^ Jump up to: а б с Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Лебо П. (1906). «Влияние фтора на хлорид и бром». Анналы химии и физики . 9 : 241–263.
- ^ Gutmann V (1950). "Die Chemie in Bromitrifluorid". Angewandte Chemie . 62 (13–14): 312–315. Bibcode : 1950AngCh..62..312G . doi : 10.1002/ange.19500621305 .
- ^ Мейнерт Х (1967). «Межгалогенные соединения». Химический журнал . 7 (2): 41–57. дои : 10.1002/zfch.19670070202 .
- ^ Розен, Шломо; Сассон, Возрождение (2007). «Трифторид брома». Энциклопедия реагентов для органического синтеза . дои : 10.1002/9780470842898.rb266.pub2 . ISBN 978-0471936237 .
- ^ Розен, Шломо (2010). «Селективные реакции трифторида брома в органической химии». Расширенный синтез и катализ . 352 (16): 2691–2707. дои : 10.1002/adsc.201000482 .
- ^ Эй Джей Эдвардс и Г. Р. Джонс. Дж. Хим. Соц. А, 1467 г. (1969)
