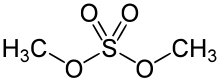
Диметилсульфат
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Диметилсульфат | |
| Другие имена
Диметилсульфат; диметиловый эфир серной кислоты; Я 2 ТАК 4 ; ДМСО 4 ; Диметиловый эфир серной кислоты; Метилсульфат, ди-
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.000.963 |
| КЕГГ | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 2 Н 6 О 4 С | |
| Молярная масса | 126.13 g/mol |
| Появление | Бесцветная маслянистая жидкость |
| Запах | слабый, луковичный [ 1 ] |
| Плотность | 1,33 г/мл, жидкость |
| Температура плавления | -32 ° C (-26 ° F; 241 К) |
| Точка кипения | 188 ° C (370 ° F, 461 К) (разлагается) |
| Реагирует | |
| Растворимость | Метанол , дихлорметан , ацетон |
| Давление пара | 0,1 мм рт.ст. (20 °С) [ 1 ] |
| −62.2 × 10 −6 см 3 /моль | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
Чрезвычайно токсичен, опасен при контакте, опасен при вдыхании, коррозионный, опасен для окружающей среды, канцерогенен, мутагенен. |
| СГС Маркировка : | |
  
| |
| Опасность | |
| Х301 , Х314 , Х317 , Х330 , Х335 , Х341 , Х350 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 83 °С; 182 °Ф; 356 К [ 1 ] |
| Летальная доза или концентрация (LD, LC): | |
ЛК 50 ( средняя концентрация )
|
8,6 частей на миллион (крыса, 4 часа) 75 частей на миллион (морская свинка, 20 мин) 53 ppm (мышь) 32 ppm (морская свинка, 1 час) [ 2 ] |
LC Lo ( самый низкий из опубликованных )
|
97 частей на миллион (человек, 10 мин) [ 2 ] |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
TWA 1 ppm (5 мг/м 3 ) [кожа] [ 1 ] |
РЕЛ (рекомендуется)
|
Ca TWA 0,1 ppm (0,5 мг/м 3 ) [кожа] [ 1 ] |
IDLH (Непосредственная опасность)
|
Са [7 частей на миллион] [ 1 ] |
| Родственные соединения | |
Родственные соединения
|
Диэтилсульфат , метилтрифлат , диметилкарбонат |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Диметилсульфат ( ДМС ) представляет собой соединение формулы SO (CH 3 O) 2 химическое 2 . Поскольку это и серной диэфир метанола кислоты , его формула часто записывается как ( CH 3 ) 2 SO 4 или Me 2 SO 4 , где CH 3 или Me представляет собой метил . Me 2 SO 4 в основном используется в качестве метилирующего агента в органическом синтезе . Me 2 SO 4 — бесцветная маслянистая жидкость со слабым луковым запахом. все сильные алкилирующие агенты , Me 2 SO 4 токсичен Как и . [ 3 ] Его использование в качестве лабораторного реагента в некоторой степени заменено метилтрифлатом CF 3 SO 3 CH 3 , метиловым эфиром трифторметансульфоновой кислоты .
История
[ редактировать ]Нечистый диметилсульфат был получен в начале 19 века. [ 4 ] Позже Дж. П. Клаессон тщательно изучил его приготовление. [ 5 ] [ 6 ]
Его исследовали на предмет возможного использования в химической войне во время Первой мировой войны. [ 7 ] [ 8 ] в смеси от 75% до 25% с метилхлорсульфонатом (CH 3 ClO 3 S) под названием «C-stoff» в Германии или с хлорсульфоновой кислотой под названием «Рационит» во Франции. [ 9 ]
Этерификация серной кислоты была метанолом описана в 1835 году: [ 10 ]
- 2 CH 3 OH + H 2 SO 4 → (CH 3 ) 2 SO 4 + 2 H 2 O
Производство
[ редактировать ]Диметилсульфат в промышленных масштабах получают путем непрерывной реакции диметилового эфира с триоксидом серы : [ 3 ]
- CH 3 OCH 3 + SO 3 → (CH 3 ) 2 SO 4
Диметилсульфат можно синтезировать в лаборатории несколькими методами. [ 11 ] Реакция метилнитрита и метилхлорсульфоната также приводит к диметилсульфату: [ 6 ]
- CH 3 ONO + (CH 3 )OSO 2 Cl → (CH 3 ) 2 SO 4 + NOCl
Реакции и использование
[ редактировать ]Диметилсульфат — реагент метилирования фенолов аминов , тиолов , для . Одна метильная группа переносится быстрее, чем вторая. Предполагается, что перенос метила происходит по реакции S N 2 . По сравнению с другими метилирующими агентами диметилсульфат предпочитается в промышленности из-за его низкой стоимости и высокой реакционной способности.
Метилирование по кислороду
[ редактировать ]Обычно диметилсульфат используется для метилирования фенолов . [ 12 ] [ 13 ]
- C 6 H 5 ONa + (CH 3 O) 2 SO 2 → C 6 H 5 OCH 3 + Na(CH 3 O)SO 3 Na
В некоторых случаях простые спирты также метилируются, о чем свидетельствует превращение трет -бутанола в трет -бутилметиловый эфир :
- (CH 3 ) 3 COH + (CH 3 O) 2 SO 2 → (CH 3 ) 3 COH + Na(CH 3 O)SO 3 H
Метилирование сахаров называется метилированием по Хаворту . [ 14 ] Метилирование кетонов называется реакцией Лаверня.
Метилирование по аминному азоту
[ редактировать ]Me 2 SO 4 используется для получения как четвертичных аммониевых солей, так и третичных аминов :
- C 6 H 5 CH=NC 4 H 9 + (CH 3 O) 2 SO 2 → C 6 H 5 CH=N + (CH 3 )C 4 H 9 [CH 3 OSO 3 ] −
Кватернизованные жирные соединения аммония используются в качестве поверхностно-активного вещества или смягчителя ткани. Метилирование с образованием третичного амина иллюстрируется следующим образом: [ 13 ]
- CH 3 (C 6 H 4 )NH 2 + (CH 3 O) 2 SO 2 (в NaHCO 3 водный) → CH 3 (C 6 H 4 )N(CH 3 ) 2 + Na(CH 3 )SO 4
Метилирование по сере
[ редактировать ]Тиолатные соли легко метилируются Me 2 SO 4 с образованием метилтиоэфиров : [ 13 ]
- RSNa + (CH 3 O) 2 SO 2 →CH 3 SR + Na(CH 3 O)SO 3 Na
В связанном примере: [ 15 ]
- p -CH 3 C 6 H 4 SO 2 Na + (CH 3 O) 2 SO 2 → p -CH 3 C 6 H 4 SO 2 CH 3 + Na(CH 3 )SO 4
Этот метод был использован для получения тиоэфиров из тиокарбоновых кислот :
- RC(O)SH + (CH 3 O) 2 SO 2 → RC(O)S(CH 3 ) + HOSO 3 CH 3
Реакции с нуклеиновыми кислотами
[ редактировать ]Диметилсульфат (ДМС) используется для определения структуры РНК вторичной . При нейтральном pH DMS метилирует неспаренные остатки аденина и цитозина на их канонических гранях Уотсона-Крика, но не может метилировать нуклеотиды, спаренные основаниями. Используя метод, известный как DMS-MaPseq , [ 16 ] РНК инкубируют с ДМС для метилирования неспаренных оснований. Затем РНК подвергается обратной транскрипции; обратная транскриптаза часто добавляет неправильное основание ДНК, когда встречает метилированное основание РНК. Эти мутации можно обнаружить с помощью секвенирования , и предполагается, что РНК является одноцепочечной по основаниям с частотой мутаций, превышающей фоновую.
Диметилсульфат может вызывать специфическое расщепление ДНК, воздействуя на имидазольные кольца, присутствующие в гуанине. [ 17 ] Диметилсульфат также метилирует аденин в одноцепочечных участках ДНК (например, в участках с белками, такими как РНК-полимераза, которые постепенно плавят и повторно отжигают ДНК). При повторном отжиге эти метильные группы мешают спариванию оснований аденин-гуанин. Затем нуклеазу S1 можно использовать для разрезания ДНК на одноцепочечные участки (в любом месте, где есть метилированный аденин). Это важный метод анализа взаимодействий белок-ДНК.
Альтернативы
[ редактировать ]Хотя диметилсульфат очень эффективен и доступен, его токсичность побудила использовать другие метилирующие реагенты. Метилиодид — это реагент, используемый для O-метилирования, как и диметилсульфат, но он менее опасен и более дорог. [ 15 ] Диметилкарбонат , который гораздо менее реакционноспособен, имеет гораздо меньшую токсичность по сравнению с диметилсульфатом и йодидом метила. [ 18 ] Высокое давление можно использовать для ускорения метилирования диметилкарбонатом. В целом токсичность метилирующих агентов коррелирует с их эффективностью в качестве реагентов для переноса метила.
Безопасность
[ редактировать ]Диметилсульфат канцерогенен. [ 19 ] и мутагенные , очень ядовитые , коррозийные и опасные для окружающей среды . [ 20 ] Он всасывается через кожу, слизистые оболочки и желудочно-кишечный тракт и может вызвать фатальную отсроченную реакцию дыхательных путей. Также часто встречается глазная реакция. Нет резкого запаха или немедленного раздражения, предупреждающих о смертельной концентрации в воздухе. LD ( 50 (острый, пероральный) составляет 205 мг/кг (крыса) и 140 мг/кг (мышь), а LC 50 острый) составляет 45 частей на миллион за 4 часа (крыса). [ 21 ] Давление пара 65 Па. [ 22 ] достаточно велика, чтобы создать смертельную концентрацию в воздухе в результате испарения при 20 °C. Отсроченная токсичность позволяет произойти потенциально смертельному воздействию до развития каких-либо предупредительных симптомов. [ 20 ] Симптомы могут проявиться через 6–24 часа. Концентрированные растворы оснований (аммиак, щелочи) можно использовать для гидролиза небольших разливов и остатков на загрязненном оборудовании, но реакция может стать бурной при использовании большего количества диметилсульфата (см. ICSC). Хотя соединение гидролизуется, нельзя предполагать, что обработка водой обеззараживает его.
Одна из гипотез относительно загадочного инцидента с «токсичной женщиной» в 1994 году заключается в том, что у человека, находившегося в центре инцидента, в крови образовались кристаллы диметилсульфона , которые неизвестным механизмом превратились в пары диметилсульфата, которые отравили лечащий медицинский персонал. [ 23 ] [ 24 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж Карманный справочник NIOSH по химическим опасностям. «#0229» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б «Диметилсульфат» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б Вайзенбергер, Карл; Майер, Дитер; Сэндлер, Стэнли Р. (2000). «Диалкилсульфаты и алкилсерные кислоты». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a08_493 . ISBN 978-3-527-30385-4 .
- ^ Дюма, Ж.; Пелиго, Э. (1835). «Мемуары о спирте дерева [т.е. метаноле] и о различных эфирных соединениях, получаемых из него». Анналы химии и физики . 2-я серия (на французском языке). 58 :5–74.
- ^ Классон, Питер (1879). «О нейтральных и кислых сульфатах метилового и этилового спирта » . Журнал практической химии . 2-я серия (на немецком языке). 19 :231-265. дои : 10.1002/prac.18790190123 .
- ^ Jump up to: а б Сутер, CM (1944). Органическая химия серы: тетраковалентные вещества серы . Джон Уайли и сыновья. стр. 49–53. LCCN 44001248 .
- ^ «Диметилсульфат 77-78-1» . Агентство по охране окружающей среды.
- ^ «Факты о яде: низкие химические вещества: диметилсульфат» . Больница Университета Канзаса.
- ^ Сартори, Марио (1939). Военные газы . Д. Ван Ностранд. стр. 262, 266.
- ^ Дюма, Ж.; Пелиго, Э. (1835). «Мемуары о спирте дерева [т.е. метаноле] и о различных эфирных соединениях, получаемых из него». Анналы химии и физики . 2-я серия (на французском языке). 58 :5–74.
- ^ Ширли, Д.А. (1966). Органическая химия . Холт, Райнхарт и Уинстон. п. 253. LCCN 64010030 .
- ^ Г.С. Хиерс, Ф.Д. Хагер (1929). «Анизол». Органические синтезы . 9:12 . дои : 10.15227/orgsyn.009.0012 .
- ^ Jump up to: а б с «Информация о продукции Dupont» . Архивировано из оригинала 19 ноября 2008 г. Проверено 8 мая 2006 г.
- ^ В. Н. Хаворт (1915). «III. Новый метод получения алкилированных сахаров». Журнал Химического общества, Сделки . 107 : 8–16. дои : 10.1039/CT9150700008 .
- ^ Jump up to: а б Физер, Л.Ф.; Физер, М. (1967). Реагенты для органического синтеза . Джон Уайли и сыновья. п. 295 . ISBN 9780471258759 .
- ^ Зубрадт, Меган; Гупта, Паромита; Персад, Ситара; Ламбовиц, Алан; Вайсман, Джонатан; Рускин, Сильви (2017). «DMS-MaPseq для полногеномного или целевого исследования структуры РНК in vivo» . Природные методы . 14 (1): 75–82. дои : 10.1038/nmeth.4057 . ПМК 5508988 . ПМИД 27819661 .
- ^ Стрейтвизер, А.; Хиткок, Швейцария ; Косовер, Э.М. (1992). Введение в органическую химию (4-е изд.). Макмиллан. п. 1169 . ISBN 978-0024181701 .
- ^ Ши, туалет; Делл, С.; Репик, О. (2001). «1,8-Диазабицикло[5.4.0]ундец-7-ен (DBU) и зеленая химия с микроволновым ускорением в метилировании фенолов, индолов и бензимидазолов диметилкарбонатом». Органические письма . 3 (26): 4279–4281. дои : 10.1021/ol016949n . ПМИД 11784197 .
- ^ «Диметилсульфат CAS № 77-78-1» (PDF) . 12-й доклад о канцерогенах (RoC) . Министерство здравоохранения и социальных служб США . 2011.
- ^ Jump up to: а б Риппи, JCR; Столлвуд, Мичиган (2005). «Девять случаев случайного воздействия диметилсульфата — потенциального химического оружия» . Журнал неотложной медицины . 22 (12): 878–879. дои : 10.1136/emj.2004.015800 . ПМК 1726642 . ПМИД 16299199 .
- ^ «Паспорт безопасности материала — Паспорт безопасности материала на диметилсульфат» . Научная лаборатория. Архивировано из оригинала 6 апреля 2012 г. Проверено 2 октября 2011 г.
- ^ КМГС
- ^ «Что за история о «токсичной даме»?» . Прямой наркотик . 22 марта 1996 г. Проверено 15 января 2024 г.
- ^ Грант, премьер-министр; Хаас, Дж. С.; Уиппл, RE; Андресен, Б.Д. (23 июня 1997 г.). «Возможное химическое объяснение событий, связанных со смертью Глории Рамирес в больнице общего профиля Риверсайд» . Международная судебно-медицинская экспертиза . 87 (3): 219–237. дои : 10.1016/s0379-0738(97)00076-5 . ISSN 0379-0738 . ПМИД 9248041 .
