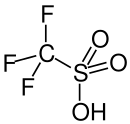
Трифликовая кислота
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Трифторметансульфоновая кислота | |||
| Другие имена Трифликовая кислота | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| КЭБ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.014.625 | ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| CF3SOCF3SO3H H | |||
| Молярная масса | 150.07121 g/mol | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 1,696 г/мл | ||
| Температура плавления | -40 ° C (-40 ° F; 233 К) | ||
| Точка кипения | 162 ° С (324 ° F; 435 К) | ||
| 1600 г/л | |||
| Давление пара | 3.2 | ||
| Кислотность ( pKa ) | −14.7 ± 2.0 [1] | ||
| Сопряженная база | Трифлат анион | ||
| Вязкость | 1,864–1,881 мм 2 /с при 20 °C | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Вызывает сильные кислотные ожоги | ||
| СГС Маркировка : | |||
  | |||
| Опасность | |||
| Х290 , Х302 , Х314 , Х335 , Х402 | |||
| P234 , P261 , P264 , P270 , P271 , P273 , P280 , P301+P312+P330 , P301+P330+P331 , P303+P361+P353 , P304+P340+P310 , P305+P351+P338+P3 10 , П363 , П390 , П403+П233 , П405 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||

Трифликовая кислота , краткое название трифторметансульфоновой кислоты , TFMS , TFSA , HOTf или TfOH , представляет собой сульфоновую кислоту с химической формулой CF 3 SO 3 H. Это одна из самых сильных известных кислот . кислота в основном используется в исследованиях в качестве катализатора этерификации Трифликовая . [2] [3] Это гигроскопичная , бесцветная, слегка вязкая жидкость, растворимая в полярных растворителях .
Синтез
[ редактировать ]Трифторметансульфоновую кислоту производят в промышленных масштабах путем электрохимического фторирования (ЭКФ) метансульфоновой кислоты :
Полученный CF 3 SO 2 F гидролизуют , а полученную трифлатную соль репротонируют. трифторметансульфоновая кислота образуется в результате окисления трифторметилсульфенилхлорида : Альтернативно , [4]
Трифликовую кислоту очищают перегонкой из трифликового ангидрида . [3]
Исторический
[ редактировать ]Трифторметансульфоновая кислота была впервые синтезирована в 1954 году Робертом Хазелдином и Киддом по следующей реакции: [5]
Реакции
[ редактировать ]В качестве кислоты
[ редактировать ]В лаборатории трифликовая кислота полезна для протонирования, поскольку сопряженное основание трифликовой кислоты ненуклеофильно. Его также используют в качестве кислотного титранта при неводном кислотно-основном титровании, поскольку он ведет себя как сильная кислота во многих растворителях ( ацетонитрил , уксусная кислота и т. д.), где обычные минеральные кислоты (такие как HCl или H 2 SO 4 ) лишь умеренно сильный.
При K a = 5 × 10 14 , п K а = −14,7 ± 2,0 , [1] трифликовая кислота относится к суперкислотам . Многие из его полезных свойств обусловлены его высокой термической и химической стабильностью. И кислота, и сопряженное с ней основание CF 3 SO −
3 , известный как трифлат , сопротивляется реакциям окисления/восстановления , тогда как многие сильные кислоты, такие как хлорная или азотная кислота , являются окисляющими . Далее рекомендуется использовать трифликовую кислоту, которая не сульфирует субстраты, что может быть проблемой при использовании серной кислоты , фторсерной кислоты и хлорсульфоновой кислоты . Ниже представлен прототип сульфирования, которому не подвергается трифликовая кислота:
Трифликовая кислота дымит во влажном воздухе и образует стабильный твердый моногидрат CF 3 SO 3 H·H 2 O, температура плавления 34 °C.
Соль и комплексообразование
[ редактировать ]Трифлатный лиганд лабилен, что отражает его низкую основность. Трифторметансульфоновая кислота экзотермически реагирует с карбонатами , гидроксидами и оксидами металлов. Показательным является синтез Cu(OTf) 2 . [6]
Хлоридные лиганды могут превращаться в соответствующие трифлаты:
Это превращение проводят в чистом HOTf при 100°C с последующим осаждением соли при добавлении эфира.
Органическая химия
[ редактировать ]Трифликовая кислота реагирует с ацилгалогенидами с образованием смешанных ангидридов трифлата, которые являются сильными ацилирующими агентами, например, в реакциях Фриделя-Крафтса .
Трифликовая кислота катализирует реакцию ароматических соединений с сульфонилхлоридами, вероятно, также через посредство смешанного ангидрида сульфоновой кислоты.
Трифликовая кислота способствует другим реакциям, подобным Фриделю-Крафтсу, включая крекинг алканов и алкилирование алкенов, которые очень важны для нефтяной промышленности. Эти катализаторы на основе производных трифликовой кислоты очень эффективны при изомеризации углеводородов с прямой или слегка разветвленной цепью, которые могут повысить октановое число конкретного топлива на нефтяной основе.
Трифликовая кислота экзотермически реагирует со спиртами с образованием простых эфиров и олефинов.
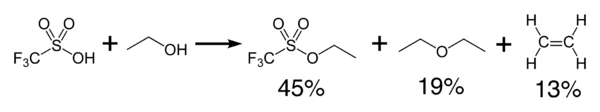
образуется ангидрид трифторметансульфокислоты При дегидратации (CF 3 SO 2 ) 2 O.
Безопасность
[ редактировать ]Трифликовая кислота – одна из самых сильных кислот. Контакт с кожей вызывает сильные ожоги с задержкой разрушения тканей. При вдыхании он вызывает смертельные спазмы, воспаление и отек . [7]
Как и серную кислоту, трифликовую кислоту необходимо медленно добавлять к полярным растворителям, чтобы предотвратить неконтролируемый температурный выход .
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Труммал, А.; Липпинг, Л.; Кальюранд, И.; Коппель, Айова; Лейто, И. (2016). «Кислотность сильных кислот в воде и диметилсульфоксиде». Журнал физической химии А. 120 (20): 3663–3669. Бибкод : 2016JPCA..120.3663T . дои : 10.1021/acs.jpca.6b02253 . ПМИД 27115918 . S2CID 29697201 .
- ^ Хауэллс, РД; МакКаун, доктор юридических наук (1977). «Трифторметансульфоновая кислота и производные». Химические обзоры . 77 (1): 69–92. дои : 10.1021/cr60305a005 .
- ^ Перейти обратно: а б Субраманиан, ЛР; Мартинес, АГ; Ханак, М.; Пракаш, ГКС; Ху, Дж. (2006). «Трифторметансульфоновая кислота». Энциклопедия реагентов для органического синтеза . Джон Уайли и сыновья. дои : 10.1002/047084289X.rt246.pub2 . ISBN 0-471-93623-5 .
- ^ Зигемунд, Г.; Швертфегер, В.; Фейринг, А.; Смарт, Б.; Бер, Ф.; Фогель, Х.; МакКьюсик, Б. (2000). «Соединения фтора органические». Энциклопедия промышленной химии Ульмана . Джон Уайли и сыновья. дои : 10.1002/14356007.a11_349 . ISBN 3527306730 .
- ^ Хазелдин, Р.Н.; Кидд, Дж. М. (1954). «Перфторалкилпроизводные серы. Часть I. Трифторметансульфокислота». Журнал Химического общества . 1954 : 4228–4232. дои : 10.1039/JR9540004228 .
- ^ Диксон, штат Невада; Лоуренс, Джорджия; Лэй, Пенсильвания; Сарджесон, AM; Таубе, Х. (1990). «Трифторметансульфонаты и трифторметансульфонато -O комплексы ». В Анджеличи, Р.Дж. (ред.). Реагенты для комплексного и металлоорганического синтеза переходных металлов . Неорганические синтезы. Том. 28. С. 70–76. дои : 10.1002/9780470132593.ch16 . ISBN 978-0-470-13259-3 .
- ^ «Паспорт безопасности трифторметансульфокислоты» . ХимCAS.





![{\displaystyle {\ce {C6H6 + H2SO4 ->[{\ce {SO3}}] C6H5(SO3H) + H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0171ff1338e1974d73935d46ca6110c9ad3f5c27)

![{\displaystyle {\ce {3 CF3SO3H + [Co(NH3)5Cl]Cl2 -> [Co(NH3)5O3SCF3](O3SCF3)2 + 3 HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/16bc6679aa18a720c03cd65ce7033a8da12409f1)

