Трифлат
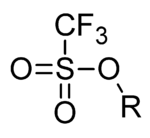

В органической химии трифлат ( систематическое название : трифторметансульфонат ) представляет собой функциональную группу с формулой R-OSO 2 CF 3 и структура R-O-S(=O) 2 -CF 3 . Группу трифлатов часто представляют −OTf , в отличие от −Tf, которая представляет собой трифлильную группу , R-SO 2 CF 3 . Например, н - бутилтрифлат можно записать как СН 3 СН 2 СН 2 СН 2 ОТф .
Соответствующий трифлат анион - CF 3 SO − 3 — чрезвычайно стабильный многоатомный ион ; это происходит от того, что трифликовая кислота ( CF 3 SO 3 H ) — суперкислота ; т. е. она более кислая, чем чистая серная кислота , которая уже является одной из самых сильных известных кислот .
Приложения
[ редактировать ]Трифлатная группа является превосходной уходящей группой, используемой в некоторых органических реакциях, таких как нуклеофильное замещение , реакции Сузуки и реакции Хека . Поскольку алкилтрифлаты чрезвычайно реакционноспособны в реакциях S N 2 , их необходимо хранить в условиях, свободных от нуклеофилов (например, в воде ). Анион обязан своей стабильностью резонансной стабилизации , которая приводит к симметричному распределению отрицательного заряда по трем атомам кислорода. Дополнительная стабилизация достигается за счет трифторметильной группы, которая действует как сильная электроноакцепторная группа, используя атом серы в качестве мостика.
Трифлаты также применяются в качестве лигандов металлов 11 и 13 групп наряду с лантанидами .
Трифлаты лития используются в некоторых литий-ионных батареях в качестве компонента электролита .
Мягким трифлатирующим реагентом является фенилтрифлимид или N , N -бис(трифторметансульфонил)анилин , где побочным продуктом является [CF 3 SO 2 N-Ph] − .
Трифлатные соли
[ редактировать ]трифлата Соли термически очень стабильны с температурой плавления до 350 °C для солей натрия , бора и серебра , особенно в безводной форме. Их можно получить непосредственно из трифликовой кислоты и гидроксида или карбоната металла в воде. Альтернативно их можно получить реакцией хлоридов металлов с чистой трифликовой кислотой или трифлатом серебра или реакцией трифлата бария с сульфатами металлов в воде: [1]
Трифлаты металлов используются в качестве катализаторов кислот Льюиса в органической химии . Особенно полезны трифлаты лантаноидов типа Ln(OTf) 3 (где Ln – лантаноид ). Родственный популярный катализатор трифлат скандия используется в таких реакциях, как альдольные реакции и реакции Дильса-Альдера . Примером может служить реакция альдольного присоединения Мукаямы между бензальдегидом и силиленольным эфиром циклогексанона с химическим 81% выходом . [2] Соответствующая реакция с солью иттрия не проходит:

Трифлат — широко используемый слабокоординирующий анион .

См. также
[ редактировать ]- Метилтрифлат
- нонафлат
- Трифторметансульфоновая кислота
- Трифлимидат металла
- Реактив Коминса
- трифлат лития
Ссылки
[ редактировать ]- ^ Диксон, штат Невада; Лоуренс, Джорджия; Лэй, Пенсильвания; Сарджесон, AM; Таубе, Х. (1990). «Трифторметансульфонаты и трифторметансульфонато -O комплексы ». Неорганические синтезы . 28 : 70–76. дои : 10.1002/9780470132593.ch16 . ISBN 9780470132593 .
- ^ Кобаяши, С. (1999). «Трифлат скандия в органическом синтезе». Европейский журнал органической химии . 1999 (1): 15–27. doi : 10.1002/(SICI)1099-0690(199901)1999:1<15::AID-EJOC15>3.0.CO;2-B .
- ^ Айхара, Ёсинори; Чатани, Наото (10 апреля 2013 г.). «Никель-катализируемое прямое алкилирование связей C – H в бензамидах и акриламидах функционализированными алкилгалогенидами посредством бидентатно-хелатного содействия». Журнал Американского химического общества . 135 (14): 5308–5311. дои : 10.1021/ja401344e . ПМИД 23495861 .
