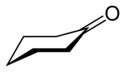
Циклогексанон
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Циклогексанон | |||
| Другие имена
оксоциклогексан, пимелиновый кетон, кетогексаметилен, циклогексилкетон, кетоциклогексан, гексанон, Гидрол-О, Секстон, К, Анон
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.003.302 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 6 Н 10 О | |||
| Молярная масса | 98.15 g/mol | ||
| Появление | Бесцветная жидкость [3] | ||
| Запах | перечную мяту или ацетон похожий на | ||
| Плотность | 0,9478 г/мл, жидкость | ||
| Температура плавления | -47 ° C (-53 ° F; 226 К) [6] | ||
| Точка кипения | 155,65 ° С (312,17 ° F; 428,80 К) | ||
| 8,6 г/100 мл (20 °С) | |||
| Растворимость во всех органических растворителях | смешивается | ||
| войти P | 0.81 | ||
| Давление пара | 5 мм рт.ст. (20°С) [4] | ||
| -62.04·10 −6 см 3 /моль | |||
Показатель преломления ( n D )
|
1.447 | ||
| Вязкость | 2,02 сП при 25 °C [5] | ||
| Термохимия | |||
Стандартный моляр
энтропия ( S ⦵ 298 ) |
+229,03 Дж.К. −1 .моль −1 | ||
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
−270,7 кДж моль −1 | ||
Стандартная энтальпия
горение (Δ c H ⦵ 298 ) |
−3519,3 кДжмоль −1 | ||
| Опасности | |||
| СГС Маркировка : | |||
  
| |||
| Опасность [7] | |||
| Х226 , Х302 , Х305 , Х312 , Х315 , Х318 , Х332 [7] | |||
| П280 , П305+П351+П338 [7] | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 44 ° С (111 ° F; 317 К) | ||
| 420 ° С (788 ° F, 693 К) | |||
| Взрывоопасные пределы | 1.1–9.4% | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза )
|
1200 мг/кг (кошка, перорально); 2362 мг/кг (крыса, перорально) [8] | ||
ЛК 50 ( средняя концентрация )
|
8000 частей на миллион (крыса, 4 часа) [9] | ||
LC Lo ( самый низкий из опубликованных )
|
4706 частей на миллион (мышь, 1,5 часа) [9] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
ПЭЛ (допустимо)
|
СВВ 50 частей на миллион (200 мг/м 3 ) [4] | ||
РЕЛ (рекомендуется)
|
СВВ 25 частей на миллион (100 мг/м 3 ) [кожа] [4] | ||
IDLH (Непосредственная опасность)
|
700 частей на миллион [4] | ||
| Родственные соединения | |||
Родственные кетоны
|
Циклопентанон , циклогептанон | ||
Родственные соединения
|
Циклогексанол | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Циклогексанон представляет собой органическое соединение с формулой (CH 2 ) 5 CO. Молекула состоит из шестиуглеродной циклической молекулы с кетоновой функциональной группой . Эта бесцветная маслянистая жидкость [3] имеет сладкий запах, напоминающий бензальдегид . Со временем образцы циклогексанона приобретают бледно-желтый цвет. [10] Циклогексанон мало растворим в воде и смешивается с обычными органическими растворителями. Ежегодно производятся миллионы тонн, в основном в качестве прекурсора нейлона . [11]
Производство
[ редактировать ]Циклогексанон получают окислением циклогексана на воздухе, обычно с использованием кобальтовых катализаторов: [11]
- С 6 Н 12 + О 2 → (СН 2 ) 5 СО + Н 2 О
образуется циклогексанол В этом процессе в качестве побочного продукта , и эта смесь, называемая «Масло КА» для кетон-спиртового масла, является основным сырьем для производства адипиновой кислоты . В окислении участвуют радикалы и гидропероксид C 6 H 11 O 2 H в качестве промежуточного продукта. очищенный циклогексанол, полученный гидратацией циклогексена В некоторых случаях предшественником является можно получить частичным гидрированием фенола : . Альтернативно циклогексанон
- C 6 H 5 OH + 2 H 2 → (CH 2 ) 5 CO
Этот процесс также можно отрегулировать, чтобы способствовать образованию циклогексанола. [11]
Компания ExxonMobil разработала процесс гидроалкилирования бензола до циклогексилбензола . Этот последний продукт окисляется до гидропероксида , а затем расщепляется на фенол и циклогексанон. [12] Таким образом, этот новый процесс без образования побочного продукта ацетона кажется привлекательным и похож на процесс с кумолом, поскольку гидропероксид образуется, а затем разлагается с образованием двух ключевых продуктов. [13]
Лабораторные методы
[ редактировать ]Циклогексанон можно получить из циклогексанола окислением триоксидом хрома ( окисление Джонса ). В альтернативном методе используется более безопасный и доступный окислитель гипохлорит натрия . [14] [15]
Использование
[ редактировать ]Подавляющее большинство циклогексанона расходуется при производстве предшественников нейлона 6,6 и нейлона 6 . Около половины мировых запасов перерабатывается в адипиновую кислоту , один из двух прекурсоров нейлона 6,6 . Для этого применения масло КА (см. выше) окисляется азотной кислотой . Другая половина поставок циклогексанона преобразуется в оксим циклогексанона . В присутствии серной кислоты катализатора оксим перегруппировывается в капролактам , предшественник нейлона 6 : [11]
Другие реакции
[ редактировать ]Помимо крупномасштабных реакций, проводимых в полимерной промышленности, было разработано множество реакций для циклогексанона.
В присутствии света он подвергается альфа-хлорированию с образованием 2-хлорциклогексанона. [16] Он образует эфир триметилсиленола при обработке триметилсилилхлоридом в присутствии основания. [17]
образует енамин С пирролидином . [18]
Обработка нитрозилхлоридом и этанолом в диоксиде серы дает сложный эфир оксиминкарбоновой кислоты: [19]
- (CH 2 ) 5 CO + C 2 H 5 OH + NOCl → HON=CH(CH 2 ) 4 CO 2 C 2 H 5 + HCl
Незаконное использование
[ редактировать ]Циклогексанон использовался при незаконном производстве фенциклидина и его аналогов. [20] и часто на него распространяются ограничения на покупку, например, он внесен в Список специального надзора в США. [21]
Безопасность
[ редактировать ]Как и циклогексанол , циклогексанон не канцерогенен и умеренно токсичен, с ПДК паров 25 частей на миллион. Это раздражитель. [11]
Ссылки
[ редактировать ]- ^ «ICSC 0425 – ЦИКЛОГЕКСАНОН» . inchem.org . Проверено 24 августа 2022 г.
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - Циклогексанон» . Центры по контролю и профилактике заболеваний (CDC) . Проверено 24 августа 2022 г.
- ^ Jump up to: а б «Циклогексанон (CID 7967)» . ПабХим .
- ^ Jump up to: а б с д Карманный справочник NIOSH по химическим опасностям. «#0166» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Ч. Вольфарт. «Вязкость циклогексанона». В MD Lechner (ред.). Вязкость чистых органических жидкостей и бинарных смесей жидкостей · Дополнение к IV/18 . Спрингер-Верлаг . дои : 10.1007/978-3-540-75486-2_192 .
- ^ «Циклогексанон» . Сигма-Олдрич.
- ^ Jump up to: а б с Sigma-Aldrich Co. , Циклогексанон .
- ^ Циклогексанон: токсичность для животных и человека.
- ^ Jump up to: а б «Циклогексанон» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Циклогексанон (CID 7967)» . ПабХим .
- ^ Jump up to: а б с д и Массер, Майкл Т. (15 октября 2011 г.). «Циклогексанол и Циклогексанон» . Энциклопедия промышленной химии Ульмана . Вайнхайм, Германия: Wiley-VCH Verlag GmbH & Co. КгаА. дои : 10.1002/14356007.a08_217.pub2 . ISBN 978-3-527-30673-2 . OCLC 46878292 . Проверено 27 января 2009 г.
- ^ Плоткин, Джеффри С. (21 марта 2016 г.). «Что нового в производстве фенола?» . Американское химическое общество. Архивировано из оригинала 27 октября 2019 г. Проверено 27 октября 2019 г.
- ^ «Фенол – важная химическая промышленность онлайн» . 11 января 2017 г. Проверено 27 октября 2019 г.
- ^ «Окисление циклогексанола в циклогексанон» . Архивировано из оригинала 26 апреля 2012 г. Проверено 9 июля 2012 г.
- ^ Мориг, Джерри Р.; Ниенхейс, Дэвид М.; Линк, Кэтрин Ф.; Ван Зоерен, Кэрол; Фокс, Брайан Г.; Махаффи, Питер Г. (июнь 1985 г.). «План лабораторных экспериментов в 1980-х годах: тематическое исследование окисления спиртов бытовым отбеливателем». Журнал химического образования . 62 (6): 519. doi : 10.1021/ed062p519 .
- ^ М. С. Ньюман; доктор медицинских наук Фарбман; Х. Хипшер (1945). «2-хлорциклогексанон». Орг. Синтез . 25:22 . дои : 10.15227/orgsyn.025.0022 .
- ^ Вальсамма Варгезе; Манаси Саха; Кеннет М. Николас (1989). «Алкилирование с использованием солей гексакарбонил(пропаргилия)дикобальта: 2-(1-метил-2-пропинил)циклогексанон». Орг. Синтез . 67 : 141. дои : 10.15227/orgsyn.067.0141 .
- ^ Р.Б. Вудворд ; Эй Джей Пэчтер; М. Л. Шейнбаум (1974). «2,2-(Триметилендитио)циклогексанон». Орг. Синтез . 54:39 . дои : 10.15227/orgsyn.054.0039 .
- ^ Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 1736, ISBN 978-0-471-72091-1
- ^ Шульгин А.Т.; Маклин, Делавэр (25 сентября 2008 г.). «Незаконный синтез фенциклидина (ПХФ) и некоторых его аналогов». Клиническая токсикология . 9 (4): 553–560. дои : 10.3109/15563657608988157 . ПМИД 975751 .
- ^ «Перечень специального надзора за химическими веществами, продуктами, материалами и оборудованием, используемыми при тайном производстве контролируемых веществ или включенных в списки химических веществ» . Архивировано из оригинала 20 апреля 2011 года.