Бензальдегид
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Бензолкарбальдегид | |||
| Предпочтительное название ИЮПАК Бензальдегид [1] | |||
| Другие имена Бензолкарбоксальдегид Фенилметаналь Бензойный альдегид | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.002.601 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1990 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 7 Н 6 О | |||
| Молярная масса | 106.124 g·mol −1 | ||
| Появление | бесцветная жидкость сильно преломляющий | ||
| Запах | миндалевидный | ||
| Плотность | 1,044 г/мл, жидкость | ||
| Температура плавления | −57.12 [2] ° C (-70,82 ° F; 216,03 К) | ||
| Точка кипения | 178,1 ° С (352,6 ° F; 451,2 К) | ||
| 6,95 г/л (25 °С) [3] | |||
| войти P | 1.64 [4] | ||
| -60.78·10 −6 см 3 /моль | |||
Показатель преломления ( n D ) | 1.5456 | ||
| Вязкость | 1321 сП (25 ° С) | ||
| Термохимия | |||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −36,8 кДж/моль | ||
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | −3525,1 кДж/моль | ||
| Опасности | |||
| СГС Маркировка : | |||
 | |||
| Предупреждение | |||
| H302 | |||
| П264 , П270 , П301+П312 , П330 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 64 ° С (147 ° F; 337 К) | ||
| 192 ° С (378 ° F; 465 К) | |||
| Взрывоопасные пределы | 1.4–8.5% | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 1300 мг/кг (крыса, перорально) | ||
| Паспорт безопасности (SDS) | Джей Ти Бейкер | ||
| Родственные соединения | |||
Родственные соединения | Бензиловый спирт Бензойная кислота Бензальдегид оксим | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Бензальдегид (C 6 H 5 CHO) – органическое соединение, состоящее из бензольного кольца с формильным заместителем. Это один из самых простых ароматических альдегидов и один из наиболее полезных в промышленном отношении.
Это бесцветная жидкость с характерным миндаля запахом газированных , обычно используемая в вишни со вкусом напитках . [5] Бензальдегид, компонент масла горького миндаля , можно извлечь из ряда других природных источников. [6] Синтетический бензальдегид является ароматизатором в искусственном экстракте миндаля, который используется для ароматизации тортов и другой выпечки. [7]
История
[ редактировать ]Бензальдегид был впервые получен в 1803 году французским фармацевтом Мартресом. Его эксперименты были сосредоточены на выяснении природы амигдалина , ядовитого соединения, обнаруженного в горьком миндале , плоде Prunus dulcis . [8] В результате дальнейшей работы над маслом двух французских химиков Пьера Робике и Антуана Бутрона Шарлара был получен бензальдегид. [9] В 1832 году Фридрих Вёлер и Юстус фон Либих впервые синтезировали бензальдегид. [10]
Производство
[ редактировать ]По состоянию на 1999 год 7000 тонн синтетического и 100 тонн природного бензальдегида. ежегодно производилось [11] хлорирование и окисление толуола . жидкофазное Основными путями являются Было разработано множество других методов, таких как частичное окисление бензилового спирта , щелочной гидролиз бензальхлорида и карбонилирование бензола ( реакция Гаттермана-Коха ). [6]
Значительное количество природного бензальдегида получают из коричного альдегида, полученного из масла кассии ретро- альдольной реакцией : [11] коричный альдегид нагревают в водном / спиртовом растворе при температуре от 90 °C до 150 °C с основанием (чаще всего натрия карбонатом или бикарбонатом ) в течение 5–80 часов, [12] с последующей отгонкой образовавшегося бензальдегида. Эта реакция также дает ацетальдегид . Природный статус полученного таким способом бензальдегида является спорным. [11]
возникновение
[ редактировать ]Бензальдегид и подобные химические вещества встречаются в природе во многих продуктах питания. Большая часть бензальдегида, который люди едят, поступает из натуральных растительных продуктов, таких как миндаль . [13]
Миндаль, абрикосы , яблоки и косточки вишни содержат значительное количество амигдалина . Этот гликозид под действием ферментативного катализа распадается на бензальдегид, цианистый водород и два эквивалента глюкозы .
Бензальдегид придает аромат вешенкам ( Pleurotus ostreatus ). [14]
Реакции
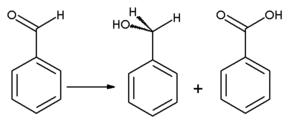
[ редактировать ]Бензальдегид легко окисляется до бензойной кислоты на воздухе при комнатной температуре. [15] вызывая обычную примесь в лабораторных образцах. Поскольку температура кипения бензойной кислоты намного выше, чем у бензальдегида, ее можно очистить перегонкой . Бензиловый спирт можно получить из бензальдегида путем гидрирования . Реакция бензальдегида с безводным ацетатом натрия и уксусным ангидридом дает коричную кислоту , а спиртовой цианид калия может быть использован для катализа конденсации бензальдегида в бензоин . Бензальдегид подвергается диспропорционированию при обработке концентрированной щелочью ( реакция Канниццаро ): одна молекула альдегида восстанавливается до бензилового спирта , а другая одновременно окисляется до бензойной кислоты .
С диолами, включая многие сахара, бензальдегид конденсируется с образованием бензилиденацеталей .
Использование
[ редактировать ]Бензальдегид обычно используется для придания миндального вкуса пище и ароматизированным продуктам, включая жидкости для электронных сигарет. Иногда его используют в косметических продуктах. [16]
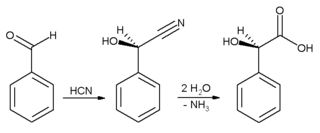
В промышленности бензальдегид используется главным образом в качестве предшественника других органических соединений, от фармацевтических препаратов до добавок к пластику. Анилиновый краситель малахитовый зеленый получают из бензальдегида и диметиланилина . Бензальдегид также является предшественником некоторых акридиновых красителей. Бензальдегид посредством альдольной конденсации превращается в производные коричного альдегида и стирола . Синтез миндальной кислоты начинается с присоединения синильной кислоты к бензальдегиду:
Образующийся циангидрин гидролизуется до . миндальной кислоты (На схеме выше изображен только один из двух образовавшихся энантиомеров ).
Нишевое использование
[ редактировать ]Бензальдегид используется как отпугиватель пчел . [17] Небольшое количество раствора бензальдегида помещают на вытяжную доску рядом с сотами. Затем пчелы отходят от сот, чтобы избежать испарений. [18] Затем пчеловод . может удалить медовые рамки из улья с меньшим риском как для пчел, так и для пчеловода
Бензальдегид реагирует с нитроэтаном в присутствии катализатора с образованием фенил-2-нитропропена , предшественника амфетамина и других химических веществ. [19]
Безопасность
[ редактировать ]При использовании в пищевых продуктах, косметике, фармацевтических препаратах и мыле бензальдегид «обычно считается безопасным» ( GRAS ) FDA США. [20] и ФЕМА . [13] Этот статус был подтвержден после проверки в 2005 году. [13] Он принят в Европейском Союзе в качестве ароматизатора. [16] Токсикологические исследования показывают, что он безопасен и неканцерогенен в концентрациях, используемых в пищевых продуктах и косметике. [16] и может даже обладать антиканцерогенными (противораковыми) свойствами. [16]
Для человека массой 70 кг смертельная доза оценивается в 50 мл. [6] / день установило допустимую суточную дозу бензальдегида в 15 мг Агентство по охране окружающей среды США . [21] Бензальдегид не накапливается в тканях человека. [16] Метаболизируется, а затем выводится с мочой. [16]
Ссылки
[ редактировать ]- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 908. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Хейнс, Уильям М. (2014), Справочник CRC по химии и физике (95-е изд.), CRC press, стр. 3–34, ISBN 9781482208689
- ^ «База данных веществ ГЕСТИС» . Институт охраны труда и здоровья Немецкого социального страхования от несчастных случаев. Архивировано из оригинала 3 марта 2016 года . Проверено 21 августа 2012 года .
- ^ «Бензальдегид_мсдс» .
- ^ Хоул, Кристина; Ройш, Хельмут; Руге, Ингрид; Годельманн, Рольф; слива, табея; Кубалла, Томас; Шумахер, Сандра; Лахенмайер, Дирк В. (2016). «Бензальдегид со вкусом вишни как предшественник образования бензола в напитках». Пищевая химия . 206 : 74–77. doi : 10.1016/j.foodchem.2016.03.034 . ПМИД 27041300 .
- ^ Перейти обратно: а б с Брюне, Фридрих и Райт, Элейн (2002) «Бензальдегид» в Энциклопедии промышленной химии Ульмана . Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a03_463
- ^ Иллюстрированная книга кулинара по выпечке . Американская тестовая кухня. 2013. ISBN 9781936493784 .
- ↑ В 1803 г. К. Марпре опубликовал рукопись о масле горького миндаля: «Исследование природы и места горечи и запаха горького миндаля». Однако мемуары по большей части игнорировались, пока в 1819 году не был опубликован отрывок: Marprès fils (1819) «О горьком миндале», Journal de Pharmacie , vol. 5, стр. 289–296.
- ^ Новые эксперименты с горьким миндалем и летучим маслом, которое они дают Робике, Бутрон-Шарлар, Анналы химии и физики, 44 (1830), 352–382,
- ^ Вёлер, Фридрих и Либих, Юстус фон (1832). «Исследования радикала бензойной кислоты» . Анналы аптеки . 3 (3): 249–282. дои : 10.1002/jlac.18320030302 . hdl : 2027/hvd.hxdg3f .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б с Инновации в пищевой инженерии: новые технологии и продукты . Пассос, Мария Лаура, Рибейро, Клаудио П. Бока Ратон, Флорида: CRC Press. 2010. с. 87. ИСБН 9781420086072 . OCLC 500683261 .
{{cite book}}: CS1 maint: другие ( ссылка ) - ^ Винс, Чарльз и Питте, Алан О. (1985) Патент США 4,617,419. Способ получения природного бензальдегида и ацетальдегида, композиций природного бензальдегида и ацетальдегида, продукты, полученные таким образом, и органолептические свойства для них.
- ^ Перейти обратно: а б с Адамс, ТБ; Коэн, С.М.; Дулл, Дж.; Ферон, виджей; Гудман, Дж.И.; Марнетт, LJ; Манро, IC; Портогезе, PS; Смит, Р.Л. (1 августа 2005 г.). «Оценка FEMA GRAS производных бензила, используемых в качестве ароматизирующих ингредиентов». Пищевая и химическая токсикология . 43 (8): 1207–1240. дои : 10.1016/j.fct.2004.11.014 . ПМИД 15950815 .
- ^ Бельтран-Гарсия, Мигель Дж.; Эстаррон-Эспиноза, Мирна; Огура, Тэцуя (1997). «Летучие соединения, выделяемые вешенкой ( Pleurotus ostreatus ), и их антибактериальная активность». Журнал сельскохозяйственной и пищевой химии . 45 (10): 4049. doi : 10.1021/jf960876i .
- ^ Санкар, Минакшисундарам (2014). «Парадокс окисления бензальдегида, объясненный перехватом пероксирадикала бензиловым спиртом» (PDF) . Природные коммуникации . 5 : 3332. Бибкод : 2014NatCo...5.3332S . дои : 10.1038/ncomms4332 . ПМИД 24567108 .
- ^ Перейти обратно: а б с д и ж Андерсен, Алан (1 января 2006 г.). «Итоговый отчет по оценке безопасности бензальдегида» . Международный журнал токсикологии . 25 (Приложение 1): 11–27. дои : 10.1080/10915810600716612 . ПМИД 16835129 . S2CID 32177208 .
- ^ Эванс, Элизабет; Батлер, Кэрол (9 февраля 2010 г.). Почему пчелы жужжат?: Почему пчелы жужжат? Увлекательные ответы на вопросы о пчелах . Издательство Университета Рутгерса. стр. 177–178. ISBN 9780813549200 .
- ^ Сэнфорд, Малкольм Т.; Бонни, Ричард Э. (1 января 2010 г.). Руководство Стори по содержанию медоносных пчел: производство меда, опыление, здоровье пчел . Стори Паблишинг. п. 167. ИСБН 9781603425506 .
- ^ «Синтез фенил-2-нитропропена» . Эровид . Проверено 7 октября 2023 г.
- ^ Фридрих Брюне; Элейн Райт (2007), «Бензальдегид», Энциклопедия промышленной химии Ульмана (7-е изд.), Wiley, стр. 11
- ^ Оценка, Национальный центр окружающей среды Агентства по охране окружающей среды США. «Профиль воздействия бензальдегида на здоровье и окружающую среду» . cfpub.epa.gov . Проверено 16 сентября 2017 г.