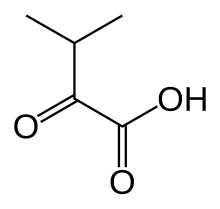
α-Кетоизовалериановая кислота
| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
3-Метил-2-оксобутановая кислота | |
| Другие имена
2-кетоизовалериановая кислота; α-кетовалин
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.010.969 |
| КЕГГ | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| C5H8OC5H8O3 | |
| Молярная масса | 116.116 g·mol −1 |
| Появление | бесцветное или белое твердое вещество или масло |
| Температура плавления | 31,5 ° C (88,7 ° F; 304,6 К) |
| Точка кипения | 170,5 ° С (338,9 ° F; 443,6 К) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
α-Кетоизовалериановая кислота представляет собой органическое соединение формулы (CH 3 ) 2 CHC(O)CO 2 H. Это кетокислота . С температурой плавления чуть выше комнатной температуры он обычно представляет собой масло или полутвердое вещество. Соединение бесцветно. Это метаболит валина и предшественник пантотеновой кислоты , простетической группы, обнаруженной в нескольких кофакторах. В биологическом контексте обычно встречается как сопряженное с ним основание кетоизовалерат , (CH 3 ) 2 CHC(O)CO 2 − . [ 1 ]
Синтез и реакции
[ редактировать ]α-кетоизовалерат подвергается гидроксиметилированию с образованием кетопантоата : [ 1 ]
- (CH 3 ) 2 CHC(O)CO 2 − + CH 2 O → HOCH 2 (CH 3 ) 2 CC(O)CO 2 −
Это превращение катализируется кетопантоатгидроксиметилтрансферазой.
Как и многие α-кетокислоты, α-кетоизовалериановая кислота склонна к декарбоксилированию с образованием изобутиральдегида :
- (CH 3 ) 2 CHC(O)CO 2 H → (CH 3 ) 2 CHCHO + CO 2
Генная инженерия использовалась для производства для биотоплива изобутанола путем восстановления изобутиральдегида, полученного из кетоизовалерата. [ 2 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б Леонарди, Роберта; Джековский, Сюзанна (апрель 2007 г.). «Биосинтез пантотеновой кислоты и кофермента А» . ЭкоСал Плюс . 2 (2). дои : 10.1128/ecosalplus.3.6.3.4 . ISSN 2324-6200 . ПМЦ 4950986 . ПМИД 26443589 .
- ^ Ацуми, Шота; Ханаи, Тайдзо; Ляо, Джеймс К. (2008). «Неферментативные пути синтеза высших спиртов с разветвленной цепью в качестве биотоплива». Природа . 451 (7174): 86–89. Бибкод : 2008Natur.451...86A . дои : 10.1038/nature06450 . ПМИД 18172501 . S2CID 4413113 .