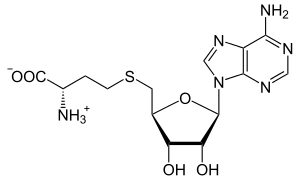
S -Аденозил- L -гомоцистеин
| |
| Имена | |
|---|---|
| Название ИЮПАК
S- (5'-Дезоксиадено-5'-ил) -L -гомоцистеин
| |
| Систематическое название ИЮПАК
(2 S )-2-Амино-4-({[(2 S ,3 S ,4 R ,5 R )-5-(6-амино-9 H -пурин-9-ил)-3,4-дигидроксиоксолан -2-ил]метил}сульфанил)бутановая кислота | |
| Другие имена
AdoHcy, 2- S -аденозил- L -гомоцистеин,
5'- S- (3-амино-3-карбоксипропил)-5'-тиоаденозин S -аденозилгомоцистеин, САК | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.012.328 |
| КЕГГ | |
| МеШ | S-аденозилгомоцистеин |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 14 Ч 20 Н 6 О 5 С | |
| Молярная масса | 384.41 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
S -Аденозил- L -гомоцистеин ( SAH ) является биосинтетическим предшественником гомоцистеина . [ 1 ] SAH образуется в результате деметилирования L S -аденозил- - метионина . [ 2 ] [ 3 ] Аденозилгомоцистеиназа превращает САК в гомоцистеин и аденозин .
Биологическая роль
[ редактировать ]ДНК-метилтрансферазы ингибируются САК. [ 4 ] Два S -аденозил- L -гомоцистеина продукта кофактора могут связывать активный сайт ДНК-метилтрансферазы 3B и предотвращать связывание дуплекса ДНК с активным сайтом , что ингибирует метилирование ДНК . [ 5 ]
Ссылки
[ редактировать ]- ^ Финкельштейн Дж. Д. (2000). «Пути и регуляция метаболизма гомоцистеина у млекопитающих». Семинары по тромбозам и гемостазу . 26 (3): 219–225. дои : 10.1055/s-2000-8466 . ПМИД 11011839 .
- ^ Риббе М.В., Ху Ю., Ходжсон Но.К., Хедман Б. (апрель 2014 г.). «Биосинтез металлокластеров нитрогеназы» . Химические обзоры . 114 (8): 4063–4080. дои : 10.1021/cr400463x . ПМК 3999185 . ПМИД 24328215 .
- ^ Джеймс С.Дж., Мельник С., Погрибна М., Погрибный И.П., Каудилл М.А. (август 2002 г.). «Повышение уровня S-аденозилгомоцистеина и гипометилирование ДНК: потенциальный эпигенетический механизм патологии, связанной с гомоцистеином» . Журнал питания . 132 (8 дополнений): 2361S–2366S. дои : 10.1093/jn/132.8.2361S . ПМИД 12163693 .
- ^ Кумар Р., Шривастава Р., Сингх Р.К., Суролия А., Рао Д.Н. (март 2008 г.). «Активация и ингибирование ДНК-метилтрансфераз аналогами S-аденозил-L-гомоцистеина». Биоорганическая и медицинская химия . 16 (5): 2276–2285. дои : 10.1016/j.bmc.2007.11.075 . ПМИД 18083524 .
- ^ Линь CC, Чен Ю.П., Ян В.З., Шен Дж.К., Юань Х.С. (апрель 2020 г.). «Структурные данные о CpG-специфическом метилировании ДНК ДНК-метилтрансферазой 3B человека» . Исследования нуклеиновых кислот . 48 (7): 3949–3961. дои : 10.1093/nar/gkaa111 . ПМК 7144912 . ПМИД 32083663 .