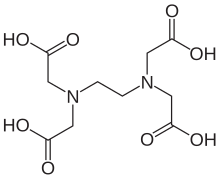
Этилендиаминтетрауксусная кислота
 | |
| Имена | |
|---|---|
| Название ИЮПАК N , N '-(Этан-1,2-диил)бис[ N- (карбоксиметил)глицин] [1] | |
| Систематическое название ИЮПАК 2,2',2'',2'''-(Этан-1,2-диилдинитрил)тетрауксусная кислота [1] | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol ) | |
| Сокращения | ЭДТА, H 4 ЭДТА |
| 1716295 | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.000.409 |
| Номер ЕС |
|
| 144943 | |
| КЕГГ | |
| МеШ | Эдетик+кислота |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ |
|
| Число | 3077 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 10 Н 16 Н 2 О 8 | |
| Молярная масса | 292.244 g·mol −1 |
| Появление | Бесцветные кристаллы |
| Плотность | 0,860 г см −3 (при 20 °С) |
| войти P | −0.836 |
| Кислотность ( pKa ) | 2.0, 2.7, 6.16, 10.26 [2] |
| Термохимия | |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | от -1765,4 до -1758,0 кДж моль −1 |
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | от -4461,7 до -4454,5 кДж моль −1 |
| Фармакология | |
| S01XA05 ( ВОЗ ) V03AB03 ( ВОЗ ) (соль) | |
| |
| Опасности | |
| СГС Маркировка : | |
 | |
| Предупреждение | |
| H319 | |
| П305+П351+П338 | |
| NFPA 704 (огненный алмаз) | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | 1000 мг/кг (перорально, крыса) [3] |
| Родственные соединения | |
Родственные алкановые кислоты | |
Родственные соединения | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Этилендиаминтетрауксусная кислота ( ЭДТА ), также называемая кислотой ЭДТА по собственному сокращению, представляет собой аминополикарбоновую кислоту с формулой [CH 2 N(CH 2 CO 2 H) 2 ] 2 . Это белое, нерастворимое в воде твердое вещество широко используется для связывания железа (Fe 2+ /Фе 3+ ) и ионы кальция (Ca 2+ ), образуя водорастворимые комплексы даже при нейтральном pH. Таким образом, его используют для растворения отложений, содержащих Fe и Ca, а также для доставки ионов железа в условиях, когда его оксиды нерастворимы. ЭДТА доступна в виде нескольких солей, в частности динатриевой ЭДТА , эдетата натрия и кальция и тетранатриевой ЭДТА , но все они действуют одинаково. [4]
Использование
[ редактировать ]Текстиль и бумага
[ редактировать ]В промышленности ЭДТА в основном используется для связывания (связывания или удержания) ионов металлов в водных растворах. В текстильной промышленности он предотвращает изменение цвета окрашенных изделий примесями ионов металлов. В целлюлозно-бумажной промышленности ЭДТА ингибирует способность ионов металлов, особенно Mn 2+ , катализируя диспропорционирование перекиси водорода , которая используется при отбеливании без хлора .
Еда
[ редактировать ]Аналогичным образом ЭДТА добавляют в некоторые продукты питания в качестве консерванта или стабилизатора для предотвращения каталитического окислительного обесцвечивания, которое катализируется ионами металлов. [5]
Смягчитель воды
[ редактировать ]Снижение жесткости воды в прачечных и растворение накипи в котлах зависят от ЭДТА и родственных комплексообразователей, связывающих Ca. 2+ , мг 2+ , а также ионы других металлов. Будучи связанными с ЭДТА, эти комплексы металлов с меньшей вероятностью образуют осадок или мешают действию мыла и моющих средств . [ нужна ссылка ] По тем же причинам чистящие растворы часто содержат ЭДТА. Подобным же образом ЭДТА используется в цементной промышленности для определения свободной извести и свободной магнезии в цементе и клинкерах . [6] [ нужна страница ]
Солюбилизация Fe 3+ близким к нейтральному или ниже, ионов с pH, можно получить с помощью ЭДТА. Это свойство полезно в сельском хозяйстве, включая гидропонику. Однако, учитывая зависимость образования лигандов от pH, ЭДТА не способствует улучшению растворимости железа в почвах выше нейтральной концентрации. [7] В противном случае, при pH, близком к нейтральному и выше, железо(III) образует нерастворимые соли, которые менее биодоступны для восприимчивых видов растений.
Чистка
[ редактировать ]Водный [Fe(ЭДТА)] − используется для удаления (« очистки ») сероводорода из газовых потоков. Это преобразование достигается путем окисления сероводорода до элементарной серы, которая нелетучая:
В этом применении центр железа(III) восстанавливается до его производного железа(II), которое затем может быть повторно окислено воздухом. Аналогичным образом оксиды азота удаляются из газовых потоков с помощью [Fe(EDTA)]. 2− .
Окислительные свойства [Fe(EDTA)] − также используются в фотографии , где его используют для растворения серебра . частиц [4]
Ионообменная хроматография
[ редактировать ]ЭДТА использовалась для разделения металлов-лантанидов с помощью ионообменной хроматографии . Усовершенствовано F.H. Spedding et al . в 1954 году метод основан на постоянном увеличении константы устойчивости комплексов лантаноидов с ЭДТА с атомным номером . [8] Использование гранул сульфированного полистирола и меди. 2+ в качестве удерживающего иона ЭДТА заставляет лантаноиды мигрировать вниз по столбцу смолы, разделяясь на полосы чистых лантаноидов. Лантаниды элюируются в порядке убывания атомного номера. Из-за дороговизны этого метода по сравнению с противоточной экстракцией растворителем ионный обмен теперь используется только для получения лантаноидов наивысшей чистоты (обычно более 99,99%). [ нужна ссылка ]
Лекарство
[ редактировать ]Эдетат натрия и кальция , производное ЭДТА, используется для связывания ионов металлов в практике хелатной терапии , например, при лечении отравлений ртутью и свинцом . [9] Аналогичным образом его используют для удаления избытка железа из организма. Эта терапия используется для лечения осложнений повторных переливаний крови , как и при лечении талассемии .
Стоматология
[ редактировать ]Стоматологи и эндодонтисты используют растворы ЭДТА для удаления неорганического мусора ( смазанного слоя ) и смазки корневых каналов в эндодонтии. Эта процедура помогает подготовить корневые каналы к обтурации . Кроме того, растворы ЭДТА с добавлением поверхностно-активного вещества разрыхляют кальцификаты внутри корневого канала, позволяют использовать инструменты (придавать форму каналу) и облегчают апикальное продвижение файла в плотном или кальцинированном корневом канале по направлению к апексу.
Глазные капли
[ редактировать ]Он служит консервантом ( обычно для усиления действия другого консерванта, такого как бензалкония хлорид или тиомерсал ) в глазных препаратах и глазных каплях .
Анализ
[ редактировать ]В медицинской диагностике и тестах функции органов (здесь, тест функции почек ) комплекс хрома (III) [Cr (ЭДТА)] − (как радиоактивный хром-51 ( 51 Кр)) вводят внутривенно его фильтрацию в мочу и контролируют . Этот метод полезен для оценки скорости клубочковой фильтрации (СКФ) в ядерной медицине . [10]
ЭДТА широко используется при анализе крови. Это антикоагулянт для образцов крови для ОАК/ОКК , где ЭДТА хелатирует кальций, присутствующий в образце крови, останавливая процесс коагуляции и сохраняя морфологию клеток крови. [11] Пробирки, содержащие ЭДТА, помечены лавандовым (фиолетовым) или розовым верхом. [12] ЭДТА также содержится в пробирках с коричневой крышкой для тестирования на свинец и может использоваться в пробирках с королевской синей крышкой для тестирования следов металлов. [12]
ЭДТА является диспергатором слизи, и было обнаружено, что он очень эффективен в снижении роста бактерий во время имплантации интраокулярных линз (ИОЛ). [13]
Альтернативная медицина
[ редактировать ]Некоторые практикующие альтернативные врачи считают, что ЭДТА действует как антиоксидант , предотвращая свободными радикалами повреждение стенок кровеносных сосудов , тем самым уменьшая атеросклероз . [14] Эти идеи не подтверждены научными исследованиями и, похоже, противоречат некоторым общепринятым принципам. [15] FDA США не одобрило его для лечения атеросклероза. [16]
Косметика
[ редактировать ]В шампунях , чистящих средствах и других средствах личной гигиены соли ЭДТА используются в качестве связывающего агента для улучшения их стабильности на воздухе. [17]
Лабораторные приложения
[ редактировать ]В лаборатории ЭДТА широко используется для удаления ионов металлов: в биохимии и молекулярной биологии истощение ионов обычно используется для дезактивации металлозависимых ферментов либо в качестве анализа их реактивности, либо для подавления повреждения ДНК , белков и полисахаридов . [18] ЭДТА также действует как селективный ингибитор ферментов, гидролизующих dNTP ( Taq-полимераза , dUTPase , MutT), [19] печени аргиназа [20] и пероксидаза хрена [21] независимо от хелатирования ионов металлов . Эти результаты требуют переосмысления использования ЭДТА в качестве биохимически неактивного поглотителя ионов металлов в ферментативных экспериментах. В аналитической химии ЭДТА используется при комплексометрическом титровании и анализе жесткости воды или в качестве маскирующего агента для связывания ионов металлов, которые могут мешать анализу.
ЭДТА находит множество специализированных применений в биомедицинских лабораториях, например, в ветеринарной офтальмологии в качестве антиколлагеназы для предотвращения обострения язв роговицы у животных . В культуре тканей ЭДТА используется в качестве хелатирующего агента, который связывается с кальцием и предотвращает соединение кадгеринов между клетками, предотвращая слипание клеток, выращенных в жидкой суспензии, или отделение прилипших клеток для пассирования . В гистопатологии ЭДТА можно использовать в качестве декальцифицирующего агента, что позволяет делать срезы с помощью микротома после деминерализации образца ткани.
Также известно, что ЭДТА ингибирует ряд металлопептидаз . Этот метод ингибирования происходит посредством хелатирования иона металла, необходимого для каталитической активности. [22] ЭДТА также можно использовать для проверки биодоступности тяжелых металлов в отложениях . Однако он может влиять на биодоступность металлов в растворе, что может вызывать опасения относительно его воздействия на окружающую среду, особенно с учетом его широкого использования и применения.
ЭДТА также используется для удаления остатков коррозии (корродированных металлов) из топливных стержней ядерных реакторов. [23]
Побочные эффекты
[ редактировать ]ЭДТА проявляет низкую острую токсичность: LD 50 (крыса) от 2,0 г/кг до 2,2 г/кг. [4] У лабораторных животных было обнаружено, что он обладает как цитотоксичностью , так и слабо генотоксичностью . Было отмечено, что пероральное воздействие оказывает воздействие на репродуктивную функцию и развитие. [17] То же исследование [17] также обнаружили, что как воздействие ЭДТА на кожу в большинстве косметических составов, так и воздействие ЭДТА при вдыхании в аэрозольных косметических составах приводит к уровням воздействия ниже тех, которые считаются токсичными в исследованиях перорального дозирования.
Синтез
[ редактировать ]Соединение было впервые описано в 1935 году Фердинандом Мюнцем . [24] который получил соединение из этилендиамина и хлоруксусной кислоты . [25] Сегодня ЭДТА в основном синтезируют из этилендиамина (1,2-диаминоэтана), формальдегида и цианида натрия . [26] Этот путь дает тетранатрий ЭДТА, который на последующем этапе превращается в кислотные формы:
- H 2 NCH 2 CH 2 NH 2 + 4 CH 2 O + 4 NaCN + 4 H 2 O → (NaO 2 CCH 2 ) 2 NCH 2 CH 2 N(CH 2 CO 2 Na) 2 + 4 NH 3
- (NaO 2 CCH 2 ) 2 NCH 2 CH 2 N(CH 2 CO 2 Na) 2 + 4 HCl → (HO 2 CCH 2 ) 2 NCH 2 CH 2 N(CH 2 CO 2 H) 2 + 4 NaCl
Этот процесс используется для производства около 80 000 тонн ЭДТА каждый год. Примеси, образующиеся таким путем, включают глицин и нитрилотриуксусную кислоту ; они возникают в результате реакций побочного продукта аммиака . [4]
Номенклатура
[ редактировать ]Чтобы описать ЭДТА и ее различные протонированные формы , химики различают ЭДТА. 4− , сопряженное основание , которое является лигандом , и H 4 EDTA, предшественник этого лиганда. При очень низком pH (очень кислая среда) полностью протонированная H 6 EDTA 2+ преобладает форма, тогда как при очень высоком pH или очень щелочном состоянии полностью депротонированная ЭДТА 4− форма преобладает. В этой статье термин ЭДТА используется для обозначения H 4− x EDTA. х - , тогда как в его комплексах ЭДТА 4− обозначает тетраанионный лиганд.
Принципы координационной химии
[ редактировать ]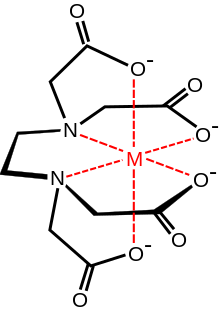

В координационной химии ЭДТА 4− является членом аминополикарбоновых кислот семейства лигандов . ЭДТА 4− обычно связывается с катионом металла через два амина и четыре карбоксилата, т. е. представляет собой гексадентатный («шестизубый») хелатирующий агент . Многие из полученных координационных соединений принимают октаэдрическую геометрию . Хотя эти октаэдрические комплексы не имеют большого значения для приложений, они являются хиральными . Анион кобальта (III) [Co(EDTA)] − был разделен на энантиомеры . [28] Многие комплексы ЭДТА 4− принимают более сложные структуры за счет либо образования дополнительной связи с водой, т. е. семикоординированных комплексов, либо замещения водой одного карбоксилатного плеча. Комплекс железа(III) ЭДТА семикоординированный. [29] Ранние работы по разработке ЭДТА были предприняты Герольдом Шварценбахом в 1940-х годах. [30] ЭДТА образует особенно прочные комплексы с Mn(II) , Cu(II) , Fe(III), Pb(II) и Co(III). [31] [ нужна страница ]
Некоторые особенности комплексов ЭДТА имеют отношение к его применению. Во-первых, из-за своей высокой дентатности этот лиганд обладает высоким сродством к катионам металлов:
- [Fe(H 2 O) 6 ] 3+ + H 4 ЭДТА ⇌ [Fe(ЭДТА)] − + 6 Н 2 О + 4 Н + К экв = 10 25.1
Записанный таким образом равновесный коэффициент показывает, что ионы металлов конкурируют с протонами за связывание с ЭДТА. Поскольку ионы металлов сильно окружены ЭДТА, их каталитические свойства часто подавляются. Наконец, поскольку комплексы ЭДТА 4− анионные . , они имеют тенденцию хорошо растворяться в воде По этой причине ЭДТА способна растворять отложения оксидов и карбонатов металлов .
p депротонирование K a Значения свободной ЭДТА составляют 0, 1,5, 2, 2,66 ( ) четырех карбоксильных групп и 6,16, 10,24 (депротонирование двух аминогрупп ). [32]
Экологические проблемы
[ редактировать ]Абиотическая деградация
[ редактировать ]ЭДТА настолько широко используется, что возникают вопросы, является ли она стойким органическим загрязнителем . Хотя ЭДТА выполняет множество положительных функций в различных отраслях промышленности, фармацевтики и других сферах, долговечность ЭДТА может создать серьезные проблемы для окружающей среды. Разложение ЭДТА происходит медленно. В основном это происходит абиотически в присутствии солнечного света. [33]
Наиболее важным процессом удаления ЭДТА из поверхностных вод является прямой фотолиз при длинах волн ниже 400 нм. [34] В зависимости от условий освещения период полураспада ЭДТА железа (III) при фотолизе в поверхностных водах может варьироваться от 11,3 минут до более 100 часов. [35] Разложение FeEDTA, но не самой ЭДТА, приводит к образованию комплексов железа триацетата (ED3A), диацетата (EDDA) и моноацетата (EDMA) – 92% EDDA и EDMA биоразлагаются в течение 20 часов, в то время как ED3A проявляет значительно более высокую устойчивость. Многие распространенные в окружающей среде виды ЭДТА (например, Mg 2+ и Ca 2+ ) более настойчивы.
Биодеградация
[ редактировать ]На многих очистных сооружениях промышленных сточных вод удаление ЭДТА может быть достигнуто примерно на 80% с помощью микроорганизмов . [36] Побочными продуктами являются ED3A и иминодиуксусная кислота (IDA), что позволяет предположить, что атаке подверглись как основная цепь, так и ацетильные группы. Обнаружено даже, что некоторые микроорганизмы образуют нитраты из ЭДТА, но оптимально они функционируют в умеренно-щелочных условиях с pH 9,0–9,5. [37]
Несколько бактериальных штаммов, выделенных на очистных сооружениях, эффективно разлагают ЭДТА. Конкретные штаммы включают Agrobacterium radiobacter ATCC 55002. [38] и ответвления Pseudomonadota, такие как BNC1, BNC2, [39] и штамм DSM 9103. [40] Эти три штамма имеют схожие свойства аэробного дыхания и классифицируются как грамотрицательные бактерии . В отличие от фотолиза, хелатные формы не ограничиваются железом (III) и подлежат разложению. Скорее, каждый штамм уникальным образом потребляет различные комплексы металл-ЭДТА посредством нескольких ферментативных путей. Agrobacterium radiobacter разлагает только Fe(III) ЭДТА. [39] в то время как BNC1 и DSM 9103 не способны разлагать ЭДТА железа(III) и больше подходят для комплексов кальция , бария , магния и марганца(II) . [41] Комплексы ЭДТА перед деградацией требуют диссоциации.
Альтернативы ЭДТА
[ редактировать ]Интерес к экологической безопасности вызвал обеспокоенность по поводу биоразлагаемости аминополикарбоксилатов, таких как ЭДТА. Эти опасения стимулируют исследование альтернативных аминополикарбоксилатов. [33] Кандидаты в хелатирующие агенты включают нитрилотриуксусную кислоту (NTA), иминодиянтарную кислоту (IDS), полиаспарагиновую кислоту , S,S -этилендиамин- N , N' -диянтарную кислоту (EDDS) , метилглициндиуксусную кислоту (MGDA) и L -глутаминовую кислоту N , N. -диуксусная кислота, тетранатриевая соль (GLDA). [42]
Иминодиянтарная кислота (ИДС)
[ редактировать ]Коммерчески используемая с 1998 года иминодиянтарная кислота (ИДС) биоразлагается примерно на 80% всего за 7 дней. IDS исключительно хорошо связывается с кальцием и образует стабильные соединения с ионами других тяжелых металлов. Помимо более низкой токсичности после хелатирования, IDS разлагается Agrobacterium tumefaciens (BY6), сбор которых можно производить в больших масштабах. Участвующие ферменты, IDS-эпимераза и C-N -лиаза , не требуют каких-либо кофакторов . [43]
Полиаспарагиновая кислота
[ редактировать ]Полиаспарагиновая кислота , как и IDS, связывается с ионами кальция и других тяжелых металлов. Он имеет множество практических применений, включая ингибиторы коррозии, добавки для сточных вод и сельскохозяйственные полимеры. на основе полиаспарагиновой кислоты Стиральный порошок стал первым стиральным порошком в мире, получившим цветочный экологический знак ЕС . [44] Способность полиаспарагиновой кислоты связывать кальций использовалась для доставки наноносителей с лекарственными препаратами в кости. [45] Приготовление гидрогелей на основе полиаспарагиновой кислоты в различных физических формах, от волокон до частиц , потенциально может обеспечить легкое отделение хелатных ионов из раствора. [46] Таким образом, несмотря на то, что полиаспарагиновая кислота слабее ЭДТА, ее все же можно рассматривать как жизнеспособную альтернативу благодаря этим особенностям, а также биосовместимости и биоразлагаемости . [47]
S , S -Этилендиамин- N , N' -диянтарная кислота (ЭДДС)
[ редактировать ]Структурный изомер ЭДТА, этилендиамин- N , N' -диянтарная кислота (ЭДДС), легко биоразлагается с высокой скоростью в своей S , S -форме. [48]
Метилглициндиуксусная кислота (МГДА)
[ редактировать ]Дикарбоксиметилаланинат тринатрия , также известный как метилглициндиуксусная кислота (MGDA), имеет высокую скорость биоразложения - более 68%, но в отличие от многих других хелатирующих агентов может разлагаться без помощи адаптированных бактерий. Кроме того, в отличие от EDDS или IDS, MGDA может выдерживать более высокие температуры, сохраняя при этом высокую стабильность, а также во всем диапазоне pH. [ нужна ссылка ] Было показано, что MGDA является эффективным хелатирующим агентом со способностью к мобилизации, сравнимой со способностью нитрилотриуксусной кислоты (НТК), при внесении в воду для промышленного использования и для удаления оксалата кальция из мочи у пациентов с камнями в почках . [49]
Методы обнаружения и анализа
[ редактировать ]Наиболее чувствительным методом обнаружения и измерения ЭДТА в биологических образцах является выбранный метод мониторинга реакций капиллярного электрофореза, масс-спектрометрии (SRM-CE/MS), который имеет предел обнаружения 7,3 нг/мл в плазме человека и предел количественного определения 15 нг/мл. . [50] Этот метод работает с объемами образцов всего 7–8 нл. [50]
ЭДТА также измерялась в безалкогольных напитках с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) на уровне 2,0 мкг/мл. [51] [52]
В популярной культуре
[ редактировать ]В фильме «Блэйд» (1998) ЭДТА используется в качестве оружия для убийства вампиров и взрывается при контакте с кровью вампира. [53]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Номенклатура органической химии: рекомендации ИЮПАК и предпочтительные названия 2013 г. (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 79, 123, 586, 754. ISBN. 978-0-85404-182-4 .
- ^ Раафлауб, Юрг (1956). «Применение металлических буферов и металлических индикаторов в биохимии» . Методы биохимического анализа . Том. 3. С. 301–325. дои : 10.1002/9780470110195.ch10 . ISBN 978-0-470-30492-1 . ПМИД 13369167 .
- ^ Название вещества: Эдетат натрия и кальция . NIH.gov
- ^ Перейти обратно: а б с д Харт, Дж. Роджер (2005). «Этилендиаминтетрауксусная кислота и родственные хелатирующие агенты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a10_095 . ISBN 978-3527306732 .
- ^ Фурия, Т. (1964). «ЭДТА в пищевых продуктах – технический обзор». Пищевая технология . 18 (12): 1874–1882.
- ^ Тейлор, HFW (1990). Цементная химия . Академическая пресса. ISBN 978-0-12-683900-5 .
- ^ Норвелл, Вашингтон; Линдси, WL (1969). «Взаимодействие комплексов ЭДТА железа, цинка, марганца и меди с почвами». Журнал Американского общества почвоведения . 33 (1): 86. Бибкод : 1969SSASJ..33...86N . дои : 10.2136/sssaj1969.03615995003300010024x .
- ^ Пауэлл, Дж. Э.; Спеддинг, FH (1956). Основные принципы макроотделения соседних редкоземельных элементов друг от друга посредством ионного обмена (Технический отчет). Государственный колледж Айовы. дои : 10.2172/4289324 . ОСТИ 4289324 . S2CID 93195586 .
- ^ ДеБаск, Рут; и др. (2002). «Этилендиаминтетрауксусная кислота (ЭДТА)» . Медицинский центр Университета Мэриленда. Архивировано из оригинала 4 мая 2007 г.
- ^ Спать, нет; Берг, Улла Б.; Бьорк, Йонас; Элиндер, Карл-Густав; Грабб, Андерс; Меджаре, Ингегерд; Штернер, Гуннар; Бек, Стен-Эрик (сентябрь 2014 г.). «Измерение СКФ: систематический обзор». Американский журнал заболеваний почек . 64 (3): 411–424. дои : 10.1053/j.ajkd.2014.04.010 . ПМИД 24840668 .
- ^ Банфи, Г; Сальваньо, Г.Л; Липпи, Дж. (2007). «Роль этилендиаминтетрауксусной кислоты (ЭДТА) как антикоагулянта in vitro в диагностических целях». Клиническая химия и лабораторная медицина . 45 (5): 565–76. дои : 10.1515/CCLM.2007.110 . ПМИД 17484616 . S2CID 23824484 .
- ^ Перейти обратно: а б «Порядок розыгрыша нескольких коллекций тюбиков» (PDF) . Мичиганские медицинские лаборатории. 15 сентября 2019 г. Архивировано из оригинала (PDF) 26 ноября 2019 г. Проверено 27 марта 2020 г.
- ^ Кадрый, А.А.; Фуда, С.И.; Шибл, AM; Абу Эль-Асрар, А.А. (2009). «Влияние диспергаторов слизи и антиадгезивов на образование in vitro биопленок Staphylococcus epidermidis на интраокулярных линзах и на активность антибиотиков». Журнал антимикробной химиотерапии . 63 (3): 480–4. дои : 10.1093/jac/dkn533 . ПМИД 19147522 .
- ^ Сили, ДМ; Ву, П.; Миллс, Э.Дж. (2005). «Хелаторная терапия ЭДТА при сердечно-сосудистых заболеваниях: систематический обзор» . Кардиоваскулярное расстройство BMC . 5 (32): 480–484. дои : 10.1186/1471-2261-5-32 . ПМЦ 1282574 . ПМИД 19147522 .
- ^ Грин, Сол; Сэмпсон, Уоллес (14 декабря 2002 г.). «Хелаторная терапия ЭДТА при атеросклерозе и дегенеративных заболеваниях: неправдоподобность и парадоксальные окислительные эффекты» . Шарлатанство . Проверено 16 декабря 2009 г.
- ^ «Постмаркетинговая информация о безопасности лекарств для пациентов и поставщиков медицинских услуг – вопросы и ответы по динатрию эдетату (продаваемому как эндрат и дженерики)» . Управление по контролю за продуктами и лекарствами США .
- ^ Перейти обратно: а б с Ланиган, РС; Ямарик, Т.А. (2002). «Заключительный отчет об оценке безопасности ЭДТА, динатрия ЭДТА кальция, диаммония ЭДТА, двухкалия ЭДТА, динатрия ЭДТА, ЧАЙ-ЭДТА, тетранатрия ЭДТА, трикалия ЭДТА, тринатрия ЭДТА, ГЭДТА и тринатрия ЭДТА». Международный журнал токсикологии . 21 Доп. 2 (5): 95–142. дои : 10.1080/10915810290096522 . ПМИД 12396676 . S2CID 83388249 .
- ^ Домингес, К.; Уорд, штат Вашингтон (декабрь 2009 г.). «Новая нуклеазная активность, активируемая Ca 2+ хелатируется с EGTA» . Системная биология в репродуктивной медицине . 55 (5–6): 193–199. : 10.3109 /19396360903234052 . PMC 2865586. . PMID 19938954 doi
- ^ Лопата, Анна; Добро пожаловать, Балаж; Сурани, Ева В.; Такач, Энико; Безур, Ласло; Лиственный, Фиолетовый; Бендес, Абрис А; Вискольч, Бела; Вертесси, Беата Г.; Тот, Юдит (октябрь 2019 г.). «Помимо хелатирования: ЭДТА прочно связывает ДНК-полимеразу Taq, MutT и dUTPase и напрямую ингибирует активность dNTPase» . Биомолекулы . 9 (10): 621. дои : 10.3390/biom9100621 . ПМК 6843921 . ПМИД 31627475 .
- ^ Карвахаль, Нельсон; Орельяна, Мария С; Боркес, Джессика; Урибе, Елена; Лопес, Вашти; Салас, Моника (1 августа 2004 г.). «Нехелатирующее ингибирование варианта H101N аргиназы печени человека с помощью ЭДТА». Журнал неорганической биохимии . 98 (8): 1465–1469. дои : 10.1016/j.jinorgbio.2004.05.005 . ISSN 0162-0134 . ПМИД 15271525 .
- ^ Бхаттачарья, ДК; Адак, С; Бандиопадхьяй, У; Банерджи, РК (1 марта 1994 г.). «Механизм ингибирования окисления йодида, катализируемого пероксидазой хрена, ЭДТА» . Биохимический журнал . 298 (Часть 2): 281–288. дои : 10.1042/bj2980281 . ISSN 0264-6021 . ПМЦ 1137937 . ПМИД 8135732 .
- ^ Олд, Д.С. (1995). «Удаление и замена ионов металлов в металлопептидазах». Протеолитические ферменты: аспарагиновая и металлопептидазы . Методы энзимологии. Том. 248. С. 228–242. дои : 10.1016/0076-6879(95)48016-1 . ISBN 978-0-12-182149-4 . ПМИД 7674923 .
- ^ Чоппин, Грегори; Лильензин, Ян-Олов; Ридберг, Ян; Экберг, Кристиан (2013). «Глава 20 – Атомные энергетические реакторы» . Радиохимия и ядерная химия (Четвертое изд.): 655–684. дои : 10.1016/B978-0-12-405897-2.00020-3 . ISBN 978-0-12-405897-2 .
- ^ Паольери, Маттео (декабрь 2017 г.). «Фердинанд Мюнц: ЭДТА и 40 лет изобретений» . Бык. Хист. Хим . 42 (2). ОКС: 133–140.
- ^ США 2130505 , Мюнц, Фердинанд , «Полиаминокарбоновые кислоты и способ их получения», опубликован 20 сентября 1938 г., передан компании General Aniline Works Ltd. Также DE 718981 , Мюнц, Фердинанд , «Процесс обезвреживания компонентов жесткости воды», опубликован 20 сентября 1938 г., передан IG Farbenindustrie.
- ^ «Промышленный синтез ЭДТА» . Бристольский университет.
- ^ Соланс, X.; Фонт Альтаба, М.; Гарсиа Орикаин, Дж. (1984). «Кристаллические структуры этилендиаминтетраацетатных комплексов металлов. V. Структуры, содержащие [Fe(C 10 H 12 N 2 O 8 )(H 2 O)]». − Анион». Acta Crystallographica Раздел C. 40 ( 4): 635–638. doi : 10.1107/S0108270184005151 .
- ^ Киршнер, С.; Дьярфас, Элеонора К. (1957). «Барий (Этилендиаминтетраацетат)кобальтат(III) 4-гидрат». Неорганические синтезы . Том. 5. С. 186–188. дои : 10.1002/9780470132364.ch52 . ISBN 978-0-470-13236-4 .
- ^ Лопес Алькала, JM; Пуэрта Вискайно, MC; Гонсалес Вильчес, Ф.; Дюслер, EN; Тапскотт, Р. Э. (1984). «Повторное определение дигидрата аква[этилендиаминтетраацетато(4-)]феррата(III) натрия, Na[Fe(C 10 H 12 N 2 O 8 )(H 2 O)] · 2H 2 O». Акта Кристаллогр C. 40 (6): 939–941. дои : 10.1107/S0108270184006338 .
- ^ Синекс, Скотт А. «ЭДТА – молекула со сложной историей» . Бристольский университет.
- ^ Холлеман, А.Ф.; Виберг, Э. (2001). Неорганическая химия . Сан-Диего: Академическая пресса. ISBN 978-0-12-352651-9 .
- ^ Ганс Петер Лача: Аналитическая химия. Спрингер Верлаг, 2013, ISBN 978-3-642-18493-2 , с. 303.
- ^ Перейти обратно: а б Бучели-Витчел, М.; Эгли, Т. (2001), «DAB: Экологическая судьба и микробная деградация аминополикарбоновых кислот», FEMS Microbiology Reviews , 25 (1): 69–106, doi : 10.1111/j.1574-6976.2001.tb00572.x , PMID 11152941
- ^ Кари, Ф.Г. (1994). Поведение этилендиаминтетраацетата (ЭДТА) в окружающей среде с особым учетом фотохимического разложения (доктор философии). Швейцарский федеральный технологический институт.
- ^ Франк, Р.; Рау, Х. (1989). «Фотохимическая трансформация в водном растворе и возможная судьба этилендиаминтетрауксусной кислоты (ЭДТА) в окружающей среде». Экотоксикология и экологическая безопасность . 19 (1): 55–63. дои : 10.1016/0147-6513(90)90078-j . ПМИД 2107071 .
- ^ Калуза, У.; Клингельхофер, П.; К., Тагер (1998). «Микробная деградация ЭДТА на очистных сооружениях промышленных сточных вод». Исследования воды . 32 (9): 2843–2845. дои : 10.1016/S0043-1354(98)00048-7 .
- ^ ВанГинкель, CG; Ванденбрук, КЛ; Калифорния, Тру (1997). «Биологическое удаление ЭДТА на обычных установках с активным илом, работающих в щелочных условиях». Биоресурсные технологии . 32 (2–3): 2843–2845. дои : 10.1016/S0960-8524(96)00158-7 .
- ^ Лауфф, Джей-Джей; Стил, Д.Б.; Куган, Луизиана; Брейтфеллер, Дж. М. (1990). «Разложение хелата железа ЭДТА чистой культурой Agrobacterium sp» . Прикладная и экологическая микробиология . 56 (11): 3346–3353. Бибкод : 1990ApEnM..56.3346L . дои : 10.1128/АЕМ.56.11.3346-3353.1990 . ПМК 184952 . ПМИД 16348340 .
- ^ Перейти обратно: а б Нортеманн, Б (1992). «Полная деградация ЭДТА смешанными культурами и бактериальным изолятом» . Прикладная и экологическая микробиология . 58 (2): 671–676. Бибкод : 1992ApEnM..58..671N . дои : 10.1128/АЕМ.58.2.671-676.1992 . ЧВК 195300 . ПМИД 16348653 .
- ^ Витшель, М.; Вейлеманн, Х.-У.; Эгли, Т. (1995). Разложение ЭДТА бактериальным изолятом. Плакат, представленный на 45-м ежегодном собрании Швейцарского общества микробиологии (выступление). Лугано, Швейцария.
- ^ Хеннекенл, Л.; Нортеманн, Б.; Хемпель, округ Колумбия (1995). «Влияние физиологических условий на деградацию ЭДТА». Прикладная и экологическая микробиология . 44 (1–2): 190–197. дои : 10.1007/bf00164501 . S2CID 30072817 .
- ^ Тэнди, Сьюзен; Боссарт, Карин; Мюллер, Роланд; Ритшель, Йенс; Хаузер, Лукас; Шулин, Райнер; Новак, Бернд (2004). «Извлечение тяжелых металлов из почв с использованием биоразлагаемых хелатирующих агентов». Экологические науки и технологии . 38 (3): 937–944. Бибкод : 2004EnST...38..937T . дои : 10.1021/es0348750 . ПМИД 14968886 .
- ^ Кокеса, З.; Накмусс, Х.; Ригер, П. (2004), «Биодеградация всех стереоизомеров иминодисукцината-заменителя ЭДТА с помощью Agrobacterium Tumefaciens BY6 требует эпимеразы и стереоселективной C-N-лиазы», Applied and Environmental Microbiology , 70 (7): 3941–3947, Bibcode : 2004ApEnM..70.3941C , doi : 10.1128/aem.70.7.3941-3947.2004 , PMC 444814 , PMID 15240267
- ^ Томас Кляйн; Ральф-Иоганн Мориц; Рене Граупнер (2008). «Полиаспартаты и полисукцинимиды». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.l21_l01 . ISBN 978-3527306732 .
- ^ Адельния, Оссейн; Тран, Хуонг Д.Н.; Литтл, Питер Дж.; Блейки, Идрисс; Та, Ханг Т. (14 июня 2021 г.). «Поли(аспарагиновая кислота) в биомедицинских применениях: от полимеризации, модификации, свойств, деградации и биосовместимости к применению». ACS Биоматериалы, наука и инженерия . 7 (6): 2083–2105. doi : 10.1021/acsbimaterials.1c00150 . hdl : 10072/404497 . ПМИД 33797239 . S2CID 232761877 .
- ^ Адельния, Оссейн; Блейки, Идрисс; Литтл, Питер Дж.; Та, Ханг Т. (2019). «Гидрогели на основе полиаспарагиновой кислоты: синтез и применение» . Границы в химии . 7 : 755. Бибкод : 2019FrCh....7..755A . дои : 10.3389/fchem.2019.00755 . ISSN 2296-2646 . ПМК 6861526 . ПМИД 31799235 .
- ^ Хэссон, Дэвид; Шемер, Хилла; Шер, Александр (15 июня 2011 г.). «Современное состояние дружественных «зеленых» ингибиторов контроля накипи: обзорная статья». Исследования в области промышленной и инженерной химии . 50 (12): 7601–7607. дои : 10.1021/ie200370v . ISSN 0888-5885 .
- ^ Тэнди, С.; Амманн, А.; Щулин Р. ; Новак, Б. (2006). «Биодеградация и видообразование остаточной SS-этилендиаминдиянтарной кислоты (ЭДДС) в почвенном растворе, оставшемся после промывки почвы». Загрязнение окружающей среды . 142 (2): 191–199. дои : 10.1016/j.envpol.2005.10.013 . ПМИД 16338042 .
- ^ Бретти, Клементе; Чигала, Розалия Мария; Де Стефано, Кончетта; Ландо, Габриэле; Саммартано, Сильвио (2017). «Термодинамические свойства раствора биоразлагаемого хеланта (MGDA) и его взаимодействие с основными компонентами природных жидкостей». Жидкостно-фазовые равновесия . 434 : 63–73. дои : 10.1016/j.fluid.2016.11.027 .
- ^ Перейти обратно: а б Шеппард, РЛ; Хенион, Дж. (1997). «Рецензируемая книга: определение ЭДТА в крови». Аналитическая химия . 69 (15): 477А–480А. дои : 10.1021/ac971726p . ПМИД 9253241 .
- ^ Лойо-Лавничак, С.; Дуч, Дж.; Бера, П. (1999). «Оптимизация аналитического обнаружения ЭДТА методом ВЭЖХ в природных водах». Журнал аналитической химии Фрезениуса . 364 (8): 727. doi : 10.1007/s002160051422 . S2CID 95648833 .
- ^ Каньяссо, CE; Лопес, Л.Б.; Родригес, В.Г.; Валенсия, Мэн (2007). «Разработка и валидация метода определения ЭДТА в безалкогольных напитках методом ВЭЖХ». Журнал пищевого состава и анализа . 20 (3–4): 248. doi : 10.1016/j.jfca.2006.05.008 .
- ^ «Блэйд (1998)» . Интернет-база данных фильмов ( IMDb ) . Проверено 14 ноября 2022 г.
Внешние ссылки
[ редактировать ]- ЭДТА: Молекула месяца
- ЭДТА Определение общей жесткости воды
- Овьедо, Клаудия; Родригес, Хайме (2003). «ЭДТА: хелатирующий агент под пристальным вниманием окружающей среды» . Нова Химия . 26 (6): 901–905. дои : 10.1590/S0100-40422003000600020 .
