токсокароз
| токсокароз | |
|---|---|
| Специальность | Паразитология , инфекционные болезни |
| Симптомы | лихорадка , увеличение лимфатических узлов , кашель, бронхоспазм , свистящее дыхание , боли в животе, головные боли, одышка , нарушение зрения |
| Осложнения | дыхательная недостаточность , менингит , энцефалит , эпилептические припадки , миокардит , слепота |
| Причины | собачья аскарида ( Toxocara canis ), кошачья аскарида ( Toxocara cati ) |
| Метод диагностики | серологическое тестирование (общий IgE в сыворотке , ИФА для выявления специфических антитоксокарных IgE) |
| Дифференциальный диагноз | Baylisascaris procyonis , филяриоз |
| Профилактика | борьба с паразитами у домашних собак и кошек, правильная утилизация фекалий домашних животных, гигиена рук |
| Уход | противогельминтные препараты |
| Медикамент | альбендазол , диэтилкарбамазин |
Токсокароз — заболевание человека, вызываемое аскаридами собак ( Toxocara canis ) и, реже, аскаридами кошек ( Toxocara cati ). [1] Это наиболее распространенные кишечные круглые черви собак , койотов, волков и лисиц и домашних кошек соответственно. [2] Люди являются одними из многих «случайных» или паратенических хозяев этих круглых червей. [3]
Хотя эта зоонозная инфекция обычно протекает бессимптомно, она может вызвать тяжелое заболевание. Выделяют три различных синдрома токсокароза: скрытый токсокароз — относительно легкое заболевание, очень похожее на синдром Леффлера . Он характеризуется лихорадкой, эозинофилией , крапивницей , увеличением лимфатических узлов , кашлем, бронхоспазмом , свистящим дыханием , болью в животе, головными болями и/или гепатоспленомегалией . Висцеральная мигрирующая личинка (ВЛМ) — более тяжелая форма заболевания; Признаки и симптомы зависят от конкретной пораженной системы органов. Поражение легких может проявляться одышкой , интерстициальным заболеванием легких , плевральным выпотом и даже дыхательной недостаточностью . Поражение головного мозга может проявляться в виде менингита , энцефалита или эпилептических припадков . Поражение сердца может проявляться в виде миокардита . Ocular larva migrans (OLM) — третий синдром, проявляющийся увеитом , эндофтальмитом , нарушением зрения или даже слепотой на пораженном глазу. [4]
Признаки и симптомы
[ редактировать ]Физиологические реакции на инфекцию Toxocara зависят от иммунного ответа хозяина и паразитарной нагрузки. Большинство случаев заражения токсокарой протекает бессимптомно , особенно у взрослых. [4] [5] [6] Если симптомы действительно возникают, они являются результатом миграции личинок токсокар второй стадии по организму. [7]
Скрытый токсокароз
[ редактировать ]Скрытый токсокароз является наименее серьезным из трех синдромов и, как полагают, возникает в результате хронического воздействия. [8] Признаками и симптомами скрытого токсокароза являются кашель, лихорадка, боли в животе, головные боли, а также изменения в поведении и способности спать. [9] При медицинском осмотре свистящее дыхание, гепатомегалию , лимфаденит . часто отмечают [4]
Висцеральная мигрирующая личинка
[ редактировать ]Высокая паразитарная нагрузка или повторное заражение могут привести к мигрирующей висцеральной личинке (ВЛМ). [5] ВЛМ в первую очередь диагностируется у детей раннего возраста, поскольку они более склонны к воздействию и проглатыванию инфекционных яиц. [7] Инфекция токсокарой обычно проходит сама по себе в течение нескольких недель, но может привести к хронической эозинофилии . При ВЛМ миграция личинок вызывает воспаление внутренних органов, а иногда и центральной нервной системы. Симптомы зависят от пораженных органов. У детей могут отмечаться бледность, утомляемость, потеря веса, анорексия, лихорадка, головная боль, крапивница на коже, кашель, астма, стеснение в груди, повышенная раздражительность, боли в животе, тошнота и рвота. [7] Иногда можно увидеть следы подкожной миграции личинок. [7] У детей обычно диагностируют пневмонию , бронхоспазмы , хроническое воспаление легких , гиперэозинофилию , гепатомегалию , гипергаммаглобулинемию (классы IgM, IgG и IgE), лейкоцитоз и повышенный уровень изогемагглютининов анти-А и анти-В. [7] [10] [5] [9] Тяжелые случаи наблюдались у людей с повышенной чувствительностью к аллергенам; в редких случаях эпилепсия , воспаление сердца , плевральный выпот , дыхательная недостаточность и смерть. в результате ВЛМ развивались [4] [9]

Глазная мигрирующая личинка
[ редактировать ]Мигрирующая глазная личинка (OLM) встречается редко по сравнению с VLM. [7] [11] Считается, что небольшое количество токсокар вызывает слабый иммунный ответ, позволяя личинке проникнуть в глаз хозяина. [9] Хотя были случаи одновременного использования OLM и VLM, они являются исключительными. [9] ОЛМ часто возникает только в одном глазу и из-за единственной личинки, мигрирующей в орбиту и инцистирующей ее. [7] [12] Потеря зрения происходит в течение нескольких дней или недель. [9] Другими признаками и симптомами являются покраснение глаз, белый зрачок , фиксированный зрачок, фиброз сетчатки , отслоение сетчатки , воспаление тканей глаза, гранулемы сетчатки и косоглазие . [7] [9] [12] [13] Глазные гранулемы, возникающие в результате ОЛМ, часто ошибочно принимают за ретинобластому . [7] токсокарой является необратимым и может привести к слепоте. Поражение глаз [5] [12]
Другой
[ редактировать ]Часто встречаются кожные проявления, включая хроническую крапивницу, хронический зуд и различные формы экземы. [14] Исследование, опубликованное в 2008 году, подтвердило гипотезу о том, что эозинофильный целлюлит также может быть вызван инфекцией токсокарой : у взрослого пациента наблюдался эозинофильный целлюлит, гепатоспленомегалия , анемия и положительный результат ИФА на T. canis . [15]
Причина
[ редактировать ]Передача инфекции
[ редактировать ]Передача токсокары человеку обычно происходит при проглатывании инфекционных яиц. [5] [16] T. canis может откладывать около 200 000 яиц в день. [17] Эти яйца передаются с фекалиями кошек или собак, но привычка собак испражняться приводит к тому, что передача T. canis более распространена, чем передача T. cati . [7] [16] Яйца Toxocara canis и Toxocara cati требуют инкубационного периода в течение нескольких недель во влажной и влажной погоде вне хозяина, прежде чем они станут инфекционными, поэтому свежие яйца не могут вызвать токсокароз. [7] [16] [17]
Многие предметы и поверхности могут быть заражены инфекционными яйцами токсокар . Мухи, питающиеся фекалиями, могут разносить яйца токсокар на поверхности или продукты питания. [9] Маленькие дети, которые кладут загрязненные предметы в рот или едят грязь ( пика ), подвергаются риску развития симптомов. [7] [10] [9] Люди также могут загрязнять продукты питания, если не моют руки перед едой. [5]
Люди – не единственные случайные хозяева токсокар . [18] Употребление в пищу недоваренного кролика, курицы или овцы может привести к заражению; инцистированные личинки в мясе могут реактивироваться и мигрировать через человека-хозяина, вызывая токсокароз. [18] Особое внимание следует уделять тщательному приготовлению потрохов и печени во избежание передачи инфекции. [7] [9]
Период инкубации
[ редактировать ]Инкубационный период яиц Toxocara canis и cati зависит от температуры и влажности. [7] [16] В частности, самки T. canis способны производить до 200 000 яиц в день, и для полного развития до инфекционной стадии требуется минимум от 2–6 недель до пары месяцев. [19] В идеальных летних условиях яйца могут созреть до инфекционной стадии уже через две недели вне хозяина. [9] [16] При наличии достаточного количества кислорода и влаги яйца токсокар могут оставаться заразными в течение многих лет, поскольку их прочная внешняя оболочка обеспечивает защиту от большинства угроз окружающей среды. [20] [21] [22] Однако, как показано в тематическом исследовании, представленном в журнале гельминтологии, вторая стадия развития личинок представляет собой серьезную уязвимость к определенным элементам окружающей среды. Высокие температуры и низкий уровень влажности быстро разрушат личинки на этой стадии роста. [20]
| токсокароз | |
|---|---|
| Научная классификация | |
| Домен: | Эукариоты |
| Королевство: | животное |
| Тип: | Нематоды |
| Сорт: | Хромадория |
| Заказ: | Аскаридида |
| Семья: | токсокариды |
| Род: | токсокара |
| Разновидность | |
Виды включают: [23] | |
водохранилище
[ редактировать ]
Переносчиками Toxocara canis являются собаки и лисы , но наибольший риск распространения инфекции среди людей представляют щенки и детеныши. [5] Инфекция у большинства взрослых собак характеризуется инцистированием личинок второй стадии. Однако эти личинки могут реактивироваться у беременных самок и проникать через плацентарный барьер, заражая детенышей. Вертикальная передача также может происходить через грудное молоко. [7] [16] [25] Заразные матери и щенки в возрасте до пяти недель выделяют яйца с фекалиями. [16] [25] Примерно 50% щенков и 20% взрослых собак инфицированы T.canis . [7]
Кошки являются резервуаром Toxocara cati . [5] Как и в случае с T. canis , инцистированные личинки второй стадии у беременных или кормящих кошек реактивируются. Однако вертикальная передача возможна только при грудном вскармливании. [16]
Мухи могут выступать в качестве механических переносчиков токсокары , но большинство инфекций происходит без переносчика. [9] Большинство случаев токсокароза являются результатом прокариотических векторов экспрессии и их передачи через прямой физический контакт с фекалиями, что приводит к заражению болезнью. [26]
Морфология
[ редактировать ]Оба вида откладывают яйца коричневого цвета с косточками. [11] [21] [22] Яйца T. canis имеют размер 75–90 мкм и сферическую форму, тогда как яйца T. cati имеют диаметр 65–70 мкм и продолговатую форму. [7] [21] [22] Из этих яиц вылупляются личинки второй стадии, их длина составляет примерно 0,5 мм, а ширина - 0,02 мм. [4] Взрослые особи обоих видов имеют полную пищеварительную систему и три губы, каждая из которых состоит из зубчатого гребня. [21] [22]
Взрослые особи T. canis встречаются только у собак и лисиц, самцы имеют длину 4–6 см с изогнутым задним концом. [10] [21] У самцов есть спикулы и по одному «трубчатому семеннику». [21] Самки могут достигать 15 см в длину, а вульва составляет одну треть длины их тела. [21] Самки не изогнуты на заднем конце. [10] [21]
Взрослые самки T. cati имеют длину примерно 10 см, а самцы обычно - 6 см или меньше. Взрослые особи T. cati встречаются только у кошек, а самцы T. cati изогнуты на заднем конце. [22]
Жизненный цикл
[ редактировать ]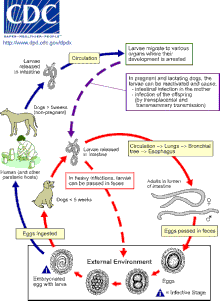
Кошки, собаки и лисы могут заразиться токсокарой при проглатывании яиц или при передаче личинок от матери потомству. [16] [25] Передача инфекции кошкам и собакам также может произойти при проглатывании инфицированных случайных хозяев, таких как дождевые черви, тараканы, грызуны, кролики, куры или овцы. [9] [22]
Яйца вылупляются как личинки второй стадии в кишечнике кошки-хозяина, собаки или лисы (для единообразия в этой статье предполагается, что личинки второй стадии появляются из яиц токсокар , хотя ведутся споры о том, действительно ли личинки находятся на второй или третьей стадии). развития). [10] [9] Личинки попадают в кровоток и мигрируют в легкие, где откашливаются и заглатываются. Личинки созревают во взрослых особей в тонком кишечнике кошки, собаки или лисы, где происходит спаривание и откладка яиц. [9] [12] [16] [21] Яйца передаются с фекалиями и становятся заразными только через три недели вне хозяина. [27] В этот инкубационный период внутри яйца происходит линька личинки первой стадии на вторую (а возможно, и на третью). [9] [22] У большинства взрослых собак, кошек и лисиц полный жизненный цикл не происходит, а вместо этого личинки второй стадии инцистируются после периода миграции по организму. Реактивация личинок встречается только у беременных или кормящих кошек, собак и лисиц. Полный жизненный цикл обычно происходит только у этих самок и их потомства. [16] [25]
Личинки второй стадии также вылупляются в тонком кишечнике случайного хозяина, например человека, после проглатывания инфекционных яиц. [28] Затем личинки мигрируют через органы и ткани случайного хозяина, чаще всего через легкие, печень, глаза и мозг. [29] Поскольку личинки L2 не могут созреть в случайных хозяевах, после этого периода миграции личинки Toxocara инцистируются как личинки второй стадии. [7] [16]
Диагностика
[ редактировать ]Обнаружение личинок токсокар у пациента является единственным окончательным диагнозом токсокароза; однако биопсия для поиска личинок второй стадии у людей, как правило, не очень эффективна. [9] ПЦР , ИФА и серологические исследования чаще используются для диагностики токсокарной инфекции. [9] Серологические тесты зависят от количества личинок у пациента и, к сожалению, не очень специфичны. [9] ИФА гораздо более надежны и в настоящее время имеют чувствительность 78% и специфичность 90%. [30] В исследовании 2007 года было объявлено об использовании ИФА, специфичного для Toxocara canis , который сведет к минимуму ложноположительные результаты перекрестных реакций с аналогичными круглыми червями и поможет отличить пациента от T. canis или T. cati . [31] ОЛМ часто диагностируется после клинического обследования. [30] Гранулемы можно обнаружить по всему телу и визуализировать с помощью ультразвука, МРТ и КТ. [9]
Профилактика
[ редактировать ]Активное вовлечение ветеринаров и владельцев домашних животных важно для контроля передачи токсокары от домашних животных человеку. Группа, очень активно занимающаяся снижением заболеваемости собак в Соединенных Штатах, — это Совет по паразитам домашних животных (CAPC) . Поскольку беременные или кормящие собаки и кошки, а также их потомство имеют самую высокую активную паразитарную нагрузку, этих животных следует подвергнуть программе дегельминтизации. [5] [9] [16] Фекалии домашних животных следует собирать и выбрасывать или закапывать, так как они могут содержать яйца токсокар . [5] Применение этой меры в общественных местах, таких как парки и пляжи, особенно важно для снижения передачи инфекции. [7] [10] До 20% образцов почвы на детских площадках в США обнаружили яйца круглых червей. [17] Кроме того, песочницы следует накрывать, когда они не используются, чтобы кошки не могли использовать их в качестве туалетного лотка. Мытье рук перед едой и после игр с домашними животными, а также после контакта с грязью снизит вероятность проглатывания яиц токсокары . [7] [5] [9] Мытье всех фруктов и овощей, не допускать домашних животных в сад и тщательно готовить мясо также может предотвратить передачу инфекции. [9] Наконец, если научить детей не класть в рот непродовольственные предметы, особенно грязь, это резко снизит вероятность заражения. [5]
Токсокароз был назван одной из забытых болезней бедности в США из-за его распространенности в Аппалачах , на юге США , в городских районах и среди меньшинств. [32]
В настоящее время вакцины нет и она находится в стадии разработки. [6] [32] Митохондриальные геномы T. cati и T. canis были секвенированы в 2008 году, что может привести к прорыву в лечении и профилактике. [33]
Уход
[ редактировать ]Токсокароз часто проходит сам по себе, поскольку личинки токсокар не могут созреть в организме человека. [7] Кортикостероиды назначают в тяжелых случаях ВЛМ или если у пациента диагностирован ОЛМ. Могут быть назначены либо альбендазол (предпочтительно), либо мебендазол («терапия второй линии»). [7] [12] [30] Гранулемы можно удалить хирургическим путем или для разрушения глазных гранулем можно использовать лазерную фотокоагуляцию и криоретинопексию. [9] [12] [30] [34]
Висцеральный токсокароз у людей можно лечить противопаразитарными препаратами, такими как альбендазол или мебендазол , тиабендазол или диэтилкарбамазин, обычно в сочетании с противовоспалительными препаратами. Стероиды использовались с некоторыми положительными результатами. Противогельминтная терапия предназначена для тяжелых инфекций (легких, головного мозга), поскольку терапия может вызвать сильную воспалительную реакцию из-за массового уничтожения личинок. Лечение глазного токсокароза более сложное и обычно состоит из мер по предотвращению прогрессирующего поражения глаза. [35]
Эпидемиология
[ редактировать ]Человек является случайным хозяином токсокары , однако токсокароз встречается во всем мире. Большинство случаев токсокароза наблюдают у людей в возрасте до двадцати лет. [6] Серораспространенность выше в развивающихся странах, но может быть значительной и в странах первого мира. [9] На Бали, Сент-Люсии, Непале и других странах распространенность серовируса превышает пятьдесят процентов. [9] До 2007 года считалось, что серологическая распространенность среди детей в США составляет около 5%. [7] Однако Вон и др. обнаружили, что серораспространенность в США на самом деле составляет 14% среди населения в целом. [6] Во многих странах токсокароз считается очень редким. В США ежегодно регистрируется около 10 000 клинических случаев, из них десять процентов приходится на ОЛМ. [6] [12] Необратимая потеря зрения происходит в 700 из этих случаев. [12]
Наибольшему риску заражения подвергаются маленькие дети, поскольку они играют на улице и склонны класть зараженные предметы и грязь в рот. [7] [10] [9] Владение собаками является еще одним известным фактором риска передачи инфекции. [10] Существует также значительная корреляция между высокими титрами антител к токсокаре и эпилепсией у детей. [7] [36]
У людей отмечена паразитарная нагрузка, достигающая 300 личинок в одном грамме печени. [9] «Экскреторно-секреторные антигены личинок… высвобождаемые из их внешней оболочки эпикутикулы [и]… легко отделяющиеся при связывании специфическими антителами» вызывают иммунный ответ хозяина. [4] Считается, что переломный момент между развитием VLM и OLM составляет от 100 до 200 личинок. [9] Считается, что более легкая инфекция при ОЛМ стимулирует более низкий иммунный ответ и способствует миграции личинки в глаз. Считается, что личинки проникают в глаз через зрительный нерв, центральную артерию сетчатки, короткие задние ресничные артерии, мягкие ткани или спинномозговую жидкость. [9] [12] Глазные гранулемы, образующиеся вокруг личинки, обычно располагаются на периферии сетчатки или диска зрительного нерва. [12]
Висцеральная мигрирующая личинка чаще поражает детей в возрасте 1–4 лет, тогда как глазная мигрирующая личинка чаще поражает детей в возрасте 7–8 лет. От 4,6% до 23% детей в США были заражены яйцами аскарид собачьих. Это число намного выше в других частях мира, в тропических странах серораспространенность достигает 80–90%, например, в Колумбии, где инфицировано до 81% детей, или в Гондурасе, где серораспространенность среди детей школьного возраста было зарегистрировано 88%. [17] [36] [37] В западной части мира серораспространенность ниже, около 35–42%. [36]
История
[ редактировать ]Вернер описал паразитическую нематоду у собак в 1782 году, которую он назвал Ascaris canis . Джонстон определил, что то, что описал Вернер, на самом деле было представителем рода Toxocara , созданного Стайлзом в 1905 году. Фюллеборн предположил, что личинки T canis могут вызывать гранулематозные узелки у людей. В 1947 году Перлингьеро и Дьёрдь описали первый случай, вероятно, токсокароза. Их пациентом был двухлетний мальчик из Флориды с классическими симптомами и эозинофильными некротизирующими гранулемами. [3] В 1950 году Кэмпбелл-Уайлдер первым описал токсокароз у людей; она опубликовала статью, описывающую глазные гранулемы у пациентов с эндофтальмитом, болезнью Коата или псевдоглиомой. Два года спустя Бивер и др. опубликовали наличие личинок Toxocara в гранулемах, удаленных у пациентов с симптомами, сходными с таковыми у пациентов Уайлдера. [9] [10] Об опасности токсокароза впервые стало известно в Великобритании в 1970-х годах, что вызвало панику среди населения. [38]
Другие животные
[ редактировать ]Кошки
[ редактировать ]Некоторые методы лечения инфекции Toxocara cati включают препараты, предназначенные для частичного наркоза взрослых червей и их отделения от слизистой оболочки кишечника, что позволяет им выводиться живыми с фекалиями. К таким препаратам относятся пиперазин и пирантел . Их часто комбинируют с препаратом празиквантел , который, по-видимому, заставляет червя терять устойчивость к перевариванию животным-хозяином. Другие эффективные методы лечения включают ивермектин , милбемицин и селамектин . [39] Дихлофос также доказал свою эффективность в качестве яда, хотя попытки запретить его из-за опасений по поводу его токсичности сделали его недоступным в некоторых регионах. [ нужна ссылка ]
Однако лечение диких кошачьих от этого паразита затруднено, поскольку обнаружение — лучший способ определить, у каких особей есть паразит. Это может быть сложно, поскольку инфицированные виды трудно обнаружить. После обнаружения инфицированных людей придется исключить из популяции, чтобы снизить риск постоянного воздействия паразитов. Основной метод, который использовался для снижения количества инфекции, - это удаление путем охоты. Выселение также может происходить через землевладельцев, как обнаружили Дэйр и Уоткинс (2012) в ходе исследования пум. Как охотники, так и землевладельцы могут предоставить образцы, которые можно использовать для обнаружения присутствия кошачьих круглых червей в этом районе, а также помочь удалить их из популяции. Этот метод более практичен, чем введение лекарств диким популяциям, поскольку диких животных, как упоминалось ранее, труднее найти для оказания медицинской помощи. [ нужна ссылка ]
Однако медикаментозное лечение является еще одним методом, используемым при исследованиях круглых червей; например, эксперимент по борьбе с аскаридами енота, проведенный Smyser et al. (2013), в которых они применили медицинскую травлю. Однако лекарства часто стоят дорого, и успех травли зависит от того, съедят ли инфицированные особи приманку. Кроме того, проверка участков с наживкой может оказаться дорогостоящей (по времени и ресурсам). Удаление путем охоты позволяет агентствам сократить расходы и дает им больше шансов удалить инфицированных людей. [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ https://academic.oup.com/ajcp/article/142/suppl_1/A104/1771175 Эозинофильная псевдолейкемия вследствие токсокароза у 3-летнего пациента: отчет о редком случае
- ^ Ву Т, Боуман Д.Д. (2020). «Висцеральные мигрирующие личинки Toxocara canis и Toxocara cati у хозяев, не относящихся к псовым и не кошачьим». Достижения паразитологии . 109 . Эльзевир: 63–88. дои : 10.1016/bs.apar.2020.02.001 . ISBN 978-0-12-820958-5 . ПМИД 32381221 . S2CID 216238751 .
- ^ Jump up to: а б Марти А. (2000). «Токсокароз Глава 27». В Мейерс В.М., Нефи Р.К., Марти А.М., Wear DJ (ред.). Патология инфекционных болезней . Том. Я: Гельминтозы. Вашингтон, округ Колумбия: Институт патологии Вооруженных сил. стр. 411–21. Архивировано из оригинала 27 декабря 2010 года . Проверено 20 ноября 2014 г.
- ^ Jump up to: а б с д и ж Токсокароз в электронной медицине
- ^ Jump up to: а б с д и ж г час я дж к л «Информационный бюллетень: токсокароз» . Отдел паразитарных болезней . Центры по контролю и профилактике заболеваний. 2007. Архивировано из оригинала 27 марта 2011 года . Проверено 17 сентября 2017 г.
- ^ Jump up to: а б с д и «Результаты нового исследования CDC показывают, что инфекция токсокарой встречается чаще, чем считалось ранее» (PDF) . Отдел паразитарных болезней . Центры по контролю и профилактике заболеваний. 2009. Архивировано (PDF) из оригинала 10 марта 2010 года . Проверено 17 сентября 2017 г.
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и Маркелл ЭК, Воге М (2006). Медицинская паразитология Маркелла и Фоге (9-е изд.). Сент-Луис: Сондерс Эльзевир.
- ^ Сарьего И., Канобана К., Рохас Л., Спейбрук Н., Полман К., Нуньес Ф.А. (2012). Карабин Х (ред.). «Токсокароз на Кубе: обзор литературы» . PLOS Забытые тропические болезни . 6 (2): e1382. дои : 10.1371/journal.pntd.0001382 . ПМК 3289590 . ПМИД 22389726 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но Холланд С., Смит Х.В., ред. (2006). Токсокара: загадочный паразит . Уоллингфорд, Великобритания и Кембридж, Массачусетс: CABI Publishing.
- ^ Jump up to: а б с д и ж г час я Деспомье Д. (2003). «Токсокароз: клинические аспекты, эпидемиология, медицинская экология и молекулярные аспекты» . Обзоры клинической микробиологии . 16 (2): 265–72. doi : 10.1128/CMR.16.2.265-272.2003 . ПМК 153144 . ПМИД 12692098 .
- ^ Jump up to: а б «Кралый червь». Ветеринарное руководство компании Merck . 2008. Архивировано из оригинала 26 мая 2011 года.
- ^ Jump up to: а б с д и ж г час я дж «Токсокароз: мигрирующая глазная личинка». Обзор онлайн-оптометрии: Справочник по лечению глазных заболеваний . Январь 2009 г. Архивировано из оригинала 19 ноября 2011 г. Проверено 3 июля 2011 г.
- ^ Стюарт Дж. М., Кубийлан Л. Д., Каннингем Э. Т. (2005). «Распространенность, клинические особенности и причины потери зрения среди больных глазным токсокарозом». Retina (Филадельфия, Пенсильвания) . 25 (8): 1005–13. дои : 10.1097/00006982-200512000-00009 . ПМИД 16340531 . S2CID 8659870 .
- ^ Гавинье, Беатрис; Пиарру, Рено; Обен, Франсуа; Миллон, Лоуренс; Гумберт, Филипп (декабрь 2008 г.). «Кожные проявления токсокароза человека» . Журнал Американской академии дерматологии . 59 (6): 1031–1042. дои : 10.1016/j.jaad.2008.06.031 . ISSN 0190-9622 . ПМИД 18793816 .
- ^ Бассукас И.Д., Гайтанис Г., Зиога А., Бобоянни С., Стергиопулу С. (2008). «Фебрильный «мигрирующий» эозинофильный целлюлит с гепатоспленомегалией: токсокароз взрослых – описание случая» . Журнал дел . 1 (1): 356. дои : 10.1186/1757-1626-1-356 . ПМК 2621125 . ПМИД 19038064 .
- ^ Jump up to: а б с д и ж г час я дж к л м «Руководство для ветеринаров: Профилактика зоонозной передачи аскарид и нематод собак и кошек» . Отдел паразитарных болезней . Центры по контролю и профилактике заболеваний. 2004. Архивировано из оригинала 21 августа 2010 года . Проверено 17 сентября 2017 г.
- ^ Jump up to: а б с д Чепрасов А (2012). «Смерть на детской площадке». Журнал «Гуру» . 11 : 59–61.
- ^ Jump up to: а б Fan CK, Holland CV, Loxton K, Barghout U (2015). «Церебральный токсокароз: тихое прогрессирование нейродегенеративных заболеваний?» . Обзоры клинической микробиологии . 28 (3): 663–86. дои : 10.1128/CMR.00106-14 . ПМЦ 4462679 . ПМИД 26062575 .
- ^ Азам Д., Укпай О.М., Саид А., Абдаллах Г.А., Морган Э.Р. (2012). «Температура, развитие и выживание инфекционных личинок Toxocara canis». Паразитологические исследования . 110 (2): 649–56. дои : 10.1007/s00436-011-2536-8 . ПМИД 21779864 . S2CID 10075744 .
- ^ Jump up to: а б Гамбоа, Мичиган (декабрь 2005 г.). «Влияние температуры и влажности на развитие яиц Toxocara canis в лабораторных условиях». Журнал гельминтологии . 79 (4): 327–31. дои : 10.1079/JOH2005287 . ПМИД 16336716 . S2CID 30220871 . ПроКвест 213503935 .
- ^ Jump up to: а б с д и ж г час я дж Харрис-Линтон М (2001). «Токсокара канис» . Зоологический музей Мичиганского университета: Сеть о разнообразии животных. Архивировано из оригинала 1 мая 2010 года . Проверено 23 февраля 2009 г.
- ^ Jump up to: а б с д и ж г Соскольне Г (2001). «Токсокара кати» . Зоологический музей Мичиганского университета: Сеть о разнообразии животных. Архивировано из оригинала 5 июня 2011 года . Проверено 17 января 2010 г.
- ^ Джонстон С. (2000). «Нэмс-темы». Нематоды . Пенсильванский университет. Архивировано из оригинала 16 февраля 2009 года . Проверено 23 февраля 2009 г.
- ^ Jump up to: а б с «Браузер таксономии» . www.ncbi.nlm.nih.gov . Проверено 14 января 2019 г.
- ^ Jump up to: а б с д «Токсокароз» . DPDx: Паразиты и здоровье . Центры по контролю и профилактике заболеваний. 2009. Архивировано из оригинала 13 мая 2006 года . Проверено 7 марта 2006 г.
- ^ Мохамад С., Азми Н.К., Нордин Р. (2009). «Разработка и оценка чувствительного и специфического метода диагностики токсокароза человека с использованием трех рекомбинантных антигенов (TES-26, TES-30USM и TES-120)» . Журнал клинической микробиологии . 47 (6): 1712–17. дои : 10.1128/JCM.00001-09 . ПМК 2691092 . ПМИД 19369434 .
- ^ Бесеррил Флорес, Массачусетс (2019). Медицинская паразитология (Пятое изд.). Мексика. ISBN 978-1-4562-6784-1 . OCLC 1117384861 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Ан С.Дж., Рю НК, Ву С.Дж. (2014). «Глазной токсокароз: клиника, диагностика, лечение и профилактика» . Аллергия в Азиатско-Тихоокеанском регионе . 4 (3): 134–41. дои : 10.5415/apallergy.2014.4.3.134 . ПМК 4116038 . ПМИД 25097848 .
- ^ Ли Р.М., Мур Л.Б., Боттацци М.Э., Хотез П.Дж. (2014). «Токсокароз в Северной Америке: систематический обзор» . PLOS Забытые тропические болезни . 8 (8): е3116. дои : 10.1371/journal.pntd.0003116 . ПМК 4148222 . ПМИД 25166906 .
- ^ Jump up to: а б с д Аувертер П. (2008). «Токсокароз» . Центр информационных технологий на местах: Руководство ABX . Джонс Хопкинс. [ постоянная мертвая ссылка ]
- ^ Иддавела Р.Д., Раджапаксе Р.П., Перера Н.А., Агацума Т. (2007). «Характеристика видоспецифического экскреторно-секреторного антигена Toxocara canis (TcES-57) и разработка двойного сэндвич-ИФА для диагностики висцеральной мигрирующей личинки» . Корейский журнал паразитологии . 45 (1): 19–26. дои : 10.3347/kjp.2007.45.1.19 . ПМЦ 2526337 . ПМИД 17374974 .
- ^ Jump up to: а б Хотез П.Дж. (2008). Брукер С. (ред.). «Забытые инфекции бедности в Соединенных Штатах Америки» . PLOS Забытые тропические болезни . 2 (6): е256. дои : 10.1371/journal.pntd.0000256 . ПМЦ 2430531 . ПМИД 18575621 .
- ^ Ли М.В., Линь РК, штаб-квартира Сун, Ву XY, Чжу XQ (2008). «Полные митохондриальные геномы трех видов токсокар, имеющих значение для здоровья человека и животных» . БМК Геномика . 9 :224. дои : 10.1186/1471-2164-9-224 . ПМК 2396643 . ПМИД 18482460 .
- ^ Вернер Дж.К., Росс Р.Д., Грин У.Р., Уоттс Дж.К. (1999). «Витрэктомия Pars plana и субретинальная хирургия при глазном токсокарозе» . Архив офтальмологии . 117 (4): 532–4. дои : 10.1001/archopht.117.4.532 . ПМИД 10206586 .
- ^ «Токсокароз». Паразиты. Центры по контролю и профилактике заболеваний, 10 января 2013 г. «CDC – Токсокароз – Лечение» . 2017. Архивировано из оригинала 6 сентября 2017 года . Проверено 17 сентября 2017 г. . 22 апреля 2014 г.
- ^ Jump up to: а б с Луна Дж., Цицерон С.Э., Рато Дж., Кватрокки Дж., Марин Б., Бруно Э. и др. (2018). Флери А. (ред.). «Обновленные данные о связи между токсокарозом и эпилепсией: систематический обзор и метаанализ» . PLOS Забытые тропические болезни . 12 (7): e0006665. дои : 10.1371/journal.pntd.0006665 . ПМК 6070292 . ПМИД 30028858 .
- ^ Эрнандес, ЮАР (2020). «Комплексное исследование инфекции токсокар у детей Гондураса: сероэпидемиология человека и загрязнение окружающей среды в прибрежном сообществе» . Троп Мед Инфекционный Дис . 5 (3): 135. doi : 10.3390/tropicalmed5030135 . ПМК 7559065 . ПМИД 32842560 .
- ^ Пембертон Н. «Собачья грязь, отвращение и британская пропаганда здоровья 1970-х годов - боеприпасы разума» . blogs.kent.ac.uk .
- ^ Боуман Д.Д., Хендрикс К.М., Линдси Д.С., Барр С.К. (2002). Клиническая паразитология кошек (Первое изд.). Эймс, Айова: Университет штата Айова. п. 275. ИСБН 978-0-8138-0333-3 . Архивировано из оригинала 26 апреля 2018 года.