Триметилглицин
| |
| |
| Имена | |
|---|---|
| Название ИЮПАК
(Триметиламмонио)ацетат
| |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 3537113 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.003.174 |
| Номер ЕС |
|
| 26434 | |
| КЕГГ | |
| МеШ | Бетаин |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 5 Ч 11 НЕТ 2 | |
| Молярная масса | 117.146 |
| Появление | Белый твердый |
| Температура плавления | 180 ° С (356 ° F; 453 К) [ 1 ] (разлагается) |
| Растворимый | |
| Растворимость | Метанол |
| Кислотность ( pKa ) | 1.84 |
| Фармакология | |
| A16AA06 ( ВОЗ ) | |
| Данные лицензии |
|
| Через рот | |
| Юридический статус | |
| Опасности | |
| СГС Маркировка : | |

| |
| Предупреждение | |
| Х315 , Х319 | |
| P264 , P280 , P302+P352 , P305+P351+P338 , P321 , P332+P313 , P337+P313 , P362 | |
| Родственные соединения | |
Родственные аминокислоты
|
Глицин Метилглицин Диметилглицин |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
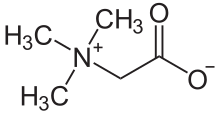
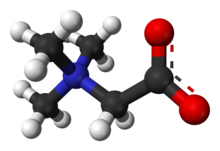
Триметилглицин — производное аминокислоты , встречающееся в растениях. Триметилглицин был первым открытым бетаином ; первоначально его называли просто бетаином , потому что в 19 веке он был обнаружен в сахарной свекле ( Beta vulgaris subsp. vulgaris ). [ 6 ]
Медицинское использование
[ редактировать ]под торговой маркой Цистадан Бетаин, продаваемый, среди прочего, , показан для дополнительного лечения гомоцистинурии, связанной с недостаточностью или дефектами метаболизма цистатионин-бета-синтазы (CBS), 5,10-метилентетрагидрофолатредуктазы (MTHFR) или метаболизма кофактора кобаламина. бл). [ 3 ] [ 4 ] [ 5 ]
Наиболее частым побочным эффектом является повышение уровня метионина в крови. [ 4 ]
ЕС утвердил утверждение о том, что бетаин «способствует нормальному метаболизму гомоцистеина ». [ 7 ]
Структура и реакции
[ редактировать ]Триметилглицин представляет собой N -метилированную аминокислоту. Это цвиттер-ион , поскольку молекула содержит как четвертичную аммониевую группу, так и карбоксильную группу. Карбоксильная группа будет частично протонирована в водном растворе при pH ниже 4, то есть примерно ниже pH, равного (p K a + 2).
- (СН 3 ) 3 Н + CH 2 CO − 2 (водн.) + ЧАС + ⇌ (СН 3 ) 3 Н + CH 2 CO 2 H (водн.)
Деметилирование триметилглицина дает диметилглицин .
Производственные и биохимические процессы
[ редактировать ]Переработка сахарозы из сахарной свеклы дает в качестве побочного продукта глицин-бетаин . Экономическая ценность триметилглицина соперничает с ценностью содержания сахара в сахарной свекле. [ 8 ]
Биосинтез
[ редактировать ]У большинства организмов глицин-бетаин биосинтезируется путем окисления холина в два этапа. Промежуточное соединение, бетаинальдегид , образуется под действием фермента митохондриальной холиноксидазы ( холиндегидрогеназа , EC 1.1.99.1). Бетаинальдегид далее окисляется в митохондриях мышей до бетаина ферментом бетаин-альдегиддегидрогеназой (EC 1.2.1.8). [ 9 ] [ 10 ] У человека активность бетаинальдегида осуществляется неспецифическим ферментом цистозольной альдегиддегидрогеназы (EC 1.2.1.3). [ 11 ]
Биологическая функция
[ редактировать ]Триметилглицин представляет собой органический осмолит . Сахарную свеклу выращивали из морской свеклы , которой необходимы осмолиты, чтобы выжить в засоленных почвах прибрежных районов. Триметилглицин также встречается в высоких концентрациях (~ 10 мМ) у многих морских беспозвоночных, таких как ракообразные и моллюски . Он служит мощным аппетитным аттрактантом для хищников широкого профиля, таких как хищный морской слизень Pleurobranchaea California . [ 12 ]
является важным кофактором метилирования Триметилглицин , процесса, который происходит в каждой клетке млекопитающих, жертвуя метильные группы (-CH 3 ) для других процессов в организме. Эти процессы включают синтез нейротрансмиттеров, таких как дофамин и серотонин . Метилирование также необходимо для биосинтеза мелатонина и цепи переноса электронов компонента коэнзима Q 10 , а также для метилирования ДНК в эпигенетических целях.
Главным этапом цикла метилирования является реметилирование гомоцистеина , соединения , которое естественным образом образуется при деметилировании незаменимой аминокислоты метионина . Несмотря на свое естественное образование, гомоцистеин связан с воспалением, депрессией, определенными формами деменции и различными типами сосудистых заболеваний. Процесс реметилирования, который детоксицирует гомоцистеин и превращает его обратно в метионин, может происходить по одному из двух путей. Путь, присутствующий практически во всех клетках, включает фермент метионинсинтазу (MS), который требует витамина B12 в качестве кофактора, а также косвенно зависит от фолиевой кислоты и других витаминов группы B. Второй путь (ограниченный печенью и почками у большинства млекопитающих) включает бетаин-гомоцистеинметилтрансферазу (BHMT) и требует триметилглицина в качестве кофактора. В нормальных физиологических условиях оба пути в равной степени способствуют удалению гомоцистеина из организма. [ 13 ] Дальнейшее расщепление бетаина с помощью фермента диметилглициндегидрогеназы приводит к образованию фолата, тем самым внося свой вклад в образование метионинсинтазы. Таким образом, бетаин участвует в синтезе многих биологически важных молекул и может быть даже более важным в ситуациях, когда основной путь регенерации метионина из гомоцистеина нарушен генетическими полиморфизмами, такими как мутации в гене рассеянного склероза.
Триметилглицин вырабатывается некоторыми цианобактериями . Габбай-Азария и др., 1988 г., используют 13 Ядерный магнитный резонанс C для обнаружения триметилглицинов, продуцируемых галофильными цианобактериями. что он обеспечивает частичную защиту их ферментов от ингибирования NaCl Они обнаружили , и KCl . [ 14 ]
Сельское хозяйство и аквакультура
[ редактировать ]На промышленных фермах добавляют в корм триметилглицин и лизин скота для увеличения мышечной массы (и, следовательно, «выхода туши», количества годного к употреблению мяса).
Лососевые фермы применяют триметилглицин для снижения осмотического давления на клетки рыб, когда рабочие переводят рыбу из пресной воды в соленую. [ 8 ] [ 15 ]
Добавки триметилглицина уменьшают количество жировой ткани у свиней; однако исследования на людях не показали никакого влияния на массу тела, состав тела или расход энергии в состоянии покоя. [ 16 ]
Питание
[ редактировать ]С точки зрения питания бетаин не нужен, если в пище присутствует достаточное количество холина для синтеза. [ 17 ] Когда бетаина недостаточно, происходит повышение уровня гомоцистеина и снижение уровня SAM в крови. Добавление бетаина в этой ситуации решит проблемы с маркерами крови, но не компенсирует другие функции холина. [ 18 ]
| Еда | Бетаин (мг/100 г) |
|---|---|
| Зародыши пшеницы , поджаренные [ 20 ] | 1240 |
| Лебеда | 630 |
| Зародыши пшеницы | 410 |
| четверти ягненка | 330 |
| Пшеничные отруби | 320 |
| Консервированная свекла | 260 |
| темная ржаная Мука | 150 |
| Шпинат | 110-130 |
Пищевая добавка
[ редактировать ]Хотя добавка триметилглицина уменьшает количество жировой ткани у свиней, исследования на людях не показали никакого влияния на массу тела, состав тела или расход энергии в состоянии покоя при использовании в сочетании с низкокалорийной диетой. [ 16 ] США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило бетаин триметилглицин (также известный под торговой маркой «Цистадан») для лечения гомоцистинурии — заболевания, вызванного аномально высоким уровнем гомоцистеина при рождении. [ 21 ] Триметилглицин также используется в виде гидрохлоридной соли (продается как гидрохлорид бетаина или гидрохлорид бетаина). Бетаин гидрохлорид продавался без рецепта (OTC) как предполагаемое средство для лечения желудка в Соединенных Штатах. Кодекс федеральных правил США, раздел 21, раздел 310.540, который вступил в силу в ноябре 1993 года, запретил продажу бетаина гидрохлорида в качестве средства для улучшения пищеварения из-за недостаточности доказательств, чтобы классифицировать его как «общепризнанный как безопасный и эффективный» для этого конкретного использования. [ 22 ]
Побочные эффекты
[ редактировать ]Прием триметилглицина может вызвать диарею , вздутие живота, судороги, диспепсию , тошноту или рвоту. [ 23 ] Хотя и редко, это также может вызывать чрезмерное повышение концентрации метионина в сыворотке мозга, что может привести к отеку мозга , опасному для жизни состоянию. [ 23 ]
Добавки триметилглицина снижают уровень гомоцистеина, но также повышают уровень холестерина ЛПНП у людей с ожирением и пациентов с почечной недостаточностью. [ 24 ]
Другое использование
[ редактировать ]Полимеразная цепная реакция
[ редактировать ]Триметилглицин может действовать как адъювант процесса полимеразной цепной реакции (ПЦР) и других анализов на основе ДНК-полимеразы, таких как секвенирование ДНК . По неизвестному механизму он помогает предотвратить образование вторичных структур в молекулах ДНК и предотвращает проблемы, связанные с амплификацией и секвенированием областей, богатых GC. Триметилглицин заставляет гуанозин и цитидин (сильные связующие) вести себя по термодинамике аналогично тимидину и аденозину (слабые связующие). Экспериментально установлено, что его лучше всего использовать при конечной концентрации 1 М. [ 25 ]
Ссылки
[ редактировать ]- ^ Ачесон Р.М., Бонд Дж.Дж. (1956). «52. Реакции присоединения гетероциклических соединений. Часть II. Фенантридин и метилацетилендикарбоксилат в метаноле». Дж. Хим. Соц . 1956 : 246. doi : 10.1039/JR9560000246 .
- ^ «Уведомление о внесении поправки: Бетаин исключен из Списка рецептурных препаратов (PDL)» . Здоровье Канады . 6 января 2023 г. Проверено 3 января 2024 г.
- ^ Jump up to: а б «Цистадан-бетаин порошок для приготовления раствора» . ДейлиМед . 3 октября 2019 года. Архивировано из оригинала 4 августа 2021 года . Проверено 29 июля 2022 г.
- ^ Jump up to: а б с «Цистадан ЭПАР» . Европейское агентство по лекарственным средствам . 17 сентября 2018 г. Архивировано из оригинала 1 июля 2022 г. Проверено 29 июля 2022 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Jump up to: а б «Амверсио ЭПАР» . Европейское агентство по лекарственным средствам . 21 февраля 2022 года. Архивировано из оригинала 30 июля 2022 года . Проверено 29 июля 2022 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Шивек Х., Кларк М., Поллах Г. «Сахар». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a25_345.pub2 . ISBN 978-3527306732 .
- ^ К. К. Тийхонен, К. Риихенен, М. Лийра, Э. Сарккинен, САС Крейг, П. Теннинг (2014). «12 - Официальные заявления ЕС о вреде для здоровья бетаина». В Сэдлере М. (ред.). Продукты питания, питательные вещества и пищевые ингредиенты с утвержденными заявлениями ЕС о вреде для здоровья . Издательство Вудхед. стр. 251–273. ISBN 978-0-85709-842-9 . Проверено 19 февраля 2024 г.
Европейское управление по безопасности пищевых продуктов (EFSA) согласилось с тем, что существует достаточное обоснование заявления о пользе бетаина для здоровья относительно его вклада в нормальный метаболизм гомоцистеина (EFSA, 2011a).
- ^ Jump up to: а б Мякеля П. (2004). «Агропромышленное использование глицинабетаина». Сахарная Техника . 6 (4): 207–212. дои : 10.1007/BF02942500 . hdl : 10138/312331 . S2CID 25219649 .
- ^ Кемпф Б., Бремер Э. (1998). «Поглощение и синтез совместимых растворенных веществ как реакция микробов на стресс в условиях среды с высокой осмоляльностью». Арх. Микробиол . 170 (5): 319–330. Бибкод : 1998ArMic.170..319K . дои : 10.1007/s002030050649 . ПМИД 9818351 . S2CID 8045279 .
- ^ «БРЕНДА – Информация о EC 1.2.1.8 – бетаин-альдегиддегидрогеназа» . Бренда-энзимы.org . Архивировано из оригинала 29 июня 2016 года . Проверено 7 июля 2016 г.
- ^ Черн М.К., Петрушко Р. (1999). «Доказательства митохондриальной локализации бетаин-альдегиддегидрогеназы в печени крыс: очистка, характеристика и сравнение с цитоплазматическим изоферментом E3 человека». Биохимия и клеточная биология . 77 (3): 179–187. дои : 10.1139/o99-030 . ПМИД 10505788 .
- ^ Джилетт Р., Хуанг Р.К., Хэтчер Н., Мороз Л.Л. (март 2000 г.). «Потенциал анализа затрат и выгод при кормлении хищной улитки путем интеграции голода, вкуса и боли» . Учеб. Натл. акад. наук. США . 97 (7): 3585–3590. Бибкод : 2000PNAS...97.3585G . дои : 10.1073/pnas.97.7.3585 . ПМК 16283 . ПМИД 10737805 .
- ^ Финкельштейн JD (24 марта 1998 г.). «Метаболизм гомоцистеина: пути и регуляция». Европейский журнал педиатрии . 157 (С2): С40–С44. дои : 10.1007/pl00014300 . ISSN 0340-6199 . ПМИД 9587024 . S2CID 38134977 .
- ^ Роудс Д., Хэнсон А.Д. (1993). «Соединения четвертичного аммония и третичного сульфония в высших растениях». Ежегодный обзор физиологии растений и молекулярной биологии растений . 44 (1). Годовые обзоры : 357–384. дои : 10.1146/annurev.pp.44.060193.002041 . ISSN 1040-2519 .
- ^ Сюэ М, Се С, Цуй Ю (2004). «Влияние кормового стимулятора на пищевую адаптацию карпа Carassius auratus gibelio (Bloch), получавшего рационы с заменой рыбной муки мясокостной мукой» . Исследования аквакультуры . 35 (5): 473–482. дои : 10.1111/j.1365-2109.2004.01041.x . S2CID 84304519 .
- ^ Jump up to: а б Шваб У., Торренен А., Топпинен Л. и др. (ноябрь 2002 г.). «Прием бетаина снижает концентрацию гомоцистеина в плазме, но не влияет на массу тела, состав тела или расход энергии в состоянии покоя у людей» . Являюсь. Дж. Клин. Нутр . 76 (5): 961–967. дои : 10.1093/ajcn/76.5.961 . ПМИД 12399266 .
- ^ Ракер Р.Б., Земплени Дж., Сатти Дж.В., МакКормик Д.Б. (2007). Справочник витаминов (4-е изд.). Тейлор и Фрэнсис. стр. 100-1 459 –477 . ISBN 978-0-8493-4022-2 .
- ^ «Диетические эталонные значения холина» . Журнал EFSA . 14 (8). 2016. doi : 10.2903/j.efsa.2016.4484 .
- ^ Паттерсон К.Ю., Бхагват С.А., Уильямс-младший, Хоу Дж.К., Холден Дж.М., Зейзель С.Х., Дакоста К.А., Мар М.Х. (1 ноября 2019 г.). «База данных Министерства сельского хозяйства США по содержанию холина в обычных продуктах питания, выпуск 2 (2008 г.)» . Министерство сельского хозяйства США . дои : 10.15482/USDA.ADC/1178141 . Архивировано из оригинала 30 июля 2022 года . Проверено 2 февраля 2021 г.
- ^ Стивен Х. Зейзель, Мей-Хенг Мар, Джульетта С. Хоу, Джоан М. Холден (май 2003 г.). «Концентрация холинсодержащих соединений и бетаина в обычных продуктах питания» . Журнал питания . 133 (5): 1302–7. дои : 10.1093/jn/133.5.1302 . ПМИД 12730414 .
- ^ Холм П.И., Уеланд П.М., Фоллсет С.Е. и др. (февраль 2005 г.). «Статус бетаина и фолиевой кислоты как кооперативные детерминанты гомоцистеина в плазме у людей» . Артериосклер. Тромб. Васк. Биол . 25 (2): 379–385. дои : 10.1161/01.ATV.0000151283.33976.e6 . ПМИД 15550695 .
- ^ «CFR — Свод федеральных правил, раздел 21» . Управление по контролю за продуктами и лекарствами США . Архивировано из оригинала 27 июля 2020 года . Проверено 4 сентября 2018 г.
- ^ Jump up to: а б «Бетаин» , LiverTox: клиническая и исследовательская информация о лекарственном повреждении печени , Bethesda (MD): Национальный институт диабета, заболеваний органов пищеварения и почек, 2012 г., PMID 31644082 , получено 14 июля 2023 г.
- ^ Олтхоф М.Р., ван Влит Т., Верхуф П., Зок П.Л., Катан М.Б. (2005). «Влияние питательных веществ, снижающих гомоцистеин, на липиды крови: результаты четырех рандомизированных плацебо-контролируемых исследований на здоровых людях» . ПЛОС Мед . 2 (5): е135. дои : 10.1371/journal.pmed.0020135 . ПМК 1140947 . ПМИД 15916468 .
- ^ Хенке В., Хердель К., Юнг К., Шнорр Д., Лёнинг С.А. (октябрь 1997 г.). «Бетаин улучшает ПЦР-амплификацию последовательностей ДНК, богатых GC» . Нуклеиновые кислоты Рез . 25 (19): 3957–3958. дои : 10.1093/нар/25.19.3957 . ПМК 146979 . ПМИД 9380524 . Архивировано из оригинала 31 июля 2013 года.
Внешние ссылки
[ редактировать ]- База данных Министерства сельского хозяйства США по содержанию холина в обычных продуктах питания , включая данные о метаболитах холина, таких как бетаин, в 434 продуктах питания.