Сфинголипид
Эта статья нуждается в дополнительных цитатах для проверки . ( январь 2023 г. ) |
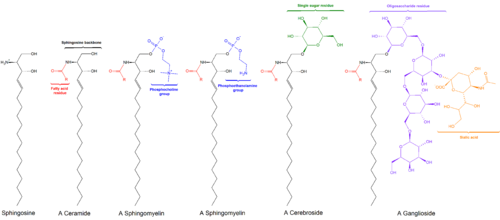
Сфинголипиды представляют собой класс липидов, основу из сфингоидных оснований, которые представляют собой набор алифатических аминоспиртов содержащих , включающий сфингозин . Они были обнаружены в экстрактах мозга в 1870-х годах и были названы в честь мифологического сфинкса из-за их загадочной природы. [1] Эти соединения играют важную роль в передаче сигналов и распознавании клеток . Сфинголипидозы , или нарушения метаболизма сфинголипидов, оказывают особое влияние на нервную ткань . Сфинголипид с концевой гидроксильной группой представляет собой церамид . Другие распространенные группы, связанные с концевым атомом кислорода, включают фосфохолин , образующий сфингомиелин , и различные мономеры или димеры сахаров, образующие цереброзиды и глобозиды соответственно. Цереброзиды и глобозиды известны под общим названием гликосфинголипиды .
Структура
[ редактировать ]Длинноцепочечные основания, иногда просто называемые сфингоидными основаниями, являются первыми непереходными продуктами синтеза сфинголипидов de novo как у дрожжей, так и у млекопитающих. Эти соединения, особенно известные как фитосфингозин и дигидросфингозин (также известный как сфинганин), [2] хотя этот термин менее распространен), в основном представляют собой соединения C 18 с несколько меньшим содержанием оснований C 20 . [3] Церамиды и гликосфинголипиды являются N -ацильными производными этих соединений. [4]
Основная цепь сфингозина O-связана с (обычно) заряженной головной группой, такой как этаноламин , серин или холин . [ нужна ссылка ]
Основная цепь также связана амидом с ацильной группой , такой как жирная кислота . [ нужна ссылка ]
Типы
[ редактировать ]Простые сфинголипиды, включающие сфингоидные основания и церамиды, составляют ранние продукты синтетических путей сфинголипидов.
- Сфингоидные основания являются фундаментальными строительными блоками всех сфинголипидов. Основными сфингоидными основаниями млекопитающих являются дигидросфингозин и сфингозин, тогда как дигидросфингозин и фитосфингозин являются основными сфингоидными основаниями у дрожжей. [5] [6] Сфингозин, дигидросфингозин и фитосфингозин могут быть фосфорилированы.
- Церамиды , как общий класс, представляют собой N -ацилированные сфингоидные основания без дополнительных головных групп.
- Дигидроцерамид получают N- ацилированием дигидросфингозина. Дигидроцерамид обнаружен как в дрожжах, так и в системах млекопитающих.
- Церамид вырабатывается в организме млекопитающих путем десатурации дигидроцерамида дигидроцерамиддесатуразой 1 (DES1). Эта высокобиоактивная молекула также может фосфорилироваться с образованием церамид-1-фосфата .
- Фитоцерамид производится в дрожжах путем гидроксилирования дигидроцерамида по C-4.
Сложные сфинголипиды могут образовываться путем присоединения головных групп к церамиду или фитоцерамиду:
- Сфингомиелины имеют молекулу фосфохолина или фосфоэтаноламина со сложноэфирной связью с 1-гидроксигруппой церамида.
- Гликосфинголипиды представляют собой церамиды с одним или несколькими остатками сахара , соединенными β- гликозидной связью в 1-гидроксильном положении (см. изображение).
- Цереброзиды содержат одну глюкозу или галактозу в 1-гидрокси-положении.
- Сульфатиды представляют собой сульфатированные цереброзиды.
- Ганглиозиды содержат по крайней мере три сахара, один из которых должен быть сиаловой кислотой .
- Цереброзиды содержат одну глюкозу или галактозу в 1-гидрокси-положении.
- Инозитолсодержащие церамиды, которые являются производными фитоцерамидов, производятся в дрожжах. К ним относятся инозитолфосфорилцерамид, маннозо -инозитолфосфорилцерамид и маннозодиинозитолфосфорилцерамид.
Метаболизм сфинголипидов млекопитающих
[ редактировать ]Синтез сфинголипидов de novo начинается с образования 3-кето-дигидросфингозина серинпальмитоилтрансферазой . [7] Предпочтительными субстратами для этой реакции являются пальмитоил-СоА и серин . Однако исследования показали, что серинпальмитоилтрансфераза обладает некоторой активностью в отношении других видов жирного ацил-КоА. [8] и альтернативные аминокислоты , [9] и недавно было рассмотрено разнообразие оснований сфингоидов. [10] Затем 3-кето-дигидросфингозин восстанавливается с образованием дигидросфингозина. Дигидросфингозин ацилируется одной из шести (дигидро)-церамидсинтаз, CerS - первоначально называемой LASS - с образованием дигидроцерамида. [11] Шесть ферментов CerS обладают разной специфичностью к субстратам ацил-КоА , что приводит к образованию дигидроцерамидов с разной длиной цепи (в диапазоне от C14 до C26). Затем дигидроцерамиды денасыщают с образованием церамида. [12]

Генерируемый de novo церамид является центральным узлом сфинголипидной сети и впоследствии имеет несколько судеб. Он может фосфорилироваться церамидкиназой с образованием церамид-1-фосфата. Альтернативно, он может быть гликозилирован глюкозилцерамидсинтазой или галактозилцерамидсинтазой . Кроме того, он может быть преобразован в сфингомиелин путем добавления фосфорилхолина головной группы сфингомиелинсинтазой . диацилглицерин В результате этого процесса образуется . Наконец, церамид может расщепляться церамидазой с образованием сфингозина . Сфингозин может фосфорилироваться с образованием сфингозин-1-фосфата. Его можно дефосфорилировать с образованием сфингозина. [13]
Пути распада позволяют превратить эти метаболиты в церамиды. Сложные гликосфинголипиды гидролизуются до глюкозилцерамида и галактозилцерамида. Эти липиды затем гидролизуются бета-глюкозидазами и бета-галактозидазами для регенерации церамидов. Аналогичным образом сфингомиелин может расщепляться сфингомиелиназой с образованием церамида. [ нужна ссылка ]
Единственный путь превращения сфинголипидов в несфинголипиды — через сфингозин-1-фосфатлиазу. При этом образуются фосфат этаноламина и гексадеценаль. [14]
Функции сфинголипидов млекопитающих
[ редактировать ]Обычно считается, что сфинголипиды защищают поверхность клетки от вредных факторов окружающей среды, образуя механически стабильный и химически стойкий внешний слой плазматической мембраны липидного бислоя . Было обнаружено, что некоторые сложные гликосфинголипиды участвуют в определенных функциях, таких как распознавание клеток и передача сигналов . Распознавание клеток зависит главным образом от физических свойств сфинголипидов, тогда как передача сигналов включает специфические взаимодействия гликановых структур гликосфинголипидов с аналогичными липидами, присутствующими на соседних клетках или с белками . [ нужна ссылка ]
Недавно было показано, что простые метаболиты сфинголипидов , такие как церамид и сфингозин-1-фосфат , являются важными медиаторами в сигнальных каскадах, участвующих в апоптозе , пролиферации , стрессовых реакциях, некрозе , воспалении , аутофагии , старении и дифференцировке . [15] [16] [17] [18] [19] Липиды на основе церамидов самоагрегируются в клеточных мембранах и образуют отдельные фазы, менее жидкие, чем основные фосфолипиды. Эти микродомены на основе сфинголипидов, или « липидные рафты », первоначально были предложены для сортировки мембранных белков по клеточным путям мембранного транспорта. В настоящее время большинство исследований сосредоточено на организующей функции при передаче сигнала. [20]
Сфинголипиды синтезируются по пути, который начинается в ЭР и завершается в аппарате Гольджи , но эти липиды накапливаются в плазматической мембране и эндосомах , где они выполняют многие из своих функций. [21] Транспорт происходит посредством везикул и мономерного транспорта в цитозоле . Сфинголипиды практически отсутствуют в митохондриях и ЭР , но составляют 20-35 молярную долю липидов плазматической мембраны. [22]
У экспериментальных животных сфинголипиды ингибируют канцерогенез в толстой кишке , снижают уровень холестерина ЛПНП и повышают уровень холестерина ЛПВП . [23]
Другие сфинголипиды
[ редактировать ]Сфинголипиды универсальны для эукариот, но редки для бактерий и архей , а это означает, что они эволюционно очень старые. Бактерии, которые производят сфинголипиды, обнаружены у некоторых представителей супертипа группы FCB ( Sphingobacteria ), особенно семейства Sphingomonadaceae , некоторых представителей Bdellovibrionota и некоторых членов Myxococcota . [24]
Дрожжевые сфинголипиды
[ редактировать ]Из-за невероятной сложности систем млекопитающих дрожжи часто используются в качестве модельного организма для разработки новых путей. Эти одноклеточные организмы зачастую более генетически более податливы, чем клетки млекопитающих, и библиотеки штаммов доступны для поставки штаммов, несущих практически любую нелетальную одиночную делецию в открытой рамке считывания . Двумя наиболее часто используемыми дрожжами являются Saccharomyces cerevisiae и Schizosaccharomyces pombe , хотя исследования также проводятся на патогенных дрожжах Candida albicans . [ нужна ссылка ]
Помимо важных структурных функций сложных сфинголипидов (инозитолфосфорилцерамид и его маннозилированные производные), сфингоидные основания фитосфингозин и дигидросфингозин (сфинганин) играют жизненно важную сигнальную роль у S. cerevisiae . Эти эффекты включают регуляцию эндоцитоза , убиквитин-зависимый протеолиз (и, таким образом, регуляцию поглощения питательных веществ). [25] ), цитоскелета динамика , клеточный цикл , трансляция , посттрансляционная модификация белка и реакция на тепловой стресс. [26] модуляция метаболизма сфинголипидов посредством фосфатидилинозитол (4,5)-бисфосфата передачи сигналов через Slm1p и Slm2p и кальциневрин . Кроме того, недавно была описана [27] Кроме того, было показано взаимодействие на уровне субстрата между синтезом сложного сфинголипида и циклическим циклом фосфатидилинозитол-4-фосфата с помощью фосфатидилинозитолкиназы Stt4p и липидфосфатазы Sac1p. [28]
Растительные сфинголипиды
[ редактировать ]Высшие растения содержат более широкий спектр сфинголипидов, чем животные и грибы. [ нужна ссылка ]
расстройства
[ редактировать ]Существует несколько нарушений метаболизма сфинголипидов, известных как сфинголипидозы . Основными представителями этой группы являются болезнь Нимана-Пика , болезнь Фабри , болезнь Краббе , болезнь Гоше , болезнь Тея-Сакса и метахроматическая лейкодистрофия . Они обычно наследуются по аутосомно-рецессивному типу, но, в частности, болезнь Фабри является Х-сцепленной . В совокупности сфинголипидозы встречаются примерно у 1 из 10 000, но значительно чаще в определенных группах населения, таких как евреи-ашкенази . Ферментозаместительная терапия доступна для лечения главным образом болезни Фабри и болезни Гоше , и люди с этими типами сфинголипидозов могут дожить до зрелого возраста. Другие типы, как правило, смертельны в возрасте от 1 до 5 лет для инфантильных форм, но прогрессирование может быть легким для ювенильных или взрослых форм. [ нужна ссылка ]
Сфинголипиды также связаны с белком фратаксином (Fxn), дефицит которого связан с атаксией Фридрейха (FRDA). Потеря Fxn в нервной системе у мышей также активирует путь железо/сфинголипид/PDK1/Mef2, указывая на то, что этот механизм эволюционно консервативен. Кроме того, уровни сфинголипидов и активность PDK1 также повышаются в сердцах пациентов с FRDA, что позволяет предположить, что при FRDA затрагивается аналогичный путь. [29] Другие исследования показали, что накопление железа в нервной системе мух усиливает синтез сфинголипидов, которые, в свою очередь, активируют 3-фосфоинозитид-зависимую протеинкиназу-1 (Pdk1) и фактор-2 усилителя миоцитов (Mef2), вызывая нейродегенерацию фоторецепторов взрослых. [30]
Сфинголипиды играют ключевую роль в выживании нейронов при болезни Паркинсона (БП), а изменение их катаболических путей в головном мозге частично представлено в спинномозговой жидкости и тканях крови (табл. 1) и имеет диагностический потенциал. [31]
Дополнительные изображения
[ редактировать ]См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Чун Дж, Хартунг Х.П. (2010). «Механизм действия перорального финголимода (FTY720) при рассеянном склерозе» . Клиническая нейрофармакология . 33 (2): 91–101. дои : 10.1097/wnf.0b013e3181cbf825 . ПМЦ 2859693 . ПМИД 20061941 .
- ^ |SIGMA&N5=SEARCH_CONCAT_PNO|BRAND_KEY&F=SPEC Страница продукта на Sigma Aldrich
- ^ Диксон RC (1998). «Функции сфинголипидов у Saccharomyces cerevisiae: сравнение с млекопитающими» . Ежегодный обзор биохимии . 67 : 27–48. doi : 10.1146/annurev.biochem.67.1.27 . ПМИД 9759481 .
- ^ Краткий, очень понятный обзор дан в Gunstone, F. (1996) Fatty Acid and Lipid Chemistry , стр. 43-44. Блэки академический и профессиональный. ISBN 0-7514-0253-2
- ^ Диксон RC (май 2008 г.). «Серия тематических обзоров: сфинголипиды. Новое понимание метаболизма и функции сфинголипидов у почкующихся дрожжей» . Журнал исследований липидов . 49 (5): 909–21. doi : 10.1194/jlr.R800003-JLR200 . ПМК 2311445 . ПМИД 18296751 .
- ^ Бартке Н., Ханнун Ю.А. (апрель 2009 г.). «Биоактивные сфинголипиды: метаболизм и функции» . Журнал исследований липидов . 50 Дополнение (Дополнение): S91-6. doi : 10.1194/jlr.R800080-JLR200 . ПМЦ 2674734 . ПМИД 19017611 .
- ^ Меррилл АХ (декабрь 1983 г.). «Характеристика активности серинпальмитоилтрансферазы в клетках яичника китайского хомячка». Biochimica et Biophysical Acta (BBA) - Липиды и липидный обмен . 754 (3): 284–91. дои : 10.1016/0005-2760(83)90144-3 . ПМИД 6652105 .
- ^ Меррилл А.Х., Уильямс Р.Д. (февраль 1984 г.). «Использование различных жирных тиоэфиров ацил-КоА серинпальмитоилтрансферазой из мозга крысы» . Журнал исследований липидов . 25 (2): 185–8. дои : 10.1016/S0022-2275(20)37838-X . ПМИД 6707526 .
- ^ Зитомер Н.К., Митчелл Т., Восс К.А., Бонди Г.С., Пруэтт С.Т., Гарнье-Амблар ЕС, Либескинд Л.С., Парк Х., Ван Э., Саллардс М.К., Меррилл А.Х., Райли Р.Т. (февраль 2009 г.). «Ингибирование церамидсинтазы фумонизином B1 вызывает накопление 1-дезоксисфинганина: новой категории биоактивных 1-дезоксисфингоидных оснований и 1-дезоксидигидроцерамидов, биосинтезируемых линиями клеток млекопитающих и животными» . Журнал биологической химии . 284 (8): 4786–95. дои : 10.1074/jbc.M808798200 . ПМЦ 2643501 . ПМИД 19095642 .
- ^ Пруэтт С.Т., Бушнев А., Хагедорн К., Адига М., Хейнс К.А., Саллардс МС, Лиотта Д.С., Меррилл А.Х. (август 2008 г.). «Биоразнообразие сфингоидных оснований («сфингозинов») и родственных аминоспиртов» . Журнал исследований липидов . 49 (8): 1621–39. doi : 10.1194/jlr.R800012-JLR200 . ПМК 2444003 . ПМИД 18499644 .
- ^ Пьюцнер-Юнг Й., Бен-Дор С., Футерман А.Х. (сентябрь 2006 г.). «Когда Lasses (гены обеспечения долголетия) становятся CerS (церамидсинтазами)?: Понимание регуляции синтеза церамидов» . Журнал биологической химии . 281 (35): 25001–5. дои : 10.1074/jbc.R600010200 . ПМИД 16793762 .
- ^ Козерет С., Герарт Л., Ван дер Хувен Г., Маннартс Г.П., Ван Вельдховен П.П. (октябрь 2000 г.). «Дальнейшая характеристика дигидроцерамиддесатуразы крысы: распределение в тканях, субклеточная локализация и специфичность субстрата». Липиды . 35 (10): 1117–25. дои : 10.1007/s11745-000-0627-6 . ПМИД 11104018 . S2CID 3962533 .
- ^ Ханнун Ю.А., Обейд Л.М. (февраль 2008 г.). «Принципы передачи сигналов биоактивных липидов: уроки сфинголипидов». Nature Reviews Молекулярно-клеточная биология . 9 (2): 139–50. дои : 10.1038/nrm2329 . ПМИД 18216770 . S2CID 8692993 .
- ^ Бандхувула П., Саба Дж.Д. (май 2007 г.). «Сфингозин-1-фосфатлиаза в иммунитете и раке: заглушить сирену». Тенденции молекулярной медицины . 13 (5): 210–7. doi : 10.1016/j.molmed.2007.03.005 . ПМИД 17416206 .
- ^ Ханнун Ю.А., Обейд Л.М. (июль 2002 г.). «Церамидоцентричная вселенная липид-опосредованной клеточной регуляции: стрессовые ситуации липидного типа» . Журнал биологической химии . 277 (29): 25847–50. дои : 10.1074/jbc.R200008200 . ПМИД 12011103 .
- ^ Шпигель С., Мильстиен С. (июль 2002 г.). «Сфингозин-1-фосфат, ключевая сигнальная молекула клетки» . Журнал биологической химии . 277 (29): 25851–4. дои : 10.1074/jbc.R200007200 . ПМИД 12011102 .
- ^ Лавье Г., Скарлатти Ф., Сала Г., Карпентье С., Леваде Т., Гидони Р., Ботти Дж., Кодоньо П. (март 2006 г.). «Регуляция аутофагии сфингозинкиназой 1 и ее роль в выживании клеток во время питательного голодания» . Журнал биологической химии . 281 (13): 8518–27. дои : 10.1074/jbc.M506182200 . ПМИД 16415355 .
- ^ Венейбл М.Э., Ли Дж.Ю., Смит М.Дж., Белявска А., Обейд Л.М. (декабрь 1995 г.). «Роль церамидов в клеточном старении» . Журнал биологической химии . 270 (51): 30701–8. дои : 10.1074/jbc.270.51.30701 . ПМИД 8530509 .
- ^ Снайдер А.Дж., Орр Ганди К.А., Обейд Л.М. (июнь 2010 г.). «Сфингозинкиназа: роль в регуляции биоактивных сфинголипидных медиаторов воспаления» . Биохимия . 92 (6): 707–15. дои : 10.1016/j.biochi.2010.02.008 . ПМЦ 2878898 . ПМИД 20156522 .
- ^ Браун Д.А., Лондон E (июнь 2000 г.). «Структура и функция мембранных рафтов, богатых сфинголипидами и холестерином» . Журнал биологической химии . 275 (23): 17221–4. дои : 10.1074/jbc.R000005200 . ПМИД 10770957 .
- ^ Футерман А.Х. (декабрь 2006 г.). «Внутриклеточный транспорт сфинголипидов: связь с биосинтезом» . Biochimica et Biophysical Acta (BBA) – Биомембраны . 1758 (12): 1885–92. дои : 10.1016/j.bbamem.2006.08.004 . ПМИД 16996025 .
- ^ ван Меер Г., Лисман К. (июль 2002 г.). «Транспорт сфинголипидов: рафты и транслокаторы» . Журнал биологической химии . 277 (29): 25855–8. дои : 10.1074/jbc.R200010200 . ПМИД 12011105 .
- ^ Веспер Х, Шмельц Э.М., Николова-Каракашян М.Н., Диллехей Д.Л., Линч Д.В., Меррилл А.Х. (июль 1999 г.). «Сфинголипиды в продуктах питания и растущая важность сфинголипидов для питания» . Журнал питания . 129 (7): 1239–50. дои : 10.1093/jn/129.7.1239 . ПМИД 10395583 .
- ^ Хивер, СЛ; Джонсон, Эл.; Лей, RE (июнь 2018 г.). «Сфинголипиды во взаимодействии хозяина и микробов» (PDF) . Современное мнение в микробиологии . 43 : 92–99. дои : 10.1016/j.mib.2017.12.011 . ПМИД 29328957 . S2CID 26181993 .
- ^ Чунг Н., Мао С., Хейтман Дж., Ханнун Ю.А., Обейд Л.М. (сентябрь 2001 г.). «Фитосфингозин как специфический ингибитор роста и импорта питательных веществ у Saccharomyces cerevisiae» . Журнал биологической химии . 276 (38): 35614–21. дои : 10.1074/jbc.m105653200 . ПМИД 11468289 .
- ^ Коварт Л.А., Обейд Л.М. (март 2007 г.). «Дрожжевые сфинголипиды: последние достижения в понимании биосинтеза, регуляции и функции» . Biochimica et Biophysical Acta (BBA) - Молекулярная и клеточная биология липидов . 1771 (3): 421–31. дои : 10.1016/j.bbalip.2006.08.005 . ПМЦ 1868558 . ПМИД 16997623 .
- ^ Диксон RC (май 2008 г.). «Серия тематических обзоров: сфинголипиды. Новое понимание метаболизма и функции сфинголипидов у почкующихся дрожжей» . Журнал исследований липидов . 49 (5): 909–21. doi : 10.1194/jlr.R800003-JLR200 . ПМК 2311445 . ПМИД 18296751 .
- ^ Брайс С.Э., Алфорд К.В., Коварт Л.А. (март 2009 г.). «Модуляция метаболизма сфинголипидов с помощью фосфатидилинозитол-4-фосфатфосфатазы Sac1p посредством регуляции фосфатидилинозитола в Saccharomyces cerevisiae» . Журнал биологической химии . 284 (12): 7588–96. дои : 10.1074/jbc.M808325200 . ПМК 2658053 . ПМИД 19139096 .
- ^ Чен К., Хо Т.С., Лин Г., Тан К.Л., Расбанд М.Н., Беллен Х.Дж. (ноябрь 2016 г.). «Потеря фратаксина активирует путь железо/сфинголипид/PDK1/Mef2 у млекопитающих» . электронная жизнь . 5 . doi : 10.7554/eLife.20732 . ПМК 5130293 . ПМИД 27901468 .
- ^ Чен К., Лин Г., Хелтерман Н.А., Хо Т.С., Ли Т., Ли З., Дюрейн Л., Грэм Б.Х., Джайсвал М., Ямамото С., Расбанд М.Н., Беллен Х.Дж. (июнь 2016 г.). «Потеря фратаксина вызывает токсичность железа, синтез сфинголипидов и активацию Pdk1/Mef2, что приводит к нейродегенерации» . электронная жизнь . 5 . doi : 10.7554/eLife.16043 . ПМЦ 4956409 . ПМИД 27343351 .
- ^ Эсфандиари, Али; Финкельштейн, Дэвид Исаак; Фелькер, Николас Ганс; Радд, Дэвид (15 апреля 2022 г.). «Клинический путь сфинголипидов при болезни Паркинсона: от GCase к открытию интегрированных биомаркеров» . Клетки . 11 (8): 1353. doi : 10.3390/cells11081353 . ISSN 2073-4409 . ПМЦ 9028315 . ПМИД 35456032 .
Внешние ссылки
[ редактировать ]- Сфинголипиды Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- Лаурила, Пиркка-Пекка; и др. (декабрь 2022 г.). «Сфинголипиды накапливаются в старых мышцах, а их уменьшение противодействует саркопении» . Природное старение . 2 (12): 1159–1175. дои : 10.1038/s43587-022-00309-6 . ISSN 2662-8465 . ПМИД 37118545 . S2CID 254819305 .