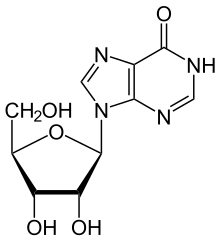
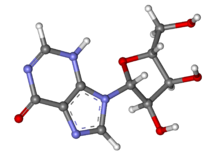
инозин
 | |
 | |
| Клинические данные | |
|---|---|
| AHFS / Drugs.com | Международные названия лекарств |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Метаболизм | Печеночный |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.000.355 |
| Химические и физические данные | |
| Формула | С 10 Н 12 Н 4 О 5 |
| Молярная масса | 268.229 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Инозин – нуклеозид , который образуется, когда гипоксантин присоединяется к рибозному кольцу (также известному как рибофураноза ) посредством β-N9 - гликозидной связи . Он был открыт в 1965 году при анализе РНК-трансферазы. [1] Инозин обычно содержится в тРНК и необходим для правильной трансляции генетического кода в колебательных парах оснований .

Знания о метаболизме инозина привели к прогрессу в иммунотерапии в последние десятилетия. Инозинмонофосфат окисляется ферментом инозинмонофосфатдегидрогеназой с образованием ксантозинмонофосфата , ключевого предшественника пуринового метаболизма. Микофенолята мофетил — антиметаболитный антипролиферативный препарат, который действует как ингибитор инозинмонофосфатдегидрогеназы. Он используется при лечении различных аутоиммунных заболеваний, включая гранулематоз с полиангиитом , поскольку поглощение пурина активно делящимися В-клетками может в 8 раз превышать поглощение нормальными клетками организма, и, следовательно, этот набор лейкоцитов (которые не могут управлять пуриновыми клетками) пути спасения) избирательно воздействует на дефицит пурина, возникающий в результате ингибирования инозинмонофосфатдегидрогеназы (ИМД).
Реакции
[ редактировать ]Аденин превращается в аденозин или инозинмонофосфат (ИМФ), каждый из которых, в свою очередь, превращается в инозин (I), который соединяется с аденином (А), цитозином (С) и урацилом (U). [ нужна ссылка ]
Пуриннуклеозидфосфорилаза интраконвертирует инозин и гипоксантин .
Инозин также является промежуточным звеном в цепи реакций пуриновых нуклеотидов, необходимых для мышечных движений.
Клиническое значение
[ редактировать ]Последующие исследования на людях показали, что добавки инозина не влияют на спортивные результаты. [2] Исследования на животных показали, что инозин обладает нейропротекторными свойствами. Было предложено при травме спинного мозга. [3] и для введения после инсульта , поскольку наблюдения показывают, что инозин вызывает перестройку аксонов. [4]
После приема внутрь инозин метаболизируется в мочевую кислоту, которая, как предполагается, является природным антиоксидантом и поглотителем пероксинитритов , имеющим потенциальную пользу для пациентов с рассеянным склерозом (РС). [5] Пероксинитрит коррелирует с дегенерацией аксонов. [6] В 2003 году в Центре рассеянного склероза Пенсильванского университета было начато исследование, чтобы определить, замедлит ли повышение уровня мочевой кислоты введением инозина прогрессирование рассеянного склероза. [7] Исследование было завершено в 2006 году, но о результатах не сообщили в НИЗ. Последующая публикация намекнула на потенциальную пользу, но размер выборки (16 пациентов) был слишком мал для того, чтобы сделать однозначный вывод. Кроме того, побочным эффектом лечения стало развитие камней в почках у четырех из 16 пациентов. [8]
После завершения II фазы исследований болезни Паркинсона инозин продолжит испытания III фазы. Более ранние исследования показали, что у пациентов с самым высоким уровнем уратов в сыворотке наблюдалось более медленное прогрессирование симптомов Паркинсона. В исследовании используется инозин для повышения уровня уратов у тех, у кого уровень ниже среднего по популяции (6 мг/дл). [9] [10] [11]
Компания Alseres Pharmaceuticals (названная Boston Life Sciences после получения патента) запатентовала использование инозина для лечения инсульта. [12] и исследовал препарат в условиях рассеянного склероза. [13]
В анатомической терапевтической химической классификационной системе он классифицируется как противовирусное средство . [14]
Связывание
[ редактировать ]Инозин является естественным лигандом сайта связывания бензодиазепина на рецепторе ГАМК А. [15]
Биотехнология
[ редактировать ]При разработке праймеров для полимеразной цепной реакции инозин полезен тем, что может соединяться с любым природным основанием. [16] Это позволяет создавать праймеры, охватывающие однонуклеотидный полиморфизм , при этом полиморфизм не нарушает эффективность отжига праймера.
Однако инозин спаривается преимущественно с цитозином (C), и его введение в РНК, например, под действием ADAR , тем самым дестабилизирует двухцепочечную РНК путем замены пар оснований AU на несоответствия IU. [17]
Фитнес
[ редактировать ]Несмотря на отсутствие клинических доказательств того, что инозин улучшает развитие мышц, он остается ингредиентом некоторых фитнес-добавок.
Кормовой стимулятор
[ редактировать ]Также было обнаружено, что инозин сам по себе или в сочетании с определенными аминокислотами является важным стимулятором корма у некоторых видов выращиваемых рыб . Например, инозин и инозин-5-монофосфат являются специфическими стимуляторами питания мальков тюрбо ( Scophthalmus maximus ). [18] и янтарник японский ( Seriola quinqueradiata ). [19] Основной проблемой использования инозина и/или инозин-5-монофосфата в качестве кормовых аттрактантов является их высокая стоимость. Однако их использование может быть экономически оправдано в составе личиночных кормов для личинок морских рыб в ранний период отъема, поскольку общее количество потребляемых кормов относительно невелико.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Шринивасан С., Торрес А.Г., Рибас де Пуплана Л. (апрель 2021 г.). «Инозин в биологии и болезнях» . Гены . 12 (4): 600. doi : 10.3390/genes12040600 . ПМЦ 8072771 . ПМИД 33921764 .
- ^ Керксик CM, Уилборн CD, Робертс MD, Смит-Райан А., Кляйнер С.М., Джагер Р. и др. (август 2018 г.). «Обновление обзора упражнений и спортивного питания ISSN: исследования и рекомендации» . Журнал Международного общества спортивного питания . 15 (1): 38. дои : 10.1186/s12970-018-0242-y . ПМК 6090881 . ПМИД 30068354 .
- ^ Лю Ф., Ю С.В., Яо Л.П., Лю Х.Л., Цзяо XY, Ши М. и др. (июль 2006 г.). «Вторичная дегенерация снижается инозином после травмы спинного мозга у крыс» . Спинной мозг . 44 (7): 421–426. дои : 10.1038/sj.sc.3101878 . ПМИД 16317421 .
- ^ Чен П., Голдберг Д.Е., Колб Б., Лансер М., Беновиц Л.И. (июнь 2002 г.). «Инозин вызывает перестройку аксонов и улучшает поведенческие результаты после инсульта» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (13): 9031–9036. Бибкод : 2002PNAS...99.9031C . дои : 10.1073/pnas.132076299 . ПМК 124418 . ПМИД 12084941 .
- ^ «Мочевая кислота при рассеянном склерозе» . Вебцит. 2018. Архивировано из оригинала 27 октября 2009 г.
- ^ Нейгауз О, Хартунг ХО. «Иммуноопосредованное повреждение, окислительная токсичность и эксайтотоксичность при рассеянном склерозе. Возможности иммунной модуляции и нейропротекции» . Архивировано из оригинала 11 марта 2007 г. Проверено 23 апреля 2006 г.
- ^ Номер клинического исследования NCT00067327 «Лечение рассеянного склероза с использованием безрецептурного инозина» на сайте ClinicalTrials.gov.
- ^ Марковиц С.Э., Спицин С., Циммерман В., Джейкобс Д., Удупа Дж.К., Хупер Д.С., Копровски Х. (июнь 2009 г.). «Лечение рассеянного склероза инозином» . Журнал альтернативной и дополнительной медицины . 15 (6): 619–625. дои : 10.1089/acm.2008.0513 . ПМК 3189001 . ПМИД 19425822 .
- ^ «Безопасность повышения уровня уратов при болезни Паркинсона» . Искатель проб Fox. 2018.
- ^ Номер клинического исследования NCT00833690 «Безопасность повышения уровня уратов при болезни Паркинсона» на сайте ClinicalTrials.gov.
- ^ Куль М.М. (1 сентября 2015 г.). «Испытание инозина обеспечивает финансирование фазы III для изучения влияния на замедление болезни Паркинсона» . Фонд Майкла Дж. Фокса.
- ^ «Boston Life Sciences объявляет о выдаче патента на инозин для лечения травм спинного мозга» . 17 ноября 2003 г. Архивировано из оригинала 3 сентября 2005 г.
- ^ Лу К.Дж. (2009). «Загадка инозина» . Наука-Бизнес ОБМЕН . 2 (29): 1132. doi : 10.1038/scibx.2009.1132 .
- ^ «Индекс ATC/DDD» . Сотрудничающий центр Всемирной организации здравоохранения . Проверено 20 декабря 2017 г.
- ^ Яром М, Тан XW, Ву Э, Карлсон Р.Г., Вандер Вельде Д, Ли Х, Ву Дж (июль 1998 г.). «Идентификация инозина как эндогенного модулятора сайта связывания бензодиазепина ГАМКА-рецепторов». Журнал биомедицинской науки . 5 (4): 274–280. дои : 10.1007/bf02255859 . ПМИД 9691220 .
- ^ Бен-Дов Э., Шапиро О.Г., Сибони Н., Кушмаро А. (ноябрь 2006 г.). «Преимущество использования инозина на 3'-концах универсальных праймеров гена 16S рРНК для изучения микробного разнообразия» . Прикладная и экологическая микробиология . 72 (11): 6902–6906. дои : 10.1128/АЕМ.00849-06 . ПМЦ 1636166 . ПМИД 16950904 .
- ^ Бас Б.Л., Вайнтрауб Х. (декабрь 1988 г.). «Активность раскручивания, которая ковалентно модифицирует двухцепочечный РНК-субстрат». Клетка . 55 (6): 1089–1098. дои : 10.1016/0092-8674(88)90253-х . ПМИД 3203381 . S2CID 11698374 .
- ^ Маки А.М. (1987). «Идентификация вкусовых стимуляторов кормления». Ин Хара Т.Дж. (ред.). Хеморецепция у рыб . Амстердам: Elsevier Scientific Publishing Co., стр. 275–291.
- ^ Такеда М., Такие К., Мацуи К. (1984). «Определение кормовых стимуляторов для молоди угря» . Бюллетень Японского общества научного рыболовства . 50 (4): 645–651. дои : 10.2331/suisan.50.645 .