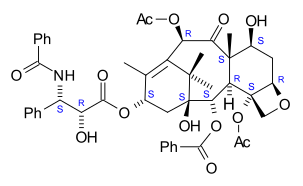
Паклитаксел
Было предложено с белками паклитаксел включить в эту статью связанный . ( Обсудить ) Предлагается с июля 2024 г. |
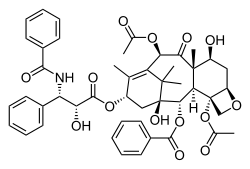 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Таксол, Абраксан и др. |
| Другие имена | ПТХ |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а607070 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | внутривенный |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 6,5% (перорально) [9] |
| Связывание с белками | от 89 до 98% |
| Метаболизм | Печень ( CYP2C8 и CYP3A4 ) |
| Период полувыведения | 5,8 часов |
| Экскреция | Фекальные и мочевые |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.127.725 |
| Химические и физические данные | |
| Формула | С 47 Н 51 Н О 14 |
| Молярная масса | 853.918 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Паклитаксел под торговой маркой Таксол , продаваемый, среди прочего, , представляет собой химиотерапевтический препарат, используемый для лечения рака яичников , рака пищевода , рака молочной железы , рака легких , саркомы Капоши , рака шейки матки и рака поджелудочной железы . [10] Его вводят внутривенно . [10] Существует также состав, связанный с альбумином . [10]
Общие побочные эффекты включают выпадение волос , угнетение функции костного мозга , онемение , аллергические реакции , мышечные боли и диарею . [10] Другие побочные эффекты включают проблемы с сердцем, повышенный риск инфекций и воспаление легких . [10] Есть опасения, что использование во время беременности может вызвать врожденные дефекты . [11] [10] Паклитаксел относится к группе таксанов . [12] Он действует путем вмешательства в нормальную функцию микротрубочек во время деления клеток . [10]
Паклитаксел был выделен в 1971 году из тиса тихоокеанского и одобрен для медицинского применения в 1993 году. [13] [14] Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . [15] Он был получен из предшественников и посредством клеточной культуры . [14]
Медицинское использование
[ редактировать ]Паклитаксел одобрен в Великобритании для лечения рака яичников, молочной железы, легких, мочевого пузыря , простаты , меланомы , пищевода и других типов солидных опухолей, а также саркомы Капоши . [16]
Он рекомендован в рекомендациях Национального института здравоохранения и совершенствования медицинской помощи (NICE) от июня 2001 г. для лечения немелкоклеточного рака легких у пациентов, не подходящих для радикального лечения, а также для лечения первой и второй линии рака яичников. В сентябре 2001 года NICE рекомендовал паклитаксел для лечения распространенного рака молочной железы после неэффективности антрациклической химиотерапии , но его использование в качестве первой линии должно быть ограничено клиническими испытаниями. В сентябре 2006 года NICE рекомендовал не использовать паклитаксел при адъювантном лечении раннего рака молочной железы с поражением лимфоузлов. [17]
По состоянию на 2018 год [update], он одобрен в США для лечения рака молочной железы, поджелудочной железы, яичников, саркомы Капоши и немелкоклеточного рака легких. [18] [19]
Подобные соединения
[ редактировать ]Связанный с альбумином паклитаксел (торговая марка Abraxane , также называемый наб-паклитаксел) представляет собой альтернативную форму, в которой паклитаксел связан с наночастицами альбумина . Большая часть клинической токсичности паклитаксела связана с растворителем Cremophor EL, в котором он растворяется при доставке. [20]
Компания Abraxis BioScience разработала Abraxane, в котором паклитаксел связан с альбумином, в качестве агента доставки, альтернативного методу доставки часто токсичных растворителей. Он был одобрен FDA в январе 2005 года для лечения рака молочной железы после неэффективности комбинированной химиотерапии по поводу метастатического заболевания или рецидива в течение шести месяцев после адъювантной химиотерапии. [21] С тех пор он был одобрен для лечения местно-распространенного или метастатического немелкоклеточного рака легких, а метастатической аденокарциномы поджелудочной железы . также [22]
Синтетические подходы к производству паклитаксела привели к разработке доцетаксела . Доцетаксел имеет те же клинические применения, что и паклитаксел, и продается под торговой маркой Таксотер.
Таксаны , в том числе паклитаксел, 10-деацетилбаккатин III , баккатин III , паклитаксел С и 7-эпипаклитаксел, были обнаружены в листьях и скорлупе лещины . [23] Обнаружение этих соединений в скорлупе, которая считается выброшенным материалом и массово производится многими предприятиями пищевой промышленности, представляет интерес для будущей доступности паклитаксела. [24]
рестеноз
[ редактировать ]Паклитаксел применяют в качестве антипролиферативного средства для профилактики рестеноза (рецидивного сужения) коронарных и периферических стентов ; при локальной доставке к стенке артерии покрытие паклитакселом ограничивает рост неоинтимы (рубцовой ткани) внутри стентов. [25] паклитакселом Стенты с лекарственным покрытием для размещения в коронарных артериях продаются под торговой маркой Taxus компанией Boston Scientific в США. Также доступны стенты с лекарственным покрытием паклитакселом для установки в бедренно-подколенную артерию.
Побочные эффекты
[ редактировать ]Общие побочные эффекты включают тошноту и рвоту, потерю аппетита , изменение вкуса , истончение или ломкость волос, боль в суставах рук или ног, продолжающуюся два-три дня, изменение цвета ногтей и покалывание в руках или ногах. пальцы ног. [26] Более серьезные побочные эффекты, такие как необычные синяки или кровотечения, боль, покраснение или отек в месте инъекции, ладонно-ногий синдром , изменение нормального режима работы кишечника более чем на два дня, лихорадка, озноб, кашель, боль в горле , затруднение глотания , головокружение. , Также могут возникнуть одышка сильное истощение, кожная сыпь , покраснение лица , женское бесплодие из-за повреждения яичников и боль в груди . [26] Также может возникнуть нейропатия . [10]
Дексаметазон назначают перед инфузией паклитаксела для смягчения некоторых побочных эффектов. [27]
Ряд этих побочных эффектов связан с используемым наполнителем Cremophor EL, полиоксиэтилированным касторовым маслом . Аллергия на циклоспорин , тенипозид и другие препараты, содержащиеся в полиоксиэтилированном касторовом масле, может увеличить риск побочных реакций на паклитаксел. [28]
Механизм действия
[ редактировать ]
Паклитаксел — один из нескольких цитоскелетных препаратов , воздействующих на тубулин . Клетки, обработанные паклитакселом, имеют дефекты сборки митотического веретена , сегрегации хромосом и деления клеток . В отличие от других препаратов, нацеленных на тубулин, таких как колхицин , которые ингибируют сборку микротрубочек , паклитаксел стабилизирует полимер микротрубочек и защищает его от разборки. Таким образом, хромосомы не могут достичь конфигурации метафазного веретена. Это блокирует прогрессирование митоза , а длительная активация митотической контрольной точки запускает апоптоз или возврат к G0-фазе клеточного цикла без клеточного деления. [29] [30]
Способность паклитаксела ингибировать функцию веретена обычно объясняется его подавлением динамики микротрубочек. [31] но другие исследования показали, что подавление динамики происходит при концентрациях ниже, чем те, которые необходимы для блокирования митоза. В более высоких терапевтических концентрациях паклитаксел, по-видимому, подавляет отслоение микротрубочек от центросом - процесс, который обычно активируется во время митоза. [32] Паклитаксел связывается с субъединицами бета-тубулина микротрубочек. [33]
Химия
[ редактировать ]Номенклатура скелете из паклитаксела построена на тетрациклическом 17 атомов. Всего имеется 11 стереоцентров. Активным стереоизомером является (-)-паклитаксел (показан здесь).
Производство
[ редактировать ]
Обработка коры
[ редактировать ]
С 1967 по 1993 год почти весь произведенный паклитаксел производился из коры тихоокеанского тиса Taxus brevifolia , сбор которого убивает дерево. [34] Используемые процессы были потомками оригинального метода изоляции Монро Уолла и Мансуха Вани ; США к 1987 году Национальный институт рака (NCI) заключил контракт с Hauser Chemical Research из Боулдера, штат Колорадо , на обработку коры в масштабах, необходимых для испытаний фазы II и III. [ нужна ссылка ] Хотя размер дикой популяции тихоокеанского тиса и величина возможного спроса на паклитаксел были неопределенными, было ясно, что альтернативный, устойчивый источник натурального продукта потребуется . Первоначальные попытки расширить источники поставок использовали хвою дерева или материал других родственных видов Taxus , в том числе культивируемых. [ нужна ссылка ] но эти попытки были оспорены относительно низкой и часто сильно варьирующейся урожайностью. В начале 1990-х годов, что совпало с возросшей чувствительностью к экологии лесов северо-западной части Тихого океана , паклитаксел был экстрагирован в клинически полезных масштабах из этих источников. [35]
Полусинтез
[ редактировать ]Одновременно с этим, начиная с конца 1970-х годов, химики-синтетики в США и Франции заинтересовались паклитакселом. [ нужна ссылка ] Как уже отмечалось, к 1992 г. предпринимались обширные усилия по полному синтезу паклитаксела, усилия, мотивированные желанием добиться нового химического понимания, а не достижения практического коммерческого производства. Напротив, французская группа Пьера Потье из Национального центра научных исследований (CNRS) рассмотрела вопрос общего выхода процесса, показав, что можно выделить относительно большие количества соединения 10-деацетилбаккатина из тиса европейского Taxus. baccata , который рос на территории кампуса CNRS и чьи иглы были доступны в большом количестве. [ нужна ссылка ] Благодаря своей структуре 10-деацетилбаккатин рассматривался как жизнеспособный исходный материал для короткого полусинтеза с получением паклитаксела. К 1988 году Пуатье и его коллеги опубликовали полусинтетический путь от игл европейского тиса до паклитаксела. [36]
Однако по мнению NCI, даже этот путь непрактичен. [ нужна ссылка ] Группа Роберта А. Холтона также выбрала практический путь производства полусинтетических продуктов; к концу 1989 года группа Холтона разработала полусинтетический путь получения паклитаксела с удвоенным выходом по сравнению с процессом Потье. [37] Главным нововведением было «соединение Одзимы-Холтона», метод раскрытия кольца, независимо открытый Холтоном и Одзимой. [38] Университет штата Флорида , где работал Холтон, подписал соглашение с Bristol-Myers Squibb (BMS) о лицензировании их полусинтеза и будущих патентов. [ нужна ссылка ] В 1992 году Холтон запатентовал улучшенный процесс с выходом 80%, а BMS взяла этот процесс на себя и начала производить паклитаксел в Ирландии из 10-деацетилбаккатина, выделенного из хвои тиса европейского. [ нужна ссылка ] В начале 1993 года BMS объявила, что к концу 1995 года прекратит использовать кору тихоокеанского тиса, что фактически положило конец экологическим спорам по поводу ее использования. [ нужна ссылка ] Это объявление также подтвердило их обязательство разработать альтернативный маршрут поставок, данное NCI в заявке на соглашение о совместных исследованиях и разработках (CRADA) от 1989 года.
По состоянию на 2013 год BMS использовала полусинтетический метод с использованием иголок тиса европейского для производства паклитаксела. [39] Еще одна компания, работавшая с BMS до 2012 года, [40] Phyton Biotech, Inc. использует технологию ферментации растительных клеток (PCF). [41] Культивируя определенную Taxus клеточную линию в ферментационных резервуарах, им больше не требуется постоянный источник материала с реальных плантаций тиса. [42] Затем паклитаксел улавливается непосредственно из суспензионного бульона смолой, что позволяет концентрировать его до высокообогащенного порошка, содержащего около 40% паклитаксела. Затем соединение очищают с помощью одной хроматографической стадии с последующей кристаллизацией . [43] По сравнению с методом полусинтеза, PCF устраняет необходимость использования многих опасных химикатов и экономит значительное количество энергии. [44]
В 1993 году паклитаксел был обнаружен как натуральный продукт у Taxomyces andreanae , недавно описанного эндофитного гриба, живущего на тисовом дереве. [45] С тех пор он был обнаружен у ряда других эндофитных грибов, включая Nodulisporium sylviforme . [ нужна ссылка ] Alternaria такси , Cladosporium cladosporioides MD2, Metarhizium anisopliae , Aspergillus candidus MD3, Mucor rouxianus , Chaetomella raphigera , Phyllosticta tabernaemontanae , Phomopsis , Pestalotiopsis pauciteta , Phyllosticta citricarpa , Podocarpus sp., Fusarium solani , Pestalotiopsis Terminaliae , Pestalotiopsis breviseta , Botryodiplodia theobromae , Gliocladium sp. , Alternaria alternata var. monosporus , Cladosporium cladosporioides , Nigrospora sp. и Песталотиопсис разноцветный . Однако имеются противоречивые данные о его продукции эндофитами, а другие исследования показали, что независимое производство маловероятно. [46] [47]
Биосинтез
[ редактировать ]
Таксол представляет собой тетрациклический дитерпен , и биосинтез дитерпенов начинается с удлинения молекулы FPP за счет добавления молекулы IPP с образованием геранилгеранилдифосфата ( GGPP ). [48] Биосинтез таксола состоит из девятнадцати стадий. [49] Эти 19 этапов можно рассматривать в несколько этапов, причем первым этапом является формирование скелета таксана, который затем подвергается серии оксигенаций. После оксигенирования промежуточного соединения происходят два ацетилирования и бензоилирование. Считается, что оксигенация ядра таксана происходит на C5 и C10, C2 и C9, C13 с последующим C7 и гидроксилированием C1 на более позднем этапе этого пути. На более позднем этапе окисление по C9 образует кетоновую функциональную группу и оксетан, образуя промежуточный баккатин III. Заключительные этапы пути включают образование боковой цепи C13, которая присоединяется к баккатину III. [50] Биосинтез таксола более подробно проиллюстрирован на рисунке, причем все этапы 1–7 происходят с помощью фермента таксадиенсинтазы (TS на рисунке). Биосинтез таксола начинается с потери E,E,E-GGPP пирофосфата по механизму SN1 (шаг 1 на рисунке). Двойная связь атакует катион посредством электрофильного присоединения, образуя третичный катион и создавая первое замыкание кольца (этап 2). Происходит еще одна электрофильная атака, приводящая к дальнейшей циклизации структуры за счет создания первого 6-членного кольца и создания еще одного третичного катиона (этап 3). Происходит внутримолекулярный перенос протона, атакующий катион вертициллила (этап 4) и образующий двойную связь, в результате чего образуется третичный катион. На этапе 5 происходит электрофильная циклизация, и внутримолекулярный перенос протона атакует таксенильный катион (этап 6). При этом образуется промежуточный продукт конденсированной кольцевой структуры, известный как таксадиен. Затем таксадиен подвергается серии из 10 окислений посредством НАДФН , образуя промежуточный таксадиен-5α-ацетокси-10β-ол (несколько этапов далее на рисунке). Происходит серия гидроксилирований и этерификаций с образованием промежуточного продукта 10-деацетилбаккатина III, который подвергается дальнейшей серии этерификаций и гидроксилированию боковой цепи. [48] В конечном итоге получается таксол.
Полный синтез
[ редактировать ]
К 1992 году по меньшей мере тридцать академических исследовательских групп по всему миру работали над полным синтезом этого натурального продукта , причем синтез осуществлялся из простых натуральных продуктов и других легкодоступных исходных материалов. [51] Эта попытка тотального синтеза была мотивирована в первую очередь желанием добиться нового понимания химии, а не ожиданием практического коммерческого производства паклитаксела. Первыми лабораториями, завершившими полный синтез из гораздо менее сложных исходных материалов, были исследовательские группы Роберта А. Холтона , чья первая статья была принята к публикации , и К. К. Николау, чья первая статья появилась в печати (автор: неделю, 7 февраля 1994 г.). Хотя представление Холтона предшествовало представлению Николау на месяц (21 декабря 1993 г. против 24 января 1994 г.), [52] близкое совпадение публикаций, возникших в результате каждой из этих масштабных многолетних усилий - 11–18 авторов фигурировали в каждой публикации за февраль 1994 года, - привело к тому, что окончание гонки было названо «ничья». [53] или «фотофиниш», [51] хотя каждая группа утверждала, что их синтетическая стратегия и тактика были лучше. [53]
По состоянию на 2006 год еще пять исследовательских групп сообщили о полном синтезе паклитаксела: Wender et al. в 1997 г. и Кувадзима и др. и Мукаяма и др. в 1998 г. с дальнейшим линейным синтезом , а Данишефский и др. в 1996 г. и Такахаши и др. в 2006 году с дальнейшим конвергентным синтезом . [ нужно обновить ] На тот момент все стратегии были направлены на получение ядра типа 10-деацетилбаккатина, содержащего кольцевую систему ABCD, с последующим, как правило, на последней стадии добавлением «хвоста» к 13- гидроксильной группе . [51]
Хотя «политический климат вокруг [паклитаксела] и [тихоокеанского тиса] в начале 1990-х годов... помог укрепить связь между полным синтезом и проблемой поставок [паклитаксела]», и хотя деятельность по полному синтезу была необходима для изучения Взаимосвязь между структурой и активностью паклитаксела посредством создания аналогов для тестирования, усилия по полному синтезу никогда не рассматривались «как серьезный коммерческий путь» для получения значительных количеств натурального продукта для медицинских испытаний или терапевтического использования. [54]
История
[ редактировать ]Открытие паклитаксела началось в 1962 году в результате программы скрининга, финансируемой NCI. [14] Несколько лет спустя он был выделен из коры тиса тихоокеанского Taxus brevifolia , отсюда и название «таксол». [14]
Открытие было сделано Монро Э. Уолл и Мансухом К. Вани в Исследовательском институте Треугольника , Парк Исследовательского треугольника , Северная Каролина, в 1971 году. [55] Эти ученые выделили натуральный продукт из коры тихоокеанского тиса, определили его структуру и назвали его «таксол» и организовали его первое биологическое тестирование. [56] Затем это соединение было коммерчески разработано компанией BMS, у которой было непатентованное название «паклитаксел». [ нужна ссылка ]
Программа скрининга растений
[ редактировать ]В 1955 году NCI в США создал Национальный центр химиотерапии рака (CCNSC), который выступал в качестве общественного центра скрининга противораковой активности соединений, предоставленных внешними учреждениями и компаниями. [57] Хотя большинство проверенных соединений имели синтетическое происхождение, один химик, Джонатан Хартвелл, который работал там с 1958 года, имел опыт работы с соединениями, полученными из натуральных продуктов, и начал операцию по проверке растений. [58]
После нескольких лет неформальных договоренностей, в июле 1960 года, NCI поручил ботаникам Министерства сельского хозяйства США (USDA) собирать образцы примерно 1000 видов растений в год. [59] 21 августа 1962 года один из этих ботаников, Артур С. Барклай, собрал кору с одного тихоокеанского тиса в лесу к северу от города Паквуд, штат Вашингтон , в рамках четырехмесячной поездки по сбору материала из более чем 200 различных растений. разновидность. один из образцов дерева оказался цитотоксичным . Затем материал был обработан рядом специализированных субподрядчиков CCNSC, и 22 мая 1964 года в ходе клеточного анализа [60]
Соответственно, в конце 1964 или начале 1965 года лаборатория фракционирования и выделения под руководством Монро Э. Уолла в Исследовательском Трейангл-Парке, Северная Каролина, начала работу над свежими образцами Taxus , выделив активный ингредиент в сентябре 1966 года и объявив о своих открытиях на конференции в апреле 1967 года. Американского химического общества Заседание в Майами-Бич . [61] В июне 1967 года они назвали чистое соединение таксолом. [60] Уолл и его коллега Вани опубликовали свои результаты, включая химическую структуру, в 1971 году. [62]
NCI продолжал заказывать работы по сбору большего количества коры Taxus и выделению растущего количества таксола. К 1969 году из почти 1200 кг (2600 фунтов) коры было выделено 28 кг (62 фунта) сырого экстракта, хотя в конечном итоге это дало только 10 г (0,35 унции) чистого материала. [63] но в течение нескольких лет NCI не использовало это соединение. В 1975 году было показано, что он активен в другой in vitro системе ; два года спустя новый руководитель отдела рассмотрел данные и, наконец, рекомендовал перейти к следующему этапу процесса открытия таксола. [64] Это потребовало увеличения количества очищенного таксола до 600 г (21 унции), и в 1977 году был сделан дополнительный запрос на 7000 фунтов (3200 кг) коры.
В 1978 году два исследователя NCI опубликовали отчет, показывающий, что таксол умеренно эффективен при лечении мышей с лейкемией. [65] была показана эффективность таксола В ноябре 1978 г. в исследованиях ксенотрансплантатов . [66] Между тем, таксол стал хорошо известен в клеточной биологии, а также в онкологических сообществах, после публикации в начале 1979 года Сьюзан Б. Хорвиц , молекулярного фармаколога из Медицинского колледжа Альберта Эйнштейна , показывающей, что таксол обладает ранее неизвестным механизмом. действия, включающего стабилизацию микротрубочек. В сочетании с проблемами с формулировкой этот возросший интерес со стороны исследователей означал, что к 1980 году NCI предусмотрел необходимость сбора 20 000 фунтов (9 100 кг) коры. [67] Токсикологические исследования на животных были завершены к июню 1982 года, а в ноябре NCI подал заявку на получение IND, необходимого для начала клинических испытаний на людях. [67]
Ранние клинические испытания, поставка и перевод в BMS
[ редактировать ]Клинические испытания I фазы начались в апреле 1984 года, а решение о начале испытаний II фазы было принято годом позже. [68] Для этих более крупных испытаний потребовалось больше коры, и был начат сбор еще 12 000 фунтов, что позволило начать II фазу испытаний к концу 1986 года. Но к тому времени было признано, что спрос на таксол может быть значительным и что более 60 000 фунтов коры может потребоваться как минимум. Эта беспрецедентно большая сумма впервые привлекла внимание к экологическим опасениям по поводу воздействия на популяцию тиса, поскольку местные политики и лесники выразили беспокойство по поводу программы. [69]
Первый публичный отчет об исследовании фазы II в мае 1988 года показал многообещающие эффекты при меланоме и рефрактерном раке яичников. [70] На данный момент Гордон Крэгг из отдела натуральных продуктов Национального института рака подсчитал, что синтез достаточного количества таксола для лечения всех случаев рака яичников и меланомы в США потребует уничтожения 360 000 деревьев ежегодно. Впервые серьезное внимание было уделено проблеме снабжения. [69] Из-за практического и, в частности, финансового масштаба необходимой программы, NCI решил искать сотрудничества с фармацевтической компанией и в августе 1989 года опубликовал Соглашение о совместных исследованиях и разработках (CRADA), предложив свои текущие запасы и поставки. от текущих запасов коры и права собственности на собранные данные до компании, готовой предоставить средства для сбора дальнейшего сырья, выделения таксола и финансирования значительной части клинических испытаний. По словам Гудмана и Уэлша, авторов обширной научной книги о таксоле, «NCI думал не о сотрудничестве, ... а о передаче таксола (и связанных с ним проблем)». [69]
Хотя предложение было широко разрекламировано, на CRADA откликнулись только четыре компании, в том числе американская фирма Bristol-Myers Squibb (BMS),которая была выбрана в качестве партнера в декабре 1989 года. Выбор BMS позже стал спорным и стал предметом слушаний в Конгрессе в 1991 и 1992 годах. Хотя кажется очевидным, что у NCI не было другого выбора, кроме как искать коммерческого партнера, были также разногласия по поводу условия сделки, что в конечном итоге привело к появлению отчета Главного бухгалтерского управления в 2003 году, в котором был сделан вывод о том, что НИЗ не смог обеспечить соотношение цены и качества. [71] В рамках соглашений CRADA с Министерством сельского хозяйства США и Министерством внутренних дел компания Bristol-Myers Squibb получила эксклюзивное право первого отказа на все федеральные поставки Taxus brevifolia .Этот эксклюзивный контракт вызвал некоторую критику за предоставление BMS « монополии на рак ». [72] Через восемнадцать месяцев после CRADA компания BMS подала заявку на новое лекарство (NDA), которая получила одобрение FDA в самом конце 1992 года. [69] Хотя на это соединение не было патента, положения Закона Ваксмана-Хэтча предоставили Bristol-Myers Squibb эксклюзивные права на маркетинг на пять лет.
В 1990 году компания BMS подала заявку на регистрацию товарного знака таксола как Taxol(R) . Это утверждение было неоднозначно одобрено в 1992 году. В то же время паклитаксел заменил таксол в качестве непатентованного ( МНН ) названия соединения. Критики, в том числе журнал Nature , утверждали, что название таксол использовалось более двух десятилетий и в более чем 600 научных статьях, и предположили, что товарный знак не должен был быть присужден и BMS должна отказаться от своих прав на него. [73] BMS утверждает, что изменение названия вызовет путаницу среди онкологов и, возможно, поставит под угрозу здоровье пациентов. BMS продолжает защищать свои права на имя в судах. [74] BMS также подверглась критике за искажение фактов со стороны Гудмана и Уолша, которые цитируют отчет компании, в котором говорится: «Только в 1971 году… испытания… позволили выделить паклитаксел, первоначально описанный как «соединение 17». [75] Эта цитата, строго говоря, точна: возражение, по-видимому, состоит в том, что она ошибочно игнорирует объяснение того, что именно ученый, проводивший выделение, назвал соединение таксолом и что оно не упоминалось каким-либо другим образом в течение более двадцати лет. Годовой объем продаж достиг своего пика в 2000 году, достигнув долларов США 1,6 миллиарда ; паклитаксел теперь доступен в непатентованной форме.
Общество и культура
[ редактировать ]Юридический статус
[ редактировать ]Паклитаксел был одобрен для медицинского применения в Европейском Союзе в 2008 году. [5]
В ноябре 2023 года Комитет по лекарственным средствам для применения человеком (CHMP) Европейского агентства по лекарственным средствам принял положительное заключение, рекомендовав выдачу регистрационного удостоверения на лекарственный препарат Наверуклиф, предназначенный для лечения метастатического рака молочной железы, метастатической аденокарциномы поджелудочной железы и немелкоклеточного рака легких. [5] Заявителем данного лекарственного препарата является Accord Healthcare SLU. [5]
В мае 2024 года CHMP принял положительное заключение, рекомендовав выдать регистрационное удостоверение на лекарственный препарат Апексельсин, предназначенный для лечения метастатического рака молочной железы, метастатической аденокарциномы поджелудочной железы и немелкоклеточного рака легких. [6] Заявителем данного лекарственного препарата является компания WhiteOak Pharmaceutical BV. [6]
Экономика
[ редактировать ]По состоянию на 2006 год [update], затраты Национальной службы здравоохранения на одного пациента с ранним раком молочной железы, при условии четырех циклов лечения, составили около 4000 фунтов стерлингов (около 6000 долларов США). [76]
Исследовать
[ редактировать ]кофеин Предполагается, что ингибирует индуцированный паклитакселом апоптоз в клетках колоректального рака. [77]
В 2016 году опухолевые клетки мышей с множественной лекарственной устойчивостью in vitro обрабатывали паклитакселом, заключенным в экзосомы . Дозы на 98% меньшие, чем обычные, имели тот же эффект. Кроме того, экзосомы, помеченные красителем, смогли маркировать опухолевые клетки, что потенциально помогает в диагностике. [78] [79]
Помимо прямого клинического применения, паклитаксел также широко используется в биологических и биомедицинских исследованиях в качестве стабилизатора микротрубочек . В целом, in vitro анализы с участием микротрубочек, такие как анализы подвижности, основаны на использовании паклитаксела для поддержания целостности микротрубочек в отсутствие различных нуклеирующих факторов и других стабилизирующих элементов, обнаруженных в клетке. Например, его используют для испытаний in vitro лекарств, целью которых является изменение поведения моторных белков микротрубочек , или для исследований мутантных моторных белков.
Паклитаксел также использовался in vitro для ингибирования фибрилляции инсулина . В молярном соотношении 10:1 (инсулин:паклитаксел) он подавлял фибрилляцию инсулина примерно на 70%. Результаты изотермической титровальной калориметрии (ИТК) показали спонтанную тенденцию паклитаксела взаимодействовать с инсулином через водородные связи и силы Ван дер Ваала . [80] Ингибирующая роль паклитаксела объясняется его влиянием на коллоидную стабильность белкового раствора, поскольку было замечено, что паклитаксел ингибировал фибрилляцию лизоцима , индуцируя образование олигомерных промежуточных продуктов «вне пути», что впоследствии увеличивало коллоидную стабильность. [81]
используется для исследований in vivo Паклитаксел иногда также . Его можно скармливать тестируемым организмам, таким как плодовые мухи , или вводить в отдельные клетки, чтобы ингибировать разборку микротрубочек или увеличивать количество микротрубочек в клетке. Паклитаксел индуцирует ремиелинизацию у демиелинизирующих мышей in vivo [82] и ингибирует пептидиларгининдеиминазу человека 2 (hPAD2) in vitro через боковую цепь метилового эфира . [83] В 1999 году компания Angiotech Pharmaceuticals Inc. начала II фазу клинических испытаний мицеллярного паклитаксела для лечения вторично-прогрессирующего рассеянного склероза . [84] но в 2002 году сообщили, что результаты не показали статистической значимости. [85]
Дополнительные изображения
[ редактировать ]- заполняющая пространство Модель паклитаксела,
- Модель вращающейся молекулы паклитаксела
- Кристаллическая структура паклитаксела
- Общая зарядовая поверхность таксола. Минимальная энергетическая конформация.
Ссылки
[ редактировать ]- ^ «Использование паклитаксела во время беременности» . Наркотики.com . 24 января 2019 года. Архивировано из оригинала 3 декабря 2020 года . Проверено 19 мая 2020 г.
- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ «Таксол (паклитаксел) для инъекций» . ДейлиМед . Проверено 28 июля 2024 г.
- ^ «Абраксан-паклитаксел для инъекций, порошок лиофилизированный для приготовления суспензии» . ДейлиМед . 31 октября 2022 г. Проверено 28 июля 2024 г.
- ^ Jump up to: а б с «Апексельсин ЭПАР» . Европейское агентство по лекарственным средствам . 30 мая 2024 г. Проверено 31 мая 2024 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ «Апексельсин ПИ» . Союзный реестр лекарственных средств . 26 июля 2024 г. Проверено 28 июля 2024 г.
- ^ Пельтье С., Огер Ж.М., Лагарс Ф., Куэ В., Бенуа Ж.П. (июнь 2006 г.). «Повышенная биодоступность паклитаксела при пероральном приеме после введения липидных нанокапсул, содержащих паклитаксел». Фармацевтические исследования . 23 (6): 1243–1250. дои : 10.1007/s11095-006-0022-2 . ПМИД 16715372 . S2CID 231917 .
- ^ Jump up to: а б с д и ж г час «Паклитаксел» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 14 сентября 2017 года . Проверено 2 января 2015 г.
- ^ Бервейлер П., Мир О (2012). «Таксаны во время беременности: вероятно, безопасны, но их еще предстоит оптимизировать» . Онкология . 83 (4): 239–240. дои : 10.1159/000341820 . ПМИД 22907122 .
- ^ Чанг А.Е., Ганц П.А., Хейс Д.Ф., Кинселла Т., Пасс Х.И., Шиллер Дж.Х. и др. (2007). Онкология: научно обоснованный подход . Springer Science & Business Media. п. 34. ISBN 9780387310565 . Архивировано из оригинала 21 декабря 2016 года.
- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 512. ИСБН 9783527607495 . Архивировано из оригинала 21 декабря 2016 года.
- ^ Jump up to: а б с д «Таксол (НСК 125973)» . Национальный институт рака. Архивировано из оригинала 5 сентября 2015 года . Проверено 14 февраля 2016 г. Машина обратного пути
- ^ Всемирная организация здравоохранения (2019). Модельный список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г. Женева: Всемирная организация здравоохранения. hdl : 10665/325771 . ВОЗ/MVP/EMP/IAU/2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Сэвилл М.В., Литзау Дж., Плуда Дж.М., Фейерштейн И., Одом Дж., Уилсон В.Х. и др. (июль 1995 г.). «Лечение ВИЧ-ассоциированной саркомы Капоши паклитакселом» . Ланцет (Представлена рукопись). 346 (8966): 26–28. дои : 10.1016/S0140-6736(95)92654-2 . ПМИД 7603142 . S2CID 44624033 . Архивировано из оригинала 26 июня 2019 года . Проверено 28 октября 2018 г.
- ^ «Британский национальный формуляр» . Архивировано из оригинала 14 марта 2020 года . Проверено 7 августа 2007 г.
- ^ «Паклитаксел, белково-связанная суспензия» . Паклитаксел, белковосвязанная суспензия . Рак.Орг. 6 января 2015 года . Проверено 24 января 2015 г. [ постоянная мертвая ссылка ]
- ^ Информация о продукте: инъекции таксола IV, инъекции паклитаксела IV. Компания Bristol-Myers Squibb, Принстон, Нью-Джерси, 2013 г. Доступ по адресу https://www.accessdata.fda.gov/drugsatfda_docs/label/2015/020262s051lbl.pdf . Архивировано 10 февраля 2017 г. в Wayback Machine 4 октября 2018 г.
- ^ Гелдерблом Х., Вервей Дж., Нутер К., Спарребум А. (сентябрь 2001 г.). «Кремофор EL: недостатки и преимущества выбора носителя для приготовления лекарств». Европейский журнал рака . 37 (13): 1590–1598. дои : 10.1016/S0959-8049(01)00171-X . ПМИД 11527683 .
- ^ « Информация о препарате Abraxane, заархивированная 26 мая 2005 г. в Wayback Machine ». Управление по контролю за продуктами и лекарствами . 7 января 2005 г. Проверено 9 марта 2007 г.
- ^ Информация о продукте: суспензия ABRAXANE® для внутривенных инъекций, суспензия для внутривенных инъекций частиц паклитаксела, связанных с белком. Celgene Corporation (согласно FDA), Саммит, Нью-Джерси, 2018 г. Доступ по адресу https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/021660s045lbl.pdf . Архивировано 26 июня 2019 г. в Wayback Machine 4 октября 2018 г.
- ^ Оттаджио Л., Бестозо Ф., Армиротти А., Бальби А., Дамонте Г., Маццеи М. и др. (январь 2008 г.). «Таксаны из ракушек и листьев Corylus avellana». Журнал натуральных продуктов . 71 (1): 58–60. дои : 10.1021/np0704046 . ПМИД 18163585 .
- ^ Чжан С., Инь Г (2022). «Безопасность покрытых паклитакселом устройств в бедренно-подколенных артериях: систематический обзор и метаанализ» . ПЛОС ОДИН . 17 (10): e0275888. Бибкод : 2022PLoSO..1775888Z . дои : 10.1371/journal.pone.0275888 . ПМЦ 9560511 . ПМИД 36227807 .
- ^ Хелдман А.В., Ченг Л., Дженкинс Г.М., Хеллер П.Ф., Ким Д.В., Уэр М. и др. (май 2001 г.). «Покрытие стента паклитакселом ингибирует неоинтимальную гиперплазию через 4 недели на свиной модели коронарного рестеноза» . Тираж . 103 (18): 2289–2295. дои : 10.1161/01.CIR.103.18.2289 . ПМИД 11342479 .
- ^ Jump up to: а б Абу-Дония М (5 февраля 2015 г.). Токсикология млекопитающих . Джон Уайли и сыновья. п. 626. ИСБН 978-1-118-68285-2 .
- ^ Хоскинс В.Дж. (2005). Принципы и практика гинекологической онкологии . Липпинкотт Уильямс и Уилкинс. п. 531. ИСБН 978-0-7817-4689-2 .
- ^ " «Паклитаксел для инъекций» . Медлайн Плюс . Национальная медицинская библиотека США. Архивировано из оригинала 12 февраля 2010 года.
- ^ Бхарадвадж Р., Ю Х (март 2004 г.). «Контрольная точка веретена, анеуплоидия и рак». Онкоген . 23 (11): 2016–2027. дои : 10.1038/sj.onc.1207374 . ПМИД 15021889 . S2CID 11114877 .
- ^ Брито Д.А., Ян З., Ридер К.Л. (август 2008 г.). «Микротрубочки не способствуют митотическому проскальзыванию, когда контрольная точка сборки веретена не может быть удовлетворена» . Журнал клеточной биологии . 182 (4): 623–629. дои : 10.1083/jcb.200805072 . ПМК 2518701 . ПМИД 18710927 .
- ^ Джордан, Массачусетс, Уилсон Л. (апрель 2004 г.). «Микротрубочки как мишень для противораковых препаратов». Обзоры природы. Рак . 4 (4): 253–265. дои : 10.1038/nrc1317 . ПМИД 15057285 . S2CID 10228718 .
- ^ Гангули А., Ян Х., Кабрал Ф. (ноябрь 2010 г.). «Паклитаксел-зависимые клеточные линии обнаруживают новую лекарственную активность» . Молекулярная терапия рака . 9 (11): 2914–2923. дои : 10.1158/1535-7163.MCT-10-0552 . ПМЦ 2978777 . ПМИД 20978163 .
- ^ Лёве Дж., Ли Х., Даунинг К.Х., Ногалес Э. (ноябрь 2001 г.). «Уточненная структура альфа-бета-тубулина при разрешении 3,5 А» . Журнал молекулярной биологии . 313 (5): 1045–1057. дои : 10.1006/jmbi.2001.5077 . ПМИД 11700061 . Архивировано из оригинала 22 января 2021 года . Проверено 29 августа 2020 г.
- ^ Герсманн Х., Олдред Дж. (10 ноября 2011 г.). «Лекарственное дерево, используемое в химиотерапевтических препаратах, находится на грани исчезновения» . Хранитель . Архивировано из оригинала 16 февраля 2017 года . Проверено 15 февраля 2017 г. .
- ^ Гудман и Уолш 2001 , стр. 172–5.
- ^ Гудман и Уолш 2001 , стр. 100–1.
- ^ Холтон Р.А., Бидигер Р.Дж., Лодочник П.Д. (1999). «Полусинтез таксола и таксотера». В Суффнессе М (ред.). Таксол: наука и применение . Бока-Ратон: пресса CRC. стр. 97–121. ISBN 978-0-13-873736-8 .
- ^ Одзима И, Ван Х, Цзин Ю, Ван С (март 2018 г.). «Поиски эффективных таксоидов нового поколения противораковых агентов и их адресной доставки к опухолям» . Журнал натуральных продуктов . 81 (3): 703–721. doi : 10.1021/acs.jnatprod.7b01012 . ПМЦ 5869464 . ПМИД 29468872 .
- ^ «Паклитаксел для инъекций, USP» (PDF) . Инъекционные фармацевтические препараты . Архивировано из оригинала (PDF) 18 сентября 2016 года . Проверено 22 апреля 2016 г.
- ^ «История» . Архивировано из оригинала 24 мая 2016 года . Проверено 22 апреля 2016 г.
- ^ «Фитон БиоТек Паклитаксел» . Архивировано из оригинала 7 августа 2016 года . Проверено 22 апреля 2016 г.
- ^ Имсенг Н., Шиллберг С., Шюрх С., Шмид Д., Шютте К., Горр Г. и др. (2014). «Суспензионная культура растительных клеток в гетеротрофных условиях». В Мейер Х.П., Шмидхальтер Д. (ред.). Суспензионная культура живых клеток в промышленном масштабе . Уайли-Блэквелл. стр. 224–257. ISBN 978-3-527-33547-3 .
- ^ Гилберт Горр и Роланд Франке. Коммерческое фармацевтическое производство сложных АФИ с помощью технологии ферментации растительных клеток (PCF). Презентация на CPhI 2015, 13 октября.
- ^ «Премия Greener Synthetic Pathways 2004 года: Компания Bristol-Myers Squibb: Разработка зеленого синтеза для производства таксола посредством ферментации и экстракции растительных клеток» . Архивировано из оригинала 2 октября 2006 года.
- ^ Стирле А., Стробель Г., Стирле Д. (апрель 1993 г.). «Продуцирование таксола и таксанов Taxomyces andreanae, эндофитным грибом тиса тихоокеанского». Наука . 260 (5105): 214–216. Бибкод : 1993Sci...260..214S . дои : 10.1126/science.8097061 . ПМИД 8097061 .
- ^ Станек А., Вурденбаг Х.Дж., Кайзер О. (декабрь 2009 г.). «Taxomyces andreanae: раскрыта тайна предполагаемого производителя паклитаксела?». Планта Медика . 75 (15): 1561–1566. дои : 10.1055/s-0029-1186181 . ПМИД 19809969 . S2CID 260283080 .
- ^ Хейниг У, Шольц С, Йенневейн С (2013). «Понимание сути биосинтеза таксола грибами» (PDF) . Грибное разнообразие . 60 : 161–170. дои : 10.1007/s13225-013-0228-7 . S2CID 18642421 . Архивировано (PDF) из оригинала 9 октября 2022 года.
- ^ Jump up to: а б Дьюик П.М. (6 февраля 2009 г.). Лекарственные натуральные продукты . Чичестер, Великобритания: John Wiley & Sons, Ltd. doi : 10.1002/9780470742761 . ISBN 978-0-470-74276-1 .
- ^ Ховат С., Пак Б., О И.С., Джин Ю.В., Ли Э.К., Лоак Г.Дж. (май 2014 г.). «Паклитаксел: биосинтез, производство и перспективы». Новая биотехнология . 31 (3): 242–245. дои : 10.1016/j.nbt.2014.02.010 . ПМИД 24614567 .
- ^ Крото Р., Кетчум Р.Э., Лонг Р.М., Каспера Р., Вильдунг М.Р. (февраль 2006 г.). «Биосинтез таксола и молекулярная генетика» . Обзоры фитохимии . 5 (1): 75–97. Бибкод : 2006ПЧРв...5...75С . дои : 10.1007/s11101-005-3748-2 . ПМК 2901146 . ПМИД 20622989 .
- ^ Jump up to: а б с Зал N (март 2003 г.). «Создание сложности – красота и логика синтеза». Химические коммуникации (6): 661–664. дои : 10.1039/b212248k . ПМИД 12703766 .
- ^ См. Н. Холл, там же. См. также Американского химического общества публикацию «Новости химии и инженерии» (C&EN), 21 февраля 1994 г., стр. 32, а также основные цитаты, встречающиеся в статьях Холтона и Николау о полном синтезе таксола.
- ^ Jump up to: а б Флам Ф (февраль 1994 г.). «Гонка за синтез таксола заканчивается вничью». Наука . 263 (5149): 911. Бибкод : 1994Sci...263..911F . дои : 10.1126/science.7906053 . ПМИД 7906053 .
- ^ Гудман и Уолш 2001 , стр. 179–182.
- ^ Уолл МЭ, Вани MC (февраль 1995 г.). «Камптотецин и таксол: открытие для клиники - тринадцатая лекция на премию Мемориала Брюса Ф. Кейна» . Исследования рака . 55 (4): 753–760. ПМИД 7850785 . Архивировано из оригинала 24 ноября 2016 года.
- ^ Донхауэр RC (1996). «Клиническая разработка паклитаксела: успешное сотрудничество научных кругов, промышленности и Национального института рака» . Стволовые клетки . 14 (1): 25–28. дои : 10.1002/stem.140025 . ISSN 1066-5099 . ПМИД 8820947 .
- ^ Гудман и Уолш 2001 , с. 17.
- ^ Гудман и Уолш 2001 , с. 22.
- ^ Goodman & Walsh 2001 , стр. 25, 28.
- ^ Jump up to: а б Гудман и Уолш 2001 , с. 51.
- ^ Уолл МЭ, Вани MC (февраль 1995 г.). «Камптотецин и таксол: открытие для клиники - тринадцатая лекция на премию Мемориала Брюса Ф. Кейна». Исследования рака . 55 (4): 753–760. ПМИД 7850785 .
- ^ Вани MC, Тейлор Х.Л., Уолл М.Э., Коггон П., Макфэйл А.Т. (май 1971 г.). «Растительные противоопухолевые средства. VI. Выделение и структура таксола, нового противолейкозного и противоопухолевого средства из Taxus brevifolia». Журнал Американского химического общества . 93 (9): 2325–2327. дои : 10.1021/ja00738a045 . ПМИД 5553076 .
- ^ Гудман и Уолш 2001 , с. 81.
- ^ Goodman & Walsh 2001 , стр. 79, 81.
- ^ Фукс Д.А., Джонсон Р.К. (август 1978 г.). «Цитологические данные о том, что таксол, противоопухолевое средство из Taxus brevifolia, действует как яд митотического веретена». Отчеты о лечении рака . 62 (8): 1219–1222. ПМИД 688258 .
- ^ Гудман и Уолш 2001 , с. 95.
- ^ Jump up to: а б Гудман и Уолш 2001 , с. 97
- ^ Гудман и Уолш 2001 , с. 115.
- ^ Jump up to: а б с д Гудман и Уолш 2001 , с. 120
- ^ Ровински Е.К., Донхауэр Р.К., Розеншейн Н.Б., Эттингер Д.С., Макгуайр В.П. (1988). «Исследование фазы II таксола при запущенных эпителиальных злокачественных новообразованиях». Труды Ассоциации клинической онкологии . 7 : 136.
- ^ «Передача технологий: партнерство NIH и частного сектора в разработке таксола» (PDF) . Архивировано из оригинала (PDF) 26 июля 2007 года . Проверено 17 июля 2016 г.
- ^ Надер Р., Лав Дж. (февраль 1993 г.). «Ограбление аптечки: как Bristol-Myers Squibb украла общественное исследование рака» . Прогрессивный . Архивировано из оригинала 24 сентября 2004 года.
- ^ «Имена для ограбления» . Природа . 373 (6513): 370. Февраль 1995 г. Бибкод : 1995Natur.373..370. . дои : 10.1038/373370a0 . ПМИД 7830775 . S2CID 31510966 .
- ^ Гудман и Уолш 2001 , с. 170.
- ^ Bristol-Myers Squibb, Разработка TAXOL (паклитаксел), март 1997 г., цитируется по Goodman & Walsh 2001 , p. 2
- ^ «Руководство NICE TA108» . 27 сентября 2006 г. Архивировано из оригинала 30 июня 2007 г.
- ^ Мхайдат Н.М., Альзуби К.Х., Аль-Аззам С.И., Альсаад А.А. (январь 2014 г.). «Кофеин ингибирует вызванный паклитакселом апоптоз в клетках колоректального рака посредством повышения уровня Mcl-1» . Отчеты о молекулярной медицине . 9 (1): 243–248. дои : 10.3892/ммр.2013.1763 . ПМИД 24173825 . Архивировано из оригинала 22 июня 2015 года.
- ^ Лаварс Н. (14 января 2016 г.). «Маскировка химиопрепаратов в клеточных пузырях уничтожает рак одной пятидесятой обычной дозы» . www.gizmag.com . Архивировано из оригинала 24 февраля 2016 года . Проверено 14 февраля 2016 г.
- ^ Ким М.С., Хейни М.Дж., Чжао Ю., Махаджан В., Дейген И., Клячко Н.Л. и др. (апрель 2016 г.). «Разработка паклитаксела, инкапсулированного в экзосомы, для преодоления МЛУ в раковых клетках» . Наномедицина . 12 (3): 655–664. дои : 10.1016/j.nano.2015.10.012 . ПМК 4809755 . ПМИД 26586551 .
- ^ Качуи Э., Мусави-Мовахеди А.А., Ходаголи Ф., Мозаффарян Ф., Садеги П., Хади-Алиджанванд Х. и др. (июнь 2014 г.). «Исследование ингибирования фибрилляции инсулина и цитотоксичности паклитакселом». Журнал биохимии . 155 (6): 361–373. дои : 10.1093/jb/mvu012 . ПМИД 24535601 .
- ^ Качуи Э., Мозаффариан Ф., Ходаголи Ф., Садеги П., Карами Л., Гасеми А. и др. (май 2018 г.). «Паклитаксел ингибировал фибрилляцию лизоцима за счет повышения коллоидной стабильности за счет образования олигомеров «вне пути» . Международный журнал биологических макромолекул . 111 : 870–879. doi : 10.1016/j.ijbiomac.2018.01.072 . ПМИД 29352977 .
- ^ Москарелло М.А., Мак Б., Нгуен Т.А., Вуд Д.Д., Мастронарди Ф., Людвин С.К. (апрель 2002 г.). «Паклитаксел (Таксол) ослабляет клиническое заболевание у трансгенных мышей со спонтанной демиелинизацией и вызывает ремиелинизацию». Рассеянный склероз . 8 (2): 130–138. дои : 10.1191/1352458502ms776oa . ПМИД 11990870 . S2CID 45994154 .
- ^ Муссе А.А., Полверини Э., Райджмейкерс Р., Харауз Г. (октябрь 2008 г.). «Кинетика человеческой пептидиларгининдеиминазы 2 (hPAD2) - снижение зависимости Ca2+ от фосфолипидов и оценка предполагаемого ингибирования боковыми цепями паклитаксела». Биохимия и клеточная биология . 86 (5): 437–447. дои : 10.1139/o08-124 . ПМИД 18923545 .
- ^ «Фаза II клинических испытаний мицеллярного паклитаксела при вторично-прогрессирующем рассеянном склерозе проводится в Канаде» . Общество рассеянного склероза Канады . 13 декабря 1999 г. Архивировано из оригинала 15 марта 2012 г.
- ^ «Ангиотек прекращает исследование мицеллярного паклитаксела, заявляя об отсутствии статистической значимости» . Общество рассеянного склероза Канады . 27 февраля 2002 г. Архивировано из оригинала 15 марта 2012 г.
Дальнейшее чтение
[ редактировать ]- Джордан Дж., Вивьен В. (5 марта 2001 г.). История таксола: природа и политика в поисках противоракового препарата . Издательство Кембриджского университета. ISBN 978-0-521-56123-5 . Архивировано из оригинала 14 января 2023 года . Проверено 2 июня 2021 г.
Внешние ссылки
[ редактировать ]- «Паклитаксел» . Национальный институт рака . 5 октября 2006 г.
- «Паклитаксел» . Словарь лекарств NCI . 2 февраля 2011 г.
- Молекула месяца: TAXOL, автор Нил Эдвардс, Бристольский университет .
- Сказка о таксоле из Университета штата Флорида .
- Беренсон А. (1 октября 2006 г.). «Надежда, по 4200 долларов за дозу» . Нью-Йорк Таймс . Проверено 31 марта 2007 г.
- Препараты, разработанные Bristol Myers Squibb
- Ингибиторы микротрубочек
- Ингибиторы митоза
- Бензоатные эфиры
- Карбоксилатные эфиры
- Бензамиды
- Вторичные спирты
- Третичные спирты
- Кетоны
- Ацетатные эфиры
- Таксаны
- Агонисты рецепторов прегнана X
- Основные лекарства Всемирной организации здравоохранения
- Растительные токсины