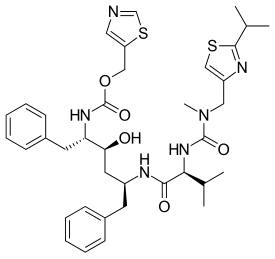
Ритонавир
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / r ɪ ˈ t ɒ ə n ˌ v ɪər / рих- ТО -не-веер |
| Торговые названия | Норвир |
| Другие имена | РТВ |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а696029 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Связывание с белками | 98–99% |
| Метаболизм | Печень , CYP3A4 |
| Период полувыведения | 3–4 часа [6] [7] |
| Экскреция | В основном фекальный |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| НИАИД Химическая база данных | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.125.710 |
| Химические и физические данные | |
| Формула | С 37 Ч 48 Н 6 О 5 С 2 |
| Молярная масса | 720.95 g·mol −1 |
| 3D model ( JSmol ) | |
Ритонавир , продаваемый под торговой маркой Норвир , представляет собой антиретровирусный препарат, используемый наряду с другими лекарствами для лечения ВИЧ/СПИДа . [4] [5] [8] Такое комбинированное лечение известно как высокоактивная антиретровирусная терапия (ВААРТ). [8] Ритонавир является ингибитором протеазы, хотя в настоящее время он главным образом служит для повышения эффективности других ингибиторов протеазы . [8] [9] Его также можно использовать в сочетании с другими лекарствами для лечения гепатита С и COVID-19 . [10] [11] Его принимают внутрь . [8]
Общие побочные эффекты ритонавира включают тошноту, рвоту, потерю аппетита, диарею и онемение рук и ног. [8] Серьезные побочные эффекты включают осложнения со стороны печени, панкреатит , аллергические реакции и аритмии . [8] Серьезные взаимодействия могут возникнуть с рядом других препаратов, включая амиодарон и симвастатин . [8] В низких дозах его можно применять во время беременности. [12] Ритонавир относится к классу ингибиторов протеазы. [8] Однако его также часто используют для ингибирования фермента, метаболизирующего другие ингибиторы протеазы. [13] Это ингибирование позволяет использовать более низкие дозы этих последних лекарств. [13]
Ритонавир был запатентован в 1989 году и начал использоваться в медицине в 1996 году. [14] [15] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [16] [17] Капсулы ритонавира были одобрены в качестве непатентованного лекарства в США в 2020 году. [18]
Медицинское использование
[ редактировать ]Этот раздел нуждается в дополнении: вступительным предложением, которое лучше описывает очень важные (фармакокинетические-фармакодинамические) наблюдения ФК-ФД для этого первого в своем классе дизайна ингибитора и его первоначальное применение. Вы можете помочь, добавив к нему . ( февраль 2020 г. ) |
ВИЧ
[ редактировать ]Ритонавир показан в сочетании с другими антиретровирусными препаратами для лечения пациентов, инфицированных ВИЧ-1. [4] [5] [8] Хотя изначально он разрабатывался как самостоятельное противовирусное средство, чаще всего он используется в качестве усилителя фармакокинетики для повышения концентрации других антиретровирусных препаратов в плазме. [19] [20] Ритонавир эффективен в предотвращении репликации ВИЧ-1. Ингибиторы протеазы, включая ритонавир, эффективно блокируют протеазу ВИЧ-1 , важнейший фермент репродуктивного цикла ВИЧ-1. [21]
COVID-19
[ редактировать ]Два SARS-CoV-2 3CL про Ингибиторы предварительно упакованы с ритонавиром для повышения их концентрации в крови. [22]
В декабре 2021 года комбинации нирмарелвира и ритонавира (FDA) выдало разрешение на экстренное использование США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов для лечения коронавирусного заболевания COVID-19 . [23] [24] [25] Лекарства в совместной упаковке продаются под торговой маркой Паксловид. [24] [25] [26] Паксловид не разрешен для доконтактной или постконтактной профилактики COVID-19, а также для начала лечения у лиц, нуждающихся в госпитализации из-за тяжелой или критической формы COVID-19. [24] 31 декабря 2021 года Агентство по регулированию лекарственных средств и товаров медицинского назначения Великобритании (MHRA) одобрило ту же комбинацию «для людей с легкой и умеренной формой COVID-19, которые подвергаются высокому риску развития тяжелой формы COVID-19». [27] [28]
В январе 2023 года симнотрелвир/ритонавир Китая был условно одобрен Национальным управлением медицинской продукции (NMPA) для лечения COVID-19. [22]
Другое использование
[ редактировать ]Использование ритонавира в качестве ингибитора CYP3A также наблюдается в от гепатита С лекарстве омбитасвир/паритапревир/ритонавир . [9]
Побочные эффекты
[ редактировать ]При введении первоначально протестированных более высоких доз, эффективных для терапии ВИЧ, побочные эффекты ритонавира показаны ниже. [4]
- Астения, недомогание
- Диарея
- Тошнота и рвота
- Боль в животе
- Головокружение
- Бессонница
- Почечная недостаточность
- Потоотделение
- Нарушение вкуса
- Метаболические эффекты, в том числе
- Гиперхолестеринемия
- Гипертриглицеридемия
- Повышенные трансаминазы
- Повышенная креатинкиназа
Побочные реакции на лекарственные средства
[ редактировать ]Ритонавир проявляет печеночную активность. [29] Он индуцирует CYP1A2 и ингибирует CYP3A4 и CYP2D6 . Сопутствующая терапия ритонавиром с различными лекарствами может привести к серьезным, а иногда и фатальным лекарственным взаимодействиям . [30]
Поскольку ритонавир является сильным ингибитором (вызывает по меньшей мере пятикратное увеличение значений AUC в плазме или снижение клиренса более чем на 80% ) ферментов цитохрома P450 CYP2D6 и CYP3A4 , он может сильно потенцировать и продлевать период полувыведения. жизнь и/или повышают концентрацию в крови фенобарбитала , примидона , карбамазепина , фенитоина , ингибиторов ФДЭ5 , таких как силденафил , опиоидов, таких как гидрокодон , оксикодон , петидин и фентанил , антиаритмических средств, таких как амиодарон , пропафенон и дизопирамид , иммунодепрессантов , таких как такролимус , воклоспорин и сиролимус , нейролептики, такие как клозапин , луразидон и пимозид , а также некоторые химиотерапевтические средства , бензодиазепины и некоторые спорыньи . производные [31] [32] FDA выпустило предупреждение об этом типе взаимодействия лекарств. [9]
Индукторы CYP3A4 могут противодействовать ингибирующему эффекту ритонавира и приводить к резкому снижению уровня «усиленных» лекарств, увеличивая риск развития лекарственной устойчивости. Другие ингибиторы CYP3A4 могут оказывать аддитивное действие с ритонавиром, вызывая повышение уровня препарата. [9]
Фармакология
[ редактировать ]Этот раздел нуждается в дополнении: точным описанием его характеристик связывания с ВИЧ-протеазой и CYP3A4, а также структурными деталями. Вы можете помочь, добавив к нему . ( февраль 2020 г. ) |

Фармакодинамика
[ редактировать ]Ритонавир изначально был разработан как ингибитор протеазы ВИЧ . [33] один из семейства псевдо- C 2 -симметричных низкомолекулярных ингибиторов. [34]
Ритонавир редко используется из-за собственного противовирусного действия, но по-прежнему широко используется в качестве усилителя действия других ингибиторов протеазы . Более конкретно, ритонавир используется для ингибирования определенного фермента в кишечнике, печени и других местах, который обычно метаболизирует ингибиторы протеазы, цитохрома P450-3A4 (CYP3A4). Препарат связывается и ингибирует CYP3A4, поэтому низкие дозы можно использовать для усиления действия других ингибиторов протеазы. Это открытие радикально уменьшило побочные эффекты и повысило эффективность ингибиторов протеазы и ВААРТ. [35] [36] . Однако из-за общей роли CYP3A4 в метаболизме ксенобиотиков прием ритонавира также влияет на эффективность многих других лекарств, что усложняет одновременное назначение препаратов. См . § Побочные реакции на лекарства выше. [9] [37]
Фармакокинетика
[ редактировать ]Ритонавир в дозе 200 мг достигает максимальной концентрации в плазме примерно через 3 часа, а период полувыведения составляет 3–4 часа. [6] [7] Важно отметить, что фармакокинетика ритонавира нелинейна: период полувыведения увеличивается при приеме более высоких доз или при повторном приеме. [6] Например, период полувыведения таблетки 500 мг составляет 4–6 часов, а не 3–4 часа для таблетки 200 мг. [6] Препарат обладает высокой биодоступностью, но около 20% теряется из-за метаболизма первого прохождения . [6] Капсулы Ривонавира не всасываются так быстро, как таблетки Ритонавира, и могут иметь различную биодоступность. [8]
Было продемонстрировано, что ритонавир обладает активностью in vitro EC 50 =0,02 мкМ в отношении протеазы ВИЧ-1 и высокой устойчивой концентрацией в плазме после перорального введения у нескольких видов животных. [38]
Химия
[ редактировать ]Ритонавир изначально был получен из умеренно мощной и биодоступной при пероральном приеме небольшой молекулы А-80987. Гетероциклические группы P3 и P2' A-80987 были переработаны для создания аналога, теперь известного как ритонавир, с улучшенными фармакокинетическими свойствами по сравнению с оригиналом. [38]
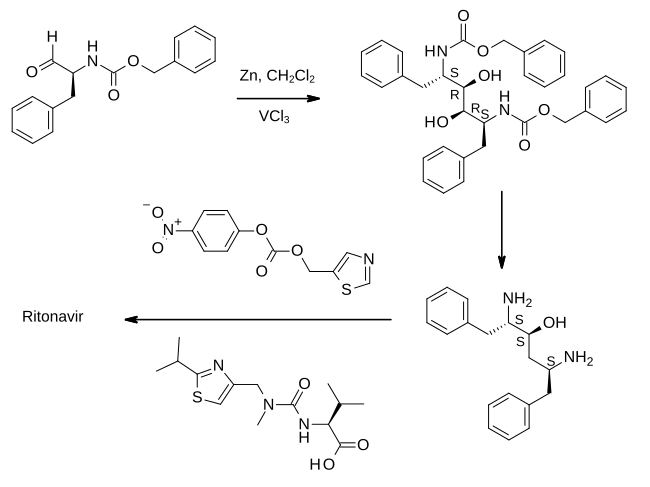
Полные подробности синтеза ритонавира впервые опубликовали ученые из Abbott Laboratories .
На первом показанном этапе альдегид , полученный из фенилаланина, обрабатывается цинковой пылью в присутствии хлорида ванадия (III) . Это приводит к реакции сочетания пинакола , которая димеризует материал с образованием промежуточного продукта, который превращается в эпоксид, а затем восстанавливается до (2S,3S,5S)-2,5-диамино-1,6-дифенилгексан-3-ола. Важно отметить, что при этом сохраняется абсолютная стереохимия предшественника аминокислоты. Затем диамин , каждое из последовательно обрабатывают двумя производными тиазола которых связано амидной связью, с получением ритонавира. [33] [39]
История
[ редактировать ]
Ритонавир продается под названием Норвир компанией AbbVie, Inc. [4] [5] США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило ритонавир 1 марта 1996 года. [41] [42] В результате внедрения «высокоактивной антиретровирусной терапии» годовой уровень смертности, связанной с ВИЧ, в США снизился с более чем 50 000 до примерно 18 000 за период в два года. [40]
В 2014 году FDA одобрило комбинацию омбитасвир/паритапревир/ритонавир для лечения генотипа 4 вируса гепатита С (ВГС). [10]
После начала пандемии COVID в 2020 году многие противовирусные препараты, в том числе ингибиторы протеазы в целом и ритонавир в частности, были перепрофилированы в целях лечения новой инфекции . Было обнаружено, что лопинавир/ритонавир не действуют при тяжелом течении COVID-19 . [43] Виртуальный скрининг с последующим анализом молекулярной динамики показал, что ритонавир блокирует связывание белка-шипа (S) SARS-CoV-2 с рецептором ангиотензинпревращающего фермента 2 человека (hACE2), что имеет решающее значение для проникновения вируса в клетки человека. [44]
Наконец, в 2021 году комбинация ритонавира с нирмарелвиром , недавно разработанным перорально активным ингибитором 3C-подобной протеазы . для лечения COVID-19 была разработана [45] [46] [47] [48] Ритонавир служит для замедления метаболизма нирмарелвира ферментами цитохрома для поддержания более высоких циркулирующих концентраций основного препарата. [49] В ноябре того же года компания Pfizer объявила о положительных результатах фазы 2/3, включая сокращение числа госпитализаций на 89% при применении в течение трех дней после появления симптомов. [50] [51]
Полиморфизм и временный уход с рынка
[ редактировать ]Ритонавир изначально выпускался в виде капсул, не требующих хранения в холодильнике. Он содержал кристаллическую форму ритонавира, которая теперь называется формой I. [52] Однако, как и многие лекарства, кристаллический ритонавир может проявлять полиморфизм , то есть одна и та же молекула может кристаллизоваться в более чем один тип кристаллов или полиморф, каждый из которых содержит одну и ту же повторяющуюся молекулу, но в разных кристаллических упаковках/расположениях. Растворимость и, следовательно, биодоступность могут варьироваться в зависимости от расположения, и это наблюдалось для форм I и II ритонавира. [53]
В ходе разработки — ритонавир был представлен в 1996 году — была обнаружена только кристаллическая форма, которая теперь называется формой I; однако в 1998 году более низкая свободная энергия , [54] был обнаружен более стабильный полиморф, форма II. Эта более стабильная кристаллическая форма была менее растворима, что приводило к значительному снижению биодоступности . Снижение пероральной биодоступности препарата привело к временному удалению капсульной формы для перорального применения с рынка. [53] Вследствие того, что даже незначительное количество формы II может привести к превращению более биодоступной формы I в форму II, присутствие формы II угрожало разрушением существующих запасов пероральной капсульной формы ритонавира; и действительно, форма II была обнаружена на производственных линиях, что фактически остановило производство ритонавира. [52] Компания Abbott (теперь AbbVie) отозвала капсулы с рынка, а врачам, назначающим препарат, было рекомендовано перейти на суспензию Норвира. [ нужна ссылка ] По оценкам, в результате компания Abbott потеряла более 250 миллионов долларов США, и этот инцидент часто называют громким примером исчезновения полиморфов . [55]
Группы исследований и разработок компании в конечном итоге решили проблему, заменив капсульную формулу охлажденной гелевой капсулой. [ когда? ] [ нужна ссылка ] В 2000 году компания Abbott (ныне AbbVie) получила одобрение FDA на таблетированную форму лопинавира/ритонавира (Калетра), которая содержала препарат ритонавира, не требующий охлаждения. [56] Было обнаружено, что таблетки ритонавира, полученные в твердой дисперсии методом экструзии из расплава, остались в форме I, и в 2010 году они были вновь выведены на рынок. [57]
Общество и культура
[ редактировать ]Экономика
[ редактировать ]В 2003 году компания Abbott (AbbVie, Inc.) подняла цену на курс Норвира с 1,71 доллара США в день до 8,57 доллара США в день, что привело к заявлениям о взвинчивании цен со стороны групп пациентов и некоторых членов Конгресса. Потребительская группа Essential Inventions обратилась в Национальный институт здравоохранения с просьбой отменить патент Норвира, но 4 августа 2004 года Национальный институт здравоохранения объявил, что у него нет законного права разрешить производство дженерика Норвира. [58]
Ссылки
[ редактировать ]- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»)» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ «Примечание: Нирмарелвир (COVID-19) добавлен в Список рецептурных препаратов (PDL)» . Здоровье Канады . 17 января 2022 года. Архивировано из оригинала 29 мая 2022 года . Проверено 25 июня 2022 г.
- ^ «Информация о продукте Норвир» . Здоровье Канады . 25 апреля 2012 года . Проверено 25 июня 2022 г.
- ^ Перейти обратно: а б с д и «Норвир-ритонавир таблетка, покрытая пленочной оболочкой, раствор Норвир-ритонавира, порошок Норвир-ритонавира» . ДейлиМед . Архивировано из оригинала 18 ноября 2021 года . Проверено 17 ноября 2021 г.
- ^ Перейти обратно: а б с д «Норвир ЭПАР» . Европейское агентство лекарственных средств (EMA) . 17 сентября 2018 года. Архивировано из оригинала 2 октября 2018 года . Проверено 20 августа 2020 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Перейти обратно: а б с д и Сюй А., Граннеман Г.Р., Витт Г., Локк С., Дениссен Дж., Молла А. и др. (май 1997 г.). «Фармакокинетика многократных доз ритонавира у субъектов, инфицированных вирусом иммунодефицита человека» . Антимикробные средства и химиотерапия . 41 (5): 898–905. дои : 10.1128/aac.41.5.898 . ПМК 163822 . ПМИД 9145841 .
- ^ Перейти обратно: а б Даннер С.А., Карр А., Леонард Х.М., Леман Л.М., Гудиоль Ф., Гонсалес Дж., Равентос А., Рубио Р., Буза Е., Пинтадо В., Агуадо А.Г., Гарсиа де Ломас Дж., Дельгадо Р., Борлеффс Х.К., Сюй А., Вальдес Х.М., Баучер Калифорния, Купер Д.А. (декабрь 1995 г.). «Краткосрочное исследование безопасности, фармакокинетики и эффективности ритонавира, ингибитора протеазы ВИЧ-1. Европейско-австралийская совместная группа по изучению ритонавира». Медицинский журнал Новой Англии . 333 (23): 1528–1533. дои : 10.1056/NEJM199512073332303 . hdl : 2445/121979 . ПМИД 7477167 .
- ^ Перейти обратно: а б с д и ж г час я дж «Ритонавир» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 17 октября 2015 года . Проверено 23 октября 2015 г.
- ^ Перейти обратно: а б с д и Талха Б., Дхамун А.С. (8 августа 2023 г.). «Ритонавир» . СтатПерлс . Издательство StatPearls. ПМИД 31335032 . Проверено 6 января 2024 г.
- ^ Перейти обратно: а б «FDA одобрило препарат Viekira Pak для лечения гепатита С» (пресс-релиз). США Управление по контролю за продуктами и лекарствами (FDA). 19 декабря 2014 г. Архивировано из оригинала 31 октября 2015 г.
- ^ Акиносоглу К., Схинас Г., Гогос С. (ноябрь 2022 г.). «Пероральное противовирусное лечение COVID-19: комплексный обзор нирмарелвира/ритонавира» . Вирусы . 14 (11): 2540. дои : 10.3390/v14112540 . ПМК 9696049 . ПМИД 36423149 .
- ^ «Предупреждения о ритонавире при беременности и грудном вскармливании» . наркотики.com . Архивировано из оригинала 7 сентября 2015 года . Проверено 23 октября 2015 г.
- ^ Перейти обратно: а б Британский национальный формуляр 69 (изд. 69). Фармацевтический Пр. 31 марта 2015. с. 426. ИСБН 9780857111562 .
- ^ Хакер М (2009). Принципы и практика фармакологии . Амстердам: Академическая пресса/Эльзевир. п. 550. ИСБН 9780080919225 . Архивировано из оригинала 17 июня 2020 года . Проверено 10 сентября 2017 г.
- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 509. ИСБН 9783527607495 . Архивировано из оригинала 20 июня 2021 года . Проверено 27 августа 2020 г.
- ^ Всемирная организация здравоохранения (2019). Модельный список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г. Женева: Всемирная организация здравоохранения. hdl : 10665/325771 . ВОЗ/MVP/EMP/IAU/2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Всемирная организация здравоохранения (2021 г.). Примерный список основных лекарственных средств Всемирной организации здравоохранения: 22-й список (2021 г.) . Женева: Всемирная организация здравоохранения. hdl : 10665/345533 . ВОЗ/MHP/HPS/EML/2021.02.
- ^ «Первое одобрение непатентованного лекарственного средства» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Архивировано из оригинала 26 января 2021 года . Проверено 13 февраля 2021 г.
- ^ «Ритонавир – Пациент» . Clinicinfo.hiv.gov . Проверено 11 января 2023 г.
- ^ «Ритонавир» . go.drugbank.com . Проверено 11 января 2023 г.
- ^ «Протеаза» . Clinicinfo.hiv.gov . Проверено 11 января 2023 г.
- ^ Перейти обратно: а б Чжу К.В. (сентябрь 2023 г.). «Деуремидевир и симнотелвир-ритонавир для лечения COVID-19». ACS Фармакология и трансляционная наука . 6 (9): 1306–1309. дои : 10.1021/acptsci.3c00134 . PMC 10496140. PMID 37705591 .
- ^ «Паксловид-нирмарелвир и набор ритонавира» . ДейлиМед . Архивировано из оригинала 31 декабря 2021 года . Проверено 30 декабря 2021 г.
- ^ Перейти обратно: а б с «FDA разрешает первый пероральный противовирусный препарат для лечения COVID-19» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 22 декабря 2021 года. Архивировано из оригинала 27 декабря 2021 года . Проверено 22 декабря 2021 г.
- ^ Перейти обратно: а б «Pfizer получила разрешение FDA США на экстренное использование нового перорального противовирусного препарата при COVID-19» (пресс-релиз). Пфайзер . 22 декабря 2021 года. Архивировано из оригинала 22 декабря 2021 года . Получено 22 декабря 2021 г. - через Business Wire.
- ^ «Часто задаваемые вопросы о разрешении на экстренное использование Паксловида для лечения COVID-19» (PDF) . США Управление по контролю за продуктами и лекарствами (FDA). 22 декабря 2021 года. Архивировано из оригинала 5 января 2022 года . Проверено 3 января 2022 г.
- ^ «Поральный противовирусный препарат от COVID-19, Паксловид, одобрен регулирующим органом Великобритании» (пресс-релиз). Агентство по регулированию лекарственных средств и товаров медицинского назначения. 31 декабря 2021 года. Архивировано из оригинала 11 января 2022 года . Проверено 3 января 2022 г.
- ^ Рид Дж. (31 декабря 2021 г.). «Паксловид: Регулятор лекарственных средств Великобритании одобрил вторую противовирусную таблетку от Covid» . Новости BBC онлайн . Архивировано из оригинала 1 января 2022 года . Проверено 3 января 2022 г.
- ^ Йе Р.Ф., Гавер В.Е., Паттерсон К.Б., Резк Н.Л., Бакстер-Мехе Ф., Блейк М.Дж. и др. (май 2006 г.). «Лопинавир/ритонавир индуцирует печеночную активность ферментов цитохрома P450 CYP2C9, CYP2C19 и CYP1A2, но ингибирует печеночную и кишечную активность CYP3A, что измерено с помощью фенотипического коктейля лекарств у здоровых добровольцев» . Журнал синдромов приобретенного иммунодефицита . 42 (1): 52–60. дои : 10.1097/01.qai.0000219774.20174.64 . ПМИД 16639344 . S2CID 39632668 .
- ^ «Ритонавир: информация о препарате предоставлена Lexi-Comp: Merck Manual Professional» . Руководства Merck Профессиональная версия . 30 апреля 2008 г. Архивировано из оригинала 30 апреля 2008 г.
- ^ Стадер Ф., Ху С., Стокл М., Бэк Д., Хирш Х.Х., Баттегей М., Марзолини К. (октябрь 2020 г.). «Остановка приема лопинавира/ритонавира у пациентов с COVID-19: продолжительность эффекта взаимодействия препаратов» . Журнал антимикробной химиотерапии . 75 (10): 3084–3086. дои : 10.1093/jac/dkaa253 . ПМЦ 7337877 . ПМИД 32556272 .
- ^ Карпентер М., Берри Х., Пеллетье А.Л. (май 2019 г.). «Клинически значимое лекарственное взаимодействие в первичной медико-санитарной помощи». Американский семейный врач . 99 (9): 558–564. ПМИД 31038898 .
- ^ Перейти обратно: а б WO 1994014436 , Kempf DJ, Norbeck DW, Sham HL, Zhao C, Sowin TJ, Reno DS, Haight AR, Cooper AJ, "Соединения, ингибирующие ретровирусную протеазу", опубликовано 7 июля 1994 г., передано Abbott Laboratories.
- ^ Kempf DJ, Norbeck DW, Codacovi L, Wang XC, Kohlbrenner WE, Wideburg NE и др. (октябрь 1990 г.). «Структурные симметричные ингибиторы C2 протеазы ВИЧ». Журнал медицинской химии . 33 (10): 2687–2689. дои : 10.1021/jm00172a002 . ПМИД 2213822 .
- ^ Зельдин Р.К., Петрушке Р.А. (январь 2004 г.). «Фармакологические и терапевтические свойства терапии ингибиторами протеазы, усиленной ритонавиром, у ВИЧ-инфицированных пациентов» . Журнал антимикробной химиотерапии . 53 (1): 4–9. дои : 10.1093/jac/dkh029 . ПМИД 14657084 .
- ^ Мерри С., Барри М.Г., Малкахи Ф., Райан М., Хиви Дж., Тиа Дж.Ф. и др. (март 1997 г.). «Фармакокинетика саквинавира отдельно и в сочетании с ритонавиром у ВИЧ-инфицированных пациентов». СПИД . 11 (4): Ф29–Ф33. дои : 10.1097/00002030-199704000-00001 . ПМИД 9084785 .
- ^ «Разработка лекарств и лекарственное взаимодействие: таблица субстратов, ингибиторов и индукторов» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 3 декабря 2019 года. Архивировано из оригинала 12 марта 2020 года . Проверено 17 февраля 2020 г.
- ^ Перейти обратно: а б Kempf DJ, Sham HL, Marsh KC, Flentge CA, Betebenner D, Green BE и др. (февраль 1998 г.). «Открытие ритонавира, мощного ингибитора протеазы ВИЧ с высокой пероральной биодоступностью и клинической эффективностью». Журнал медицинской химии . 41 (4): 602–617. дои : 10.1021/jm970636+ . ПМИД 9484509 .
- ^ Варданян Р., Грубий В. (2016). «34: Противовирусные препараты». Синтез лекарств-бестселлеров . стр. 698–701. дои : 10.1016/B978-0-12-411492-0.00034-1 . ISBN 9780124114920 . S2CID 75449475 .
- ^ Перейти обратно: а б с Центры по профилактике заболеваний (CDC) (июнь 2011 г.). «Эпиднадзор за ВИЧ – США, 1981–2008 гг.» (PDF) . ММВР. Еженедельный отчет о заболеваемости и смертности . 60 (21): 689–93. ПМИД 21637182 . Архивировано из оригинала (PDF) 24 сентября 2015 г.
- ^ «Пакет одобрения ритонавира FDA» (PDF) . 1 марта 1996 г. Архивировано (PDF) из оригинала 1 марта 2021 г. . Проверено 20 августа 2020 г.
- ^ «Одобрение FDA препаратов против ВИЧ» . ВИЧИНФО . Проверено 29 сентября 2022 г.
- ^ Цао Б., Ван Ю., Вэнь Д., Лю В., Ван Дж., Фань Дж. и др. (май 2020 г.). «Испытание лопинавира-ритонавира у взрослых, госпитализированных с тяжелой формой Covid-19» . Медицинский журнал Новой Англии . 382 (19): 1787–1799. дои : 10.1056/NEJMoa2001282 . ПМК 7121492 . ПМИД 32187464 .
- ^ Багери М., Ниаварани А. (октябрь 2020 г.). «Анализ молекулярной динамики предсказывает, что ритонавир и налоксегол сильно блокируют связывание спайкового белка SARS-CoV-2 с hACE2». Журнал биомолекулярной структуры и динамики . 40 (4): 1597–1606. дои : 10.1080/07391102.2020.1830854 . ПМИД 33030105 . S2CID 222217607 .
- ^ Вандик К., Деваль Дж. (август 2021 г.). «Соображения относительно открытия и разработки ингибиторов 3-химотрипсиноподобной цистеиновой протеазы, нацеленных на инфекцию SARS-CoV-2» . Современное мнение в вирусологии . 49 : 36–40. дои : 10.1016/j.coviro.2021.04.006 . ПМЦ 8075814 . ПМИД 34029993 .
- ^ Скули Р.Т., Карлин А.Ф., Бидл Дж.Р., Валяева Н., Чжан XQ, Кларк А.Е. и др. (сентябрь 2021 г.). «Переосмысление Ремдесивира: синтез, противовирусная активность и фармакокинетика пероральных липидных пролекарств» . Антимикробные средства и химиотерапия . 65 (10): e0115521. дои : 10.1128/AAC.01155-21 . ISSN 0066-4804 . ПМЦ 8448143 . ПМИД 34310217 . S2CID 236450769 .
- ^ Ахмад Б., Батул М., Айн Цюй, Ким М.С., Чой С. (август 2021 г.). «Изучение механизма связывания ингибитора протеазы SARS-CoV-2 PF-07321332 посредством молекулярной динамики и моделирования свободной энергии связывания» . Международный журнал молекулярных наук . 22 (17): 9124. doi : 10.3390/ijms22179124 . ПМЦ 8430524 . ПМИД 34502033 .
- ^ «Pfizer начинает дозирование противовирусного препарата для лечения Covid-19 в рамках фазы II/III» . Арена клинических испытаний . 2 сентября 2021 г. Архивировано из оригинала 5 ноября 2021 г. Проверено 5 ноября 2021 г.
- ^ Вудли М. (19 октября 2021 г.). «Каково потенциальное новое лечение COVID в Австралии?» . Новостигп . Архивировано из оригинала 5 ноября 2021 года . Проверено 6 ноября 2021 г.
- ^ «Новый кандидат на пероральное противовирусное лечение COVID-19 от Pfizer снизил риск госпитализации или смерти на 89% по данным промежуточного анализа фазы 2/3 исследования EPIC-HR» . 5 ноября 2021 г. Архивировано из оригинала 16 ноября 2021 г. Проверено 17 ноября 2021 г.
- ^ Вайнтрауб К. (5 ноября 2021 г.). «Противовирусный препарат Pfizer может почти положить конец смертности от COVID-19, предполагает исследование компании» . США сегодня . Архивировано из оригинала 5 ноября 2021 года . Проверено 5 ноября 2021 г.
- ^ Перейти обратно: а б Бауэр Дж., Спантон С., Генри Р., Квик Дж., Дзики В., Портер В., Моррис Дж. (июнь 2001 г.). «Ритонавир: необычайный пример конформационного полиморфизма». Фармацевтические исследования . 18 (6): 859–866. дои : 10.1023/А:1011052932607 . ПМИД 11474792 . S2CID 20923508 .
- ^ Перейти обратно: а б Мориссетт С.Л., Сукасен С., Левинсон Д., Сима М.Дж., Альмарссон О. (март 2003 г.). «Выявление разнообразия кристаллических форм ритонавира, ингибитора протеазы ВИЧ, путем высокопроизводительной кристаллизации» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (5): 2180–2184. дои : 10.1073/pnas.0437744100 . ПМК 151315 . ПМИД 12604798 .
- ^ Люттге А (1 февраля 2006 г.). «Кинетика растворения кристаллов и свободная энергия Гиббса». Журнал электронной спектроскопии и связанных с ней явлений . 150 (2): 248–259. дои : 10.1016/j.elspec.2005.06.007 .
- ^ Бучар Д.К., Ланкастер Р.В., Бернштейн Дж. (июнь 2015 г.). «Возвращение к исчезающим полиморфам» . Ангеванде Хеми . 54 (24): 6972–6993. дои : 10.1002/anie.201410356 . ПМК 4479028 . ПМИД 26031248 .
- ^ «Калетра FAQ» . Информация о продукте AbbVie Kaletra . ЭббВи. 2011. Архивировано из оригинала 7 июля 2014 года . Проверено 5 июля 2014 г.
- ^ Чжан С., Мацгер А.Дж. (февраль 2017 г.). «Недавно открытое рацемическое соединение пиоглитазона гидрохлорида более стабильно, чем коммерческий конгломерат» . Рост и дизайн кристаллов . 17 (2): 414–417. дои : 10.1021/acs.cgd.6b01638 . ПМЦ 6752731 . ПМИД 31537981 .
- ^ Коннолли С. (5 августа 2004 г.). «НИЗ отказывается вступать в битву за цены на лекарства от СПИДа» . Вашингтон Пост . Архивировано из оригинала 20 августа 2008 года . Проверено 16 января 2006 г.
Дальнейшее чтение
[ редактировать ]- Чембуркар С.Р., Бауэр Дж., Деминг К., Спивек Х., Патель К., Моррис Дж. и др. (2000). «Решение вопроса о влиянии полиморфов ритонавира на поздние стадии разработки процесса массового производства лекарств». Исследования и разработки органических процессов . 4 (5): 413–417. дои : 10.1021/op000023y .