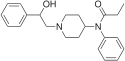
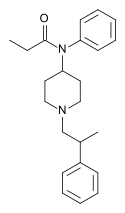
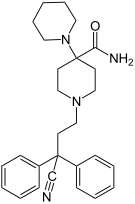
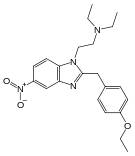
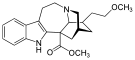
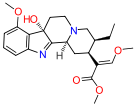
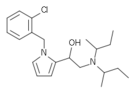
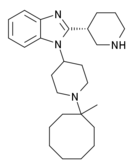
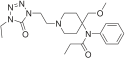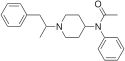Опиоид
| Опиоид | |
|---|---|
| Класс препарата | |
 | |
| Идентификаторы классов | |
| Использовать | Облегчение боли |
| код АТС | N02A |
| Способ действия | Опиоидный рецептор |
| Внешние ссылки | |
| МеШ | Д000701 |
| Юридический статус | |
| В Викиданных | |
Опиоиды — это класс наркотиков или имитируют их , которые получают из натуральных веществ, содержащихся в растении опийного мака, . Опиоиды воздействуют на мозг, оказывая различные эффекты, включая облегчение боли. Как класс веществ, они действуют на опиоидные рецепторы , вызывая морфиноподобный эффект. [2] [3]
Термины «опиоид» и «опиат» иногда используются как синонимы, но существуют ключевые различия, основанные на процессах производства этих лекарств. [4]
В медицине они в основном используются для облегчения боли , включая анестезию . [5] Другие медицинские применения включают подавление диареи , заместительную терапию расстройств, вызванных употреблением опиоидов , устранение передозировки опиоидов и подавление кашля . [5] Чрезвычайно сильные опиоиды, такие как карфентанил, разрешены только для использования в ветеринарии . [6] [7] [8] Опиоиды также часто используются в рекреационных целях из-за их эйфорического эффекта или для предотвращения абстиненции . [9] Опиоиды могут привести к смерти и использовались для казней в Соединенных Штатах .
Побочные эффекты опиоидов могут включать зуд , седативный эффект , тошноту , угнетение дыхания , запор и эйфорию . Длительное применение может вызвать толерантность , то есть для достижения того же эффекта требуются повышенные дозы, и физическую зависимость , то есть резкое прекращение приема препарата приводит к неприятным симптомам отмены. [10] Эйфория влечет за собой рекреационное употребление опиоидов, а частое и возрастающее рекреационное употребление опиоидов обычно приводит к зависимости. Передозировка таких или одновременное применение других депрессантов, как бензодиазепины, обычно приводит к смерти от угнетения дыхания . [11]
Опиоиды действуют путем связывания с опиоидными рецепторами, которые находятся главным образом в центральной и периферической нервной системе и желудочно-кишечном тракте . Эти рецепторы опосредуют как психоактивные , так и соматические эффекты опиоидов. Опиоидные препараты включают частичные агонисты , такие как противодиарейный препарат лоперамид , и антагонисты , такие как налоксегол, при запорах, вызванных опиоидами, которые не проникают через гематоэнцефалический барьер , но могут вытеснять другие опиоиды из связывания с этими рецепторами в миентеральном сплетении .
Поскольку опиоиды вызывают привыкание и могут привести к смертельной передозировке, большинство из них являются контролируемыми веществами . В 2013 году от 28 до 38 миллионов человек незаконно употребляли опиоиды (0,6–0,8% мирового населения в возрасте от 15 до 65 лет). [12] По оценкам, в 2011 году около 4 миллионов человек в Соединенных Штатах употребляли опиоиды в рекреационных целях или были от них зависимы. [13] По состоянию на 2015 год рост уровня рекреационного употребления и зависимости объясняется чрезмерным назначением опиоидных препаратов и недорогого запрещенного героина . [14] [15] [16] И наоборот, опасения по поводу чрезмерного назначения препаратов, преувеличенных побочных эффектов и зависимости от опиоидов также обвиняются в недостаточном лечении боли. [17] [18]
Терминология
[ редактировать ]
К опиоидам относятся опиаты — более старый термин, обозначающий такие препараты, полученные из опия , включая морфин . сам [19] Другие опиоиды представляют собой полусинтетические и синтетические наркотики, такие как гидрокодон , оксикодон и фентанил ; препараты-антагонисты, такие как налоксон ; и эндогенные пептиды, такие как эндорфины . [20] Термины «опиат» и «наркотик» иногда встречаются как синонимы опиоида. Правильно, опиаты ограничиваются природными алкалоидами, содержащимися в смоле опийного мака, хотя некоторые из них включают полусинтетические производные. [19] [21] Наркотик , образованный от слов, означающих «онемение» или «сон», как американский юридический термин, относится к кокаину и опиоидам, а также к их исходным материалам; его также широко применяют к любому нелегальному или контролируемому психоактивному веществу. [22] [23] В некоторых юрисдикциях все контролируемые наркотики по закону классифицируются как наркотики . Этот термин может иметь уничижительный оттенок, и его использование в таких случаях обычно не рекомендуется. [24] [25]
Медицинское использование
[ редактировать ]Боль
[ редактировать ]Слабый опиоид кодеин в низких дозах и в сочетании с одним или несколькими другими препаратами обычно доступен в рецептурных лекарствах и без рецепта для лечения легкой боли. [26] [27] [28] Другие опиоиды обычно используются для облегчения умеренной и сильной боли. [27]
Острая боль
[ редактировать ]Опиоиды эффективны для лечения острой боли (например, боли после операции). [29] Для немедленного облегчения острой боли средней и сильной степени опиоиды часто являются методом выбора из-за их быстрого начала действия, эффективности и снижения риска развития зависимости. Тем не менее, новый отчет показал явный риск длительного употребления опиоидов, когда опиоидные анальгетики назначаются для снятия острой боли после операции или травмы. [30] Также было обнаружено, что они важны в паллиативной помощи, помогая при тяжелой, хронической, инвалидизирующей боли, которая может возникать при некоторых неизлечимых состояниях, таких как рак, и дегенеративных состояниях, таких как ревматоидный артрит . Во многих случаях опиоиды являются успешной стратегией долгосрочного ухода за людьми с хронической болью, вызванной раком .
Чуть более половины всех штатов США приняли законы, ограничивающие назначение или отпуск опиоидов при острой боли. [31]
Хроническая нераковая боль
[ редактировать ]Рекомендации предполагают, что риск опиоидов, вероятно, превышает их пользу при использовании при большинстве нераковых хронических состояний, включая головные боли , боли в спине и фибромиалгию . [32] Таким образом, их следует использовать с осторожностью при хронической нераковой боли. [33] В случае использования польза и вред должны переоцениваться не реже одного раза в три месяца. [34]
При лечении хронической боли можно попробовать опиоиды после того, как будут рассмотрены другие менее опасные обезболивающие, включая парацетамол /ацетаминофен или НПВП, такие как ибупрофен или напроксен . [35] Некоторые виды хронической боли, включая боль, вызванную фибромиалгией или мигренью , преимущественно лечат другими препаратами, кроме опиоидов. [36] [37] Эффективность использования опиоидов для уменьшения хронической нейропатической боли неясна. [38]
Опиоиды противопоказаны в качестве лечения головной боли первой линии, поскольку они ухудшают концентрацию внимания, создают риск зависимости и повышают риск того, что эпизодические головные боли станут хроническими. [39] Опиоиды также могут вызывать повышенную чувствительность к головной боли. [39] Когда другие методы лечения неэффективны или недоступны, для лечения головной боли могут подойти опиоиды, если за пациентом можно наблюдать, чтобы предотвратить развитие хронической головной боли. [39]
Опиоиды все чаще используются для лечения незлокачественной хронической боли . [40] [41] [42] Эта практика в настоящее время привела к новой и растущей проблеме зависимости и злоупотребления опиоидами. [33] [43] Из-за различных негативных эффектов использование опиоидов для длительного лечения хронической боли не показано, за исключением случаев, когда другие менее опасные обезболивающие оказываются неэффективными. Хроническую боль, которая возникает лишь периодически, например, от нервных болей , мигрени и фибромиалгии , часто лучше лечить другими лекарствами, а не опиоидами. [36] Парацетамол / тайленол / ацетаминофен и нестероидные противовоспалительные препараты, включая ибупрофен и напроксен, считаются более безопасной альтернативой. [44] Их часто используют в сочетании с опиоидами, такими как парацетамол в сочетании с оксикодоном ( Перкосет ) и ибупрофен в сочетании с гидрокодоном ( Викопрофен ), что усиливает облегчение боли , но также предназначено для предотвращения использования в рекреационных целях. [45] [46]
Другой
[ редактировать ]Кашель
[ редактировать ]Кодеин когда-то считался «золотым стандартом» средств для подавления кашля , но теперь эта позиция подвергается сомнению. [47] Некоторые недавние плацебо -контролируемые исследования показали, что в некоторых случаях, включая острый кашель у детей, оно может быть не лучше, чем плацебо. [48] [49] Как следствие, он не рекомендуется детям. [49] Кроме того, нет никаких доказательств того, что гидрокодон полезен детям. [50] Аналогичным образом, голландское руководство 2012 года по лечению острого кашля не рекомендует его использование. [51] (Аналог опиоида декстрометорфан , который долгое время считался столь же эффективным средством подавления кашля, как и кодеин, [52] также продемонстрировал небольшую пользу в нескольких недавних исследованиях. [53] )
Низкие дозы морфина могут помочь при хроническом кашле, но его применение ограничено побочными эффектами. [54]
Диарея
[ редактировать ]В случаях синдрома раздраженного кишечника с преобладанием диареи для подавления диареи можно использовать опиоиды. Лоперамид — это периферически селективный опиоид, доступный без рецепта и используемый для подавления диареи.
Способность подавлять диарею также приводит к запорам, если опиоиды используются в течение нескольких недель. [55] Налоксегол , периферически селективный антагонист опиоидов, теперь доступен для лечения запоров, вызванных опиоидами. [56]
Одышка
[ редактировать ]Опиоиды могут помочь при одышке, особенно при запущенных заболеваниях, таких как рак и ХОБЛ . [57] [58] Однако результаты двух недавних систематических обзоров литературы показали, что опиоиды не обязательно более эффективны при лечении одышки у пациентов с поздней стадией рака. [59] [60]
Синдром беспокойных ног
[ редактировать ], обычно не являются первой линией лечения, Опиоиды, такие как оксикодон и метадон но иногда используются для лечения тяжелого и резистентного синдрома беспокойных ног . [61]
Гипералгезия
Опиоид-индуцированная гипералгезия (ОГГ) была очевидна у пациентов после хронического воздействия опиоидов. [62] [63]
Побочные эффекты
[ редактировать ]Обычный и краткосрочный
Другой
- Когнитивные эффекты
- Опиоидная зависимость
- Головокружение
- Потеря аппетита
- Задержка опорожнения желудка
- Снижение полового влечения
- Нарушение сексуальной функции
- Снижение уровня тестостерона
- Депрессия
- Иммунодефицит
- Повышенная болевая чувствительность
- Нерегулярные менструации
- Повышенный риск падений
- Замедленное дыхание
- Есть
Каждый год 69 000 человек во всем мире умирают от передозировки опиоидов, а 15 миллионов человек страдают опиоидной зависимостью. [65]
У пожилых людей употребление опиоидов связано с усилением побочных эффектов, таких как «седативный эффект, тошнота, рвота, запор, задержка мочи и падения». [66] В результате пожилые люди, принимающие опиоиды, подвергаются большему риску травм. [67] Опиоиды не вызывают какой-либо специфической органной токсичности, в отличие от многих других препаратов, таких как аспирин и парацетамол. Они не связаны с кровотечением из верхних отделов желудочно-кишечного тракта и токсичностью для почек . [68]
Назначение опиоидов при острой боли в пояснице и лечение остеоартрита, по-видимому, имеет долгосрочные побочные эффекты [69] [70]
По данным USCDC , метадон был причиной 31% смертей, связанных с опиоидами, в США в период с 1999 по 2010 год, а в качестве единственного наркотика - 40%, что намного выше, чем другие опиоиды. [71] Исследования долгосрочного применения опиоидов показали, что многие прекращают их прием и что незначительные побочные эффекты были обычным явлением. [72] Пристрастие возникло примерно у 0,3%. [72] В США в 2016 году передозировка опиоидами привела к смерти 1,7 из 10 000 человек. [73]
Нарушения подкрепления
[ редактировать ]Толерантность
[ редактировать ]Толерантность – это процесс, характеризующийся нейроадаптациями , которые приводят к снижению воздействия лекарств. Хотя активация рецепторов часто может играть важную роль, известны и другие механизмы. [74] Толерантность к некоторым эффектам более выражена, чем к другим; Толерантность развивается медленно к влиянию на настроение, зуду, задержке мочи и угнетению дыхания, но быстрее развивается к аналгезии и другим физическим побочным эффектам. Однако толерантность не развивается к запорам или миозу (сужению зрачка глаза менее или равным двум миллиметрам). Однако эта идея была оспорена: некоторые авторы утверждают, что толерантность действительно развивается до миоза. [75]
Толерантность к опиоидам ослабляется рядом веществ, в том числе:
- блокаторы кальциевых каналов [76] [77] [78]
- интратекальный магний [79] [80] и цинк [81]
- Антагонисты NMDA , такие как декстрометорфан , кетамин , [82] и мемантин . [83]
- антагонисты холецистокинина , такие как проглумид [84] [85] [86]
- новые агенты, такие как ингибитор фосфодиэстеразы ибудиласт . Для этого применения также исследовались [87]
Толерантность — это физиологический процесс, при котором организм приспосабливается к часто принимаемому лекарству, обычно требуя с течением времени более высоких доз того же лекарства для достижения того же эффекта. Это обычное явление у людей, принимающих высокие дозы опиоидов в течение длительного времени, но оно не указывает на какую-либо связь со злоупотреблением или зависимостью.
Физическая зависимость
[ редактировать ]Физическая зависимость – это физиологическая адаптация организма к присутствию вещества, в данном случае опиоидного препарата. Это определяется развитием синдрома отмены при прекращении приема вещества, при резком снижении дозы или, особенно в случае опиоидов, при антагониста ( например , налоксона ) или агониста-антагониста ( например , пентазоцина введении ). . Физическая зависимость является нормальным и ожидаемым аспектом приема некоторых лекарств и не обязательно означает, что у пациента есть зависимость.
Симптомы отмены опиатов могут включать тяжелую дисфорию , тягу к еще одной дозе опиатов, раздражительность, потливость , тошноту , ринорею , тремор , рвоту и миалгию . Медленное снижение потребления опиоидов в течение нескольких дней и недель может уменьшить или устранить симптомы абстиненции. [88] Скорость и тяжесть синдрома отмены зависят от периода полувыведения опиоида; Отказ от героина и морфина происходит быстрее, чем отказ от метадона . За острой фазой отмены часто следует затяжная фаза депрессии и бессонницы, которая может длиться месяцами. Симптомы отмены опиоидов можно лечить другими лекарствами, такими как клонидин . [89] Физическая зависимость не предсказывает злоупотребление наркотиками или настоящую зависимость и тесно связана с тем же механизмом, что и толерантность. Хотя существуют неофициальные заявления о пользе ибогаина , данные, подтверждающие его использование при зависимости от психоактивных веществ, недостаточны. [90]
У пациентов в критическом состоянии, получавших регулярные дозы опиоидов, ятрогенная абстиненция является частым синдромом. [91]
Зависимость
[ редактировать ]Наркомания – это сложный комплекс поведения, обычно связанный со злоупотреблением определенными наркотиками, развивающийся с течением времени и при более высоких дозах наркотиков. Зависимость включает в себя психологическое принуждение в той степени, в которой пострадавший человек упорствует в действиях, ведущих к опасным или нездоровым результатам. Опиоидная зависимость включает в себя инсуффляцию или инъекцию, а не прием опиоидов перорально, как это предписано по медицинским показаниям. [88]
В европейских странах, таких как Австрия, Болгария и Словакия, с медленным высвобождением пероральные формы морфина используются в опиатной заместительной терапии (ОЗТ) для пациентов, которые плохо переносят побочные эффекты бупренорфина или метадона . Бупренорфин также можно использовать вместе с налоксоном для более длительного лечения зависимости. В других европейских странах, включая Великобританию, это также легально используется для ОЗТ, хотя и с разной степенью приемлемости.
Лекарственные формы с медленным высвобождением предназначены для сдерживания злоупотреблений и снижения уровня зависимости, одновременно пытаясь обеспечить законное облегчение боли и простоту использования для пациентов, страдающих болью. Однако остаются вопросы об эффективности и безопасности этих типов препаратов. В настоящее время FDA рассматривает возможность получения одобрения на продажу других лекарств, устойчивых к несанкционированному вмешательству. [92] [93]
Количество имеющихся доказательств позволяет сделать лишь слабый вывод, но это предполагает, что врач, правильно контролирующий употребление опиоидов у пациентов, у которых в анамнезе нет расстройств, связанных с употреблением психоактивных веществ, может обеспечить долгосрочное облегчение боли с небольшим риском развития зависимости или других серьезных побочных эффектов. . [72]
Проблемы, связанные с опиоидами, включают следующее:
- Некоторые люди обнаруживают, что опиоиды не полностью облегчают боль. [94]
- Некоторые люди обнаруживают, что побочные эффекты опиоидов вызывают проблемы, которые перевешивают пользу от терапии. [72]
- У некоторых людей со временем вырабатывается толерантность к опиоидам. Это требует от них увеличения дозировки лекарств для сохранения эффекта, а это, в свою очередь, также увеличивает нежелательные побочные эффекты. [72]
- Длительное употребление опиоидов может вызвать опиоид-индуцированную гипералгезию , то есть состояние, при котором у пациента повышается чувствительность к боли. [95]
Все опиоиды могут вызывать побочные эффекты. [64] Общие побочные реакции у пациентов, принимающих опиоиды для облегчения боли, включают тошноту и рвоту, сонливость , зуд, сухость во рту, головокружение и запор . [64] [88]
Тошнота и рвота
[ редактировать ]Толерантность к тошноте развивается в течение 7–10 дней, в течение которых противорвотные средства ( например, низкие дозы галоперидола один раз на ночь). очень эффективны [ нужна ссылка ] Из-за серьезных побочных эффектов, таких как поздняя дискинезия, галоперидол в настоящее время используется редко. родственный препарат, прохлорперазин Чаще используется , хотя он имеет аналогичные риски. Более сильные противорвотные средства, такие как ондансетрон или трописетрон, иногда используются, когда тошнота сильная или продолжительная и беспокоит, несмотря на их более высокую стоимость. Менее дорогой альтернативой являются антагонисты дофамина, такие как домперидон и метоклопрамид. Домперидон не проникает через гематоэнцефалический барьер и не оказывает побочных центральных антидофаминергических эффектов, но блокирует рвотное действие опиоидов в триггерной зоне хеморецепторов . Этот препарат недоступен в США.
Некоторые антигистаминные препараты с антихолинергическими свойствами (например, орфенадрин , димедрол ) также могут быть эффективны. первого поколения Очень часто используется антигистаминный препарат гидроксизин , его дополнительные преимущества заключаются в том, что он не вызывает двигательных нарушений, а также обладает анальгезирующими свойствами. Δ 9 - тетрагидроканнабинол снимает тошноту и рвоту; [96] [97] он также вызывает анальгезию, которая может позволить снизить дозы опиоидов с уменьшением тошноты и рвоты. [98] [99]
- 5-HT3 ( Антагонисты например, ондансетрон )
- Антагонисты дофамина ( например, домперидон )
- Антихолинергические антигистаминные препараты ( например , димедрол )
- Д 9 -тетрагидроканнабинол ( например, дронабинол )
Рвота обусловлена желудочным застоем (объемная рвота, кратковременная тошнота, купируемая рвотой, пищеводный рефлюкс, чувство переполнения желудка, раннее насыщение), а также прямым действием на хеморецепторную триггерную зону area postrema — рвотный центр головного мозга. Таким образом, рвоту можно предотвратить с помощью прокинетиков ( например , домперидона или метоклопрамида ). Если рвота уже началась, эти препараты следует вводить неперорально ( например, подкожно для метоклопрамида, ректально для домперидона).
- Прокинетики ( например, домперидон )
- Антихолинергические средства ( например, орфенадрин )
Имеющиеся данные свидетельствуют о том, что опиоидная анестезия связана с послеоперационной тошнотой и рвотой. [100]
Пациенты с хронической болью, употребляющие опиоиды, имели небольшое улучшение боли и физического функционирования, а также повышенный риск рвоты. [101]
Сонливость
[ редактировать ]Толерантность к сонливости обычно развивается в течение 5–7 дней, но в случае возникновения проблем часто помогает переход на альтернативный опиоид. Определенные опиоиды, такие как фентанил , морфин и диаморфин (героин), имеют тенденцию оказывать особенное седативное действие, в то время как другие, такие как оксикодон , тилидин и меперидин (петидин), имеют тенденцию вызывать сравнительно меньший седативный эффект, но реакции отдельных пациентов могут заметно различаться и в некоторой степени могут варьироваться. ошибка может быть необходима для подбора наиболее подходящего препарата для конкретного пациента. В противном случае лечение ЦНС стимуляторами , как правило, эффективно. [102] [103]
- Стимуляторы ( например , кофеин , модафинил , амфетамин , метилфенидат )
Зуд
[ редактировать ]Зуд , как правило, не является серьезной проблемой, когда опиоиды используются для облегчения боли, но антигистаминные препараты полезны для противодействия зуду, когда он возникает. Неседативные антигистаминные препараты, такие как фексофенадин, часто являются предпочтительными, поскольку они позволяют избежать усиления сонливости, вызванной опиоидами. Однако некоторые седативные антигистаминные препараты, такие как орфенадрин, могут оказывать синергический обезболивающий эффект, позволяя использовать меньшие дозы опиоидов. В связи с этим на рынке появилось несколько комбинированных продуктов опиоидов и антигистаминных препаратов, таких как мепрозин ( меперидин / прометазин ) и диконал ( дипипанон / циклизин ), которые также могут уменьшить тошноту, вызванную опиоидами.
- Антигистаминные препараты ( например, фексофенадин )
Запор
[ редактировать ], вызванный опиоидами Запор (ОИК), развивается у 90–95% людей, длительно принимающих опиоиды. [104] Поскольку толерантность к этой проблеме обычно не развивается, большинству людей, длительно принимающих опиоиды, необходимо принимать слабительные средства или клизмы . [105]
Лечение ОИК последовательное и зависит от степени тяжести. [106] Первый способ лечения является немедикаментозным и включает в себя изменения образа жизни, такие как увеличение количества пищевых волокон , потребление жидкости (около 1,5 л (51 жидкая унция США) в день) и физическую активность . [106] Если нефармакологические меры неэффективны, слабительные , в том числе размягчители стула ( например , полиэтиленгликоль ), объемообразующие слабительные ( например , добавки с клетчаткой ), стимулирующие слабительные ( например , бисакодил , сенна ) и/или клизмы . можно использовать [106] Распространенным слабительным режимом при ОИК является комбинация докузата и бисакодила. [106] [107] [108] [ нужно обновить ] Осмотические слабительные , в том числе лактулоза , полиэтиленгликоль и магнезиальное молоко (гидроксид магния), а также минеральное масло ( смазывающее слабительное ), также часто используются при ОИК. [107] [108]
Если слабительные средства недостаточно эффективны (что часто бывает), [109] опиоидные препараты или схемы лечения, включающие периферически селективный опиоидный антагонист , такой как метилналтрексон бромид , налоксегол , алвимопан или налоксон (как в случае оксикодона/налоксона ). Можно попробовать [106] [108] [110] Кокрейновский обзор 2018 года (обновленный в 2022 году) показал, что доказательства в отношении алвимопана, налоксона или метилналтрексона бромида были умеренными, но с повышенным риском побочных эффектов. [111] Налоксон внутрь кажется наиболее эффективным. [112] Было показано, что ежедневная доза налдемедина в дозе 0,2 мг значительно улучшает симптомы у пациентов с ОИК. [113]
Смена опиоидов — один из методов, предложенных для минимизации последствий запоров у длительных потребителей. [114] Хотя все опиоиды вызывают запор, между препаратами существуют некоторые различия: исследования показывают, что трамадол , тапентадол , метадон и фентанил могут вызывать относительно меньшие запоры, тогда как при использовании кодеина , морфина , оксикодона или гидроморфона запор может быть сравнительно более тяжелым.
Угнетение дыхания
[ редактировать ]Угнетение дыхания является наиболее серьезной побочной реакцией, связанной с употреблением опиоидов, но обычно оно наблюдается при применении однократной внутривенной дозы у пациентов, ранее не принимавших опиоиды. У пациентов, регулярно принимающих опиоиды для облегчения боли, быстро развивается толерантность к угнетению дыхания, поэтому это не является клинической проблемой. Было разработано несколько препаратов, которые могут частично блокировать угнетение дыхания, хотя единственным стимулятором дыхания, одобренным в настоящее время для этой цели, является доксапрам , эффективность которого в этом применении ограничена. [115] [116] Новые препараты, такие как BIMU-8 и CX-546, могут оказаться гораздо более эффективными. [117] [118] [119] [ нужен неосновной источник ]
- Стимуляторы дыхания: агонисты каротидных хеморецепторов ( например, доксапрам ), 5-HT 4 агонисты ( например, BIMU8 ), агонисты δ-опиоидов ( например, BW373U86 ) и AMPAkines ( например, CX717 ) могут уменьшать угнетение дыхания, вызванное опиоидами, не влияя на анальгезию, но большинство эти препараты умеренно эффективны или имеют побочные эффекты, которые не позволяют использовать их у людей. Агонисты 5- HT1A, такие как 8-OH-DPAT и репинотан, также противодействуют угнетению дыхания, вызванному опиоидами, но в то же время уменьшают аналгезию, что ограничивает их полезность для этого применения.
- Антагонисты опиоидов ( например , налоксон , налмефен , дипренорфин )
Первые 24 часа после приема опиоидов кажутся наиболее критическими с точки зрения опасного для жизни ОИРЗ, но их можно предотвратить при более осторожном подходе к употреблению опиоидов. [120]
Пациенты с сердечными, респираторными заболеваниями и/или обструктивным апноэ во сне подвергаются повышенному риску развития ОИРЗ. [121]
Повышенная болевая чувствительность
[ редактировать ]гипералгезия, вызванная опиоидами – когда люди, использующие опиоиды для облегчения боли, парадоксальным образом У некоторых людей наблюдалась испытывают усиление боли в результате приема этого лекарства. Это явление, хотя и редкое, наблюдается у некоторых людей, получающих паллиативную помощь , чаще всего при быстром увеличении дозы. [122] [123] Если это произойдет, чередование нескольких различных опиоидных обезболивающих может уменьшить развитие усиления боли . [124] [125] Опиоидная гипералгезия чаще возникает при хроническом применении или кратковременном приеме высоких доз, но некоторые исследования показывают, что она может возникать и при очень низких дозах. [126] [127]
Побочные эффекты, такие как гипералгезия и аллодиния , иногда сопровождающиеся усилением нейропатической боли , могут быть последствиями длительного лечения опиоидными анальгетиками, особенно когда повышение толерантности приводит к потере эффективности и последующему постепенному увеличению дозы с течением времени. По-видимому, это во многом является результатом действия опиоидных препаратов на мишени, отличные от трех классических опиоидных рецепторов, включая ноцицептиновый рецептор , сигма-рецептор и Toll-подобный рецептор 4 , и на животных моделях этому можно противодействовать с помощью антагонистов этих мишеней, таких как J-113,397 , BD-1047 или (+)-налоксон соответственно. [128] В настоящее время не одобрено никаких препаратов, специально предназначенных для противодействия гипералгезии, вызванной опиоидами, у людей, и в тяжелых случаях единственным решением может быть прекращение использования опиоидных анальгетиков и замена их неопиоидными анальгетиками. Однако, поскольку индивидуальная чувствительность к развитию этого побочного эффекта сильно зависит от дозы и может варьироваться в зависимости от того, какой опиоидный анальгетик используется, многие пациенты могут избежать этого побочного эффекта просто за счет снижения дозы опиоидного препарата (обычно сопровождаемого добавлением дополнительного препарата). неопиоидный анальгетик), чередование различных опиоидных препаратов или переход на более мягкий опиоид со смешанным механизмом действия, который также противодействует нейропатической боли, особенно трамадол или тапентадол . [129] [130] [131]
- Антагонисты рецепторов NMDA, такие как кетамин.
- SNRIs, такие как милнаципран
- Противосудорожные препараты, такие как габапентин или прегабалин.
Другие побочные эффекты
[ редактировать ]Низкий уровень половых гормонов
[ редактировать ]Клинические исследования неизменно связывают употребление опиоидов в медицинских и рекреационных целях с гипогонадизмом (низким уровнем половых гормонов ) у представителей разных полов. Эффект является дозозависимым . Большинство исследований показывают, что у большинства (возможно, до 90%) хронических потребителей опиоидов развивается гипогонадизм. 2015 года Систематический обзор и метаанализ показали, что опиоидная терапия подавляет уровень тестостерона у мужчин в среднем примерно на 165 нг/дл (5,7 нмоль/л), что означает снижение уровня тестостерона почти на 50%. [132] И наоборот, опиоидная терапия существенно не повлияла на уровень тестостерона у женщин. [132] Однако опиоиды также могут влиять на менструацию у женщин, ограничивая выработку лютеинизирующего гормона (ЛГ). Гипогонадизм, вызванный опиоидами, вероятно, вызывает сильную связь употребления опиоидов с остеопорозом и переломами костей из-за дефицита эстрадиола . Это также может усилить боль и тем самым помешать ожидаемому клиническому эффекту лечения опиоидами. Гипогонадизм, вызванный опиоидами, вероятно, вызван их агонизмом к опиоидным рецепторам в гипоталамусе и гипофизе . [133] Одно исследование показало, что пониженный уровень тестостерона у героиновых наркоманов возвращается к норме в течение одного месяца после воздержания, что позволяет предположить, что этот эффект легко обратим и не является постоянным. [ нужна ссылка ] По состоянию на 2013 год [update]Влияние низких доз или острого употребления опиоидов на систему неясно эндокринную . [134] [135] [136] [137] Длительное употребление опиоидов может повлиять на другие гормональные системы . и [134]
Нарушение работы
[ редактировать ]Употребление опиоидов может быть фактором риска невозможности вернуться на работу. [138] [139]
Лица, выполняющие любую работу, связанную с безопасностью, не должны использовать опиоиды. [140] Медицинские работники не должны рекомендовать работникам, которые водят машину или используют тяжелое оборудование , включая краны или вилочные погрузчики, лечить хроническую или острую боль опиоидами. [140] Рабочие места, где руководят работниками, выполняющими операции, требующие соблюдения техники безопасности, должны поручать работникам менее деликатные обязанности до тех пор, пока их врачи лечат опиоидами. [140]
Люди, которые принимают опиоиды в течение длительного времени, имеют повышенную вероятность остаться безработными. [141] Прием опиоидов может еще больше разрушить жизнь пациента, а побочные эффекты самих опиоидов могут стать серьезным препятствием для ведения активной жизни пациентов, трудоустройства и продолжения карьеры.
Кроме того, отсутствие занятости может быть предиктором аномального использования рецептурных опиоидов. [142]
Повышенная аварийность
[ редактировать ]Употребление опиоидов может повысить вероятность несчастных случаев . Опиоиды могут увеличить риск дорожно-транспортных происшествий [143] [144] и случайные падения . [145]
Снижение внимания
Было показано, что опиоиды снижают внимание, особенно при использовании с антидепрессантами и/или противосудорожными препаратами. [146]
Редкие побочные эффекты
[ редактировать ]Нечастые побочные реакции у пациентов, принимающих опиоиды для облегчения боли, включают: дозозависимое угнетение дыхания (особенно при приеме более сильнодействующих опиоидов), спутанность сознания, галлюцинации , делирий , крапивницу , гипотермию , брадикардию / тахикардию , ортостатическую гипотензию , головокружение, головную боль, задержку мочи, мочеточниковую недостаточность. или спазм желчных путей, мышечная ригидность, миоклонус (при высоких дозах) и приливы (из-за высвобождения гистамина, за исключением фентанила и ремифентанила). [88] Как терапевтическое, так и хроническое употребление опиоидов может поставить под угрозу функцию иммунной системы . Опиоиды уменьшают пролиферацию клеток-предшественников макрофагов и лимфоцитов и влияют на дифференцировку клеток (Roy & Loh, 1996). Опиоиды также могут ингибировать миграцию лейкоцитов . Однако значимость этого в контексте облегчения боли неизвестна.
Беременность
[ редактировать ]Употребление опиоидов во время беременности может иметь серьезные последствия как для матери, так и для развивающегося плода.
Опиоиды — это класс наркотиков, в который входят отпускаемые по рецепту обезболивающие (например, оксикодон , гидрокодон ) и запрещенные вещества, такие как героин . Употребление опиоидов во время беременности связано с повышенным риском осложнений, включая повышенный риск преждевременных родов , низкого веса при рождении , задержки внутриутробного развития и мертворождения . Опиоиды — это вещества, которые могут проникать через плаценту, подвергая развивающийся плод воздействию лекарств. Это воздействие потенциально может привести к различным неблагоприятным последствиям для развития плода, включая повышенный риск врожденных дефектов . Одним из наиболее известных последствий употребления опиоидов матерью во время беременности является риск неонатального абстинентного синдрома (НАС). НАС возникает, когда у новорожденного после рождения возникают симптомы абстиненции из -за воздействия опиоидов в утробе матери. Употребление опиоидов матерью во время беременности также может иметь долгосрочные последствия для развития ребенка. Эти эффекты могут включать когнитивные и поведенческие проблемы, а также повышенный риск расстройств, связанных с употреблением психоактивных веществ. позже в жизни.Взаимодействия
[ редактировать ]Врачи, лечащие пациентов, употребляющих опиоиды в сочетании с другими лекарственными средствами, постоянно ведут документацию о том, что показано дальнейшее лечение, и осведомлены о возможностях корректировки лечения, если состояние пациента изменится и потребует менее рискованной терапии. [147]
С другими депрессантами
[ редактировать ]Одновременное применение опиоидов с другими депрессантами, такими как бензодиазепины или этанол, увеличивает частоту побочных эффектов и передозировок. [147] Несмотря на это, во многих местах одновременно отпускаются опиоиды и бензодиазепины. [148] [149] Как и в случае передозировки одного опиоида, комбинация опиоида и другого депрессанта может вызвать угнетение дыхания, часто приводящее к смерти. [150] Эти риски уменьшаются при тщательном наблюдении со стороны врача, который может проводить постоянный скрининг изменений в поведении пациентов и соблюдении режима лечения. [147]
Опиоидный антагонист
[ редактировать ]Эффекты опиоидов (неблагоприятные или иные) можно обратить вспять с помощью опиоидных антагонистов, таких как налоксон или налтрексон . [151] Эти конкурентные антагонисты связываются с опиоидными рецепторами с более высоким сродством, чем агонисты, но не активируют рецепторы. Это вытесняет агонист, ослабляя или обращая вспять его эффекты. Однако период полувыведения налоксона может быть короче, чем период полувыведения самого опиоида, поэтому может потребоваться повторное введение дозы или непрерывная инфузия, или антагонист более длительного действия, такой как налмефен может быть использован . У пациентов, регулярно принимающих опиоиды, важно, чтобы опиоид был отменен лишь частично, чтобы избежать тяжелой и мучительной реакции пробуждения с мучительной болью. Это достигается не введением полной дозы, а введением ее небольшими дозами до тех пор, пока частота дыхания не улучшится. Затем начинают инфузию, чтобы сохранить реверс на этом уровне, сохраняя при этом облегчение боли. Антагонисты опиоидов остаются стандартным методом лечения угнетения дыхания после передозировки опиоидами, причем наиболее часто используется налоксон, хотя антагонист длительного действия налмефен может использоваться для лечения передозировок опиоидов длительного действия, таких как метадон, а дипренорфин используется для купирования симптомов. эффекты чрезвычайно сильных опиоидов, используемых в ветеринарной медицине, таких как эторфин и карфентанил. Однако, поскольку опиоидные антагонисты также блокируют полезные эффекты опиоидных анальгетиков, они, как правило, полезны только для лечения передозировки, при этом опиоидные антагонисты используются вместе с опиоидными анальгетиками для уменьшения побочных эффектов, что требует тщательного титрования дозы и часто оказывается малоэффективным в дозах, достаточно низких, чтобы позволяют сохранить анальгезию.
Налтрексон, по-видимому, не увеличивает риск серьезных нежелательных явлений, что подтверждает безопасность перорального приема налтрексона. [152] Смертность или серьезные нежелательные явления из-за рикошетной токсичности у пациентов, принимавших налоксон, были редки. [153]
Фармакология
[ редактировать ]| Лекарство | Родственник потенция [154] | Неионизированный Фракция | Белок Связывание | Липид Растворимость [155] [156] [157] |
|---|---|---|---|---|
| Морфий | 1 | ++ | ++ | ++ |
| Петидин (меперидин) | 0.1 | + | +++ | +++ |
| гидроморфон | 10 | + | +++ | |
| Альфентанил | 10–25 | ++++ | ++++ | +++ |
| Фентанил | 50–100 [158] [159] [160] | + | +++ | ++++ |
| Ремифентанил | 250 [ нужна ссылка ] | +++ | +++ | ++ |
| Суфентанил | 500–1000 | ++ | ++++ | ++++ |
| Эторфин | 1000–3000 | |||
| Карфентанил | 10000 |
Опиоиды связываются со специфическими опиоидными рецепторами в нервной системе и других тканях. Существует три основных класса опиоидных рецепторов: μ , κ , δ (мю, каппа и дельта), хотя сообщалось о семнадцати, включая ε, ι, λ и ζ (эпсилон, йота, лямбда и дзета). ) рецепторы. И наоборот, σ ( сигма ) рецепторы больше не считаются опиоидными рецепторами, поскольку их активация не реверсируется опиоидным обратным агонистом налоксоном , они не обладают высоким сродством связывания с классическими опиоидами и стереоселективны в отношении правовращающих изомеров. в то время как другие опиоидные рецепторы стереоселективны в отношении левовращающих изомеров. Кроме того, существует три подтипа μ -рецептора: μ 1 и μ 2 , а также недавно открытый μ 3 . Другим рецептором, имеющим клиническое значение, является опиоидный рецептор-подобный рецептор 1 (ORL1), который участвует в болевых реакциях, а также играет важную роль в развитии толерантности к мю-опиоидным агонистам, используемым в качестве анальгетиков. Все это рецепторы, связанные с G-белком. действует на ГАМКергическую нейротрансмиссию .
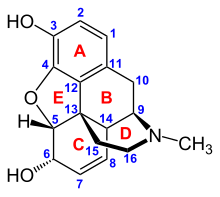
Фармакодинамический опиоид ответ на опиоид зависит от рецептора, с которым он связывается, его сродства к этому рецептору, а также от того, является ли агонистом или антагонистом . Например, супраспинальные анальгетические свойства опиоидного агониста морфина опосредованы активацией рецептора μ 1 ; угнетение дыхания и физическая зависимость от рецептора μ 2 ; а также седация и спинальная аналгезия с помощью κ-рецептора. [ нужна ссылка ] . Каждая группа опиоидных рецепторов вызывает отдельный набор неврологических реакций, при этом подтипы рецепторов (например, µ 1 и µ 2 ) обеспечивают еще более [измеримо] специфические реакции. Уникальным для каждого опиоида является его различное сродство связывания с различными классами опиоидных рецепторов ( например, опиоидные рецепторы μ, κ и δ активируются с разной силой в соответствии со специфическим сродством связывания опиоида с рецептором). Например, опиатный алкалоид морфин проявляет высокое сродство к μ-опиоидному рецептору, тогда как кетазоцин проявляет высокое сродство к θ-рецепторам. Именно этот комбинаторный механизм позволяет существовать такому широкому классу опиоидов и молекулярных конструкций, каждый из которых имеет свой уникальный профиль эффекта. Их индивидуальная молекулярная структура также отвечает за разную продолжительность их действия, при этом метаболический распад (например, N -дезалкилирование) отвечает за метаболизм опиоидов.

Функциональная избирательность
[ редактировать ]Новая стратегия разработки лекарств учитывает передачу сигналов рецепторов . Эта стратегия направлена на усиление активации желаемых сигнальных путей при одновременном снижении воздействия на нежелательные пути. Этой дифференциальной стратегии дали несколько названий, включая функциональную селективность и предвзятый агонизм. Первым опиоидом, который был намеренно разработан как необъективный агонист и прошел клиническую оценку, является препарат олицеридин . Он проявляет анальгетическую активность и снижает побочные эффекты. [162]
Сравнение опиоидов
[ редактировать ]Были проведены обширные исследования для определения коэффициентов эквивалентности, сравнивающих относительную эффективность опиоидов. Учитывая дозу опиоида, эквианальгезии для определения эквивалентной дозировки другого опиоида используется таблица . Такие таблицы используются в практике ротации опиоидов, а также для описания опиоидов в сравнении с морфином, эталонным опиоидом. В таблицах эквианальгезии обычно указаны периоды полураспада лекарств, а иногда и эквианальгетические дозы одного и того же препарата при введении, например морфина: перорально и внутривенно.
Привязка профилей
[ редактировать ]Использование
[ редактировать ]| Вещество | Лучший оценивать | Низкий оценивать | Высокий оценивать |
|---|---|---|---|
| Амфетамин- типа стимуляторы | 34.16 | 13.42 | 55.24 |
| Каннабис | 192.15 | 165.76 | 234.06 |
| Кокаин | 18.20 | 13.87 | 22.85 |
| Экстази | 20.57 | 8.99 | 32.34 |
| Опиаты | 19.38 | 13.80 | 26.15 |
| Опиоиды | 34.26 | 27.01 | 44.54 |
Количество рецептов на опиоиды в США увеличилось с 76 миллионов в 1991 году до 207 миллионов в 2013 году. [185]
В 1990-е годы значительно возросло назначение опиоидов. Когда-то опиоиды использовались почти исключительно для лечения острой боли или боли, вызванной раком, теперь их широко прописывают людям, испытывающим хроническую боль. Это сопровождалось ростом случаев случайной зависимости и случайных передозировок, приводящих к смерти. По данным Международного комитета по контролю над наркотиками , США и Канада лидируют по потреблению рецептурных опиоидов на душу населения. [186] Число рецептов на опиоиды на душу населения в США и Канаде вдвое превышает потребление в Европейском Союзе, Австралии и Новой Зеландии. [187] Определенные группы населения пострадали от кризиса опиоидной зависимости больше, чем другие, включая первого мира . сообщества стран [188] и население с низкими доходами. [189] Специалисты общественного здравоохранения говорят, что это может быть результатом недоступности или высокой стоимости альтернативных методов лечения хронической боли. [190] Опиоиды описываются как экономически эффективное средство лечения хронической боли, но при оценке их экономической эффективности следует учитывать влияние опиоидной эпидемии и смертей, вызванных передозировкой опиоидов. [191] Данные за 2017 год показывают, что в США около 3,4 процента населения США прописывают опиоиды для ежедневного обезболивания. [192] Призывы к отмене назначения опиоидов привели к широкомасштабной практике снижения дозы опиоидов при небольшом количестве научных доказательств, подтверждающих безопасность или пользу для пациентов с хронической болью.
История
[ редактировать ]Натуральные опиоиды
[ редактировать ]
Опиоиды являются одними из старейших известных наркотиков в мире. [193] Самые ранние известные свидетельства присутствия Papaver somniferum на археологических раскопках человека относятся к периоду неолита около 5700–5500 гг. До н.э. Его семена были найдены в Куэва-де-лос-Мурсьелагос на Пиренейском полуострове и в Ла-Мармотте на Итальянском полуострове . [194] [195] [196]
Использование опийного мака в медицинских, развлекательных и религиозных целях восходит к четвертому веку до нашей эры, когда иероглифы на шумерских глиняных табличках упоминают использование «Хул Гиль», «растения радости». [197] [198] [199] Опиум был известен египтянам и упоминается в папирусе Эберса как ингредиент смеси для успокоения детей. [200] [199] и для лечения абсцессов молочной железы. [201]
Опиум был известен и грекам. [200] ) и его ученики ценили его Гиппократ ( ок. 460 – ок. 370 до н.э. за его снотворные свойства и использовали для лечения боли. [202] Латинская поговорка «Sedare dolorem opus divinum est», пер. «Облегчение боли — дело божественное» приписывалось по-разному Гиппократу и Галену из Пергама . [203] Медицинское использование опиума позднее обсуждается Педанием Диоскоридом ( ок. 40–90 гг. н.э.), греческим врачом, служившим в римской армии, в его пятитомном труде De Materia Medica . [204]
Во время Золотого века ислама употребление опиума подробно обсуждалось Авиценной ( ок. 980 – июнь 1037 г. н.э.) в «Каноне медицины» . Пять томов книги включают информацию о приготовлении опиума, ряде физических эффектов, его использовании для лечения различных заболеваний, противопоказаниях к его употреблению, его потенциальной опасности как яда и возможной зависимости. Авиценна не одобрял употребление опиума, кроме как в крайнем случае, предпочитая устранять причины боли, а не пытаться свести ее к минимуму с помощью анальгетиков . Многие наблюдения Авиценны были подтверждены современными медицинскими исследованиями. [205] [200]
Точно неизвестно, когда мир узнал об опиуме в Индии и Китае, но опиум упоминается в китайском медицинском труде Кай-пао-пен-цдо (973 г. н.э.). [199] К 1590 году нашей эры опийный мак был основной весенней культурой в субахах региона Агры . [206]
Врачу Парацельсу ( ок. 1493–1541 ) часто приписывают повторное введение опиума в медицинское применение в Западной Европе во время немецкого Возрождения . Он превозносил преимущества опиума в медицинских целях. Он также утверждал, что у него есть «арканум», таблетка, которую он называл лауданум , которая превосходила все другие, особенно когда нужно было обмануть смерть. («Ich hab' ein Arcanum – heiss' ich Laudanum, ist über das Alles, wo es zum Tode reichen will».) [207] Более поздние авторы утверждали, что рецепт лауданума Парацельса содержал опиум, но его состав остается неизвестным. [207]
Laudanum
[edit]The term laudanum was used generically for a useful medicine until the 17th century. After Thomas Sydenham introduced the first liquid tincture of opium, "laudanum" came to mean a mixture of both opium and alcohol.[207] Sydenham's 1669 recipe for laudanum mixed opium with wine, saffron, clove and cinnamon.[208] Sydenham's laudanum was used widely in both Europe and the Americas until the 20th century.[200][208] Other popular medicines, based on opium, included Paregoric, a much milder liquid preparation for children; Black-drop, a stronger preparation; and Dover's powder.[208]
The opium trade
[edit]Opium became a major colonial commodity, moving legally and illegally through trade networks involving India, the Portuguese, the Dutch, the British and China, among others.[209]The British East India Company saw the opium trade as an investment opportunity in 1683 AD.[206] In 1773 the Governor of Bengal established a monopoly on the production of Bengal opium, on behalf of the East India Company. The cultivation and manufacture of Indian opium was further centralized and controlled through a series of acts, between 1797 and 1949.[206][210] The British balanced an economic deficit from the importation of Chinese tea by selling Indian opium which was smuggled into China in defiance of Chinese government bans. This led to the First (1839–1842) and Second Opium Wars (1856–1860) between China and Britain.[211][210][209][212]
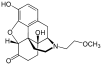
Morphine
[edit]In the 19th century, two major scientific advances were made that had far-reaching effects. Around 1804, German pharmacist Friedrich Sertürner isolated morphine from opium. He described its crystallization, structure, and pharmacological properties in a well-received paper in 1817.[211][213][208][214] Morphine was the first alkaloid to be isolated from any medicinal plant, the beginning of modern scientific drug discovery.[211][215]
The second advance, nearly fifty years later, was the refinement of the hypodermic needle by Alexander Wood and others. Development of a glass syringe with a subcutaneous needle made it possible to easily administer controlled measurable doses of a primary active compound.[216][208][199][217][218]
Morphine was initially hailed as a wonder drug for its ability to ease pain.[219] It could help people sleep,[211] and had other useful side effects, including control of coughing and diarrhea.[220] It was widely prescribed by doctors, and dispensed without restriction by pharmacists. During the American Civil War, opium and laudanum were used extensively to treat soldiers.[221][219] It was also prescribed frequently for women, for menstrual pain and diseases of a "nervous character".[222]: 85 At first it was assumed (wrongly) that this new method of application would not be addictive.[211][222]
Codeine
[edit]Codeine was discovered in 1832 by Pierre Jean Robiquet. Robiquet was reviewing a method for morphine extraction, described by Scottish chemist William Gregory (1803–1858). Processing the residue left from Gregory's procedure, Robiquet isolated a crystalline substance from the other active components of opium. He wrote of his discovery: "Here is a new substance found in opium ... We know that morphine, which so far has been thought to be the only active principle of opium, does not account for all the effects and for a long time the physiologists are claiming that there is a gap that has to be filled."[223] His discovery of the alkaloid led to the development of a generation of antitussive and antidiarrheal medicines based on codeine.[224]
Semisynthetic and synthetic opioids
[edit]Synthetic opioids were invented, and biological mechanisms for their actions discovered, in the 20th century.[199] Scientists have searched for non-addictive forms of opioids, but have created stronger ones instead. In England Charles Romley Alder Wright developed hundreds of opiate compounds in his search for a nonaddictive opium derivative. In 1874 he became the first person to synthesize diamorphine (heroin), using a process called acetylation which involved boiling morphine with acetic anhydride for several hours.[211]
Heroin received little attention until it was independently synthesized by Felix Hoffmann (1868–1946), working for Heinrich Dreser (1860–1924) at Bayer Laboratories.[225] Dreser brought the new drug to market as an analgesic and a cough treatment for tuberculosis, bronchitis, and asthma in 1898. Bayer ceased production in 1913, after heroin's addictive potential was recognized.[211][226][227]
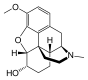
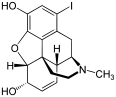
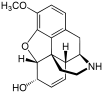
Several semi-synthetic opioids were developed in Germany in the 1910s. The first, oxymorphone, was synthesized from thebaine, an opioid alkaloid in opium poppies, in 1914.[228]Next, Martin Freund and Edmund Speyer developed oxycodone, also from thebaine, at the University of Frankfurt in 1916.[229]In 1920, hydrocodone was prepared by Carl Mannich and Helene Löwenheim, deriving it from codeine. In 1924, hydromorphone was synthesized by adding hydrogen to morphine. Etorphine was synthesized in 1960, from the oripavine in opium poppy straw. Buprenorphine was discovered in 1972.[228]
The first fully synthetic opioid was meperidine (later demerol), found serendipitously by German chemist Otto Eisleb (or Eislib) at IG Farben in 1932.[228] Meperidine was the first opiate to have a structure unrelated to morphine, but with opiate-like properties.[199] Its analgesic effects were discovered by Otto Schaumann in 1939.[228]Gustav Ehrhart and Max Bockmühl, also at IG Farben, built on the work of Eisleb and Schaumann. They developed "Hoechst 10820" (later methadone) around 1937.[230]In 1959 the Belgian physician Paul Janssen developed fentanyl, a synthetic drug with 30 to 50 times the potency of heroin.[211][231]Nearly 150 synthetic opioids are now known.[228]
Criminalization and medical use
[edit]Non-clinical use of opium was criminalized in the United States by the Harrison Narcotics Tax Act of 1914, and by many other laws.[232][233] The use of opioids was stigmatized, and it was seen as a dangerous substance, to be prescribed only as a last resort for dying patients.[211] The Controlled Substances Act of 1970 eventually relaxed the harshness of the Harrison Act.[citation needed]
In the United Kingdom the 1926 report of the Departmental Committee on Morphine and Heroin Addiction under the Chairmanship of the President of the Royal College of Physicians reasserted medical control and established the "British system" of control—which lasted until the 1960s.[234]
In the 1980s the World Health Organization published guidelines for prescribing drugs, including opioids, for different levels of pain. In the U.S., Kathleen Foley and Russell Portenoy became leading advocates for the liberal use of opioids as painkillers for cases of "intractable non-malignant pain".[235][236]With little or no scientific evidence to support their claims, industry scientists and advocates suggested that people with chronic pain would be resistant to addiction.[211][237][235]
The release of OxyContin in 1996 was accompanied by an aggressive marketing campaign promoting the use of opioids for pain relief. Increasing prescription of opioids fueled a growing black market for heroin. Between 2000 and 2014 there was an "alarming increase in heroin use across the country and an epidemic of drug overdose deaths".[237][211][238]
As a result, health care organizations and public health groups, such as Physicians for Responsible Opioid Prescribing, have called for decreases in the prescription of opioids.[237] In 2016, the Centers for Disease Control and Prevention (CDC) issued a new set of guidelines for the prescription of opioids "for chronic pain outside of active cancer treatment, palliative care, and end-of-life care" and the increase of opioid tapering.[239]
"Remove the Risk"
[edit]In April 2019 the U.S. Food and Drug Administration announced the launch of a new education campaign to help Americans understand the important role they play in removing and properly disposing of unused prescription opioids from their homes. This new initiative is part of the FDA's continued efforts to address the nationwide opioid crisis (see below) and aims to help decrease unnecessary exposure to opioids and prevent new addiction. The "Remove the Risk" campaign is targeting women ages 35–64, who are most likely to oversee household health care decisions and often serve as the gatekeepers to opioids and other prescription medications in the home.[240]
Society and culture
[edit]Definition
[edit]The term "opioid" originated in the 1950s.[241] It combines "opium" + "-oid" meaning "opiate-like" ("opiates" being morphine and similar drugs derived from opium). The first scientific publication to use it, in 1963, included a footnote stating, "In this paper, the term, 'opioid', is used in the sense originally proposed by George H. Acheson (personal communication) to refer to any chemical compound with morphine-like activities".[242] By the late 1960s, research found that opiate effects are mediated by activation of specific molecular receptors in the nervous system, which were termed "opioid receptors".[243] The definition of "opioid" was later refined to refer to substances that have morphine-like activities that are mediated by the activation of opioid receptors. One modern pharmacology textbook states: "the term opioid applies to all agonists and antagonists with morphine-like activity, and also the naturally occurring and synthetic opioid peptides".[244] Another pharmacology reference eliminates the morphine-like requirement: "Opioid, a more modern term, is used to designate all substances, both natural and synthetic, that bind to opioid receptors (including antagonists)".[2] Some sources define the term opioid to exclude opiates, and others use opiate comprehensively instead of opioid, but opioid used inclusively is considered modern, preferred and is in wide use.[19]
Efforts to reduce recreational use in the US
[edit]In 2011, the Obama administration released a white paper describing the administration's plan to deal with the opioid crisis. The administration's concerns about addiction and accidental overdosing have been echoed by numerous other medical and government advisory groups around the world.[190][245][246][247]
As of 2015, prescription drug monitoring programs exist in every state, except for Missouri.[248] These programs allow pharmacists and prescribers to access patients' prescription histories in order to identify suspicious use. However, a survey of US physicians published in 2015 found that only 53% of doctors used these programs, while 22% were not aware that the programs were available to them.[249] The Centers for Disease Control and Prevention was tasked with establishing and publishing a new guideline, and was heavily lobbied.[250] In 2016, the United States Centers for Disease Control and Prevention published its Guideline for Prescribing Opioids for Chronic Pain, recommending that opioids only be used when benefits for pain and function are expected to outweigh risks, and then used at the lowest effective dosage, with avoidance of concurrent opioid and benzodiazepine use whenever possible.[34] Research suggests that the prescription of high doses of opioids related to chronic opioid therapy (COT) can at times be prevented through state legislative guidelines and efforts by health plans that devote resources and establish shared expectations for reducing higher doses.[251]
On 10 August 2017, Donald Trump declared the opioid crisis a (non-FEMA) national public health emergency.[252]
Global shortages
[edit]Morphine and other poppy-based medicines have been identified by the World Health Organization as essential in the treatment of severe pain. As of 2002, seven countries (USA, UK, Italy, Australia, France, Spain and Japan) use 77% of the world's morphine supplies, leaving many emerging countries lacking in pain relief medication.[253] The current system of supply of raw poppy materials to make poppy-based medicines is regulated by the International Narcotics Control Board under the provision of the 1961 Single Convention on Narcotic Drugs. The amount of raw poppy materials that each country can demand annually based on these provisions must correspond to an estimate of the country's needs taken from the national consumption within the preceding two years. In many countries, underprescription of morphine is rampant because of the high prices and the lack of training in the prescription of poppy-based drugs. The World Health Organization is now working with administrations from various countries to train healthworkers and to develop national regulations regarding drug prescription to facilitate a greater prescription of poppy-based medicines.[254]
Another idea to increase morphine availability is proposed by the Senlis Council, who suggest, through their proposal for Afghan Morphine, that Afghanistan could provide cheap pain relief solutions to emerging countries as part of a second-tier system of supply that would complement the current INCB regulated system by maintaining the balance and closed system that it establishes while providing finished product morphine to those in severe pain and unable to access poppy-based drugs under the current system.
Recreational use
[edit]
Opioids can produce strong feelings of euphoria[255] and are frequently used recreationally. Traditionally associated with illicit opioids such as heroin, prescription opioids are misused recreationally.
Drug misuse and non-medical use include the use of drugs for reasons or at doses other than prescribed. Opioid misuse can also include providing medications to persons for whom it was not prescribed. Such diversion may be treated as crimes, punishable by imprisonment in many countries.[256][257] In 2014, almost 2 million Americans abused or were dependent on prescription opioids.[258][259]
Classification
[edit]There are a number of broad classes of opioids:[260]
- Natural opiates: alkaloids contained in the resin of the opium poppy, primarily morphine, codeine, and thebaine, but not papaverine and noscapine which have a different mechanism of action
- Esters of morphine opiates: slightly chemically altered but more natural than the semi-synthetics, as most are morphine prodrugs, diacetylmorphine (morphine diacetate; heroin), nicomorphine (morphine dinicotinate), dipropanoylmorphine (morphine dipropionate), desomorphine, acetylpropionylmorphine, dibenzoylmorphine, diacetyldihydromorphine;[261][262]
- Semi-synthetic opioids: created from either the natural opiates or morphine esters, such as hydromorphone, hydrocodone, oxycodone, oxymorphone, ethylmorphine and buprenorphine;
- Fully synthetic opioids: such as fentanyl, pethidine, levorphanol, methadone, tramadol, tapentadol, and dextropropoxyphene;
- Endogenous opioid peptides, produced naturally in the body, such as endorphins, enkephalins, dynorphins, and endomorphins.
- Endogenous opioids, non-peptide: Morphine, and some other opioids, which are produced in small amounts in the body, are included in this category.
- Natural opioids, non-animal, non-opiate: the leaves from Mitragyna speciosa (kratom) contain a few naturally-occurring opioids, active via Mu- and Delta receptors. Salvinorin A, found naturally in the Salvia divinorum plant, is a kappa-opioid receptor agonist.[263]
Tramadol and tapentadol, which act as monoamine uptake inhibitors also act as mild and potent agonists (respectively) of the μ-opioid receptor.[264] Both drugs produce analgesia even when naloxone, an opioid antagonist, is administered.[265]
Some minor opium alkaloids and various substances with opioid action are also found elsewhere, including molecules present in kratom, Corydalis, and Salvia divinorum plants and some species of poppy aside from Papaver somniferum. There are also strains which produce copious amounts of thebaine, an important raw material for making many semi-synthetic and synthetic opioids. Of all of the more than 120 poppy species, only two produce morphine.
Amongst analgesics there are a small number of agents which act on the central nervous system but not on the opioid receptor system and therefore have none of the other (narcotic) qualities of opioids although they may produce euphoria by relieving pain—a euphoria that, because of the way it is produced, does not form the basis of habituation, physical dependence, or addiction. Foremost amongst these are nefopam, orphenadrine, and perhaps phenyltoloxamine or some other antihistamines. Tricyclic antidepressants have painkilling effect as well, but they're thought to do so by indirectly activating the endogenous opioid system. Paracetamol is predominantly a centrally acting analgesic (non-narcotic) which mediates its effect by action on descending serotoninergic (5-hydroxy triptaminergic) pathways, to increase 5-HT release (which inhibits release of pain mediators). It also decreases cyclo-oxygenase activity. It has recently been discovered that most or all of the therapeutic efficacy of paracetamol is due to a metabolite, AM404, which enhances the release of serotonin and inhibits the uptake of anandamide.[citation needed]
Other analgesics work peripherally (i.e., not on the brain or spinal cord). Research is starting to show that morphine and related drugs may indeed have peripheral effects as well, such as morphine gel working on burns. Recent investigations discovered opioid receptors on peripheral sensory neurons.[266] A significant fraction (up to 60%) of opioid analgesia can be mediated by such peripheral opioid receptors, particularly in inflammatory conditions such as arthritis, traumatic or surgical pain.[267] Inflammatory pain is also blunted by endogenous opioid peptides activating peripheral opioid receptors.[268]
It was discovered in 1953,[citation needed] that humans and some animals naturally produce minute amounts of morphine, codeine, and possibly some of their simpler derivatives like heroin and dihydromorphine, in addition to endogenous opioid peptides. Some bacteria are capable of producing some semi-synthetic opioids such as hydromorphone and hydrocodone when living in a solution containing morphine or codeine respectively.
Many of the alkaloids and other derivatives of the opium poppy are not opioids or narcotics; the best example is the smooth-muscle relaxant papaverine. Noscapine is a marginal case as it does have CNS effects but not necessarily similar to morphine, and it is probably in a category all its own.
Dextromethorphan (the stereoisomer of levomethorphan, a semi-synthetic opioid agonist) and its metabolite dextrorphan have no opioid analgesic effect at all despite their structural similarity to other opioids; instead they are potent NMDA antagonists and sigma 1 and 2-receptor agonists and are used in many over-the-counter cough suppressants.
Salvinorin A is a unique selective, powerful ĸ-opioid receptor agonist. It is not properly considered an opioid nevertheless, because:
- chemically, it is not an alkaloid; and
- it has no typical opioid properties: absolutely no anxiolytic or cough-suppressant effects. It is instead a powerful hallucinogen.
| Opioid peptides | Skeletal molecular images |
|---|---|
| Adrenorphin |  |
| Amidorphin |  |
| Casomorphin | |
| DADLE | |
| DAMGO |  |
| Dermorphin | |
| Endomorphin |  |
| Morphiceptin |  |
| Nociceptin |  |
| Octreotide |  |
| Opiorphin |  |
| TRIMU 5 |  |
Endogenous opioids
[edit]Opioid-peptides that are produced in the body include:
β-endorphin is expressed in Pro-opiomelanocortin (POMC) cells in the arcuate nucleus, in the brainstem and in immune cells, and acts through μ-opioid receptors. β-endorphin has many effects, including on sexual behavior and appetite. β-endorphin is also secreted into the circulation from pituitary corticotropes and melanotropes. α-neoendorphin is also expressed in POMC cells in the arcuate nucleus.
Met-enkephalin is widely distributed in the CNS and in immune cells; [met]-enkephalin is a product of the proenkephalin gene, and acts through μ and δ-opioid receptors. leu-enkephalin, also a product of the proenkephalin gene, acts through δ-opioid receptors.
Dynorphin acts through κ-opioid receptors, and is widely distributed in the CNS, including in the spinal cord and hypothalamus, including in particular the arcuate nucleus and in both oxytocin and vasopressin neurons in the supraoptic nucleus.
Endomorphin acts through μ-opioid receptors, and is more potent than other endogenous opioids at these receptors.
Opium alkaloids and derivatives
[edit]Opium alkaloids
[edit]Phenanthrenes naturally occurring in (opium):
Preparations of mixed opium alkaloids, including papaveretum, are still occasionally used.
Esters of morphine
[edit]- Diacetylmorphine (morphine diacetate; heroin)
- Nicomorphine (morphine dinicotinate)
- Dipropanoylmorphine (morphine dipropionate)
- Diacetyldihydromorphine
- Acetylpropionylmorphine
- Desomorphine
- Methyldesorphine
- Dibenzoylmorphine
Ethers of morphine
[edit]Semi-synthetic alkaloid derivatives
[edit]- Buprenorphine
- Etorphine
- Hydrocodone
- Hydromorphone
- Oxycodone (sold as OxyContin)
- Oxymorphone
Synthetic opioids
[edit]Anilidopiperidines
[edit]Benzimidazoles
[edit]Benzimidazoles opioids are also known as nitazenes.
Phenylpiperidines
[edit]Diphenylpropylamine derivatives
[edit]- Propoxyphene
- Dextropropoxyphene
- Dextromoramide
- Bezitramide
- Piritramide
- Methadone
- Dipipanone
- Levomethadyl acetate (LAAM)
- Difenoxin
- Diphenoxylate
- Loperamide (does cross the blood–brain barrier but is quickly pumped into the non-central nervous system by P-Glycoprotein. Mild opiate withdrawal in animal models exhibits this action after sustained and prolonged use including rhesus monkeys, mice, and rats.)
Benzomorphan derivatives
[edit]- Dezocine—agonist/antagonist
- Pentazocine—agonist/antagonist
- Phenazocine
Oripavine derivatives
[edit]- Buprenorphine—partial agonist
- Dihydroetorphine
- Etorphine
Morphinan derivatives
[edit]- Butorphanol—agonist/antagonist
- Nalbuphine—agonist/antagonist
- Levorphanol
- Levomethorphan
- Racemethorphan
Others
[edit]Allosteric modulators
[edit]Plain allosteric modulators do not belong to the opioids, instead they are classified as opioidergics.
- Nalmefene
- Naloxone
- Naltrexone
- Methylnaltrexone (Methylnaltrexone is only peripherally active as it does not cross the blood–brain barrier in sufficient quantities to be centrally active. As such, it can be considered the antithesis of loperamide.)
- Naloxegol (Naloxegol is only peripherally active as it does not cross the blood–brain barrier in sufficient quantities to be centrally active. As such, it can be considered the antitheses of loperamide.)
Tables of opioids
[edit]Table of morphinan opioids
[edit]| Table of morphinan opioids: click to |
|---|
Table of non-morphinan opioids
[edit]| Table of non-morphinan opioids: click to |
|---|
See also
[edit]References
[edit]- ^ Ogura T, Egan TD (2013). "Chapter 15 – Opioid Agonists and Antagonists". Pharmacology and physiology for anesthesia : foundations and clinical application. Philadelphia, PA: Elsevier/Saunders. ISBN 978-1-4377-1679-5. Archived from the original on 26 March 2019. Retrieved 19 July 2017.
- ^ Jump up to: a b Hemmings HC, Egan TD (2013). Pharmacology and Physiology for Anesthesia: Foundations and Clinical Application: Expert Consult – Online and Print. Elsevier Health Sciences. p. 253. ISBN 978-1-4377-1679-5.
Opiate is the older term classically used in pharmacology to mean a drug derived from opium. Opioid, a more modern term, is used to designate all substances, both natural and synthetic, that bind to opioid receptors (including antagonists).
- ^ "Opioids". www.hopkinsmedicine.org. 11 May 2023. Archived from the original on 2 November 2023. Retrieved 2 November 2023.
- ^ "Alcohol and Drug Policy Commission : Opiates or Opioids — What's the difference? : State of Oregon". www.oregon.gov. Archived from the original on 2 November 2023. Retrieved 2 November 2023.
- ^ Jump up to: a b Stromgaard K, Krogsgaard-Larsen P, Madsen U (2009). Textbook of Drug Design and Discovery, Fourth Edition. CRC Press. ISBN 978-1-4398-8240-5.
- ^ Walzer C (2014). "52 Nondomestic Equids". In West G, Heard D, Caulkett N (eds.). Zoo Animal and Wildlife Immobilization and Anesthesia. Vol. 51 (2nd ed.). Ames, USA: John Wiley & Sons. pp. 723, 727. doi:10.1002/9781118792919. ISBN 978-1-118-79291-9. PMC 2871358. Retrieved 8 July 2019.
{{cite book}}:|journal=ignored (help) - ^ "Carfentanil". www.drugbank.ca. Archived from the original on 6 August 2020. Retrieved 8 July 2019.
- ^ Sterken J, Troubleyn J, Gasthuys F, Maes V, Diltoer M, Verborgh C (October 2004). "Intentional overdose of Large Animal Immobilon". European Journal of Emergency Medicine. 11 (5): 298–301. doi:10.1097/00063110-200410000-00013. PMID 15359207.
- ^ Lembke A (2016). Drug Dealer, MD: How Doctors Were Duped, Patients Got Hooked, and Why It's So Hard to Stop. Johns Hopkins University Press. ISBN 978-1-4214-2140-7.
- ^ "Drug Facts: Prescription Opioids". NIDA. June 2019. Archived from the original on 12 June 2019. Retrieved 5 July 2019.
- ^ "FDA requires strong warnings for opioid analgesics, prescription opioid cough products, and benzodiazepine labeling related to serious risks and death from combined use". FDA. 31 August 2016. Archived from the original on 23 April 2019. Retrieved 1 September 2016.
- ^ "Status and Trend Analysis of Illict [sic] Drug Markets" (PDF). World Drug Report 2015. Archived (PDF) from the original on 27 June 2015. Retrieved 26 June 2015.
- ^ "Report III: FDA Approved Medications for the Treatment of Opiate Dependence: Literature Reviews on Effectiveness & Cost- Effectiveness, Treatment Research Institute". Advancing Access to Addiction Medications: Implications for Opioid Addiction Treatment. p. 41. Archived from the original on 24 February 2021. Retrieved 14 February 2016.
- ^ Tetrault JM, Butner JL (September 2015). "Non-Medical Prescription Opioid Use and Prescription Opioid Use Disorder: A Review". The Yale Journal of Biology and Medicine. 88 (3): 227–33. PMC 4553642. PMID 26339205.
- ^ Tarabar AF, Nelson LS (April 2003). "The resurgence and abuse of heroin by children in the United States". Current Opinion in Pediatrics. 15 (2): 210–5. doi:10.1097/00008480-200304000-00013. PMID 12640281. S2CID 21900231.
- ^ Gray E (4 February 2014). "Heroin Gains Popularity as Cheap Doses Flood the U.S". TIME.com. Archived from the original on 2 December 2020. Retrieved 12 February 2016.
- ^ Maltoni M (January 2008). "Opioids, pain, and fear". Annals of Oncology. 19 (1): 5–7. doi:10.1093/annonc/mdm555. PMID 18073220. Archived from the original on 10 September 2015. Retrieved 14 February 2016.
[A] number of studies, however, have also reported inadequate pain control in 40%–70% of patients, resulting in the emergence of a new type of epidemiology, that of 'failed pain control', caused by a series of obstacles preventing adequate cancer pain management.... The cancer patient runs the risk of becoming an innocent victim of a war waged against opioid abuse and addiction if the norms regarding the two kinds of use (therapeutic or nontherapeutic) are not clearly distinct. Furthermore, health professionals may be worried about regulatory scrutiny and may opt not to use opioid therapy for this reason.
- ^ McCarberg BH (March 2011). "Pain management in primary care: strategies to mitigate opioid misuse, abuse, and diversion". Postgraduate Medicine. 123 (2): 119–30. doi:10.3810/pgm.2011.03.2270. PMID 21474900. S2CID 25935364.
- ^ Jump up to: a b c Offermanns S (2008). Encyclopedia of Molecular Pharmacology. Vol. 1 (2 ed.). Springer Science & Business Media. p. 903. ISBN 978-3-540-38916-3.
In the strict sense, opiates are drugs derived from opium and include the natural products morphine, codeine, thebaine and many semi-synthetic congeners derived from them. In the wider sense, opiates are morphine-like drugs with non-peptidic structures. The older term opiates is now more and more replaced by the term opioids which applies to any substance, whether endogenous or synthetic, peptidic or non-peptidic, that produces morphine-like effects through action on opioid receptors.
- ^ Freye E (2008). "Part II. Mechanism of action of opioids and clinical effects". Opioids in Medicine: A Comprehensive Review on the Mode of Action and the Use of Analgesics in Different Clinical Pain States. Springer Science & Business Media. p. 85. ISBN 978-1-4020-5947-6.
Opiate is a specific term that is used to describe drugs (natural and semi-synthetic) derived from the juice of the opium poppy. For example morphine is an opiate but methadone (a completely synthetic drug) is not. Opioid is a general term that includes naturally occurring, semi-synthetic, and synthetic drugs, which produce their effects by combining with opioid receptors and are competitively antagonized by nalaxone. In this context the term opioid refers to opioid agonists, opioid antagonists, opioid peptides, and opioid receptors.
- ^ Davies PS, D'Arcy YM (26 September 2012). Compact Clinical Guide to Cancer Pain Management: An Evidence-Based Approach for Nurses. Springer Publishing Company. ISBN 978-0-8261-0974-3.
- ^ "21 U.S. Code § 802 – Definitions". LII / Legal Information Institute. Archived from the original on 25 January 2021. Retrieved 12 February 2016.
- ^ "Definition of NARCOTIC". www.merriam-webster.com. Archived from the original on 14 November 2020. Retrieved 12 February 2016.
- ^ Satoskar RS, Rege N, Bhandarkar SD (2015). Pharmacology and Pharmacotherapeutics. Elsevier Health Sciences. ISBN 978-81-312-4371-8.
- ^ Эберт М.Х., Кернс Р.Д. (2010). Поведенческое и психофармакологическое лечение боли . Издательство Кембриджского университета. ISBN 978-1-139-49354-3 .
- ^ Мур Р.А., Виффен П.Дж., Дерри С., Магуайр Т., Рой Ю.М., Тиррелл Л. (ноябрь 2015 г.). «Безрецептурные (безрецептурные) пероральные анальгетики при острой боли – обзор Кокрейновских обзоров» . Кокрановская база данных систематических обзоров . 11 (11): CD010794. дои : 10.1002/14651858.CD010794.pub2 . ПМК 6485506 . ПМИД 26544675 .
- ^ Jump up to: а б Флейшер Г.Р., Людвиг С. (2010). Учебник детской неотложной медицины . Липпинкотт Уильямс и Уилкинс. п. 61. ИСБН 978-1-60547-159-4 .
- ^ «Кодеин» . Наркотики.com. 15 мая 2022 года. Архивировано из оригинала 16 июля 2017 года . Проверено 31 января 2023 г.
- ^ Александр Г.К., Крушевский С.П., Вебстер Д.В. (ноябрь 2012 г.). «Переосмысление назначения опиоидов для защиты безопасности пациентов и общественного здоровья». ДЖАМА . 308 (18): 1865–6. дои : 10.1001/jama.2012.14282 . ПМИД 23150006 .
- ^ Мохамади А., Чан Дж. Дж., Лиан Дж., Райт К. Л., Марин А. М., Родригес Е. К. и др. (август 2018 г.). «Факторы риска и совокупная частота длительного употребления опиоидов после травмы или операции: систематический обзор и мета-(регрессионный) анализ». Журнал костной и суставной хирургии. Американский том . 100 (15): 1332–1340. дои : 10.2106/JBJS.17.01239 . ПМИД 30063596 . S2CID 51891341 .
- ^ Дэвис К.С., Либерман А.Дж., Эрнандес-Дельгадо Х., Суба С. (1 января 2019 г.). «Законы, ограничивающие назначение или отпуск опиоидов при острой боли в Соединенных Штатах: национальный систематический юридический обзор». Наркотическая и алкогольная зависимость . 194 : 166–172. doi : 10.1016/j.drugalcdep.2018.09.022 . ISSN 1879-0046 . ПМИД 30445274 . S2CID 53567522 .
- ^ Франклин Г.М. (сентябрь 2014 г.). «Опиоиды при хронической нераковой боли: документ с изложением позиции Американской академии неврологии» . Неврология . 83 (14): 1277–84. дои : 10.1212/WNL.0000000000000839 . ПМИД 25267983 .
- ^ Jump up to: а б Оки С. (ноябрь 2010 г.). «Поток опиоидов, растущая волна смертей» . Медицинский журнал Новой Англии . 363 (21): 1981–5. дои : 10.1056/NEJMp1011512 . ПМИД 21083382 . S2CID 7092234 .
Ответы на точку зрения Оки: Рич Дж.Д., Грин Т.К., Маккензи М.С. (февраль 2011 г.). «Опиоиды и смерть» . Медицинский журнал Новой Англии . 364 (7): 686–687. дои : 10.1056/NEJMc1014490 . ПМЦ 10347760 . ПМИД 21323559 . - ^ Jump up to: а б Доуэлл Д., Хэгерих Т.М., Чоу Р. (апрель 2016 г.). «Руководство CDC по назначению опиоидов при хронической боли – США, 2016 г.» . ДЖАМА . 315 (15): 1624–45. дои : 10.1001/jama.2016.1464 . ПМК 6390846 . ПМИД 26977696 .
- ^ Ян Дж., Бауэр Б.А., Ванер-Рёдлер Д.Л., Чон Т.Ю., Сяо Л. (17 февраля 2020 г.). «Модифицированная анальгетическая лестница ВОЗ: подходит ли она при хронической нераковой боли?» . Журнал исследований боли . 13 : 411–417. дои : 10.2147/JPR.S244173 . ПМК 7038776 . ПМИД 32110089 .
- ^ Jump up to: а б Информацию об использовании и чрезмерном употреблении опиоидов для лечения мигрени см. Американская академия неврологии (февраль 2013 г.), «Пять вопросов, которые должны задать врачи и пациенты» , «Выбирая мудро »: инициатива Фонда ABIM , Американская академия неврологии, заархивировано из оригинала 1 сентября 2013 г. , получено 1 августа 2013 г. , в котором цитируются
- Зильберштейн С.Д. (сентябрь 2000 г.). «Практический параметр: научно обоснованные рекомендации по лечению мигрени (обзор фактических данных): отчет Подкомитета по стандартам качества Американской академии неврологии» . Неврология . 55 (6): 754–62. дои : 10.1212/WNL.55.6.754 . ПМИД 10993991 .
- Эверс С., Афра Дж., Фрезе А., Гоудсби П.Дж., Линде М., Мэй А. и др. (сентябрь 2009 г.). «Руководство EFNS по медикаментозному лечению мигрени — пересмотренный отчет целевой группы EFNS» . Европейский журнал неврологии . 16 (9): 968–81. дои : 10.1111/j.1468-1331.2009.02748.x . ПМИД 19708964 . S2CID 9204782 .
- Институт улучшения клинических систем (2011 г.), Головная боль, диагностика и лечение , Институт улучшения клинических систем, заархивировано из оригинала 29 октября 2013 г. , получено 18 декабря 2013 г.
- ^ Художник Дж.Т., Кроффорд Л.Дж. (март 2013 г.). «Хроническое употребление опиоидов при синдроме фибромиалгии: клинический обзор». Журнал клинической ревматологии . 19 (2): 72–7. дои : 10.1097/RHU.0b013e3182863447 . ПМИД 23364665 .
- ^ Макникол Э.Д., Мидбари А., Айзенберг Э. (август 2013 г.). «Опиоиды при нейропатической боли» . Кокрановская база данных систематических обзоров . 8 (8): CD006146. дои : 10.1002/14651858.CD006146.pub2 . ПМК 6353125 . ПМИД 23986501 .
- ^ Jump up to: а б с Американское общество головной боли (сентябрь 2013 г.), «Пять вопросов, которые должны задать врачи и пациенты» , «Выбирая мудро : инициатива Фонда ABIM» , Американское общество головной боли , заархивировано из оригинала 3 декабря 2013 г. , получено 10 декабря 2013 г. , в котором цитируются
- Бигал М.Э., Липтон Р.Б. (апрель 2009 г.). «Чрезмерное употребление опиоидов и развитие хронической мигрени». Боль . 142 (3): 179–82. дои : 10.1016/j.pain.2009.01.013 . ПМИД 19232469 . S2CID 27949021 .
- Бигал М.Э., Серрано Д., Бусе Д., Шер А., Стюарт В.Ф., Липтон Р.Б. (сентябрь 2008 г.). «Лекарства от острой мигрени и эволюция от эпизодической мигрени к хронической: продольное популяционное исследование» . Головная боль . 48 (8): 1157–68. дои : 10.1111/j.1526-4610.2008.01217.x . ПМИД 18808500 .
- Шер А.И., Стюарт В.Ф., Риччи Дж.А., Липтон Р.Б. (ноябрь 2003 г.). «Факторы, связанные с возникновением и ремиссией хронической ежедневной головной боли в популяционном исследовании» . Боль . 106 (1–2): 81–9. дои : 10.1016/S0304-3959(03)00293-8 . ПМИД 14581114 . S2CID 29000302 .
- Кацарава З., Шневайс С., Курт Т., Кронер У., Фриче Г., Эйкерманн А. и др. (март 2004 г.). «Заболеваемость и предикторы хронической головной боли у пациентов с эпизодической мигренью». Неврология . 62 (5): 788–90. дои : 10.1212/01.WNL.0000113747.18760.D2 . ПМИД 15007133 . S2CID 20759425 .
- ^ Манчиканти Л., Хелм С., Феллоуз Б., Джаната Дж.В., Пампати В., Гридер Дж.С. и др. (июль 2012 г.). «Опиоидная эпидемия в США» . Врач боли . 15 (3 приложения): ES9-38. дои : 10.36076/ppj.2012/15/ES9 . ПМИД 22786464 .
- ^ Чоу Р., Баллантайн Дж.К., Фанчулло Г.Дж., Файн П.Г., Мясковски С. (февраль 2009 г.). «Пробелы в исследованиях по использованию опиоидов при хронической нераковой боли: результаты обзора доказательств для руководства по клинической практике Американского общества боли и Американской академии медицины боли» . Журнал боли . 10 (2): 147–59. дои : 10.1016/j.jpain.2008.10.007 . ПМИД 19187891 .
- ^ "БОЛЬ" . Painjournalonline.com. 1 сентября 2015 года. Архивировано из оригинала 6 августа 2020 года . Проверено 7 января 2016 г.
- ^ Кисин I (28 сентября 2015 г.). «Долгосрочное лечение хронической доброкачественной боли опиоидами: недоказанная эффективность и пренебрегаемая безопасность?» . Журнал исследований боли . 6 : 513–29. дои : 10.2147/JPR.S47182 . ПМЦ 3712997 . ПМИД 23874119 .
- ^ Дхалла И.А., Гомес Т., Мамдани М.М., Юурлинк Д.Н. (январь 2012 г.). «Опиоиды по сравнению с нестероидными противовоспалительными препаратами при нераковой боли» . Канадский семейный врач . 58 (1):30. ПМК 3264005 . ПМИД 22267615 .
- ^ Маррет Э., Белойл Х., Лежус К. (март 2009 г.). «[Каковы преимущества и риски неопиоидных анальгетиков в сочетании с послеоперационными опиоидами?]». Французские анналы анестезии и интенсивной терапии . 28 (3): е135-51. дои : 10.1016/j.annfar.2009.01.006 . ПМИД 19304445 .
- ^ Франчески Ф., Якомини П., Марсилиани Д., Кордиски С., Антонини Э.Ф., Алези А. и др. (август 2013 г.). «Безопасность и эффективность комбинации ацетаминофен-кодеин при лечении боли различного происхождения» (PDF) . Европейский обзор медицинских и фармакологических наук . 17 (16): 2129–35. ПМИД 23893177 . Архивировано (PDF) из оригинала 26 октября 2020 г. Проверено 26 февраля 2016 г.
- ^ Чунг К.Ф., Виддикомб Дж. (2008). Фармакология и терапия кашля . Берлин: Шпрингер. п. 248. ИСБН 978-3-540-79842-2 .
- ^ Болсер, округ Колумбия, Давенпорт П.В. (февраль 2007 г.). «Кодеин и кашель: неэффективный золотой стандарт» . Современное мнение в области аллергии и клинической иммунологии . 7 (1): 32–6. дои : 10.1097/ACI.0b013e3280115145 . ПМЦ 2921574 . ПМИД 17218808 .
- ^ Jump up to: а б Голдман Р.Д. (декабрь 2010 г.). «Кодеин при остром кашле у детей» . Канадский семейный врач . 56 (12): 1293–4. ПМК 3001921 . ПМИД 21156892 .
- ^ Павел И.М. (февраль 2012 г.). «Возможности лечения острого кашля, вызванного инфекциями верхних дыхательных путей у детей». Легкое . 190 (1): 41–4. дои : 10.1007/s00408-011-9319-y . ПМИД 21892785 . S2CID 23865647 .
- ^ Верли Л., Верхей Т.Дж., Хопстакен Р.М., Принс Дж.М., Саломе П.Л., Бинделс П.Дж. (2012). «[Краткое содержание практического руководства NHG «Острый кашель»]». Голландский медицинский журнал . 156 : А4188. ПМИД 22917039 .
- ^ Маттис Х, Блейхер Б, Блейхер У (1983). «Декстрометорфан и кодеин: объективная оценка противокашлевой активности у больных хроническим кашлем». Журнал международных медицинских исследований . 11 (2): 92–100. дои : 10.1177/030006058301100206 . ПМИД 6852361 . S2CID 30521239 .
- ^ Ван Амбург Дж.А. «Работают ли средства от кашля?» . Медскейп . Архивировано из оригинала 31 марта 2019 года . Проверено 10 апреля 2016 г. .
- ^ Болсер, округ Колумбия (февраль 2010 г.). «Фармакологическое лечение кашля» . Отоларингологические клиники Северной Америки . 43 (1): 147–55, xi. дои : 10.1016/j.otc.2009.11.008 . ПМЦ 2827356 . ПМИД 20172264 .
- ^ Вебстер Л.Р. (октябрь 2015 г.). «Запор, вызванный опиоидами» . Лекарство от боли . 16 (Приложение 1): С16-21. дои : 10.1111/pm.12911 . ПМИД 26461071 .
- ^ «Сообщения для прессы – FDA одобрило Мовантик для лечения запоров, вызванных опиоидами» . www.fda.gov . Архивировано из оригинала 16 февраля 2017 года . Проверено 18 февраля 2016 г.
- ^ Галлахер Р. (июль 2011 г.). «Использование опиоидов при одышке на поздних стадиях заболевания» . CMAJ . 183 (10): 1170. doi : 10.1503/cmaj.110024 . ПМК 3134725 . ПМИД 21746829 .
- ^ Уайзман Р., Роуэтт Д., Олкрофт П., Абернети А., Карроу, округ Колумбия (март 2013 г.). «Хроническая рефрактерная одышка - лечение, основанное на фактических данных». Австралийский семейный врач . 42 (3): 137–40. ПМИД 23529525 .
- ^ Дай С.М., Гупта А., Вальдфогель Дж.М., Шарма Р., Чжан А., Фелисиано Дж.Л. и др. (19 ноября 2020 г.). «Вмешательства при одышке у пациентов с поздними стадиями рака» . JAMA Онкология . doi : 10.23970/ahrqepccer232 . ПМИД 33289989 .
- ^ Фелисиано Дж.Л., Вальдфогель Дж.М., Шарма Р., Чжан А., Гупта А., Седхом Р. и др. (февраль 2021 г.). «Фармакологические вмешательства при одышке у пациентов с поздними стадиями рака: систематический обзор и метаанализ» . Открытая сеть JAMA . 4 (2): e2037632. doi : 10.1001/jamanetworkopen.2020.37632 . ПМЦ 7907959 . ПМИД 33630086 .
- ^ «Синдром беспокойных ног | Бэйлор Медицина» . www.bcm.edu . Архивировано из оригинала 5 ноября 2023 года . Проверено 6 ноября 2023 г.
- ^ Хиггинс С., Смит Б.Х., Мэтьюз К. (июнь 2019 г.). «Доказательства гипералгезии, вызванной опиоидами, в клинических популяциях после хронического воздействия опиоидов: систематический обзор и метаанализ» (PDF) . Британский журнал анестезии . 122 (6): е114–е126. дои : 10.1016/j.bja.2018.09.019 . ПМИД 30915985 . S2CID 81293413 . Архивировано (PDF) из оригинала 18 сентября 2020 г. Проверено 24 апреля 2020 г.
- ^ Ян Д.З., Син Б., Бекхузен Дж., Ся Д., Хаимова Р., Илиев И. (май – июнь 2019 г.). «Опиоид-индуцированная гипералгезия в нехирургических условиях: систематический обзор». Американский журнал терапии . 26 (3): е397–е405. дои : 10.1097/MJT.0000000000000734 . ISSN 1536-3686 . ПМИД 29726847 . S2CID 19181545 .
- ^ Jump up to: а б с д и ж г час Фурлан А.Д., Сандовал Дж.А., Майлис-Ганьон А., Танкс Э. (май 2006 г.). «Опиоиды при хронической нераковой боли: метаанализ эффективности и побочных эффектов» . CMAJ . 174 (11): 1589–94. дои : 10.1503/cmaj.051528 . ПМЦ 1459894 . ПМИД 16717269 .
- ^ Партхви Р., Агравал А., Ханиджо С., Цегайе А., Талвар А. (май – июнь 2019 г.). «Острая передозировка опиатами: обновленная информация о стратегиях управления в отделениях неотложной помощи и отделениях интенсивной терапии». Американский журнал терапии . 26 (3): е380–е387. дои : 10.1097/MJT.0000000000000681 . ПМИД 28952972 . S2CID 24720660 .
- ^ Бауманн С (2009). «Сестринский подход к боли у пожилых людей». Медсург Сестринское дело . 18 (2): 77–82, викторина 83. PMID 19489204 .
- ^ Бакеридж Д., Хуанг А., Хэнли Дж., Келоме А., Рейдел К., Верма А. и др. (сентябрь 2010 г.). «Риск травм, связанных с употреблением опиоидов у пожилых людей». Журнал Американского гериатрического общества . 58 (9): 1664–70. дои : 10.1111/j.1532-5415.2010.03015.x . ПМИД 20863326 . S2CID 25941322 .
- ^ Шнайдер Дж. П. (2010). «Рациональное использование опиоидных анальгетиков при хронической скелетно-мышечной боли» . J Musculoskel Med . 27 : 142–148. Архивировано из оригинала 3 марта 2012 года . Проверено 14 апреля 2010 г.
- ^ Сэнгер Н., Бхатт М., Сингхал Н., Рамсден К., Баптист-Мохсени Н., Панесар Б. и др. (март 2019 г.). «Неблагоприятные последствия, связанные с назначением опиоидов, отпускаемых по рецепту, при острой боли в пояснице: систематический обзор и метаанализ». Врач боли . 22 (2): 119–138. ПМИД 30921976 .
- ^ Фаггл Н., Кертис Э., Шоу С., Спунер Л., Брюйер О., Нтани Г. и др. (апрель 2019 г.). «Безопасность опиоидов при остеоартрите: результаты систематического обзора и метаанализа» . Наркотики и старение . 36 (Приложение 1): 129–143. дои : 10.1007/s40266-019-00666-9 . ПМК 6509215 . ПМИД 31073926 .
- ^ Стивенс Э. (23 ноября 2015 г.). «Опиоидная токсичность» . Медскейп . Архивировано из оригинала 4 декабря 2020 года . Проверено 24 февраля 2016 г. .
CDC сообщил, что метадон стал причиной 31,4% смертей, связанных с опиоидами, в Соединенных Штатах в 1999–2010 годах. На метадон также приходилось 39,8% всех смертей, связанных с приемом одного наркотика-опиоида. Уровень смертности от передозировки, связанной с метадоном, был значительно выше, чем уровень смертности, связанный с другими смертями, связанными с опиоидами, среди смертей от нескольких наркотиков и от одного препарата.
- ^ Jump up to: а б с д и Ноубл М., Тредвелл Дж.Р., Трегир С.Дж., Коутс В.Х., Виффен П.Дж., Акафомо С. и др. (январь 2010 г.). Благородный М (ред.). «Долгосрочное лечение опиоидами хронической нераковой боли» . Кокрановская база данных систематических обзоров . 2018 (1): CD006605. дои : 10.1002/14651858.CD006605.pub2 . ПМК 6494200 . ПМИД 20091598 .
- ^ «Смерть от передозировки наркотиков в США, 1999–2016 гг.» (PDF) . CDC . Архивировано (PDF) из оригинала 16 января 2021 года . Проверено 23 декабря 2017 г.
- ^ Прадхан А.А., Уолвин В., Нозаки С., Филлиол Д., Эрбс Е., Матифас А. и др. (декабрь 2010 г.). «Лиганд-направленный транспорт δ-опиоидного рецептора in vivo: два пути к анальгетической толерантности» . Журнал неврологии . 30 (49): 16459–68. doi : 10.1523/JNEUROSCI.3748-10.2010 . ПМК 3086517 . ПМИД 21147985 .
- ^ Колларс Дж. П., Ларсон, доктор медицинских наук (март 2005 г.). «Толерантность к миотическим эффектам опиоидов» . Анестезиология . 102 (3): 701. doi : 10.1097/00000542-200503000-00047 . ПМИД 15731628 .
- ^ Сантильян Р., Маэстре Х.М., Хурле М.А., Флорес Х. (июль 1994 г.). «Усиление опиатной аналгезии нимодипином у онкологических больных, хронически получающих морфин: предварительный отчет». Боль . 58 (1): 129–32. дои : 10.1016/0304-3959(94)90192-9 . ПМИД 7970835 . S2CID 35138704 .
- ^ Сантильян Р., Хурле М.А., Армихо Х.А., де лос Мосос Р., Флорес Х. (май 1998 г.). «Опиатная аналгезия, усиленная нимодипином, у онкологических больных, требующих повышения дозы морфина: двойное слепое плацебо-контролируемое исследование». Боль . 76 (1–2): 17–26. дои : 10.1016/S0304-3959(98)00019-0 . ПМИД 9696455 . S2CID 30963675 .
- ^ Смит Ф.Л., Домбровский Д.С., Дьюи В.Л. (февраль 1999 г.). «Участие внутриклеточного кальция в толерантности к морфину у мышей». Фармакология, биохимия и поведение . 62 (2): 381–8. дои : 10.1016/S0091-3057(98)00168-3 . ПМИД 9972707 . S2CID 37434490 .
- ^ Маккарти Р.Дж., Кроин Дж.С., Туман К.Дж., Пенн Р.Д., Иванкович А.Д. (апрель 1998 г.). «Антиноцицептивное усиление и ослабление толерантности путем интратекальной совместной инфузии сульфата магния и морфина у крыс» . Анестезия и анальгезия . 86 (4): 830–6. дои : 10.1097/00000539-199804000-00028 . ПМИД 9539610 . Архивировано из оригинала 11 февраля 2010 года . Проверено 12 ноября 2007 г.
- ^ Моррисон А.П., Хантер Дж.М., Халперн С.Х., Банерджи А. (май 2013 г.). «Эффект интратекального магния в присутствии или отсутствии местного анестетика с липофильными опиоидами и без них: систематический обзор и метаанализ» . Британский журнал анестезии . 110 (5): 702–12. дои : 10.1093/bja/aet064 . ПМИД 23533255 .
- ^ Ларсон А.А., Ковач К.Дж., Спарц А.К. (ноябрь 2000 г.). «Интратекальный Zn2+ ослабляет антиноцицепцию морфина и развитие острой толерантности». Европейский журнал фармакологии . 407 (3): 267–72. дои : 10.1016/S0014-2999(00)00715-9 . ПМИД 11068022 .
- ^ Вонг CS, Чернг CH, Лук HN, Хо ST, Tung CS (февраль 1996 г.). «Влияние антагонистов рецепторов NMDA на ингибирование толерантности к морфину у крыс: связывание мю-опиоидных рецепторов». Европейский журнал фармакологии . 297 (1–2): 27–33. дои : 10.1016/0014-2999(95)00728-8 . ПМИД 8851162 .
- ^ Малец Д., Мандрик М., Фидецка С. (март – апрель 2008 г.). «Взаимодействие мемантина и кетамина при антиноцицепции, вызванной морфином и пентазоцином, у мышей» (PDF) . Фармакологические отчеты . 60 (2): 149–55. ПМИД 18443375 . Архивировано (PDF) из оригинала 30 сентября 2020 г. Проверено 17 сентября 2011 г.
- ^ Макклин Дж.Дж. (2003). «Антагонист холецистокинина проглумид усиливает анальгетический эффект дигидрокодеина». Клинический журнал боли . 19 (3): 200–1. дои : 10.1097/00002508-200305000-00008 . ПМИД 12792559 . S2CID 29229782 .
- ^ Уоткинс Л.Р., Кинсчек И.Б., Майер DJ (апрель 1984 г.). «Усиление опиатной анальгезии и явное изменение толерантности к морфину под действием проглумида». Наука . 224 (4647): 395–6. Бибкод : 1984Sci...224..395W . дои : 10.1126/science.6546809 . ПМИД 6546809 .
- ^ Тан Дж., Чоу Дж., Ядарола М., Ян Х.И., Коста Э. (июнь 1984 г.). «Проглумид предотвращает и снижает острую толерантность к морфию у крыс». Нейрофармакология . 23 (6): 715–8. дои : 10.1016/0028-3908(84)90171-0 . ПМИД 6462377 . S2CID 33168040 .
- ^ Ледебур А., Хатчинсон М.Р., Уоткинс Л.Р., Джонсон К.В. (июль 2007 г.). «Ибудиласт (AV-411). Кандидат нового класса в терапии нейропатической боли и синдромов отмены опиоидов». Экспертное заключение об исследуемых препаратах . 16 (7): 935–50. дои : 10.1517/13543784.16.7.935 . ПМИД 17594181 . S2CID 22321634 .
- ^ Jump up to: а б с д Дойл Д., Хэнкс Г., Черный И., Калман К., ред. (2004). Оксфордский учебник паллиативной медицины (3-е изд.). Издательство Оксфордского университета. ISBN 978-0-19-856698-4 .
- ^ Герман Д., Клагес Э., Вельцель Х., Манн К., Круассан Б. (июнь 2005 г.). «Низкая эффективность неопиоидных препаратов при синдроме отмены опиоидов». Биология наркомании . 10 (2): 165–9. дои : 10.1080/13556210500123514 . ПМИД 16191669 . S2CID 8017503 .
- ^ Браун Т.К. (март 2013 г.). «Ибогаин в лечении зависимости от психоактивных веществ». Текущие обзоры злоупотребления наркотиками . 6 (1): 3–16. дои : 10.2174/15672050113109990001 . ПМИД 23627782 .
- ^ Дюсепп М.А., Перро М.М., Френетт А.Дж., Берри Л.Д., Рико П., Лавуа А. и др. (апрель 2019 г.). «Частота, факторы риска и симптоматика ятрогенной отмены опиоидов и бензодиазепинов у новорожденных, детей и взрослых в критическом состоянии: систематический обзор клинических исследований» . Журнал клинической фармации и терапии . 44 (2): 148–156. дои : 10.1111/jcpt.12787 . ISSN 1365-2710 . ПМИД 30569508 .
- ^ Баннварт Б. (сентябрь 2012 г.). «Будут ли препараты опиоидных анальгетиков, сдерживающие злоупотребление, достичь своей цели?». Наркотики . 72 (13): 1713–23. дои : 10.2165/11635860-000000000-00000 . ПМИД 22931520 . S2CID 26082561 .
- ^ Шнайдер Дж. П., Мэтьюз М., Джеймисон Р. Н. (октябрь 2010 г.). «Опиоидные составы, сдерживающие злоупотребление и устойчивые к несанкционированному вмешательству: какова их роль в борьбе со злоупотреблением рецептурными опиоидами?». Препараты ЦНС . 24 (10): 805–10. дои : 10.2165/11584260-000000000-00000 . ПМИД 20839893 . S2CID 17830622 .
- ^ Сюй Ю, Джонсон А (2013). «Фармакогеномика опиоидной терапии при нераковой боли: эффективность, побочные эффекты и затраты» . Исследование и лечение боли . 2013 : 943014. doi : 10.1155/2013/943014 . ПМЦ 3791560 . ПМИД 24167729 .
- ^ Кисть DE (декабрь 2012 г.). «Осложнения долгосрочной терапии опиоидами для лечения хронической боли: парадокс гипералгезии, вызванной опиоидами» . Журнал медицинской токсикологии . 8 (4): 387–92. дои : 10.1007/s13181-012-0260-0 . ПМК 3550256 . ПМИД 22983894 .
- ^ Малик З., Байк Д., Шей Р. (февраль 2015 г.). «Роль каннабиноидов в регуляции тошноты и рвоты, а также висцеральной боли». Текущие отчеты гастроэнтерологии . 17 (2): 429. doi : 10.1007/s11894-015-0429-1 . ПМИД 25715910 . S2CID 32705478 .
- ^ Абрамс Д.И., Гузман М. (июнь 2015 г.). «Каннабис в лечении рака». Клиническая фармакология и терапия . 97 (6): 575–86. дои : 10.1002/cpt.108 . ПМИД 25777363 . S2CID 2488112 .
- ^ «Исследование UCSF показало, что медицинская марихуана может помочь пациентам уменьшить боль при приеме опиатов» . Калифорнийский университет в Сан-Франциско . 6 декабря 2011 г. Архивировано из оригинала 17 декабря 2020 г. . Проверено 4 марта 2016 г.
- ^ Абрамс Д.И., Коуи П., Шейд С.Б., Келли М.Э., Беновиц Н.Л. (декабрь 2011 г.). «Взаимодействие каннабиноидов и опиоидов при хронической боли». Клиническая фармакология и терапия . 90 (6): 844–51. дои : 10.1038/clpt.2011.188 . ПМИД 22048225 . S2CID 4823659 .
- ^ Фрауенкнехт Дж., Киркхэм К.Р., Жако-Гийярмод А., Альбрехт Э. (май 2019 г.). «Обезболивающее воздействие интраоперационных опиоидов по сравнению с безопиоидной анестезией: систематический обзор и метаанализ» . Анестезия . 74 (5): 651–662. дои : 10.1111/anae.14582 . ПМИД 30802933 . S2CID 73469631 . Архивировано из оригинала 15 декабря 2023 года . Проверено 15 сентября 2022 г.
- ^ Буссе Дж.В., Ван Л., Камалельдин М., Крейги С., Рива Дж.Дж., Монтойя Л. и др. (18 декабря 2018 г.). «Опиоиды при хронической нераковой боли: систематический обзор и метаанализ» . ДЖАМА . 320 (23): 2448–2460. дои : 10.1001/jama.2018.18472 . ISSN 0098-7484 . ПМК 6583638 . ПМИД 30561481 .
- ^ Рейссиг Дж. Э., Рыбарчик А. М. (апрель 2005 г.). «Фармакологическое лечение опиоидной седации при хронической боли». Анналы фармакотерапии . 39 (4): 727–31. дои : 10.1345/aph.1E309 . ПМИД 15755795 . S2CID 39058371 .
- ^ Кори П.Дж., Хек А.М., Weathermon RA (декабрь 1999 г.). «Амфетамины для противодействия седативному эффекту, вызванному опиоидами». Анналы фармакотерапии . 33 (12): 1362–6. дои : 10.1345/aph.19024 . ПМИД 10630837 . S2CID 23733242 .
- ^ Канадское агентство по лекарствам и технологиям в здравоохранении (26 июня 2014 г.). «Диоктилсульфосукцинат или докузат (кальция или натрия) для профилактики или лечения запоров: обзор клинической эффективности». ПМИД 25520993 .
- ^ Маккарберг Б.Х. (июль 2013 г.). «Обзор и лечение запора, вызванного опиоидами». Последипломное образование по медицине . 125 (4): 7–17. дои : 10.3810/pgm.2013.07.2651 . ПМИД 23782897 . S2CID 42872181 .
- ^ Jump up to: а б с д и Кумар Л., Баркер С., Эммануэль А. (2014). «Запор, вызванный опиоидами: патофизиология, клинические последствия и лечение» . Гастроэнтерологические исследования и практика . 2014 : 141737. doi : 10.1155/2014/141737 . ПМК 4027019 . ПМИД 24883055 .
- ^ Jump up to: а б Альгуайр ПК, Американский колледж врачей, директор по внутренним болезням (2009). Основы внутренней медицины для студентов 2 . АКП Пресс. стр. 272–. ISBN 978-1-934465-13-4 .
- ^ Jump up to: а б с Эллиотт Дж. А., Смит Х. С. (19 апреля 2016 г.). Справочник по лечению острой боли . ЦРК Пресс. стр. 89–. ISBN 978-1-4665-9635-1 .
- ^ Поулсен Дж.Л., Брок С., Олесен А.Е., Нильссон М., Древес А.М. (ноябрь 2015 г.). «Развивающиеся парадигмы в лечении дисфункции кишечника, вызванной опиоидами» . Терапевтические достижения в гастроэнтерологии . 8 (6): 360–72. дои : 10.1177/1756283X15589526 . ПМЦ 4622283 . ПМИД 26557892 .
- ^ Депутат Дэвиса, Гофорт HW (2016). «Оксикодон с антагонистом опиоидных рецепторов: обзор». Журнал управления опиоидами . 12 (1): 67–85. дои : 10.5055/jom.2016.0313 . ПМИД 26908305 .
- ^ Кэнди Б., Джонс Л., Викерстафф В., Ларкин П.Дж., Стоун П. (15 сентября 2022 г.). «Антагонисты мю-опиоидов при опиоидной дисфункции кишечника у людей, больных раком, и людей, получающих паллиативную помощь» . Кокрановская база данных систематических обзоров . 2022 (9): CD006332. дои : 10.1002/14651858.CD006332.pub4 . ISSN 1469-493X . ПМЦ 9476137 . ПМИД 36106667 .
- ^ Лутра П., Берр Н.Э., Бреннер Д.М., Ford AC (май 2018 г.). «Эффективность фармакологической терапии для лечения запоров, вызванных опиоидами: систематический обзор и сетевой метаанализ» (PDF) . Гут . 68 (3): 434–444. дои : 10.1136/gutjnl-2018-316001 . ПМИД 29730600 . S2CID 13677764 . Архивировано из оригинала 6 августа 2020 года . Проверено 23 сентября 2019 г.
- ^ Эсмади М., Ахмад Д., Хьюлетт А. (март 2019 г.). «Эффективность налдемедина для лечения запоров, вызванных опиоидами: метаанализ» . Журнал желудочно-кишечных заболеваний и заболеваний печени . 28 (1): 41–46. doi : 10.15403/jgld.2014.1121.281.any . ПМИД 30851171 .
- ^ Дорн С., Лембо А., Кремонини Ф. (сентябрь 2014 г.). «Опиоид-индуцированная дисфункция кишечника: эпидемиология, патофизиология, диагностика и начальный терапевтический подход». Американский журнал гастроэнтерологических добавок . 2 (1): 31–7. дои : 10.1038/ajgsup.2014.7 . ПМИД 25207610 .
- ^ Йост CS (2006). «Новый взгляд на стимулятор дыхания доксапрам» . Обзоры препаратов для ЦНС . 12 (3–4): 236–49. дои : 10.1111/j.1527-3458.2006.00236.x . ПМК 6506195 . ПМИД 17227289 .
- ^ Тан З.М., Лю Дж.Х., Донг Т., Ли Дж.С. (август 2006 г.). «[Клиническое наблюдение целенаправленной инфузии ремифентанила в сочетании с пропофолом и доксапрамом при безболезненном искусственном аборте]». Нань Фан И Кэ да Сюэ Сюэ Бао = Журнал Южного медицинского университета . 26 (8): 1206–8. ПМИД 16939923 .
- ^ Манцке Т., Гюнтер У., Понимаскин Э.Г., Халлер М., Дачманн М., Шварцахер С. и др. (июль 2003 г.). «5-HT4(a) рецепторы предотвращают угнетение дыхания, вызванное опиоидами, без потери анальгезии». Наука . 301 (5630): 226–9. Бибкод : 2003Sci...301..226M . дои : 10.1126/science.1084674 . ПМИД 12855812 . S2CID 13641423 .
- ^ Ван X, Дергачева О, Каменди Х, Горини С, Менделовиц Д (август 2007 г.). «5-гидрокситриптаминовые 1А/7 и 4-альфа-рецепторы дифференциально предотвращают опиоид-индуцированное угнетение кардиореспираторной функции ствола мозга» . Гипертония . 50 (2): 368–76. doi : 10.1161/ГИПЕРТЕНЗИЯ.107.091033 . ПМИД 17576856 .
- ^ Рен Дж., Пун Б.И., Тан Ю., Фанк Г.Д., Грир Дж.Дж. (декабрь 2006 г.). «Ампакины облегчают угнетение дыхания у крыс». Американский журнал респираторной медицины и медицины интенсивной терапии . 174 (12): 1384–91. дои : 10.1164/rccm.200606-778OC . ПМИД 16973981 .
- ^ Козович С., Чунг Ф., Дуфас А.Г., Нагаппа М., Мемцудис С.Г. (октябрь 2018 г.). «Опиоиды для лечения острой боли у пациентов с обструктивным апноэ во сне: систематический обзор». Анестезия и анальгезия . 127 (4): 988–1001. дои : 10.1213/ANE.0000000000003549 . ISSN 1526-7598 . ПМИД 29958218 . S2CID 49614405 .
- ^ Гупта К., Нагаппа М., Прасад А., Абрамян Л., Вонг Дж., Вайнгартен Т.Н. и др. (14 декабря 2018 г.). «Факторы риска угнетения дыхания, вызванного опиоидами, у хирургических пациентов: систематический обзор и метаанализ» . БМЖ Опен . 8 (12): e024086. doi : 10.1136/bmjopen-2018-024086 . ISSN 2044-6055 . ПМК 6303633 . ПМИД 30552274 .
- ^ Уилсон Г. Р., Рейсфилд Г. М. (2003). «Морфиновая гипералгезия: отчет о случае». Американский журнал хосписной и паллиативной помощи . 20 (6): 459–61. дои : 10.1177/104990910302000608 . ПМИД 14649563 . S2CID 22690630 .
- ^ Велла-Бринкат Дж., Маклеод А.Д. (2007). «Побочное воздействие опиоидов на центральную нервную систему пациентов паллиативной помощи». Журнал фармакотерапии боли и паллиативной помощи . 21 (1): 15–25. дои : 10.1080/J354v21n01_05 . ПМИД 17430825 . S2CID 17757207 .
- ^ Меркаданте С., Аркури Э. (2005). «Гипералгезия и переключение на опиоиды». Американский журнал хосписной и паллиативной помощи . 22 (4): 291–4. дои : 10.1177/104990910502200411 . ПМИД 16082916 . S2CID 39647898 .
- ^ Fine PG (2004). «Информация об опиоидах: гипералгезия, вызванная опиоидами, и ротация опиоидов». Журнал фармакотерапии боли и паллиативной помощи . 18 (3): 75–9. дои : 10.1080/J354v18n03_08 . ПМИД 15364634 . S2CID 45555785 .
- ^ Ли М., Сильверман С.М., Хансен Х., Патель В.Б., Манчиканти Л. (2011). «Всесторонний обзор гипералгезии, вызванной опиоидами» . Врач боли . 14 (2): 145–61. дои : 10.36076/ppj.2011/14/145 . ПМИД 21412369 . Архивировано из оригинала 14 декабря 2020 года . Проверено 11 ноября 2016 г.
- ^ Томпкинс Д.А., Кэмпбелл К.М. (апрель 2011 г.). «Опиоид-индуцированная гипералгезия: клинически значимый или посторонний исследовательский феномен?» . Текущие отчеты о боли и головной боли . 15 (2): 129–36. дои : 10.1007/s11916-010-0171-1 . ПМК 3165032 . ПМИД 21225380 .
- ^ Диас Х.Л., Заманильо Д., Корбера Дж., Байенс Х.М., Мальдонадо Р., Перикас М.А. и др. (сентябрь 2009 г.). «Селективные антагонисты рецепторов сигма-1 (сигма1): новая мишень для лечения нейропатической боли». Агенты центральной нервной системы в медицинской химии . 9 (3): 172–83. дои : 10.2174/1871524910909030172 . ПМИД 20021351 .
- ^ Митра С (2018). «Опиоид-индуцированная гипералгезия: патофизиология и клинические последствия». Журнал управления опиоидами . 4 (3): 123–30. дои : 10.5055/jom.2008.0017 . ПМИД 18717507 .
- ^ Барон Р. (2009). «Нейропатическая боль: Клиническая перспектива». Сенсорные нервы . Справочник по экспериментальной фармакологии. Том. 194. стр. 3–30. дои : 10.1007/978-3-540-79090-7_1 . ISBN 978-3-540-79089-1 . ПМИД 19655103 .
- ^ Кандиотти К.А., Гитлин MC (июль 2010 г.). «Обзор влияния побочных эффектов, связанных с опиоидами, на недостаточное лечение умеренной и тяжелой хронической нераковой боли: тапентадол, шаг к решению?». Текущие медицинские исследования и мнения . 26 (7): 1677–84. дои : 10.1185/03007995.2010.483941 . ПМИД 20465361 . S2CID 9713245 .
- ^ Jump up to: а б Бавор М., Бами Х., Деннис Б.Б., Платер С., Ворстер А., Варенбут М. и др. (апрель 2015 г.). «Подавление тестостерона у потребителей опиоидов: систематический обзор и метаанализ» . Зависимость от алкоголя и наркотиков . 149 : 1–9. doi : 10.1016/j.drugalcdep.2015.01.038 . ПМИД 25702934 .
- ^ Колуцци Ф., Биллечи Д., Магги М., Корона Дж. (декабрь 2018 г.). «Дефицит тестостерона у нераковых пациентов, получающих опиоиды» . Журнал эндокринологических исследований . 41 (12): 1377–1388. дои : 10.1007/s40618-018-0964-3 . ПМК 6244554 . ПМИД 30343356 .
- ^ Jump up to: а б Фонтас А, Чай С.Т., Куркути С., Каравитаки Н. (октябрь 2018 г.). «МЕХАНИЗМЫ ЭНДОКРИНОЛОГИИ: Эндокринология опиоидов» . Европейский журнал эндокринологии . 179 (4): Р183–Р196. дои : 10.1530/EJE-18-0270 . ПМИД 30299887 .
- ^ Бреннан MJ (март 2013 г.). «Влияние опиоидной терапии на эндокринную функцию». Американский медицинский журнал . 126 (3 Приложение 1): С12-8. doi : 10.1016/j.amjmed.2012.12.001 . ПМИД 23414717 .
- ^ Коламеко С., Корен Дж.С. (январь 2009 г.). «Опиоид-индуцированная эндокринопатия». Журнал Американской остеопатической ассоциации . 109 (1): 20–5. ПМИД 19193821 .
- ^ Смит Х.С., Эллиот Дж.А. (июль 2012 г.). «Опиоид-индуцированный дефицит андрогенов (ОПИАД)». Врач боли . 15 (3 дополнения): ES145-56. ПМИД 22786453 .
- ^ Бреде Э., Майер Т.Г., Гатчел Р.Дж. (февраль 2012 г.). «Прогнозирование неспособности сохранить работу через 1 год после междисциплинарного функционального восстановления при производственном травматизме». Архив физической медицины и реабилитации . 93 (2): 268–74. дои : 10.1016/j.apmr.2011.08.029 . ПМИД 22289236 .
- ^ Волинн Э., Фарго Джей Ди, Файн ПГ (апрель 2009 г.). «Опиоидная терапия неспецифической боли в пояснице и последствий хронической потери работы». Боль . 142 (3): 194–201. дои : 10.1016/j.pain.2008.12.017 . ПМИД 19181448 .
- ^ Jump up to: а б с Американский колледж профессиональной и экологической медицины (февраль 2014 г.), «Пять вопросов, которые должны задать врачи и пациенты» , «Выбирая мудро : инициатива Фонда ABIM» , Американский колледж профессиональной и экологической медицины, заархивировано из оригинала 11 сентября 2014 г. , получено 24 февраля 2014 г. , в котором цитируется
- Вайс М.С., Боуден К., Бранко Ф. и др. (2011). «Руководство по опиоидам». В Хегманне КТ (ред.). Рекомендации по практике медицины труда: оценка и лечение распространенных проблем со здоровьем и функциональное восстановление у работников (онлайн, март 2014 г.) (3-е изд.). Элк-Гроув-Виллидж, Иллинойс: Американский колледж профессиональной и экологической медицины. п. 11. ISBN 978-0-615-45227-2 .
- ^ Керубино П., Сарзи-Путтини П., Зуккаро С.М., Лабианка Р. (февраль 2012 г.). «Управление хронической болью у важных подгрупп пациентов». Клиническое исследование лекарственных средств . 32 (Приложение 1): 35–44. дои : 10.2165/11630060-000000000-00000 . ПМИД 23389874 . S2CID 47576095 .
- ^ Уайт К.Т., Диллингем Т.Р., Гонсалес-Фернандес М., Ротфилд Л. (декабрь 2009 г.). «Опиаты при хронических незлокачественных болевых синдромах: можно ли определить подходящих кандидатов для управления амбулаторной клиникой?». Американский журнал физической медицины и реабилитации . 88 (12): 995–1001. дои : 10.1097/PHM.0b013e3181bc006e . ПМИД 19789432 . S2CID 43241757 .
- ^ Кэй А.М., Кэй А.Д., Лофтон EC (2013). «Основные концепции назначения опиоидов и современные концепции воздействия опиоидов на вождение» . Журнал Окснера . 13 (4): 525–32. ПМЦ 3865831 . ПМИД 24358001 .
- ^ Орриолс Л., Делорм Б., Гадегбеку Б., Трикотел А., Контранд Б., Лаумон Б. и др. (ноябрь 2010 г.). Пирмохамед М. (ред.). «Лекарства, отпускаемые по рецепту, и риск дорожно-транспортных происшествий: исследование на основе французского реестра» . ПЛОС Медицина . 7 (11): e1000366. дои : 10.1371/journal.pmed.1000366 . ПМК 2981588 . ПМИД 21125020 .
- ^ Миллер М., Штюрмер Т., Азраэль Д., Левин Р., Соломон Д.Х. (март 2011 г.). «Опиоидные анальгетики и риск переломов у пожилых людей с артритом» . Журнал Американского гериатрического общества . 59 (3): 430–8. дои : 10.1111/j.1532-5415.2011.03318.x . ПМЦ 3371661 . ПМИД 21391934 .
- ^ Аллегри Н., Меннуни С., Рулли Э., Ванакор Н., Корли О., Флориани И. и др. (март 2019 г.). «Систематический обзор и метаанализ нейропсихологических эффектов длительного применения опиоидов у пациентов с хронической нераковой болью». Болевая практика . 19 (3): 328–343. дои : 10.1111/папр.12741 . ПМИД 30354006 . S2CID 53023743 .
- ^ Jump up to: а б с Гудин Дж.А., Могали С., Джонс Дж.Д., Комер С.Д. (июль 2013 г.). «Риски, управление и мониторинг комбинированного употребления опиоидов, бензодиазепинов и/или алкоголя» . Последипломное образование по медицине . 125 (4): 115–30. дои : 10.3810/pgm.2013.07.2684 . ПМК 4057040 . ПМИД 23933900 .
- ^ Ислам ММ, Воллерсхайм Д (2019). «Сравнение отпуска опиоидов и бензодиазепинов в Австралии» . ПЛОС ОДИН . 14 (8): e0221438. Бибкод : 2019PLoSO..1421438I . дои : 10.1371/journal.pone.0221438 . ПМК 6699700 . ПМИД 31425552 .
- ^ Ислам ММ, Воллерсхайм Д (2020). «Тенденции и изменения в одновременном отпуске рецептурных опиоидов и бензодиазепинов в Австралии: ретроспективный анализ». Современные проблемы наркотиков . 47 (2): 136–148. дои : 10.1177/0091450920919443 . S2CID 218780209 .
- ^ Стут Э.А., Штуке АГ, Зуперку Э.Дж. (2012). «Влияние анестетиков, седативных средств и опиоидов на контроль вентиляции». Комплексная физиология . 2 (4): 2281–2367. дои : 10.1002/cphy.c100061 . ISBN 978-0-470-65071-4 . ПМИД 23720250 .
- ^ Гоуинг Л., Али Р., Уайт Дж. М. (май 2017 г.). «Антагонисты опиоидов с минимальной седацией при отмене опиоидов» . Кокрановская база данных систематических обзоров . 2017 (5): CD002021. дои : 10.1002/14651858.CD002021.pub4 . ПМК 6481395 . ПМИД 28553701 .
- ^ Болтон М., Ходкинсон А., Бода С., Молд А., Панагиоти М., Роудс С. и др. (15 января 2019 г.). «Серьезные нежелательные явления, зарегистрированные в рандомизированных контролируемых исследованиях плацебо при пероральном применении налтрексона: систематический обзор и метаанализ» . БМК Медицина . 17 (1): 10. дои : 10.1186/s12916-018-1242-0 . ISSN 1741-7015 . ПМК 6332608 . ПМИД 30642329 .
- ^ Грин Дж.А., Дево Б.Дж., Дол Дж.С., Батлер М.Б. (апрель 2019 г.). «Частота смертности из-за рикошетной токсичности после практики «вылечить и выпустить» при догоспитальной помощи при передозировке опиоидов: систематический обзор» . Журнал неотложной медицины . 36 (4): 219–224. doi : 10.1136/emermed-2018-207534 . ISSN 1472-0213 . ПМИД 30580317 .
- ^ Миллер Р.Д. (2010). Анестезия Миллера (7-е изд.). Elsevier Науки о здоровье. ISBN 978-0-443-06959-8 .
- ^ Морган Дж.Э., Михаил М.С., Мюррей М.Дж. (2006). Клиническая анестезиология (4-е изд.). МакГроу Хилл. ISBN 978-0-07-110515-6 .
- ^ Честнат Д.Х., Вонг К.А., Цен Л.К., Ки В.Д., Бейлин Ю., Майр Дж. (2014). Акушерская анестезия Каштана: принципы и практика . Elsevier Науки о здоровье. п. 468. ИСБН 978-0-323-11374-8 .
Липидная растворимость гидроморфона находится между морфином и фентанилом, но ближе к растворимости морфина.
- ^ Мусацци У.М., Матера С., Далланоче С., Вакондио Ф., Де Амичи М., Вистоли Г. и др. (июль 2015 г.). «О выборе опиоида для местной анальгезии кожи: взаимосвязь проницаемости структуры и кожи». Международный фармацевтический журнал . 489 (1–2): 177–85. doi : 10.1016/j.ijpharm.2015.04.071 . ПМИД 25934430 .
- ^ Комер С.Д., Кэхилл К.М. (ноябрь 2019 г.). «Фентанил: фармакология рецепторов, потенциал злоупотребления и последствия для лечения» . Неврологические и биоповеденческие обзоры . 106 : 49–57. doi : 10.1016/j.neubiorev.2018.12.005 . ISSN 1873-7528 . ПМЦ 7233332 . ПМИД 30528374 .
- ^ Вольпе Д.А., МакМахон Тобин Г.А., Меллон Р.Д., Катки А.Г., Паркер Р.Дж., Колацки Т. и др. (апрель 2011 г.). «Единая оценка и ранжирование констант связывания опиоидных μ-рецепторов для выбранных опиоидных препаратов» . Нормативная токсикология и фармакология . 59 (3): 385–390. дои : 10.1016/j.yrtph.2010.12.007 . ISSN 1096-0295 . ПМИД 21215785 . Архивировано из оригинала 4 декабря 2023 года . Проверено 4 декабря 2023 г.
- ^ Хигашикава Ю., Сузуки С. (1 июня 2008 г.). «Исследование 1-(2-фенетил)-4-(N-пропиониланилино)пиперидина (фентанила) и родственных ему соединений. VI. Связь структуры и анальгетической активности фентанила, метилзамещенных фентанилов и других аналогов» . Судебная токсикология . 26 (1): 1–5. дои : 10.1007/s11419-007-0039-1 . ISSN 1860-8973 . S2CID 22092512 . Архивировано из оригинала 15 декабря 2023 года . Проверено 4 декабря 2023 г.
- ^ Ле Наур М., Лунцер М.М., Пауэрс М.Д., Калюжный А.Е., Бенниворт М.А., Томас М.Дж. и др. (август 2014 г.). «Предполагаемые гетеромеры каппа-опиоидов как мишени для разработки анальгетиков, свободных от побочных эффектов» . Журнал медицинской химии . 57 (15): 6383–92. дои : 10.1021/jm500159d . ПМК 4136663 . ПМИД 24978316 .
- ^ ДеВайр С.М., Ямасита Д.С., Ромингер Д.Х., Лю Г., Коуэн С.Л., Грачик Т.М. и др. (март 2013 г.). «Смещенный к AG-белку лиганд на мю-опиоидном рецепторе обладает сильным анальгетическим действием и снижает желудочно-кишечную и респираторную дисфункцию по сравнению с морфином». Журнал фармакологии и экспериментальной терапии . 344 (3): 708–17. дои : 10.1124/jpet.112.201616 . ПМИД 23300227 . S2CID 8785003 .
- ^ Джонсон Н., Ицхак Ю., Пастернак Г.В. (июнь 1984 г.). «Взаимодействие двух опиатноподобных производных фенциклидина с сайтами связывания 3H-опиоидов». Европейский журнал фармакологии . 101 (3–4): 281–284. дои : 10.1016/0014-2999(84)90171-7 . ПМИД 6088255 .
- ^ Jump up to: а б с Такаяма Х., Исикава Х., Курихара М., Китадзима М., Аими Н., Понглукс Д. и др. (апрель 2002 г.). «Исследования синтеза и опиоидной агонистической активности родственных митрагинину индольных алкалоидов: открытие опиоидных агонистов, структурно отличающихся от других опиоидных лигандов». Журнал медицинской химии . 45 (9): 1949–56. дои : 10.1021/jm010576e . ПМИД 11960505 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и аль являюсь а Рейнор К., Конг Х., Чен Ю., Ясуда К., Ю Л., Белл Г.И. и др. (февраль 1994 г.). «Фармакологическая характеристика клонированных каппа-, дельта- и мю-опиоидных рецепторов». Молекулярная фармакология . 45 (2): 330–4. ПМИД 8114680 .
- ^ Альбургес МЭ (1992). «Использование радиорецепторного анализа для анализа аналогов фентанила в моче» . J Анальный токсикол . 16 (1): 36–41. дои : 10.1093/jat/16.1.36 . ПМИД 1322477 . Архивировано из оригинала 21 ноября 2023 года . Проверено 21 ноября 2023 г.
- ^ Jump up to: а б с д и ж г Филизола М., Вильяр Х.О., Лоу Г.Х. (январь 2001 г.). «Молекулярные детерминанты неспецифического распознавания дельта-, мю- и каппа-опиоидных рецепторов». Биоорганическая и медицинская химия . 9 (1): 69–76. дои : 10.1016/S0968-0896(00)00223-6 . ПМИД 11197347 .
- ^ Jump up to: а б с д и ж г час Там С.В. (февраль 1985 г.). «(+)-[3H]SKF 10,047, (+)-[3H]этилкетоциклазоцин, сайты связывания мю, каппа, дельта и фенциклидина в мембранах головного мозга морской свинки». Европейский журнал фармакологии . 109 (1): 33–41. дои : 10.1016/0014-2999(85)90536-9 . ПМИД 2986989 .
- ^ Jump up to: а б с д и ж г час я Корбетт А.Д., Патерсон С.Дж., Костерлиц Х.В. (1993). «Селективность лигандов опиоидных рецепторов». Опиоиды . Справочник по экспериментальной фармакологии. Том. 104/1. С. 645–679. дои : 10.1007/978-3-642-77460-7_26 . ISBN 978-3-642-77462-1 . ISSN 0171-2004 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с Кодд Э.Э., Шэнк Р.П., Шупски Дж.Дж., Раффа Р.Б. (сентябрь 1995 г.). «Активность анальгетиков центрального действия, ингибирующая захват серотонина и норадреналина: структурные детерминанты и роль в антиноцицепции». Журнал фармакологии и экспериментальной терапии . 274 (3): 1263–70. ПМИД 7562497 .
- ^ Линц К., Кристоф Т., Чентке Т.М., Кох Т., Шине К., Готруа М. и др. (июнь 2014 г.). «Цебранопадол: новый мощный анальгетический пептид ноцицептин/орфанин FQ и агонист опиоидных рецепторов». Журнал фармакологии и экспериментальной терапии . 349 (3): 535–548. дои : 10.1124/jpet.114.213694 . ПМИД 24713140 . S2CID 6942770 .
- ^ Фринк MC, Хеннис Х.Х., Энглбергер В., Хауранд М., Уилферт Б. (ноябрь 1996 г.). «Влияние трамадола на нейромедиаторные системы мозга крыс». Исследования наркотиков . 46 (11): 1029–36. ПМИД 8955860 .
- ^ Почка Х, Фридрихс Э, Лёшер В (сентябрь 2000 г.). «Противосудорожное и проконвульсивное действие трамадола, его энантиомеров и его метаболита М1 на крысиной модели эпилепсии» . Британский журнал фармакологии . 131 (2): 203–12. дои : 10.1038/sj.bjp.0703562 . ПМЦ 1572317 . ПМИД 10991912 .
- ^ Кацумата С., Минами М., Накагава Т., Ивамура Т., Сато М. (ноябрь 1995 г.). «Фармакологическое исследование дигидроэторфина на клонированных мю-, дельта- и каппа-опиоидных рецепторах». Европейский журнал фармакологии . 291 (3): 367–73. дои : 10.1016/0922-4106(95)90078-0 . ПМИД 8719422 .
- ^ Анткевич-Михалюк Л., Ветулани Дж., Хавеманн У., Кущинский К. (1982). «Сайты связывания 3H-дигидроморфина в субклеточных фракциях полосатого тела крысы». Пол Джей Фармакол Фарм . 34 (1–3): 73–78. ПМИД 6300816 .
- ^ Барт Г., Шлюгер Дж. Х., Борг Л., Хо А., Бидлак Дж. М., Крик М. Дж. (декабрь 2005 г.). «Налмефен вызывал повышение уровня пролактина в сыворотке крови у нормальных добровольцев: частичная активность агониста каппа-опиоидов?» . Нейропсихофармакология . 30 (12): 2254–62. дои : 10.1038/sj.npp.1300811 . ПМИД 15988468 .
- ^ Wentland MP, Lou R, Lu Q, Bu Y, VanAlstine MA, Cohen DJ и др. (январь 2009 г.). «Синтез и свойства связывания карбоксамидозамещенных опиоидов с опиоидными рецепторами». Письма по биоорганической и медицинской химии . 19 (1): 203–8. дои : 10.1016/j.bmcl.2008.10.134 . ПМИД 19027293 .
- ^ Jump up to: а б Гарагозлу П., Демирчи Х., Дэвид Кларк Дж., Ламех Дж. (январь 2003 г.). «Активность опиоидных лигандов в клетках, экспрессирующих клонированные мю-опиоидные рецепторы» . БМК Фармакология . 3 :1. дои : 10.1186/1471-2210-3-1 . ПМК 140036 . ПМИД 12513698 . Гарагозлу П., Демирчи Х., Кларк Дж.Д., Ламех Дж. (ноябрь 2002 г.). «Профили активации опиоидных лигандов в клетках HEK, экспрессирующих дельта-опиоидные рецепторы» . BMC Нейронаука . 3:19 . дои : 10.1186/1471-2202-3-19 . ПМК 137588 . ПМИД 12437765 . Гарагозлу П., Хашеми Э., Делори Т.М., Кларк Дж.Д., Ламех Дж. (январь 2006 г.). «Фармакологические профили опиоидных лигандов каппа-опиоидных рецепторов» . БМК Фармакология . 6 :3. дои : 10.1186/1471-2210-6-3 . ПМК 1403760 . ПМИД 16433932 .
- ^ Рот Б.Л. , Банер К., Весткемпер Р., Зиберт Д., Райс К.С., Стейнберг С. и др. (сентябрь 2002 г.). «Сальвинорин А: мощный природный безазотистый селективный агонист каппа-опиоидов» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (18): 11934–9. Бибкод : 2002PNAS...9911934R . дои : 10.1073/pnas.182234399 . ПМК 129372 . ПМИД 12192085 .
- ^ Вентланд М.П., Лу Р., Лу К., Бу Ю., Денхардт С., Джин Дж. и др. (апрель 2009 г.). «Синтез новых лигандов с высоким сродством к опиоидным рецепторам» . Письма по биоорганической и медицинской химии . 19 (8): 2289–94. дои : 10.1016/j.bmcl.2009.02.078 . ПМК 2791460 . ПМИД 19282177 .
- ^ Гассауэй М.М., Ривс М.Л., Крюгель А.С., Джавич Дж.А., Самес Д. (июль 2014 г.). «Атипичный антидепрессант и нейровосстановительный агент тианептин является агонистом μ-опиоидных рецепторов» . Трансляционная психиатрия . 4 (7): е411. дои : 10.1038/tp.2014.30 . ПМЦ 4119213 . ПМИД 25026323 .
- ^ Трувер М.Т., Смит Ч.Р., Гарибай Н., Копайтик Т.А., Свортвуд М.Дж., Бауманн М.Х. (2020). «Фармакодинамика и фармакокинетика нового синтетического опиоида U-47700 у крыс-самцов» . Нейрофармакология . 177 . doi : 10.1016/j.neuropharm.2020.108195 . ПМЦ 7554234 . ПМИД 32533977 .
- ^ Фудзимото Р.А., Боксер Дж., Джексон Р.Х., Симке Дж.П., Нил Р.Ф., Сноухилл Э.В. и др. (июнь 1989 г.). «Синтез, профиль связывания опиоидных рецепторов и антиноцицептивная активность 1-азаспиро[4.5]декан-10-иламидов». Журнал медицинской химии . 32 (6): 1259–65. дои : 10.1021/jm00126a019 . ПМИД 2542556 .
- ^ «Годовая распространенность употребления наркотиков по регионам и в мире, 2016 г.» . Всемирный доклад о наркотиках, 2018 год . Управление ООН по наркотикам и преступности. 2018 . Проверено 7 июля 2018 г.
- ^ Волков Н.Д. «Зависимость Америки от опиоидов: героин и злоупотребление лекарствами, отпускаемыми по рецепту» . DrugAbuse.GOV . Национальный институт по борьбе со злоупотреблением наркотиками. Архивировано из оригинала 25 мая 2018 года . Проверено 30 апреля 2017 г. .
- ^ «Наркотические средства Stupéfiants Estupefacientes» (PDF) . МЕЖДУНАРОДНЫЙ КОМИТЕТ ПО КОНТРОЛЮ НАРКОТИКОВ. 2012. Архивировано (PDF) из оригинала 21 октября 2020 года . Проверено 6 марта 2017 г.
- ^ «Данные о потреблении опиоидов | Группа исследований боли и политики» . Painpolicy.wisc.edu. Архивировано из оригинала 30 января 2019 года . Проверено 7 января 2016 г.
- ^ Делл К.А., Робертс Г., Килти Дж., Тейлор К., Дащук М., Хопкинс С. и др. (2012). «Исследование злоупотребления рецептурными препаратами среди коренных народов Канады: начиная с системы укрепления здоровья» . Злоупотребление психоактивными веществами . 6 : 23–31. дои : 10.4137/SART.S9247 . ПМЦ 3411531 . ПМИД 22879752 .
- ^ «Социально обездоленным жителям Онтарио прописывают опиоиды на постоянной основе и в дозах, значительно превышающих канадские рекомендации» . Ices.on.ca. 25 января 2011 г. Архивировано из оригинала 12 ноября 2019 г. . Проверено 7 января 2016 г.
- ^ Jump up to: а б «Избежание злоупотребления, достижение баланса: преодоление опиоидного кризиса общественного здравоохранения» (PDF) . Колледж врачей и хирургов Онтарио. 8 сентября 2010 г. Архивировано из оригинала (PDF) 7 июня 2016 г. . Проверено 6 марта 2017 г.
- ^ Бакхаус I, Манноччи А, Ла Торре Дж (2019). «Систематический обзор исследований по экономической оценке лекарственного лечения незлокачественной хронической боли». Современная фармацевтическая биотехнология . 20 (11): 910–919. дои : 10.2174/1389201020666190717095443 . ПМИД 31322067 . S2CID 197664630 .
- ^ Моджтабай Р. (май 2018 г.). «Национальные тенденции в долгосрочном использовании рецептурных опиоидов» . Фармакоэпидемиология и безопасность лекарственных средств . 27 (5): 526–534. дои : 10.1002/pds.4278 . ПМИД 28879660 . S2CID 19047621 .
- ^ Манглик А., Крузе А.С., Кобилка Т.С., Тиан Ф.С., Матисен Дж.М., Сунахара Р.К. и др. (март 2012 г.). «Кристаллическая структура µ-опиоидного рецептора, связанного с антагонистом морфинана» . Природа . 485 (7398): 321–6. Бибкод : 2012Natur.485..321M . дои : 10.1038/nature10954 . ПМЦ 3523197 . ПМИД 22437502 .
Опий является одним из старейших наркотиков в мире, а его производные морфин и кодеин входят в число наиболее часто используемых клинических препаратов для облегчения сильной боли.
- ^ Колледж С., Конолли Дж. (10 августа 2007 г.). Происхождение и распространение домашних растений в Юго-Западной Азии и Европе . Уолнат-Крик, Калифорния: Left Coast Press. стр. 179–181. ISBN 978-1-59874-988-5 . Архивировано из оригинала 15 декабря 2023 года . Проверено 28 августа 2018 г.
- ^ Кунциг Р., Царь Дж (1 ноября 2002 г.). «Ла Мармотта» . Обнаружить . Архивировано из оригинала 22 января 2019 года . Проверено 28 августа 2018 г.
- ^ Шевалье А., Маринова Е., Пенья-Чокарро Л. (1 апреля 2014 г.). Растения и люди: выбор и разнообразие во времени . Книги Оксбоу. стр. 97–99. ISBN 978-1-84217-514-9 . Архивировано из оригинала 15 декабря 2023 года . Проверено 28 августа 2018 г.
- ^ Критикос П.Г., Пападаки С.П. (1967). «История мака и опиума и их распространение в древности в восточном Средиземноморье» . Бюллетень о наркотиках . XIX (4). Архивировано из оригинала 16 декабря 2020 года . Проверено 23 августа 2018 г.
- ^ Зоннедекер Г (1962). «Возникновение концепции опиатной зависимости». Журнал Mondial de Pharmacie . 3 : 275–290.
- ^ Jump up to: а б с д и ж Браунштейн MJ (июнь 1993 г.). «Краткая история опиатов, опиоидных пептидов и опиоидных рецепторов» . Труды Национальной академии наук Соединенных Штатов Америки . 90 (12): 5391–3. Бибкод : 1993PNAS...90.5391B . дои : 10.1073/pnas.90.12.5391 . ПМК 46725 . ПМИД 8390660 .
- ^ Jump up to: а б с д Дуарте Д.Ф. (февраль 2005 г.). «Краткая история опиума и опиоидов» (PDF) . Бразильский журнал анестезиологии . 55 (1). дои : 10.1590/S0034-70942005000100015 . Архивировано (PDF) из оригинала 10 января 2021 года . Проверено 13 сентября 2019 г.
- ^ Россо А.М. (2010). «Мак и опиум в древности: лекарство или наркотик?». Биомедицина Интернэшнл . 1 : 81–87. CiteSeerX 10.1.1.846.221 .
- ^ Астиракаки Э., Папайоанну А., Аскитопулу Х. (январь 2010 г.). «Ссылки на анестезию, боль и анальгезию в Сборнике Гиппократа» . Анестезия и анальгезия . 110 (1): 188–94. дои : 10.1213/ane.0b013e3181b188c2 . ПМИД 19861359 . S2CID 25919738 .
- ^ Тюре Х., Тюре У., Гёгюс Ф.Ю., Валаванис А., Ясаргиль М.Г. (сентябрь 2006 г.). «987 Искусство облегчения боли в греческой мифологии». Европейский журнал боли . 10 (С1): С255б–С255. дои : 10.1016/S1090-3801(06)60990-7 . S2CID 26539333 .
Sedare dolorem opus divinum est – старинная латинская надпись – означает «облегчение боли – дело божественное». Эту надпись часто приписывают либо Гиппократу Косскому, либо Галену Пергамскому, но, скорее всего, это анонимная пословица.
- ^ Осбалдестон Т.А. (2000). Диоскорид (перевод ) Йоханнесбург, Южная Африка: Ibidis Press. стр. 100-1 607–611. ISBN 978-0-620-23435-1 .
- ^ Хейдари М., Хашемпур М.Х., Заргаран А. (2013). «Лечебные аспекты опиума, описанные в «Каноне медицины» Авиценны» . Acta Medico-historica Adriatica . 11 (1): 101–12. ПМИД 23883087 . Архивировано из оригинала 13 февраля 2023 года . Проверено 28 августа 2018 г.
- ^ Jump up to: а б с Астана С.Н. (1954). «Выращивание опиумного мака в Индии» . Бюллетень по наркотикам (3). Архивировано из оригинала 6 августа 2020 года . Проверено 5 сентября 2018 г.
- ^ Jump up to: а б с Сигерист Х.Э. (1941). «Лауданум в трудах Парацельса» (PDF) . Бык. Хист. Мед . 9 : 530–544. Архивировано (PDF) из оригинала 9 октября 2022 года . Проверено 5 сентября 2018 г.
- ^ Jump up to: а б с д и Хэмилтон GR, Baskett TF (апрель 2000 г.). «В объятиях Морфеуса разработка морфия для послеоперационного обезболивания» . Канадский журнал анестезии . 47 (4): 367–74. дои : 10.1007/BF03020955 . ПМИД 10764185 .
- ^ Jump up to: а б Фаруки А. (декабрь 2016 г.). «Глобальная карьера индийского опиума и местные судьбы» (PDF) . Альманах (14): 52–73. дои : 10.1590/2236-463320161404 . Архивировано (PDF) из оригинала 27 июля 2018 года . Проверено 5 сентября 2018 г.
- ^ Jump up to: а б Деминг С. (2011). «Экономическое значение индийского опиума и торговли с Китаем для британской экономики, 1843–1890» . Экономические рабочие документы . 25 (Весна). Архивировано из оригинала (PDF) 12 ноября 2020 года . Проверено 5 сентября 2018 г.
- ^ Jump up to: а б с д и ж г час я дж к Ринде М (2018). «Разрушительное возвращение опиоидов» . Дистилляции . 4 (2): 12–23. Архивировано из оригинала 5 сентября 2018 года . Проверено 23 августа 2018 г.
- ^ Миллс Дж. Х. (2016). Обзор книги «Опиум и империя в Юго-Восточной Азии: регулирование потребления в Британской Бирме» . Серия Кембриджских имперских и постколониальных исследований. Пэлгрейв Макмиллан. дои : 10.14296/RiH/2014/2010 . ISBN 978-0-230-29646-6 . Архивировано из оригинала 1 октября 2020 года . Проверено 5 сентября 2018 г.
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Кришнамурти С., Рао С.К. (ноябрь 2016 г.). «Выделение морфия Сертернером» . Индийский журнал анестезии . 60 (11): 861–862. дои : 10.4103/0019-5049.193696 . ПМК 5125194 . ПМИД 27942064 .
- ^ Кортрайт Д.Т. (2009). Силы привычки к наркотикам и создание современного мира (1-е изд.). Кембридж, Массачусетс: Издательство Гарвардского университета. стр. 36–37. ISBN 978-0-674-02990-3 .
- ^ Атанасов А.Г., Вальтенбергер Б., Пферши-Венциг Э.М., Линдер Т., Ваврош С., Урин П. и др. (декабрь 2015 г.). «Открытие и пополнение запасов фармакологически активных натуральных продуктов растительного происхождения: обзор» . Достижения биотехнологии . 33 (8): 1582–1614. doi : 10.1016/j.biotechadv.2015.08.001 . ПМЦ 4748402 . ПМИД 26281720 .
- ^ Котвал А. (март 2005 г.). «Инновации, распространение и безопасность медицинских технологий: обзор литературы по инъекционной практике». Социальные науки и медицина . 60 (5): 1133–47. doi : 10.1016/j.socscimed.2004.06.044 . ПМИД 15589680 .
- ^ Мошер CJ (2013). Наркотики и наркополитика: контроль над изменением сознания . Публикации SAGE. п. 123. ИСБН 978-1-4833-2188-2 .
- ^ Фишер Г.Л. (2009). Энциклопедия профилактики, лечения и выздоровления от злоупотребления психоактивными веществами . Лос-Анджелес: SAGE. п. 564. ИСБН 978-1-4522-6601-5 .
- ^ Jump up to: а б Трики Э (4 января 2018 г.). «Из истории опиатной зависимости Америки XIX века» . Смитсоновский институт . Архивировано из оригинала 23 декабря 2020 года . Проверено 6 сентября 2018 г.
- ^ Шехтер Н.Л. (1993). Боль у младенцев, детей и подростков . Уильямс и Уилкинс. ISBN 978-0-683-07588-5 . Архивировано из оригинала 15 декабря 2023 года . Проверено 6 сентября 2018 г.
- ^ Хикс Р.Д. (2011). «Аптеки на передовой» . Журнал «Химическое наследие» . Фонд химического наследия . Архивировано из оригинала 30 сентября 2020 года . Проверено 29 октября 2018 г.
- ^ Jump up to: а б Бут М (12 июня 1999 г.). Опиум: история (1-е изд. США). Пресса Святого Мартина. ISBN 978-0-312-20667-3 .
- ^ Вишняк Дж. (март 2013 г.). «Пьер-Жан Робике» . Химическое образование . 24 : 139–149. дои : 10.1016/S0187-893X(13)72507-2 .
- ^ Филан К (2011). Сила мака: использование самого опасного растения-союзника природы . Парк Стрит Пресс. п. 69. ИСБН 978-1-59477-399-0 . Архивировано из оригинала 15 декабря 2023 года . Проверено 30 октября 2018 г.
- ^ «Феликс Гофман» . Институт истории науки . Июнь 2016. Архивировано из оригинала 21 марта 2018 года . Проверено 21 марта 2018 г.
- ^ Купер Р., Дикин Дж.Дж. (22 февраля 2016 г.). Ботанические чудеса: химия растений, изменивших мир . ЦРК Пресс. п. 137. ИСБН 978-1-4987-0428-1 . Архивировано из оригинала 15 декабря 2023 года . Проверено 30 октября 2018 г.
- ^ Снидер В. (ноябрь 1998 г.). «Открытие героина» (PDF) . Ланцет . 352 (9141): 1697–9. дои : 10.1016/S0140-6736(98)07115-3 . ПМИД 9853457 . S2CID 1819676 . Архивировано из оригинала 17 декабря 2020 года . Проверено 30 октября 2018 г.
Байер зарегистрировал название «героин» в июне 1898 года.
- ^ Jump up to: а б с д и Ньютон Д.Э. (2016). Злоупотребление психоактивными веществами среди молодежи: справочное пособие . Санта-Барбара, Калифорния: ABC-CLIO. стр. 41–60. ISBN 978-1-4408-3983-2 . Архивировано из оригинала 15 декабря 2023 года . Проверено 30 октября 2018 г.
- ^ Кроу Дж. М. (3 января 2017 г.). «Пристрастие к лечению» . Химический мир . Архивировано из оригинала 7 ноября 2020 года . Проверено 30 октября 2018 г.
- ^ Метадон имеет значение: развитие метадонового лечения опиатной зависимости в сообществе . ЦРК Пресс. 2003. с. 13. ISBN 978-0-203-63309-0 . Архивировано из оригинала 23 декабря 2015 года.
- ^ «Информационный бюллетень: фентанил и синтетические опиоиды» (PDF) . Альянс по наркополитике . Сентябрь 2016 г. Архивировано из оригинала (PDF) 29 августа 2020 г. . Проверено 30 октября 2018 г.
- ^ «Законы Узнайте о законах, касающихся опиоидов с 1800-х годов до наших дней» . Национальный альянс сторонников лечения бупренорфином . Архивировано из оригинала 22 декабря 2020 года . Проверено 30 октября 2018 г.
- ^ Белый ВЛ. «Ранняя криминализация наркотической зависимости» (PDF) . Белые книги Уильяма . Архивировано из оригинала (PDF) 26 октября 2020 года . Проверено 30 октября 2018 г.
- ^ Марс С (2003). «Давление со стороны коллег и навязанный консенсус: разработка Руководства по надлежащей клинической практике лечения злоупотребления наркотиками 1984 года». Клио Медика . 75 (2): 149–83. дои : 10.1163/9789004333109_009 . ISBN 978-90-04-33310-9 . ПМИД 16212730 .
- ^ Jump up to: а б Джейкобс Х (26 мая 2016 г.). «Это письмо, состоящее из одного абзаца, возможно, положило начало опиоидной эпидемии» . Бизнес-инсайдер . Архивировано из оригинала 6 августа 2020 года . Проверено 30 октября 2018 г.
- ^ Портеной Р.К., Фоли К.М. (май 1986 г.). «Хроническое использование опиоидных анальгетиков при доброкачественной боли: отчет о 38 случаях». Боль . 25 (2): 171–86. дои : 10.1016/0304-3959(86)90091-6 . ПМИД 2873550 . S2CID 23959703 .
- ^ Jump up to: а б с Мелдрам М.Л. (август 2016 г.). «Продолжающаяся эпидемия рецептов на опиоиды: исторический контекст» . Американский журнал общественного здравоохранения . 106 (8): 1365–6. дои : 10.2105/AJPH.2016.303297 . ПМЦ 4940677 . ПМИД 27400351 .
- ^ Хиноны С (2015). Страна грез: правдивая история опиатной эпидемии в Америке . Блумсбери Пресс. ISBN 978-1-62040-251-1 .
- ^ Доуэлл Д., Хэгерих Т.М., Чоу Р. (март 2016 г.). «Руководство CDC по назначению опиоидов при хронической боли – США, 2016 г.» . ММВР. Рекомендации и отчеты . 65 (1): 1–49. doi : 10.15585/mmwr.rr6501e1 . ПМК 6390846 . ПМИД 26987082 .
- ^ «FDA запускает просветительскую кампанию для поощрения безопасного удаления из домов неиспользованных опиоидных обезболивающих препаратов» . FDA . 24 марта 2020 г. Архивировано из оригинала 2 декабря 2020 г. Проверено 15 декабря 2023 г.
- ^ «опиоид: определение опиоида в Оксфордском словаре (американский английский) (США)» . www.oxforddictionaries.com . Архивировано из оригинала 27 июня 2014 года . Проверено 14 февраля 2016 г.
Опиоид: 1950-е годы: из опиума + -оид.
- ^ Виклер А., Мартин В.Р., Пескор Ф.Т., Идс К.Г. (октябрь 1963 г.). «Факторы, регулирующие пероральное употребление опиоида (этонитазена) крысами, зависимыми от морфия». Психофармакология . 5 : 55–76. дои : 10.1007/bf00405575 . ПМИД 14082382 . S2CID 38073529 .
В этой статье термин «опиоид» используется в том смысле, первоначально предложенном DR. ДЖОРДЖ Х. АЧЕСОН (личное сообщение) для обозначения любого химического соединения, обладающего морфиноподобной активностью.
- ^ Мартин В.Р. (декабрь 1967 г.). «Антагонисты опиоидов». Фармакологические обзоры . 19 (4): 463–521. ПМИД 4867058 .
- ^ Мехди Б (2008). «Опиоидные анальгетики и антагонисты». В Сете С.Д., Сете В. (ред.). Учебник фармакологии . Эльзевир Индия. п. III.137. ISBN 978-81-312-1158-8 .
- ^ «Эпидемия: ответ на кризис злоупотребления рецептурными лекарствами в Америке» (PDF) . Белый дом. 2011. Архивировано из оригинала (PDF) 3 марта 2012 года.
- ^ «Прежде всего, не навреди: реагирование на кризис рецептурных лекарств в Канаде» (PDF) . Март 2013 г. Архивировано из оригинала 2 марта 2019 г. . Проверено 8 марта 2017 г.
- ^ «Великобритания: Целевая группа предлагает идеи решения проблемы опиоидной зависимости» . Delhidailynews.com. 11 июня 2014 года. Архивировано из оригинала 6 июня 2017 года . Проверено 7 января 2016 г.
- ^ Кайт А (29 апреля 2018 г.). «В каждом штате, кроме Миссури, есть отслеживание опиоидных наркотиков. Почему сенаторы против этого?» . Звезда Канзас-Сити . Архивировано из оригинала 27 декабря 2020 года . Проверено 5 ноября 2018 г.
- ^ Руткоу Л., Тернер Л., Лукас Э., Хван С., Александр Г.К. (март 2015 г.). «Большинство врачей первичной медико-санитарной помощи знают о программах мониторинга рецептурных препаратов, но многим трудно получить доступ к этим данным» . Дела здравоохранения . 34 (3): 484–92. дои : 10.1377/hlthaff.2014.1085 . ПМИД 25732500 .
- ^ Перроне М (20 декабря 2015 г.). «Политика обезболивающих: усилия по ограничению выписывания рецептов под огнем» . Филли.ком. Ассошиэйтед Пресс. Архивировано из оригинала 22 декабря 2018 года . Проверено 7 января 2016 г.
- ^ Фон Корфф М., Дублин С., Уокер Р.Л., Парчман М., Шортрид С.М., Хансен Р.Н. и др. (январь 2016 г.). «Влияние инициатив по снижению риска опиоидов на назначение высоких доз опиоидов пациентам, проходящим хроническую опиоидную терапию» . Журнал боли . 17 (1): 101–10. дои : 10.1016/j.jpain.2015.10.002 . ПМК 4698093 . ПМИД 26476264 .
- ^ Ахенбах Дж., Вагнер Дж., Бернштейн Л. «Трамп говорит, что опиоидный кризис является чрезвычайной ситуацией в стране, и обещает больше денег и внимания» . Вашингтон Пост . Архивировано из оригинала 24 ноября 2020 года . Проверено 11 августа 2017 г.
- ^ «Технико-экономическое обоснование лицензирования опия в Афганистане для производства морфина и других основных лекарственных средств» . ICoS. Сентябрь 2005 г. Архивировано из оригинала 3 марта 2016 г. Проверено 3 марта 2015 г.
- ^ «Обеспечение доступности опиоидных анальгетиков» (PDF) . Всемирная организация здравоохранения. Архивировано из оригинала (PDF) 1 декабря 2009 года.
- ^ Гелардини С., Ди Чезаре Маннелли Л., Бьянки Э. (2015). «Фармакологическая основа опиоидов» . Клинические случаи минерального и костного обмена . 12 (3): 219–21. дои : 10.11138/ccmbm/2015.12.3.219 . ПМК 4708964 . ПМИД 26811699 .
Эффекты опиоидов, выходящие за рамки обезболивания, включают седативный эффект, угнетение дыхания, запор и сильное чувство эйфории.
- ^ Барретт С.П., Мейснер-младший, Стюарт Ш. (ноябрь 2008 г.). «Что представляет собой злоупотребление рецептурными лекарствами? Проблемы и подводные камни современных концепций» (PDF) . Текущие обзоры злоупотребления наркотиками . 1 (3): 255–62. дои : 10.2174/1874473710801030255 . ПМИД 19630724 . Архивировано из оригинала (PDF) 15 июня 2010 года.
- ^ Маккейб С.Э., Бойд С.Дж., Тетер С.Дж. (июнь 2009 г.). «Подтипы немедицинского злоупотребления рецептурными лекарствами» . Наркотическая и алкогольная зависимость . 102 (1–3): 63–70. doi : 10.1016/j.drugalcdep.2009.01.007 . ПМЦ 2975029 . ПМИД 19278795 .
- ^ «Данные о передозировке рецептурных опиоидов | Передозировка наркотиками | Центр травм CDC» . www.cdc.gov . 31 августа 2018 года. Архивировано из оригинала 24 августа 2019 года . Проверено 17 января 2017 г.
- ^ «Управление хронической болью и злоупотребление опиоидами: проблема общественного здравоохранения (документ с изложением позиции)» . Американская академия семейных врачей . Архивировано из оригинала 4 октября 2023 года . Проверено 9 сентября 2023 г.
- ^ «Опиоидный препарат» . Наука Дейли . Архивировано из оригинала 19 апреля 2021 года . Проверено 25 июня 2021 г.
- ^ «Эфиры морфия» . Управление ООН по наркотикам и преступности . 1953. Архивировано из оригинала 24 декабря 2018 года . Проверено 10 марта 2012 г.
- ^ «Эфиры морфиноопиоидов» . эОпиаты . 28 мая 2014 года . Проверено 12 февраля 2016 г. [ постоянная мертвая ссылка ]
- ^ Рот Б.Л., Банер К., Весткемпер Р., Зиберт Д., Райс К.С., Стейнберг С. и др. (3 сентября 2002 г.). «Сальвинорин А: мощный природный безазотистый селективный агонист κ-опиоидов» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (18): 11934–11939. Бибкод : 2002PNAS...9911934R . дои : 10.1073/pnas.182234399 . ISSN 0027-8424 . ПМК 129372 . ПМИД 12192085 .
- ^ Раффа Р.Б., Бушманн Х., Кристоф Т., Эйхенбаум Г., Энглбергер В., Флорес С.М. и др. (июль 2012 г.). «Механистическая и функциональная дифференциация тапентадола и трамадола». Экспертное заключение по фармакотерапии . 13 (10): 1437–49. дои : 10.1517/14656566.2012.696097 . ПМИД 22698264 . S2CID 24226747 .
- ^ Рохас-Корралес М.О., Гиберт-Рахола Х., Мико Х.А. (1998). «Трамадол вызывает у мышей эффекты антидепрессивного типа». Науки о жизни . 63 (12): PL175-80. дои : 10.1016/S0024-3205(98)00369-5 . ПМИД 9749830 .
- ^ Штейн С., Шефер М., Мачелска Х (август 2003 г.). «Атака боли у ее источника: новые взгляды на опиоиды». Природная медицина . 9 (8): 1003–8. дои : 10.1038/nm908 . ПМИД 12894165 . S2CID 25453057 .
- ^ Штейн С., Ланг LJ (февраль 2009 г.). «Периферические механизмы опиоидной анальгезии». Современное мнение в фармакологии . 9 (1): 3–8. дои : 10.1016/j.coph.2008.12.009 . ПМИД 19157985 .
- ^ Буш-Динстфертиг М., Штейн С. (июль 2010 г.). «Опиоидные рецепторы и лейкоциты, продуцирующие опиоидные пептиды, при воспалительной боли - основные и терапевтические аспекты». Мозг, поведение и иммунитет . 24 (5): 683–94. дои : 10.1016/j.bbi.2009.10.013 . ПМИД 19879349 . S2CID 40205179 .
- ^ Оделл Л.Р., Скопец Дж., МакКласки А. (март 2008 г.). «Выделение и идентификация уникальных маркерных соединений из тасманского мака Papaver somniferum N. Значение для идентификации незаконного героина тасманского происхождения». Международная судебно-медицинская экспертиза . 175 (2–3): 202–8. doi : 10.1016/j.forsciint.2007.07.002 . ПМИД 17765420 .
Внешние ссылки
[ редактировать ]- Симптомы отмены опиоидов. Архивировано 10 августа 2018 г. на Wayback Machine. Информация о проблемах отмены опиоидов и опиатов.
- Рекомендации Всемирной организации здравоохранения по наличию и доступности контролируемых веществ
- Рекомендации CDC по назначению опиоидов при хронической боли — США, 2016 г.
- Список ссылок на предыдущую публикацию
- Ссылки на все языковые версии предыдущей публикации
- Видео: Побочные эффекты опиоидов (Vimeo) (YouTube) — короткий образовательный фильм о практическом лечении побочных эффектов опиоидов.