δ-опиоидный рецептор
| ОПРД1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | OPRD1 , OPRD, Δ-опиоидный рецептор, опиоидный рецептор дельта 1, DOP, DOR1, DOR | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 165195 ; МГИ : 97438 ; Гомологен : 20252 ; GeneCards : OPRD1 ; ОМА : OPRD1 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
δ -опиоидный рецептор , также известный как дельта-опиоидный рецептор или просто дельта-рецептор , сокращенно DOR или DOP , представляет собой ингибирующий 7-трансмембранный рецептор, связанный с G-белком, связанный с G-белком G i /G 0, и имеет энкефалины в качестве своих эндогенных лигандов. . [5] Области мозга, в которых δ- опиоидный рецептор, в значительной степени экспрессируется варьируются от видовой модели к видовой модели. У людей δ-опиоидный рецептор наиболее сильно экспрессируется в базальных ганглиях и неокортикальных областях мозга. [6]
Функция
[ редактировать ]Эндогенная система опиоидных рецепторов хорошо известна своим анальгетическим потенциалом; однако точная роль активации δ-опиоидных рецепторов в модуляции боли во многом остается предметом дискуссий. Это также зависит от рассматриваемой модели, поскольку известно, что активность рецепторов меняется от вида к виду. Активация дельта-рецепторов вызывает анальгезию , возможно, в качестве значительного потенциатора агонистов мю-опиоидных рецепторов. Однако похоже, что дельта-агонизм обеспечивает сильное усиление любого мю-агонизма. Таким образом, даже селективные мю-агонисты при правильных условиях могут вызывать аналгезию, тогда как при других не могут вообще ее вызвать. [7] [8] Однако также предполагается, что боль, модулируемая мю-опиоидным рецептором, и боль, модулируемая дельта-опиоидным рецептором, представляют собой разные типы, при этом утверждается, что DOR модулирует ноцицепцию хронической боли, а MOR модулирует острую боль. [9]
Доказательства того, вызывают ли дельта-агонисты угнетение дыхания , неоднозначны; высокие дозы дельта-агониста пептида DPDPE вызывали у овец угнетение дыхания. [10] Напротив, как пептидный дельта-агонист Дельторфин II, так и непептидный дельта-агонист (+)-BW373U86 фактически стимулировали дыхательную функцию и блокировали респираторный депрессивный эффект мощного мю-опиоидного агониста альфентанила , не влияя на облегчение боли. [11] Таким образом, представляется вероятным, что, хотя дельта-опиоидные агонисты могут вызывать угнетение дыхания в очень высоких дозах, в более низких дозах они оказывают противоположный эффект. Этот факт может сделать смешанные мю/дельта-агонисты, такие как DPI-3290, потенциально очень полезными препаратами, которые могут быть намного безопаснее, чем µ-агонисты, используемые в настоящее время для облегчения боли. Многие дельта-агонисты также могут вызывать судороги в высоких дозах, хотя не все дельта-агонисты оказывают такой эффект. [12]
Дополнительный интерес представляет возможность разработки дельта-агонистов для использования в качестве нового класса антидепрессантов после убедительных доказательств обоих антидепрессивных эффектов. [13] а также усиление выработки BDNF в мозге на животных моделях депрессии . [14] Эти антидепрессивные эффекты связаны с эндогенными опиоидными пептидами, действующими на δ- и μ-опиоидные рецепторы. [15] и поэтому также может быть продуцирован ингибиторами энкефалиназы, такими как RB-101. [16] Однако данные о действии антидепрессантов на людях остаются неубедительными. В клиническом исследовании фазы 2, проведенном компанией Astra Zeneca в 2008 году, NCT00759395, 15 пациентов получали селективный дельта-агонист AZD 2327. Результаты не выявили существенного влияния на настроение, что позволяет предположить, что модуляция δ-опиоидных рецепторов может не участвовать в регуляции настроения у людей. . Однако дозы вводились в низких дозах, и фармакологические данные также остаются неубедительными. [17] [18] Требуются дальнейшие испытания.
Еще одним интересным аспектом функции δ-опиоидных рецепторов является предположение о взаимодействии µ/δ-опиоидных рецепторов. Крайним вариантом этого предположения является возможность существования олигомера опиоидного рецептора μ/δ. Доказательства этого основаны на различных профилях связывания типичных мю- и дельта-агонистов, таких как морфин и DAMGO соответственно, в клетках, которые коэкспрессируют оба рецептора, по сравнению с клетками, которые экспрессируют их индивидуально. Кроме того, работа Fan и сотр. показывает восстановление профилей связывания, когда дистальные карбоксильные концы усекаются у любого рецептора, указывая тем самым, что концы играют роль в олигомеризации. [19] Хотя это и интересно, опровержение Джавича и его коллег предполагает, что идея олигомеризации может быть преувеличена. Опираясь на RET , Джавич и его коллеги показали, что сигналы RET были более характерны для случайной близости между рецепторами, а не для фактического образования связей между рецепторами, предполагая, что расхождения в профилях связывания могут быть результатом последующих взаимодействий, а не новых эффектов, вызванных олигомеризацией. . [20] Тем не менее, коэкспрессия рецепторов остается уникальной и потенциально полезной при лечении расстройств настроения и боли.
Недавние исследования показывают, что экзогенные лиганды, которые активируют дельта-рецепторы, имитируют явление, известное как ишемическое предварительное кондиционирование . [21] Экспериментально, если вызвать короткие периоды транзиторной ишемии , нижележащие ткани будут надежно защищены, если затем произойдет более продолжительное прерывание кровоснабжения. Опиаты и опиоиды с активностью DOR имитируют этот эффект. На крысиной модели введение лигандов DOR приводит к значительной кардиопротекции. [22]
Лиганды
[ редактировать ]До сравнительно недавнего времени существовало мало фармакологических инструментов для изучения δ-рецепторов. Как следствие, наше понимание их функции гораздо более ограничено, чем понимание других опиоидных рецепторов, для которых уже давно доступны селективные лиганды.
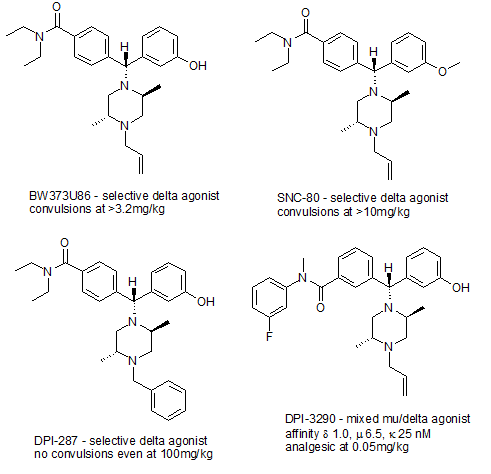
Однако в настоящее время доступно несколько селективных агонистов δ-опиоидных рецепторов, включая пептиды, такие как DPDPE и дельторфин II, а также непептидные препараты, такие как SNC-80 . [23] более мощный (+)- BW373U86 , [24] новый препарат DPI-287 , который не вызывает проблем с судорогами, наблюдавшихся при приеме более ранних препаратов, [25] и смешанный агонист μ/δ DPI-3290 , который является гораздо более сильным анальгетиком, чем более селективные агонисты δ. [26] Также доступны селективные антагонисты δ-рецептора, наиболее известным из которых является производное опиата налтриндол . [27]
Агонисты
[ редактировать ]
- Пептиды
- Непептиды
- АДЛ-5859 [28]
- БУ-48
- БВ373У86
- ДПИ-221
- ДПИ-287
- ДПИ-3290
- RWJ-394674 -
- СНС-80
- ТАН-67
- Амоксапин (частичный агонист) [29]
- Каннабидиол (аллостерический модулятор, неселективный) [30]
- Десметилклозапин
- Митрагинин [31]
- Митрагинин псевдоиндоксил [31]
- Норбупренорфин (периферически ограничено)
- N-фенетил-14-этоксиметопон
- 7-спироинданилоксиморфон
- Тетрагидроканнабинол (аллостерический модулятор, неселективный) [30]
- Ксорфанол
Антагонисты
[ редактировать ]Взаимодействия
[ редактировать ]Было показано, что δ-опиоидные рецепторы взаимодействуют с β2 - адренергическими рецепторами . [32] аррестин β 1 [33] и GPRASP1 . [34]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с GRCh38: Версия Ensembl 89: ENSG00000116329 – Ensembl , май 2017 г.
- ^ Jump up to: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000050511 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Куок Р.М., Берки Т.Х., Варга Э., Хосохата Ю., Хосохата К., Коуэлл С.М. и др. (сентябрь 1999 г.). «Дельта-опиоидный рецептор: молекулярная фармакология, передача сигнала и определение эффективности лекарств» . Фармакологические обзоры . 51 (3): 503–532. ПМИД 10471416 .
- ^ Пеппин Дж. Ф., Раффа Р.Б. (апрель 2015 г.). «Дельта-опиоидные агонисты: краткая информация о потенциальных терапевтических применениях» . Журнал клинической фармации и терапии . 40 (2): 155–166. дои : 10.1111/jcpt.12244 . ПМИД 25726896 . S2CID 25483387 .
- ^ Варга Е.В., Навратилова Е., Стропова Д., Джамбросич Дж., Роске В.Р., Ямамура Х.И. (декабрь 2004 г.). «Агонист-специфическая регуляция дельта-опиоидного рецептора». Науки о жизни . 76 (6): 599–612. дои : 10.1016/j.lfs.2004.07.020 . ПМИД 15567186 .
- ^ Алвимопан
- ^ Беррокозо Э., Санчес-Бласкес П., Гарсон Х., Мико Х.А. (2009). «Опиаты как антидепрессанты». Текущий фармацевтический дизайн . 15 (14): 1612–1622. дои : 10.2174/138161209788168100 . hdl : 10261/62156 . ПМИД 19442177 .
- ^ Клапп Дж.Ф., Кетт А., Олариу Н., Омонийи А.Т., Ву Д., Ким Х. и др. (февраль 1998 г.). «Сердечно-сосудистые и метаболические реакции на два селективных опиоидных агониста у беременных овец». Американский журнал акушерства и гинекологии . 178 (2): 397–401. дои : 10.1016/S0002-9378(98)80032-X . ПМИД 9500506 .
- ^ Су Ю.Ф., МакНатт Р.В., Чанг К.Дж. (декабрь 1998 г.). «Дельта-опиоидные лиганды устраняют вызванную альфентанилом депрессию дыхания, но не антиноцицепцию» . Журнал фармакологии и экспериментальной терапии . 287 (3): 815–823. ПМИД 9864259 .
- ^ Юткевич Э.М., Балади М.Г., Фолк Дж.Э., Райс К.К., Вудс Дж.Х. (июнь 2006 г.). «Судорожные и электроэнцефалографические изменения, вызванные непептидными дельта-опиоидными агонистами у крыс: сравнение с пентилентетразолом». Журнал фармакологии и экспериментальной терапии . 317 (3): 1337–1348. дои : 10.1124/jpet.105.095810 . ПМИД 16537798 . S2CID 21838231 .
- ^ Брум Д.С., Юткевич Э.М., Райс К.К., Трейнор-младший, Вудс Дж.Х. (сентябрь 2002 г.). «Поведенческие эффекты агонистов дельта-опиоидных рецепторов: потенциальные антидепрессанты?» . Японский журнал фармакологии . 90 (1): 1–6. дои : 10.1254/jjp.90.1 . ПМИД 12396021 .
- ^ Торрегросса М.М., Юткевич Э.М., Мосберг Х.И., Бальбони Дж., Уотсон С.Дж., Вудс Дж.Х. (январь 2006 г.). «Пептидные агонисты дельта-опиоидных рецепторов оказывают антидепрессивное действие в тесте принудительного плавания и регулируют экспрессию мРНК BDNF у крыс» . Исследования мозга . 1069 (1): 172–181. дои : 10.1016/j.brainres.2005.11.005 . ПМК 1780167 . ПМИД 16364263 .
- ^ Чжан Х., Торрегросса М.М., Юткевич Э.М., Ши Ю.Г., Райс К.С., Вудс Дж.Х. и др. (февраль 2006 г.). «Эндогенные опиоиды активируют мРНК нейротрофического фактора головного мозга через дельта- и микроопиоидные рецепторы независимо от эффектов, подобных антидепрессантам» . Европейский журнал неврологии . 23 (4): 984–994. дои : 10.1111/j.1460-9568.2006.04621.x . ПМК 1462954 . ПМИД 16519663 .
- ^ Юткевич Э.М., Торрегросса М.М., Собчик-Коджиро К., Мосберг Х.И., Фолк Дж.Э., Райс К.С. и др. (февраль 2006 г.). «Поведенческие и нейробиологические эффекты ингибитора энкефалиназы RB101 по сравнению с его антидепрессивным действием» . Европейский журнал фармакологии . 531 (1–3): 151–159. дои : 10.1016/j.ejphar.2005.12.002 . ПМК 1828120 . ПМИД 16442521 .
- ^ Худжик Т.Дж., Макиаг С., Смит М.А., Каччезе Р., Пьетрас М.Р., Буй К.Х. и др. (июль 2011 г.). «Доклиническая фармакология AZD2327: высокоселективный агонист δ-опиоидного рецептора». Журнал фармакологии и экспериментальной терапии . 338 (1): 195–204. дои : 10.1124/jpet.111.179432 . ПМИД 21444630 . S2CID 10313748 .
- ^ «Исследование антидепрессивной эффективности селективного энкефалинэргического агониста с высоким сродством при тревожном большом депрессивном расстройстве (AMDD) - полнотекстовый просмотр - ClinicalTrials.gov» . www.clinicaltrials.gov . 10 октября 2012 года . Проверено 11 декабря 2015 г.
- ^ Фан Т., Варгезе Г., Нгуен Т., Це Р., О'Дауд Б.Ф., Джордж С.Р. (ноябрь 2005 г.). «Роль дистальных карбоксильных хвостов в создании новой фармакологии и профиля активации G-белка гетероолигомеров мю- и дельта-опиоидных рецепторов» . Журнал биологической химии . 280 (46): 38478–38488. дои : 10.1074/jbc.M505644200 . ПМИД 16159882 . S2CID 32785318 .
- ^ Ламберт Н.А., Явич Дж.А. (июнь 2014 г.). «Опровержение Невина А. Ламберта и Джонатана А. Джавича» . Журнал физиологии . 592 (12): 2449. doi : 10.1113/jphysical.2014.274241 . ПМК 4080929 . ПМИД 24931947 .
- ^ Чжан Дж, Цянь Х, Чжао П, Хун СС, Ся Ю (апрель 2006 г.). «Быстрая предварительная подготовка к гипоксии защищает кортикальные нейроны от токсичности глутамата через дельта-опиоидный рецептор» . Гладить . 37 (4): 1094–1099. дои : 10.1161/01.STR.0000206444.29930.18 . ПМИД 16514101 . S2CID 21120257 .
- ^ Го Л, Чжан Л, Чжан округ Колумбия (октябрь 2005 г.). «[Механизмы кардиопротекторного действия дельта-опиоидов при ишемии и их потенциальное клиническое применение]». Шэн Ли Кэ Сюэ Цзинь Чжань [Прогресс в физиологии] (на китайском языке). 36 (4): 333–336. ПМИД 16408774 .
- ^ Кальдерон С.Н., Ротман Р.Б., Поррека Ф., Флиппен-Андерсон Дж.Л., МакНатт Р.В., Сюй Х. и др. (июль 1994 г.). «Зонды на явления, опосредованные наркотическими рецепторами. 19. Синтез (+)-4-[(альфа R)-альфа-((2S,5R)-4-аллил-2,5-диметил-1-пиперазинил)-3- метоксибензил]-N,N-диэтилбензамид (SNC 80): высокоселективный непептидный агонист дельта-опиоидных рецепторов». Журнал медицинской химии . 37 (14): 2125–2128. дои : 10.1021/jm00040a002 . ПМИД 8035418 .
- ^ Кальдерон С.Н., Райс К.С., Ротман Р.Б., Поррека Ф., Флиппен-Андерсон Дж.Л., Каякири Х. и др. (февраль 1997 г.). «Зоны явлений, опосредованных наркотическими рецепторами. 23. Синтез, связывание опиоидных рецепторов и биоанализ высокоселективного дельта-агониста (+)-4-[(альфа R)-альфа-((2S,5R)-4-аллил-2) ,5-диметил-1-пиперазинил)-3-метоксибензил]-N,N-диэтилбензамид (SNC 80) и родственные ему новые непептидные лиганды дельта-опиоидных рецепторов». Журнал медицинской химии . 40 (5): 695–704. дои : 10.1021/jm960319n . ПМИД 9057856 .
- ^ Юткевич Э.М. (июнь 2006 г.). «Антидепрессантоподобные эффекты агонистов дельта-опиоидных рецепторов». Молекулярные вмешательства . 6 (3): 162–169. дои : 10.1124/ми.6.3.7 . ПМИД 16809477 .
- ^ Анантан С. (март 2006 г.). «Опиоидные лиганды со смешанными взаимодействиями мю/дельта-опиоидных рецепторов: новый подход к новым анальгетикам» . Журнал AAPS . 8 (1): Е118–Е125. дои : 10.1208/aapsj080114 . ПМК 2751430 . ПМИД 16584118 .
- ^ Портогезе П.С., Султана М., Такемори А.Е. (январь 1988 г.). «Налтриндол, высокоселективный и мощный непептидный антагонист дельта-опиоидных рецепторов». Европейский журнал фармакологии . 146 (1): 185–186. дои : 10.1016/0014-2999(88)90502-X . ПМИД 2832195 .
- ^ Ле Бурдоннек Б., Винд Р.Т., Аджелло К.В., Лейстер Л.К., Гу М., Чу Г.Х. и др. (октябрь 2008 г.). «Мощные пероральные биодоступные агонисты дельта-опиоидных рецепторов для лечения боли: открытие N,N-диэтил-4-(5-гидроксиспиро[хромен-2,4'-пиперидин]-4-ил)бензамида (ADL5859)». Журнал медицинской химии . 51 (19): 5893–5896. дои : 10.1021/jm8008986 . ПМИД 18788723 .
- ^ Онали П., Дедони С., Олианас М.С. (январь 2010 г.). «Прямая агонистическая активность трициклических антидепрессантов в отношении различных подтипов опиоидных рецепторов». Журнал фармакологии и экспериментальной терапии . 332 (1): 255–265. дои : 10.1124/jpet.109.159939 . ПМИД 19828880 . S2CID 18893305 .
- ^ Jump up to: а б Катманн М., Флау К., Редмер А., Транкль С., Шликер Э. (февраль 2006 г.). «Каннабидиол является аллостерическим модулятором мю- и дельта-опиоидных рецепторов». Архив фармакологии Наунина-Шмидеберга . 372 (5): 354–361. дои : 10.1007/s00210-006-0033-x . ПМИД 16489449 . S2CID 4877869 .
- ^ Jump up to: а б с Такаяма Х., Исикава Х., Курихара М., Китадзима М., Аими Н., Понглукс Д. и др. (апрель 2002 г.). «Исследования синтеза и опиоидной агонистической активности родственных митрагинину индольных алкалоидов: открытие опиоидных агонистов, структурно отличающихся от других опиоидных лигандов». Журнал медицинской химии . 45 (9): 1949–1956. дои : 10.1021/jm010576e . ПМИД 11960505 .
- ^ Маквей М., Рамзи Д., Келлетт Э., Рис С., Уилсон С., Поуп А.Дж. и др. (апрель 2001 г.). «Мониторинг олигомеризации рецепторов с использованием резонансного переноса энергии флуоресценции с временным разрешением и резонансного переноса энергии биолюминесценции. Человеческий дельта-опиоидный рецептор демонстрирует конститутивную олигомеризацию на поверхности клетки, которая не регулируется занятостью рецептора» . Журнал биологической химии . 276 (17): 14092–14099. дои : 10.1074/jbc.M008902200 . ПМИД 11278447 . S2CID 25191463 .
- ^ Цен Б, Юй Ц, Го Дж, Ву Ю, Лин К, Ченг З и др. (март 2001 г.). «Прямое связывание бета-аррестинов с двумя отдельными внутриклеточными доменами дельта-опиоидного рецептора» . Журнал нейрохимии . 76 (6): 1887–1894. дои : 10.1046/j.1471-4159.2001.00204.x . ПМИД 11259507 . S2CID 83485138 .
- ^ Уистлер Дж.Л., Энквист Дж., Марли А., Фонг Дж., Гладхер Ф., Цуруда П. и др. (июль 2002 г.). «Модуляция постэндоцитарной сортировки рецепторов, связанных с G-белком». Наука . 297 (5581): 615–620. дои : 10.1126/science.1073308 . ПМИД 12142540 . S2CID 1219372 .
Дальнейшее чтение
[ редактировать ]- Нарита М., Фунада М., Сузуки Т. (январь 2001 г.). «Регуляция опиоидной зависимости типами опиоидных рецепторов». Фармакология и терапия . 89 (1): 1–15. дои : 10.1016/S0163-7258(00)00099-1 . ПМИД 11316510 .
- Эванс С.Дж., Кейт Д.Е., Моррисон Х., Магендзо К., Эдвардс Р.Х. (декабрь 1992 г.). «Клонирование дельта-опиоидного рецептора путем функциональной экспрессии». Наука . 258 (5090): 1952–1955. Бибкод : 1992Sci...258.1952E . дои : 10.1126/science.1335167 . ПМИД 1335167 .
- Офферманнс С., Шульц Г., Розенталь В. (февраль 1991 г.). «Доказательства опосредованной опиоидными рецепторами активации G-белков Go и Gi2 в мембранах гибридных клеток нейробластомы и глиомы (NG108-15)» . Журнал биологической химии . 266 (6): 3365–3368. дои : 10.1016/S0021-9258(19)67799-9 . ПМИД 1671672 .
- Симонин Ф., Бефор К., Гаверио-Руфф С., Маттес Х., Наппи В., Ланн Б. и др. (декабрь 1994 г.). «Человеческий дельта-опиоидный рецептор: геномная организация, клонирование кДНК, функциональное выражение и распределение в мозгу человека». Молекулярная фармакология . 46 (6): 1015–1021. ПМИД 7808419 .
- Бефорт К., Маттеи М.Г., Рокель Н., Киффер Б. (март 1994 г.). «Хромосомная локализация гена дельта-опиоидного рецептора в полосах 1p34.3-p36.1 человека и мышиных 4D путем гибридизации in situ». Геномика . 20 (1): 143–145. дои : 10.1006/geno.1994.1146 . ПМИД 8020949 .
- Кнапп Р.Дж., Малатинска Э., Фанг Л., Ли Х, Бабин Э., Нгуен М. и др. (1994). «Идентификация человеческого дельта-опиоидного рецептора: клонирование и экспрессия». Науки о жизни . 54 (25): PL463–PL469. дои : 10.1016/0024-3205(94)90138-4 . ПМИД 8201839 .
- Георгусси З., Карр С., Миллиган Дж. (июль 1993 г.). «Прямые измерения in situ взаимодействий опиоидных рецепторов мозга крысы с гуанин-нуклеотидсвязывающим белком Go». Молекулярная фармакология . 44 (1): 62–69. ПМИД 8393523 .
- Бздега Т., Чин Х., Ким Х., Юнг Х.Х., Козак К.А., Клее В.А. (октябрь 1993 г.). «Региональная экспрессия и хромосомная локализация гена дельта-опиатного рецептора» . Труды Национальной академии наук Соединенных Штатов Америки . 90 (20): 9305–9309. Бибкод : 1993PNAS...90.9305B . дои : 10.1073/pnas.90.20.9305 . ПМК 47556 . ПМИД 8415697 .
- Хо МК, Вонг Й.Х. (июнь 1997 г.). «Функциональная роль аминоконцевого серина 16 и серина 27 G альфаZ в соединении рецепторов и эффекторов» . Журнал нейрохимии . 68 (6): 2514–2522. дои : 10.1046/j.1471-4159.1997.68062514.x . ПМИД 9166747 . S2CID 24703413 .
- Хедин К.Э., Bell MP, Калли КР, Хантун СиДжей, Sharp BM, McKean DJ (декабрь 1997 г.). «Дельта-опиоидные рецепторы, экспрессируемые Т-клетками Jurkat, усиливают секрецию IL-2 за счет увеличения комплексов AP-1 и активности промоторного элемента, связывающего NF-AT/AP-1» . Журнал иммунологии . 159 (11): 5431–5440. дои : 10.4049/jimmunol.159.11.5431 . ПМИД 9548483 .
- Джордан Б.А., Деви Л.А. (июнь 1999 г.). «Гетеродимеризация рецептора, связанного с G-белком, модулирует функцию рецептора» . Природа . 399 (6737): 697–700. Бибкод : 1999Natur.399..697J . дои : 10.1038/21441 . ПМК 3125690 . ПМИД 10385123 .
- Петажа-Репо У.Э., Хог М., Лаперьер А., Уокер П., Бувье М. (май 2000 г.). «Экспорт из эндоплазматического ретикулума представляет собой лимитирующую стадию созревания и экспрессии на клеточной поверхности человеческого дельта-опиоидного рецептора» . Журнал биологической химии . 275 (18): 13727–13736. дои : 10.1074/jbc.275.18.13727 . ПМИД 10788493 . S2CID 8293320 .
- Гелернтер Дж., Кранцлер Х.Р. (июль 2000 г.). «Обнаружение вариантов в локусе дельта-опиоидного рецептора (OPRD1) и популяционная генетика нового варианта, влияющего на последовательность белка». Генетика человека . 107 (1): 86–88. дои : 10.1007/s004390050016 . ПМИД 10982041 .
- Го Дж., Ву Ю., Чжан В., Чжао Дж., Деви Л.А., Пей Г. и др. (ноябрь 2000 г.). «Идентификация сайтов фосфорилирования киназы 2, связанной с G-белком, ответственных за фосфорилирование дельта-опиоидных рецепторов, стимулируемое агонистами». Молекулярная фармакология . 58 (5): 1050–1056. дои : 10.1124/моль.58.5.1050 . ПМИД 11040053 .
- Гомес И., Джордан Б.А., Гупта А., Трапаидзе Н., Надь В., Деви Л.А. (ноябрь 2000 г.). «Гетеродимеризация мю- и дельта-опиоидных рецепторов: роль в опиатной синергии» . Журнал неврологии . 20 (22): RC110. doi : 10.1523/JNEUROSCI.20-22-j0007.2000 . ПМЦ 3125672 . ПМИД 11069979 .
- Сюй В., Чен С., Хуан П., Ли Дж., Де Риель Дж.К., Джавич Дж.А. и др. (ноябрь 2000 г.). «Консервативный остаток цистеина 7.38 по-разному доступен в щелях сайта связывания мю-, дельта- и каппа-опиоидных рецепторов». Биохимия . 39 (45): 13904–13915. дои : 10.1021/bi001099p . ПМИД 11076532 .
- Хартли Дж.Л., Темпл Г.Ф., Браш Массачусетс (ноябрь 2000 г.). «Клонирование ДНК с использованием сайт-специфической рекомбинации in vitro» . Геномные исследования . 10 (11): 1788–1795. дои : 10.1101/гр.143000 . ПМК 310948 . ПМИД 11076863 .
- Саид Р.В., Стефано ГБ, Мурга Дж.Д., Шорт Т.В., Ци Ф, Bilfinger TV и др. (декабрь 2000 г.). «Экспрессия функциональных дельта-опиоидных рецепторов в гладких мышцах сосудов». Международный журнал молекулярной медицины . 6 (6): 673–677. дои : 10.3892/ijmm.6.6.673 . ПМИД 11078827 .
- Сян Б., Ю Г.Х., Го Дж., Чен Л., Ху В., Пей Г. и др. (февраль 2001 г.). «Гетерологичная активация протеинкиназы C стимулирует фосфорилирование дельта-опиоидного рецептора по серину 344, что приводит к интернализации рецептора, опосредованной бета-аррестином и клатрином» . Журнал биологической химии . 276 (7): 4709–4716. дои : 10.1074/jbc.M006187200 . ПМИД 11085981 . S2CID 84945988 .
- Йео А., Сэмвейс Д.С., Фаулер С.Э., Ганн-Мур Ф., Хендерсон Дж. (март 2001 г.). «Совпадающая передача сигналов между Gi/Go-связанным дельта-опиоидным рецептором и Gq-связанным мускариновым рецептором m3 на уровне внутриклеточного свободного кальция в клетках SH-SY5Y». Журнал нейрохимии . 76 (6): 1688–1700. дои : 10.1046/j.1471-4159.2001.00185.x . ПМИД 11259487 . S2CID 2755275 .
Внешние ссылки
[ редактировать ]- «Опиоидные рецепторы: δ» . База данных IUPHAR по рецепторам и ионным каналам . Международный союз фундаментальной и клинической фармакологии. Архивировано из оригинала 23 февраля 2014 г. Проверено 23 июля 2007 г.
- дельта + опиоид + рецептор в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)