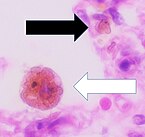
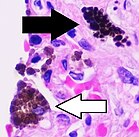
Макрофаг
| Макрофаг | |
|---|---|
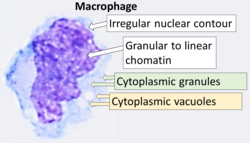 Цитология макрофагов с типичными особенностями. Пятно Райта . | |
| Подробности | |
| Произношение | /ˈmakrə(ʊ)feɪdʒ/ |
| Система | Иммунная система |
| Функция | Фагоцитоз |
| Идентификаторы | |
| латинский | макрофагоцит |
| Акроним(ы) | М φ , МΦ |
| МеШ | D008264 |
| ТД | Х2.00.03.0.01007 |
| ФМА | 63261 |
| Анатомические термины микроанатомии | |
Макрофаги (сокращенно Mφ « , MΦ или MP ) ( греч . большие едоки» , от греческого μακρός ( makrós ) = большой, φαγεῖν ( фагин ) = есть) — тип лейкоцитов врожденной иммунной системы , которые поглощают и переваривают патогены, такие как раковые клетки , микробы , клеточный мусор и инородные вещества, на поверхности которых нет белков, специфичных для здоровых клеток организма. [1] [2] Этот процесс называется фагоцитозом , который защищает хозяина от инфекции и травм. [3]
Макрофаги обнаруживаются практически во всех тканях. [4] где они патрулируют потенциальные патогены посредством амебоидного движения . Они принимают различные формы (с разными названиями) по всему организму (например, гистиоциты , клетки Купфера , альвеолярные макрофаги , микроглия и др.), но все они являются частью системы мононуклеарных фагоцитов . Помимо фагоцитоза, они играют решающую роль в неспецифической защите ( врожденный иммунитет ), а также помогают инициировать специфические защитные механизмы ( адаптивный иммунитет ), привлекая другие иммунные клетки, такие как лимфоциты . Например, они важны как презентаторы антигена для Т-клеток . У людей дисфункциональные макрофаги вызывают тяжелые заболевания, такие как хроническая гранулематозная болезнь , которая приводит к частым инфекциям.
Помимо усиления воспаления и стимуляции иммунной системы, макрофаги также играют важную противовоспалительную роль и могут снижать иммунные реакции за счет высвобождения цитокинов . Макрофаги, которые способствуют воспалению, называются макрофагами М1, тогда как те, которые уменьшают воспаление и способствуют восстановлению тканей, называются макрофагами М2. [5] Эта разница отражается на их метаболизме; Макрофаги М1 обладают уникальной способностью метаболизировать аргинин до «киллерной» молекулы оксида азота , тогда как макрофаги М2 обладают уникальной способностью метаболизировать аргинин до «восстанавливающей» молекулы орнитина . [6] Однако эта дихотомия недавно была поставлена под сомнение, поскольку была обнаружена дополнительная сложность. [7]
Макрофаги человека имеют диаметр около 21 микрометра (0,00083 дюйма). [8] и производятся путем дифференцировки моноцитов в тканях. Их можно идентифицировать с помощью проточной цитометрии или иммуногистохимического окрашивания по специфической экспрессии белков, таких как CD14 , CD40 , CD11b , CD64 , F4/80 (мыши)/ EMR1 (человек), лизоцим M, MAC-1 /MAC-3 и CD68. . [9]
Макрофаги были впервые обнаружены и названы Эли Мечниковым в 1884 году. зоологом Российской империи [10] [11]
Структура [ править ]
Типы [ править ]
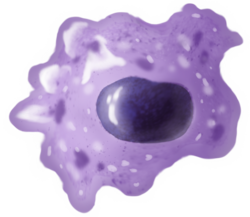
Большинство макрофагов расположены в стратегических точках, где может произойти микробная инвазия или скопление инородных частиц. Эти клетки вместе образуют группу, которая известна как система мононуклеарных фагоцитов , а ранее была известна как ретикулоэндотелиальная система. Каждый тип макрофагов, определяемый его местоположением, имеет определенное название:
| Имя ячейки | Анатомическое расположение |
| Макрофаги жировой ткани | Жировая ткань (жир) |
| Моноциты | Костный мозг / кровь |
| Купферовы клетки | Печень |
| Синусовые гистиоциты | Лимфатические узлы |
| Альвеолярные макрофаги (пылевые клетки) | Легочные альвеолы |
| Тканевые макрофаги (гистиоциты), ведущие к гигантским клеткам. | Соединительная ткань |
| Микроглия | Центральная нервная система |
| Клетки Хофбауэра | Плацента |
| Внутриклубочковые мезангиальные клетки [12] | Почка |
| Остеокласты [13] | Кость |
| клетки Лангерганса | Кожа |
| Эпителиоидные клетки | Гранулемы |
| Макрофаги красной пульпы ( клетки синусоидальной выстилки) | Красная пульпа селезенки |
| Перитонеальные макрофаги | Брюшная полость |
| периваскулярные макрофаги [14] | тесно связан с кровеносными сосудами |
Исследования, касающиеся клеток Купфера, затруднены, поскольку у людей клетки Купфера доступны только для иммуногистохимического анализа из биопсии или аутопсии. От крыс и мышей их трудно выделить, и после очистки от одной мыши можно получить лишь примерно 5 миллионов клеток.
Макрофаги могут выполнять паракринные функции внутри органов, специфичные для функции этого органа. Например, было показано, что в семенниках макрофаги способны взаимодействовать с клетками Лейдига , секретируя 25-гидроксихолестерин , оксистерин , который может превращаться в тестостерон соседними клетками Лейдига. [15] Кроме того, тестикулярные макрофаги могут участвовать в создании иммунно-привилегированной среды в яичках и опосредовать бесплодие во время воспаления яичка.
Кардиальные резидентные макрофаги участвуют в электропроводности посредством через щелевые контакты связи с сердечными миоцитами . [16]
Макрофаги можно классифицировать на основе основной функции и активации. Согласно этой группе, различают классически активированные (М1) макрофаги , ранозаживляющие макрофаги (также известные как альтернативно активированные (М2) макрофаги ) и регуляторные макрофаги (Mregs). [17]
Развитие [ править ]
Макрофаги, которые находятся в здоровых тканях взрослого человека, либо происходят из циркулирующих моноцитов, либо формируются до рождения и затем сохраняются в течение взрослой жизни независимо от моноцитов. [18] [19] Напротив, большая часть макрофагов, которые накапливаются в пораженных участках, обычно происходят из циркулирующих моноцитов. [20] Экстравазация лейкоцитов описывает проникновение моноцитов в поврежденную ткань через эндотелий кровеносных сосудов , когда они становятся макрофагами. Моноциты привлекаются к поврежденному участку химическими веществами посредством хемотаксиса , вызываемого рядом стимулов, включая поврежденные клетки, патогены и цитокины, высвобождаемые макрофагами, уже находящимися в этом месте. Было показано, что в некоторых местах, таких как семенники, макрофаги заселяют орган посредством пролиферации. [21] В отличие от короткоживущих нейтрофилов , макрофаги дольше выживают в организме, до нескольких месяцев.
Функция [ править ]
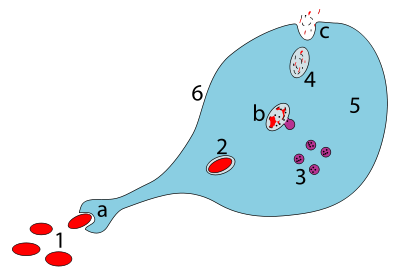
а. При попадании в организм путем фагоцитоза образуется фагосома.
б. Слияние лизосом с фагосомой создает фаголизосому ; возбудитель расщепляется ферментами
в. Отходы удаляются или ассимилируются (последний не показан)
Части:
1. Патогены
2. Фагосома
3. Лизосомы
4. Отходы
5. Цитоплазма
6. Клеточная мембрана
Фагоцитоз [ править ]
Макрофаги являются профессиональными фагоцитами и узкоспециализированы в удалении отмирающих или мертвых клеток и клеточного мусора. Эта роль важна при хроническом воспалении, поскольку на ранних стадиях воспаления преобладают нейтрофилы, которые по мере достижения совершеннолетия поглощаются макрофагами ( см. в CD31 ). описание этого процесса [22]
Нейтрофилы сначала привлекаются к участку, где они выполняют свою функцию, и погибают, прежде чем они или их нейтрофильные внеклеточные ловушки будут фагоцитированы макрофагами. [22] [23] Находясь в этом месте, первая волна нейтрофилов после процесса старения и через первые 48 часов стимулирует появление макрофагов, в результате чего эти макрофаги затем поглощают старые нейтрофилы. [22]
Удалением отмирающих клеток в большей степени занимаются фиксированные макрофаги , которые остаются в стратегически важных местах, таких как легкие, печень, нервная ткань , кости, селезенка и соединительная ткань, поглощая инородные материалы, такие как патогены, и привлекая дополнительные макрофаги. если необходимо. [24]
Когда макрофаг поглощает патоген, он попадает в фагосому , которая затем сливается с лизосомой . Внутри фаголизосомы ферменты и токсичные пероксиды переваривают возбудитель. Однако некоторые бактерии, такие как Mycobacterium Tuberculosis , стали устойчивыми к этим методам пищеварения. Тифоидные сальмонеллы индуцируют собственный фагоцитоз макрофагами хозяина in vivo и ингибируют пищеварение лизосомальным действием, тем самым используя макрофаги для собственной репликации и вызывая апоптоз макрофагов. [25] Макрофаги могут переварить более 100 бактерий, прежде чем они окончательно погибнут из-за собственных пищеварительных соединений.
Роль во врожденном ответе иммунном
Когда патоген проникает, резидентные в тканях макрофаги оказываются одними из первых клеток, которые реагируют. [26] Две основные роли тканевых макрофагов заключаются в фагоцитозе входящего антигена и секреции провоспалительных цитокинов, которые вызывают воспаление и привлекают в этот участок другие иммунные клетки. [27]
Фагоцитоз возбудителей [ править ]

Макрофаги могут усваивать антигены посредством рецептор-опосредованного фагоцитоза. [28] Макрофаги имеют широкий спектр рецепторов распознавания образов (PRR), которые могут распознавать молекулярные паттерны, связанные с микробами (MAMP) патогенов. Многие PRR, такие как toll-подобные рецепторы (TLR), рецепторы-мусорщики (SR), лектиновые рецепторы C-типа и другие, распознают патогены для фагоцитоза. [28] Макрофаги также могут распознавать патогены для фагоцитоза косвенно через опсонины , которые представляют собой молекулы, которые прикрепляются к патогенам и маркируют их для фагоцитоза. [29] Опсонины могут вызывать более сильную адгезию между макрофагами и патогеном во время фагоцитоза, следовательно, опсонины имеют тенденцию усиливать фагоцитарную активность макрофагов. [30] Как белки комплемента , так и антитела могут связываться с антигенами и опсонизировать их. Макрофаги имеют рецепторы комплемента 1 (CR1) и 3 (CR3), которые распознают связанные с патогеном белки комплемента C3b и iC3b соответственно, а также фрагментированные γ-рецепторы (FcγR), которые распознают кристаллизующийся фрагмент (Fc) область антигенсвязанного иммуноглобулина. G (IgG) антитела. [29] [31] При фагоцитозе и переваривании патогенов макрофаги подвергаются дыхательному взрыву , при котором потребляется больше кислорода для обеспечения энергией, необходимой для производства активных форм кислорода (АФК) и других антимикробных молекул, которые переваривают израсходованные патогены. [27] [32]
Секреция цитокинов [ править ]
Распознавание MAMP с помощью PRR может активировать резидентные в тканях макрофаги для секреции провоспалительных цитокинов, которые рекрутируют другие иммунные клетки. Среди PRRs TLRs играют важную роль в передаче сигналов, приводящих к продукции цитокинов. [28] Связывание MAMP с TLR запускает серию последующих событий, которые в конечном итоге активируют транскрипционный фактор NF-κB и приводят к транскрипции генов нескольких провоспалительных цитокинов, включая IL-1β , IL-6 , TNF-α , IL-12B и интерфероны типа I, такие как IFN-α и IFN-β. [33] Системно IL-1β, IL-6 и TNF-α вызывают лихорадку и инициируют ответ острой фазы, при котором печень секретирует белки острой фазы . [26] [27] [34] Локально IL-1β и TNF-α вызывают расширение сосудов, при котором промежутки между эпителиальными клетками кровеносных сосудов расширяются, и активацию молекул клеточной поверхностной адгезии на эпителиальных клетках, вызывая экстравазацию лейкоцитов . [26] [27]
Нейтрофилы являются одними из первых иммунных клеток, рекрутируемых макрофагами для выхода из крови путем экстравазации и прибытия в очаг инфекции. [34] Макрофаги секретируют множество хемокинов, таких как CXCL1 , CXCL2 и CXCL8 (IL-8), которые привлекают нейтрофилы к месту инфекции. [26] [34] После того, как нейтрофилы завершили фагоцитоз и очистку антигена в конце иммунного ответа, они подвергаются апоптозу, и макрофаги рекрутируются из моноцитов крови, чтобы помочь очистить апоптозный мусор. [35]
Макрофаги также рекрутируют другие иммунные клетки, такие как моноциты, дендритные клетки, естественные клетки-киллеры, базофилы, эозинофилы и Т-клетки, посредством хемокинов, таких как CCL2 , CCL4 , CCL5 , CXCL8 , CXCL9 , CXCL10 и CXCL11 . [26] [34] Наряду с дендритными клетками макрофаги помогают активировать естественные клетки-киллеры (NK) посредством секреции интерферонов I типа (IFN-α и IFN-β) и IL-12 . IL-12 действует совместно с IL-18, стимулируя выработку NK-клетками провоспалительного цитокина интерферона гамма (IFN-γ), который служит важным источником IFN-γ до активации адаптивной иммунной системы. [34] [36] IFN-γ усиливает врожденный иммунный ответ, индуцируя более агрессивный фенотип макрофагов, что позволяет макрофагам более эффективно убивать патогены. [34]
Некоторые из хемоаттрактантов Т-клеток, секретируемых макрофагами, включают CCL5 , CXCL9 , CXCL10 и CXCL11 . [26]
в адаптивном иммунитете Роль

Взаимодействие с CD4 + клетки хелперные - Т
Макрофаги являются профессиональными антигенпрезентирующими клетками (APC), что означает, что они могут представлять пептиды из фагоцитированных антигенов на молекулах главного комплекса гистосовместимости (MHC) II на своей клеточной поверхности для Т-хелперных клеток. [38] Макрофаги не являются первичными активаторами наивных Т-хелперов, которые никогда ранее не активировались, поскольку тканевые макрофаги не перемещаются в лимфатические узлы, где находятся наивные Т-хелперы. [39] [40] Хотя макрофаги также обнаруживаются во вторичных лимфоидных органах, таких как лимфатические узлы, они не находятся в зонах Т-клеток и не эффективны для активации наивных Т-хелперных клеток. [39] Макрофаги в лимфоидных тканях более активно участвуют в поглощении антигенов и предотвращении их попадания в кровь, а также в поглощении остатков апоптотических лимфоцитов. [39] [41] Таким образом, макрофаги взаимодействуют преимущественно с ранее активированными Т-хелперными клетками, покинувшими лимфатический узел и прибывшими в место инфекции, или с резидентными в тканях Т-клетками памяти. [40]
Макрофаги поставляют оба сигнала, необходимые для активации Т-хелперных клеток: 1) макрофаги представляют связанную с антигенным пептидом молекулу MHC класса II, которая распознается соответствующим рецептором Т-клеток (TCR), и 2) распознавание патогенов с помощью PRR побуждает макрофаги активировать коагуляцию. -стимулирующие молекулы CD80 и CD86 (также известные как B7 ), которые связываются с CD28 на Т-хелперных клетках для подачи костимулирующего сигнала. [34] [38] Эти взаимодействия позволяют Т-хелперным клеткам достигать полной эффекторной функции и обеспечивают Т-хелперным клеткам сигналы продолжения выживания и дифференцировки, предотвращая их апоптоз из-за отсутствия передачи сигналов TCR. [38] Например, передача сигналов IL-2 в Т-клетках усиливает экспрессию антиапоптотического белка Bcl-2 , но продукция IL-2 Т-клетками и высокоаффинный рецептор IL-2 IL-2RA требуют постоянного сигнала от распознавания TCR MHC-связанный антиген. [34] [42]
Активация [ править ]
Макрофаги могут достигать разных фенотипов активации посредством взаимодействия с различными подмножествами Т-хелперных клеток, такими как TH 1 и TH 2 . [17] Хотя существует широкий спектр фенотипов активации макрофагов, существует два основных общепризнанных фенотипа. [17] Это классически активированные макрофаги, или макрофаги М1, и альтернативно активированные макрофаги, или макрофаги М2. Макрофаги М1 обладают провоспалительным действием, тогда как макрофаги М2 в основном обладают противовоспалительным действием. [17]
Классический [ править ]
Клетки TH против внутриклеточных патогенов 1 играют важную роль в классической активации макрофагов как часть иммунного ответа типа 1 (таких как внутриклеточные бактерии ), которые могут выживать и реплицироваться внутри клеток-хозяев, особенно тех патогенов, которые реплицируются даже после фагоцитоза макрофагами. [43] После того, как TCR клеток TH 1 распознает специфические молекулы MHC класса II, связанные с антигенным пептидом, на макрофагах, клетки TH 1 1) секретируют IFN-γ и 2) повышают экспрессию лиганда CD40 (CD40L), который связывается с CD40 на макрофагах. . [44] [34] Эти два сигнала активируют макрофаги и повышают их способность убивать внутриклеточные патогены за счет увеличения производства антимикробных молекул, таких как оксид азота (NO) и супероксид (O). 2- ). [26] [34] Это усиление антимикробной способности макрофагов клетками TH 1 известно как классическая активация макрофагов, а активированные макрофаги известны как классически активированные макрофаги или макрофаги M1. Макрофаги M1, в свою очередь, активируют молекулы B7 и презентацию антигена через молекулы MHC класса II, обеспечивая сигналы, поддерживающие помощь Т-клеток. [44] Активация макрофагов TH 1 и M1 представляет собой петлю положительной обратной связи, при этом IFN-γ из клеток TH 1 усиливает экспрессию CD40 на макрофагах; взаимодействие между CD40 на макрофагах и CD40L на Т-клетках активирует макрофаги для секреции IL-12; и IL-12 способствует большей секреции IFN-γ клетками T H 1. [34] [44] Первоначальный контакт между MHC II, связанным с макрофаговым антигеном, и TCR служит точкой контакта между двумя клетками, где концентрируется большая часть секреции IFN-γ и CD-40L на Т-клетках, поэтому только макрофаги, непосредственно взаимодействующие с T H клетками 1, концентрируются. скорее всего будет активирован. [34]
Помимо активации макрофагов M1, лиганд клетки TH 1 экспрессируют Fas (FasL) и бета-лимфотоксин (LT-β), помогая уничтожать хронически инфицированные макрофаги, которые больше не могут убивать патогены. [34] Уничтожение хронически инфицированных макрофагов приводит к высвобождению патогенов во внеклеточное пространство, которые затем могут быть уничтожены другими активированными макрофагами. [34] Клетки TH 1 также помогают привлечь больше моноцитов, предшественников макрофагов, в очаг инфекции. TH чтобы 1 секретирует TNF-α и LT-α, облегчить моноцитам связывание и выход из кровеносных сосудов. [34] T H Секреция 1 CCL2 как хемоаттрактанта для моноцитов. IL-3 и GM-CSF, высвобождаемые клетками T H 1, стимулируют выработку большего количества моноцитов в костном мозге. [34]
Когда внутриклеточные патогены не могут быть устранены, например, в случае микобактерий туберкулеза , патоген сдерживается посредством образования гранулемы — скопления инфицированных макрофагов, окруженных активированными Т-клетками. [45] Макрофаги, граничащие с активированными лимфоцитами, часто сливаются, образуя многоядерные гигантские клетки, которые, по-видимому, обладают повышенной антимикробной способностью из-за их близости к клеткам TH 1 , но со временем клетки в центре начинают умирать и образовывать некротическую ткань. [40] [45]
Альтернатива [ править ]
Клетки T H 2 играют важную роль в альтернативной активации макрофагов как часть иммунного ответа 2 типа против крупных внеклеточных патогенов, таких как гельминты . [34] [46] Клетки TH 2 секретируют IL-4 и IL-13, которые активируют макрофаги , превращая их в макрофаги М2, также известные как альтернативно активированные макрофаги. [46] [47] Макрофаги М2 экспрессируют аргиназу-1 , фермент, который превращает аргинин в орнитин и мочевину . [46] Орнитин помогает увеличить сокращение гладких мышц для изгнания червя, а также участвует в заживлении тканей и ран. Орнитин может далее метаболизироваться до пролина , который необходим для синтеза коллагена . [46] Макрофаги М2 также могут уменьшать воспаление, продуцируя антагонист рецептора IL-1 (IL-1RA) и рецепторы IL-1, которые не приводят к последующей воспалительной передаче сигналов (IL-1RII). [34] [48]
Взаимодействие с CD8 + цитотоксические Т-клетки [ править ]
Другая часть активации адаптивного иммунитета включает стимуляцию CD8. + путем перекрестной презентации антигенных пептидов на молекулах MHC класса I. Исследования показали, что провоспалительные макрофаги способны к перекрестной презентации антигенов на молекулах MHC класса I, но играет ли роль перекрестная презентация макрофагов в наивном или запоминающемся CD8? + Активация Т-клеток до сих пор неясна. [27] [49] [41]
Взаимодействие с B-клетками [ править ]
Было показано, что макрофаги секретируют цитокины BAFF и APRIL, которые важны для переключения изотипа плазматических клеток. APRIL и IL-6, секретируемые предшественниками макрофагов в костном мозге, помогают поддерживать выживаемость плазматических клеток, находящихся в костном мозге. [50]
Подтипы [ править ]
Существует несколько активированных форм макрофагов. [17] Несмотря на спектр способов активации макрофагов, существуют две основные группы, обозначенные М1 и М2 . Макрофаги M1: как упоминалось ранее (ранее называемые классически активированными макрофагами), [52] Макрофаги-киллеры М1 активируются ЛПС и ИФН-гамма и секретируют высокие уровни IL-12 и низкие уровни IL-10 . Макрофаги М1 выполняют провоспалительную, бактерицидную и фагоцитарную функции. [53] Напротив, обозначение «восстановления» M2 (также называемое альтернативно активированными макрофагами) в широком смысле относится к макрофагам, которые участвуют в конструктивных процессах, таких как заживление ран и восстановление тканей, а также к макрофагам, которые отключают повреждающую активацию иммунной системы, продуцируя противовоспалительные цитокины, такие как Ил-10 . М2 представляет собой фенотип резидентных тканевых макрофагов, уровень которого может дополнительно повышаться под действием IL-4 . Макрофаги М2 продуцируют высокие уровни IL-10, TGF-бета и низкие уровни IL-12. Опухолеассоциированные макрофаги в основном относятся к фенотипу М2 и, по-видимому, активно способствуют росту опухоли. [54]
Макрофаги существуют в различных фенотипах, которые определяются ролью, которую они играют в созревании ран. Фенотипы можно преимущественно разделить на две основные категории; М1 и М2. Макрофаги M1 представляют собой доминирующий фенотип, наблюдаемый на ранних стадиях воспаления, и активируются четырьмя ключевыми медиаторами: интерфероном-γ (IFN-γ), фактором некроза опухоли (TNF) и молекулярными структурами, связанными с повреждением (DAMP). Эти молекулы-медиаторы создают провоспалительную реакцию, которая в свою очередь производит провоспалительные цитокины, такие как интерлейкин-6 и TNF. В отличие от макрофагов М1, макрофаги М2 секретируют противовоспалительный ответ за счет добавления интерлейкина-4 или интерлейкина-13. Они также играют роль в заживлении ран и необходимы для реваскуляризации и реэпителизации. Макрофаги M2 делятся на четыре основных типа в зависимости от их роли: M2a, M2b, M2c и M2d. То, как определяются фенотипы M2, все еще остается предметом обсуждения, но исследования показали, что окружающая среда позволяет им приспосабливаться к тому фенотипу, который наиболее подходит для эффективного заживления раны. [53]
Макрофаги М2 необходимы для стабильности сосудов. Они продуцируют фактор роста эндотелия сосудов-А и TGF-β1 . [53] При острых ранах наблюдается сдвиг фенотипа от макрофагов М1 к макрофагам М2, однако этот сдвиг нарушается при хронических ранах. Эта дисрегуляция приводит к недостаточному количеству макрофагов М2 и соответствующих им факторов роста, которые способствуют заживлению ран. При недостатке этих факторов роста/противовоспалительных цитокинов и избытке провоспалительных цитокинов макрофагов М1 хронические раны не могут заживать своевременно. Обычно после того, как нейтрофилы поедают остатки/патогены, они выполняют апоптоз и удаляются. На этом этапе воспаление не требуется, и М1 переключается на М2 (противовоспалительный). Однако нарушение регуляции происходит, поскольку макрофаги M1 неспособны/не фагоцитируют нейтрофилы, подвергшиеся апоптозу, что приводит к усилению миграции макрофагов и воспалению. [53]
Макрофаги М1 и М2 играют роль в развитии атеросклероза . Макрофаги М1 способствуют развитию атеросклероза путем воспаления. Макрофаги М2 могут удалять холестерин из кровеносных сосудов, но когда холестерин окисляется, макрофаги М2 становятся апоптозными пенистыми клетками, способствующими образованию атероматозных бляшек при атеросклерозе. [55] [56]
Роль в регенерации мышц [ править ]
Первый шаг к пониманию важности макрофагов в восстановлении, росте и регенерации мышц заключается в том, что существуют две «волны» макрофагов с началом использования повреждаемых мышц — субпопуляции, которые оказывают или не оказывают непосредственное влияние на восстановление мышц. Начальная волна представляет собой популяцию фагоцитов, которая появляется в периоды повышенного использования мышц, достаточных для того, чтобы вызвать лизис мышечной мембраны и воспаление мембраны, которые могут проникнуть в поврежденные мышечные волокна и разрушить их. [57] [58] [59] Эти ранние фагоцитирующие макрофаги достигают своей максимальной концентрации примерно через 24 часа после начала той или иной формы повреждения мышечных клеток или перезагрузки. [60] Их концентрация быстро снижается через 48 часов. [58] Вторая группа — нефагоцитарные типы, располагающиеся вблизи регенеративных волокон. Они достигают пика между двумя и четырьмя днями и остаются повышенными в течение нескольких дней, пока мышечная ткань восстанавливается. [58] Первая субпопуляция не имеет прямой пользы для восстановления мышц, тогда как вторая нефагоцитарная группа имеет.
Считается, что макрофаги выделяют растворимые вещества, которые влияют на пролиферацию, дифференцировку, рост, восстановление и регенерацию мышц, но в настоящее время фактор, который вырабатывает эти эффекты, неизвестен. [60] Известно, что участие макрофагов в восстановлении тканей не является специфичным для мышц; они накапливаются во многих тканях на этапе заживления после травмы. [61]
Роль в заживлении ран [ править ]
Макрофаги необходимы для заживления ран . [62] Они заменяют полиморфно-ядерные нейтрофилы в качестве преобладающих клеток в ране ко второму дню после травмы. [63] Привлеченные к месту раны факторами роста, выделяемыми тромбоцитами и другими клетками, моноциты из кровотока попадают в эту область через стенки кровеносных сосудов. [64] Пик количества моноцитов в ране приходится на один-полтора дня после травмы. Попадая на место раны, моноциты созревают в макрофаги. Селезенка . содержит половину моноцитов организма в резерве, готовых к использованию в поврежденных тканях [65] [66]
Основная роль макрофагов заключается в фагоцитировании бактерий и поврежденных тканей. [62] и они также очищают поврежденную ткань, высвобождая протеазы. [67] Макрофаги также секретируют ряд факторов, таких как факторы роста и другие цитокины, особенно в течение третьих и четвертых дней после ранения. Эти факторы привлекают в эту область клетки, участвующие в стадии пролиферации и заживления. [68] Макрофаги также могут сдерживать фазу сокращения. [69] Макрофаги стимулируются низким содержанием кислорода в окружающей среде и вырабатывают факторы, которые индуцируют и ускоряют ангиогенез. [70] а также они стимулируют клетки, которые реэпителизируют рану, создают грануляционную ткань и образуют новый внеклеточный матрикс . [71] [ нужен лучший источник ] Секретируя эти факторы, макрофаги способствуют переходу процесса заживления ран на следующую фазу.
в регенерации конечностей Роль
Ученые выяснили, что макрофаги не только поедают материальные остатки, но и участвуют в типичной регенерации конечностей саламандры. [72] [73] Они обнаружили, что удаление макрофагов из саламандры привело к нарушению регенерации конечностей и образованию рубцов. [72] [73]
в железа Роль гомеостазе
Как описано выше, макрофаги играют ключевую роль в удалении отмирающих или мертвых клеток и клеточного мусора. Эритроциты живут в среднем 120 дней и поэтому постоянно разрушаются макрофагами селезенки и печени. Макрофаги также поглощают макромолекулы и поэтому играют ключевую роль в фармакокинетике парентеральных препаратов железа . [ нужна ссылка ]
Железо, которое высвобождается из гемоглобина, либо хранится внутри в ферритине , либо высвобождается в кровообращение через ферропортин . В случаях, когда системный уровень железа повышен или присутствует воспаление, повышенные уровни гепсидина действуют на ферропортиновые каналы макрофагов, что приводит к тому, что железо остается внутри макрофагов. [ нужна ссылка ]
Роль сохранении в пигмента

Меланофаги представляют собой подмножество тканерезидентных макрофагов, способных поглощать пигмент, как собственный для организма, так и экзогенный (например, татуировки ) из внеклеточного пространства. В отличие от дендритных соединительных меланоцитов , синтезирующих меланосомы и содержащих различные стадии их развития, меланофаги накапливают только фагоцитированный меланин в лизосомоподобных фагосомах. [74] [75] Это происходит неоднократно, поскольку пигмент мертвых дермальных макрофагов фагоцитируется их преемниками, сохраняя татуировку на том же месте. [76]
гомеостазе тканевом Роль в
Каждая ткань содержит свою собственную специализированную популяцию резидентных макрофагов, которые поддерживают взаимные связи со стромой и функциональной тканью. [77] [78] Эти резидентные макрофаги являются сидячими (немигрирующими), обеспечивают важные факторы роста для поддержания физиологической функции ткани (например, перекрестные помехи макрофагов и нейронов в кишечнике). [79] и может активно защищать ткани от воспалительного повреждения. [80]
- ассоциированные Нервно макрофаги
Связанные с нервами макрофаги или NAM — это тканерезидентные макрофаги, которые связаны с нервами. Известно, что некоторые из них имеют удлиненную морфологию размером до 200 мкм. [81]
Клиническое значение
Благодаря своей роли в фагоцитозе макрофаги участвуют во многих заболеваниях иммунной системы. Например, они участвуют в образовании гранулем — воспалительных поражений, которые могут быть вызваны большим количеством заболеваний. Описаны, например, некоторые нарушения, преимущественно редкие, неэффективного фагоцитоза и функции макрофагов. [82]
хозяин внутриклеточных патогенов Как
Макрофаги, играя роль фагоцитирующих иммунных клеток, отвечают за поглощение патогенов и их уничтожение. Некоторые патогены нарушают этот процесс и вместо этого живут внутри макрофагов. Это обеспечивает среду, в которой возбудитель скрыт от иммунной системы и позволяет ему размножаться. [ нужна ссылка ]
К заболеваниям с таким типом поведения относятся туберкулез (вызванный Mycobacterium Tuberculosis ) и лейшманиоз (вызванный видами Leishmania ). [ нужна ссылка ]
Чтобы свести к минимуму возможность стать хозяином внутриклеточных бактерий, макрофаги развили защитные механизмы, такие как индукция оксида азота и промежуточных продуктов активного кислорода. [83] которые токсичны для микробов. Макрофаги также развили способность ограничивать снабжение микробов питательными веществами и вызывать аутофагию . [84]
Туберкулез [ править ]
Попадая в макрофаг, возбудитель туберкулеза, микобактерия туберкулеза , [85] избегает клеточной защиты и использует клетку для репликации. Недавние данные свидетельствуют о том, что в ответ на легочную инфекцию Mycobacterium Tuberculosis периферические макрофаги созревают до фенотипа M1. Фенотип макрофага М1 характеризуется повышенной секрецией провоспалительных цитокинов (IL-1β, TNF-α и IL-6) и повышенной гликолитической активностью, необходимой для устранения инфекции. [1]
Лейшманиоз [ править ]
При фагоцитозе макрофага паразит Leishmania попадает в фагоцитарную вакуоль. В нормальных условиях эта фагоцитарная вакуоль разовьется в лизосому, и ее содержимое переварится. Лейшмания изменяет этот процесс и избегает уничтожения; вместо этого они устраивают дом внутри вакуоли. [ нужна ссылка ]
Чикунгунья [ править ]
Инфицирование макрофагов суставов связано с местным воспалением во время и после острой фазы чикунгуньи (вызванной CHIKV или вирусом чикунгунья). [86]
Другие [ править ]
Аденовирус (наиболее частая причина конъюнктивита) может оставаться в латентном состоянии в макрофагах хозяина с продолжающимся выделением вируса в течение 6–18 месяцев после первоначального заражения. [ нужна ссылка ]
Бруцеллы виды. может оставаться латентным в макрофаге за счет ингибирования фагосом с лизосомами ; слияния вызывает бруцеллез (волнистую лихорадку). [ нужна ссылка ]
Legionella pneumophila , возбудитель болезни легионеров , также поселяется в макрофагах. [ нужна ссылка ]
Болезнь сердца [ править ]
Макрофаги являются преобладающими клетками, участвующими в создании прогрессирующих бляшечных поражений при атеросклерозе . [87]
Очаговое рекрутирование макрофагов происходит после начала острого инфаркта миокарда . Эти макрофаги выполняют функцию удаления остатков, апоптотических клеток и подготовки тканей к регенерации . [88] Макрофаги защищают от желудочковой тахикардии, вызванной ишемией, у мышей с гипокалиемией. [89]
ВИЧ-инфекция [ править ]
Макрофаги также играют роль в инфекции вируса иммунодефицита человека (ВИЧ). Как и Т-клетки , макрофаги могут быть инфицированы ВИЧ и даже стать резервуаром продолжающейся репликации вируса по всему организму. ВИЧ может проникнуть в макрофаги посредством связывания gp120 с CD4 и вторым мембранным рецептором CCR5 (хемокиновым рецептором). Резервуаром вируса служат как циркулирующие моноциты, так и макрофаги. [90] Макрофаги лучше противостоят заражению ВИЧ-1, чем CD4+ Т-клетки, хотя восприимчивость к ВИЧ-инфекции различается в зависимости от подтипа макрофагов. [91]
Рак [ править ]
Макрофаги могут способствовать росту и прогрессированию опухоли, способствуя пролиферации и инвазии опухолевых клеток, способствуя ангиогенезу опухоли и подавляя противоопухолевые иммунные клетки. [92] [93] Воспалительные соединения, такие как фактор некроза опухоли (TNF)-альфа, высвобождаемые макрофагами, активируют ядерный фактор-переключатель гена-каппа B. Затем NF-κB проникает в ядро опухолевой клетки и запускает выработку белков, которые останавливают апоптоз и способствуют пролиферации клеток и воспалению. [94] Кроме того, макрофаги служат источником многих проангиогенных факторов, включая фактор эндотелия сосудов (VEGF), фактор некроза опухоли-альфа (TNF-альфа), колониестимулирующий фактор макрофагов (M-CSF/CSF1), а также IL-1 и IL. -6 , [95] способствуя дальнейшему росту опухоли.
Было показано, что макрофаги проникают в ряд опухолей. Их количество коррелирует с плохим прогнозом при некоторых видах рака, включая рак молочной железы, шейки матки, мочевого пузыря, головного мозга и простаты. [96] [97] Некоторые опухоли также могут продуцировать факторы, в том числе M-CSF/CSF1, MCP-1/CCL2 и ангиотензин II , которые запускают амплификацию и мобилизацию макрофагов в опухолях. [98] [99] [100] Кроме того, макрофаги субкапсулярного синуса в дренирующих опухоль лимфатических узлах могут подавлять прогрессирование рака, сдерживая распространение опухолевых материалов. [101]
рака Терапия
Экспериментальные исследования показывают, что макрофаги могут влиять на все терапевтические методы, включая хирургическое вмешательство , химиотерапию , лучевую терапию , иммунотерапию и таргетную терапию . [93] [102] [103] Макрофаги могут влиять на результаты лечения как положительно, так и отрицательно. Макрофаги могут защищать по-разному: они могут удалять мертвые опухолевые клетки (в процессе, называемом фагоцитозом ) после лечения, убивающего эти клетки; они могут служить складами некоторых противораковых препаратов; [104] их также можно активировать с помощью некоторых методов лечения для повышения противоопухолевого иммунитета. [105] Макрофаги также могут быть вредными по нескольким причинам: например, они могут подавлять различные виды химиотерапии, [106] [107] лучевая терапия [108] [109] и иммунотерапия. [110] [111] Поскольку макрофаги могут регулировать прогрессирование опухоли, на больных раком в настоящее время тестируются терапевтические стратегии по уменьшению количества этих клеток или манипулированию их фенотипами. [112] [113] Однако макрофаги также участвуют в антитело-опосредованной цитотоксичности (ADCC), и этот механизм считается важным для некоторых антител для иммунотерапии рака. [114]
Ожирение [ править ]
Было замечено, что увеличение количества провоспалительных макрофагов в жировой ткани при ожирении способствует осложнениям ожирения, включая резистентность к инсулину и диабет 2 типа. [115]
Таким образом, модуляция воспалительного состояния макрофагов жировой ткани считается возможной терапевтической целью для лечения заболеваний, связанных с ожирением. [116] Хотя макрофаги жировой ткани подвергаются противовоспалительному гомеостатическому контролю посредством симпатической иннервации, эксперименты с использованием мышей с нокаутом гена ADRB2 показывают, что этот эффект осуществляется косвенно через модуляцию функции адипоцитов, а не через прямую активацию бета-2-адренергических рецепторов , что позволяет предположить, что адренергические рецепторы Стимуляция макрофагов может оказаться недостаточной для воздействия на воспаление или функцию жировой ткани при ожирении. [117]
В жировой CCR2 ткани наблюдается с дефицитом мышей повышенное количество эозинофилов , большая активация альтернативных макрофагов и склонность к экспрессии цитокинов 2 типа . Более того, этот эффект был преувеличен, когда мыши страдали ожирением из-за диеты с высоким содержанием жиров. [118] Частично это вызвано переключением фенотипа макрофагов, вызванным некрозом жировых клеток ( адипоцитов ). У человека с ожирением некоторые адипоциты лопаются и подвергаются некротической гибели, что приводит к переключению резидентных макрофагов М2 на фенотип М1. Это одна из причин системного хронического воспалительного процесса низкой степени тяжести, связанного с ожирением. [119] [120]
Кишечные макрофаги [ править ]
Несмотря на то, что кишечные макрофаги очень похожи по структуре на тканевые макрофаги, они приобрели специфические характеристики и функции, учитывая их естественную среду, которая находится в пищеварительном тракте. Макрофаги и кишечные макрофаги обладают высокой пластичностью, что приводит к изменению их фенотипа под воздействием окружающей среды. [121] Как и макрофаги, кишечные макрофаги представляют собой дифференцированные моноциты, хотя кишечные макрофаги должны сосуществовать с микробиомом кишечника . Это сложная задача, поскольку бактерии, обнаруженные в кишечнике, не распознаются как «собственные» и могут быть потенциальными мишенями для фагоцитоза макрофагов. [122]
Чтобы предотвратить разрушение кишечных бактерий, кишечные макрофаги приобрели ключевые отличия от других макрофагов. Прежде всего, кишечные макрофаги не вызывают воспалительных реакций. В то время как тканевые макрофаги выделяют различные воспалительные цитокины, такие как IL-1, IL-6 и TNF-α, кишечные макрофаги не производят и не секретируют воспалительные цитокины. Это изменение напрямую вызвано средой кишечных макрофагов. Окружающие эпителиальные клетки кишечника выделяют TGF-β , который индуцирует переход от провоспалительных макрофагов к невоспалительным макрофагам. [122]
Несмотря на то, что воспалительная реакция в кишечных макрофагах подавлена, фагоцитоз все равно осуществляется. Эффективность фагоцитоза не снижается, поскольку кишечные макрофаги способны эффективно фагоцитировать бактерии S. typhimurium и E. coli , но кишечные макрофаги по-прежнему не выделяют цитокины даже после фагоцитоза. Кроме того, кишечные макрофаги не экспрессируют рецепторы липополисахаридов (ЛПС), IgA или IgG. [123] Отсутствие рецепторов ЛПС важно для кишечника, поскольку кишечные макрофаги не обнаруживают ассоциированные с микробами молекулярные структуры (MAMPS/PAMPS) кишечного микробиома. Они также не экспрессируют рецепторы факторов роста IL-2 и IL-3. [122]
в болезни Роль
Было показано, что кишечные макрофаги играют роль в воспалительных заболеваниях кишечника (ВЗК), таких как болезнь Крона (БК) и язвенный колит (ЯК). В здоровом кишечнике кишечные макрофаги ограничивают воспалительную реакцию в кишечнике, но при болезненном состоянии количество и разнообразие кишечных макрофагов изменяются. Это приводит к воспалению кишечника и появлению симптомов воспалительного заболевания кишечника. Кишечные макрофаги имеют решающее значение для поддержания гомеостаза кишечника . Наличие воспаления или патогена изменяет этот гомеостаз и одновременно изменяет кишечные макрофаги. [124] До сих пор не установлен определенный механизм изменения кишечных макрофагов путем привлечения новых моноцитов или изменений в уже имеющихся кишечных макрофагах. [123]
Кроме того, новое исследование показывает, что макрофаги ограничивают доступ железа к бактериям, высвобождая внеклеточные везикулы, улучшая исход сепсиса. [125]
СМИ [ править ]
- Видно, что активный макрофаг J774 поглощает четыре конидии совместно . Клетки J774 обрабатывали 5 нг/мл интерферона-γ за ночь перед съемкой конидий. Наблюдения проводились каждые 30 секунд в течение 2,5 часов.
- два высокоактивных альвеолярных макрофага, Можно увидеть поглощающих конидии . Таймлапс составляет 30 секунд на кадр в течение 2,5 часов.
История [ править ]
Этот раздел нуждается в расширении . Вы можете помочь, добавив к нему . ( март 2018 г. ) |
Макрофаги были впервые обнаружены в конце 19 века Эли Мечниковым . [126] Эли Мечников произвел революцию в области макрофагов, объединив философские идеи и эволюционные исследования жизни. [127] Позже, в 1960-х годах, Ван Фюрт выдвинул идею о том, что циркулирующие в крови моноциты у взрослых способствуют возникновению всех тканевых макрофагов. [128] В последние годы публикации о макрофагах заставили людей поверить в то, что множественные резидентные тканевые макрофаги не зависят от моноцитов крови, поскольку они формируются на эмбриональной стадии развития. [129] В 21 веке все идеи о происхождении макрофагов (присутствующих в тканях) объединяются, чтобы предположить, что физиологически сложные организмы образуют макрофаги независимо с помощью механизмов, которые не обязательно зависят от моноцитов крови. [130]
См. также [ править ]
- Бактериофаг
- Дендритная клетка
- Гистиоцит
- Список различных типов клеток в организме взрослого человека
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б Махла Р.С., Кумар А., Тутилл Х.Дж., Кришнаджи С.Т., Сатьямурти Б., Нурсадеги М. и др. (январь 2021 г.). «NIX-опосредованная митофагия регулирует метаболическое перепрограммирование в фагоцитирующих клетках во время микобактериальной инфекции». Туберкулез . 126 (январь): 102046. doi : 10.1016/j.tube.2020.102046 . ПМИД 33421909 . S2CID 231437641 .
- ^ «Партнерство регенеративной медицины в образовании» . Архивировано из оригинала 25 апреля 2015 года . Проверено 7 мая 2015 г.
- ^ Нарендорф М., Хойер Ф.Ф., Меервальдт А.Е., ван Леент М.М., Сендерс М.Л., Кальканьо С. и др. (октябрь 2020 г.). «Визуализация сердечно-сосудистых и легочных макрофагов с помощью датчика позитронно-эмиссионной томографии» 64 Cu-Макрин у мышей, кроликов и свиней» . Тираж: Сердечно-сосудистая визуализация . 13 (10): e010586. doi : /CIRCIMAGING.120.010586 . PMC 7583675. 10.1161 PMID 33076700 .
- ^ Овчинников Д.А. (сентябрь 2008 г.). «Макрофаги в эмбрионе и за его пределами: гораздо больше, чем просто гигантские фагоциты» . Бытие . 46 (9): 447–462. дои : 10.1002/dvg.20417 . ПМИД 18781633 . S2CID 38894501 .
Макрофаги присутствуют практически во всех тканях, начиная с эмбрионального развития, и, помимо их роли в защите хозяина и удалении апоптотических клеток, все чаще признаются их трофические функции и роль в регенерации.
- ^ Компакт-диск Миллса (2012). «Макрофаги M1 и M2: предсказания здоровья и болезней». Критические обзоры по иммунологии . 32 (6): 463–488. doi : 10.1615/CritRevImmunol.v32.i6.10 . ПМИД 23428224 .
- ^ Мерфи К., Уивер С. (2006). Иммунобиология Джейнвей . Гарланд Сайенс, Нью-Йорк. стр. 464, 904. ISBN. 978-0-8153-4551-0 .
- ^ Рансохофф Р.М. (июль 2016 г.). «Полярный вопрос: существуют ли микроглия M1 и M2?». Природная неврология . 19 (8): 987–991. дои : 10.1038/nn.4338 . ПМИД 27459405 . S2CID 27541569 .
- ^ Кромбах Ф., Мюнцинг С., Аллмелинг А.М., Герлах Дж.Т., Бер Дж., Дёргер М. (сентябрь 1997 г.). «Размер клеток альвеолярных макрофагов: межвидовое сравнение» . Перспективы гигиены окружающей среды . 105 (Приложение 5): 1261–1263. дои : 10.2307/3433544 . JSTOR 3433544 . ПМК 1470168 . ПМИД 9400735 .
- ^ Хазен В., Мбика Дж.П., Томкевич С., Бенелли С., Чани С., Ачур А. и др. (октябрь 2005 г.). «Экспрессия селективных к макрофагам маркеров в адипоцитах человека и грызунов» . Письма ФЭБС . 579 (25): 5631–5634. дои : 10.1016/j.febslet.2005.09.032 . ПМИД 16213494 . S2CID 6066984 .
- ^ Залкинд С (2001). Илья Мечников: его жизнь и творчество . Гонолулу, Гавайи: Тихоокеанское университетское издательство. стр. 78, 210. ISBN. 978-0-89875-622-7 .
- ^ Шапури-Могаддам А., Мохаммадиан С., Вазини Х., Тагадоси М., Эсмаили С.А., Мардани Ф. и др. (сентябрь 2018 г.). «Пластичность, поляризация и функции макрофагов в здоровье и болезни» . Журнал клеточной физиологии . 233 (9): 6425–6440. дои : 10.1002/jcp.26429 . ПМИД 29319160 . S2CID 3621509 .
- ^ Лоте Си Джей. Принципы физиологии почек, 5-е издание . Спрингер. п. 37.
- ^ Ширази С., Равиндран С., Купер Л.Ф. (декабрь 2022 г.). «Топографически-опосредованная иммуномодуляция при остеоинтеграции; союзник или враг» . Биоматериалы . 291 : 121903. doi : 10.1016/j.bimaterials.2022.121903 . ПМЦ 10148651 . ПМИД 36410109 .
- ^ Сирет С., ван Лессен М., Бавайс Дж., Чон Х.В., Редди Самавар С.К., Капупара К. и др. (2022). «Расшифровка гетерогенности периваскулярных макрофагов Lyve1+ в мозге мыши» . Природные коммуникации . 13 (1): 7366. Бибкод : 2022NatCo..13.7366S . дои : 10.1038/s41467-022-35166-9 . ПМЦ 9712536 . ПМИД 36450771 .
- ^ Нес В.Д., Лукьяненко Ю.О., Цзя Ж.Х., Кидо С., Ховальд В.Н., Пратум Т.К. и др. (март 2000 г.). «Идентификация липофильного фактора, продуцируемого макрофагами, который стимулирует стероидогенез» . Эндокринология . 141 (3): 953–958. дои : 10.1210/endo.141.3.7350 . ПМИД 10698170 .
- ^ Хулсманс М., Клаусс С., Сяо Л., Агирре А.Д., Кинг К.Р., Хэнли А. и др. (апрель 2017 г.). «Макрофаги облегчают электрическую проводимость в сердце» . Клетка . 169 (3): 510–522.e20. дои : 10.1016/j.cell.2017.03.050 . ПМК 5474950 . ПМИД 28431249 .
- ^ Jump up to: Перейти обратно: а б с д и Моссер Д.М., Эдвардс Дж.П. (декабрь 2008 г.). «Изучение всего спектра активации макрофагов» . Обзоры природы. Иммунология . 8 (12): 958–969. дои : 10.1038/nri2448 . ПМК 2724991 . ПМИД 19029990 .
- ^ Пердигеро Э.Г., Гейссманн Ф. (январь 2016 г.). «Развитие и поддержание резидентных макрофагов» . Природная иммунология . 17 (1): 2–8. дои : 10.1038/ni.3341 . ПМК 4950995 . ПМИД 26681456 .
- ^ Жинху Ф., Гильямс М. (март 2016 г.). «Онтогенез и гомеостаз тканерезидентных макрофагов» . Иммунитет . 44 (3): 439–449. doi : 10.1016/j.immuni.2016.02.024 . ПМИД 26982352 .
- ^ Питтет М.Дж., Нарендорф М., Свирски Ф.К. (июнь 2014 г.). «Путешествие от стволовой клетки к макрофагу» . Анналы Нью-Йоркской академии наук . 1319 (1): 1–18. Бибкод : 2014NYASA1319....1P . дои : 10.1111/nyas.12393 . ПМЦ 4074243 . ПМИД 24673186 .
- ^ Ван М., Ян Й., Кансевер Д., Ван Й., Канторес С., Мессиан С. и др. (январь 2021 г.). «Две популяции самоподдерживающихся моноцит-независимых макрофагов существуют во взрослых придатках и семенниках» . Труды Национальной академии наук Соединенных Штатов Америки . 118 (1): e2013686117. Бибкод : 2021PNAS..11813686W . дои : 10.1073/pnas.2013686117 . ПМЦ 7817195 . ПМИД 33372158 .
- ^ Jump up to: Перейти обратно: а б с Эминг С.А., Криг Т., Дэвидсон Дж.М. (март 2007 г.). «Воспаление при заживлении ран: молекулярные и клеточные механизмы» . Журнал исследовательской дерматологии . 127 (3): 514–25. дои : 10.1038/sj.jid.5700701 . ПМИД 17299434 .
=Моноциты/макрофаги. Если в месте раны не сохраняются стимулы для рекрутирования нейтрофилов, инфильтрация нейтрофилов прекращается через несколько дней, а израсходованные нейтрофилы сами фагоцитируются макрофагами, которые присутствуют на стороне раны в течение 2 дней после травмы.
- ^ Монтейт А.Дж., Миллер Дж.М., Максвелл К.Н., Чейзин В.Дж., Скаар Е.П. (сентябрь 2021 г.). «Внеклеточные ловушки нейтрофилов усиливают уничтожение бактериальных патогенов макрофагами» . Достижения науки . 7 (37): eabj2101. Бибкод : 2021SciA....7.2101M . дои : 10.1126/sciadv.abj2101 . ПМЦ 8442908 . ПМИД 34516771 .
- ^ Верма Н., Сараф С. (15 ноября 2017 г.). «Роль макрофагов: обзор» . Журнал доставки лекарств и терапии . 7 (6): 91–103. дои : 10.22270/jddt.v7i6.1521 . ISSN 2250-1177 .
- ^ ЯшРой RC (2000). «Захват макрофагов сальмонеллой (310r) посредством секреции типа III, подобной экзоцитозной передаче сигналов: механизм заражения подвздошной кишки кур» . Индийский журнал птицеводства . 35 (3): 276–281.
- ^ Jump up to: Перейти обратно: а б с д и ж г Аранго Дуке Дж., Деското А (7 октября 2014 г.). «Макрофагальные цитокины: участие в иммунитете и инфекционных заболеваниях» . Границы в иммунологии . 5 : 491. дои : 10.3389/fimmu.2014.00491 . ПМЦ 4188125 . ПМИД 25339958 .
- ^ Jump up to: Перейти обратно: а б с д и Пунт Дж., Стрэнфорд С., Джонс П., Оуэн Дж. (25 мая 2018 г.). Куби Иммунология (8-е изд.). Нью-Йорк, Нью-Йорк: WH Freeman. ISBN 978-1-4641-8978-4 .
- ^ Jump up to: Перейти обратно: а б с Фу Ю.Л., Харрисон Р.Э. (29 апреля 2021 г.). «Микробные фагоцитарные рецепторы и их потенциальное участие в индукции цитокинов в макрофагах» . Границы в иммунологии . 12 : 662063. дои : 10.3389/fimmu.2021.662063 . ПМЦ 8117099 . ПМИД 33995386 .
- ^ Jump up to: Перейти обратно: а б Хираяма Д., Иида Т., Накасе Х. (декабрь 2017 г.). «Фагоцитарная функция макрофагов, обеспечивающая врожденный иммунитет и тканевый гомеостаз» . Международный журнал молекулярных наук . 19 (1): 92. дои : 10.3390/ijms19010092 . ПМК 5796042 . ПМИД 29286292 .
- ^ Урибе-Керол Э., Росалес К (2 июня 2020 г.). «Фагоцитоз: наше современное понимание универсального биологического процесса» . Границы в иммунологии . 11 : 1066. дои : 10.3389/fimmu.2020.01066 . ПМК 7280488 . ПМИД 32582172 .
- ^ Закон СК (1 января 1988 г.). «Рецепторы C3 на макрофагах». Журнал клеточной науки. Добавка . 9 (Дополнение_9): 67–97. doi : 10.1242/jcs.1988.Supplement_9.4 . ПМИД 2978518 . S2CID 29387085 .
- ^ Форман Х.Дж., Торрес М. (декабрь 2002 г.). «Активные формы кислорода и передача сигналов в клетках: респираторный взрыв в передаче сигналов макрофагов». Американский журнал респираторной медицины и медицины интенсивной терапии . 166 (12 Пт 2): С4–С8. дои : 10.1164/rccm.2206007 . ПМИД 12471082 . S2CID 22246117 .
- ^ Лю Т, Чжан Л, Джу Д, Сунь СК (14 июля 2017 г.). «Передача сигналов NF-κB при воспалении» . Сигнальная трансдукция и таргетная терапия . 2 (1): 17023–. дои : 10.1038/sigtrans.2017.23 . ПМК 5661633 . ПМИД 29158945 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д р Мерфи К., Уивер С., Берг Л. (2022). Иммунобиология Джейнвей (10-е изд.). Нью-Йорк, Нью-Йорк: WW Norton & Company. ISBN 978-0-393-88487-6 .
- ^ Эминг С.А., Криг Т., Дэвидсон Дж.М. (март 2007 г.). «Воспаление при заживлении ран: молекулярные и клеточные механизмы» . Журнал исследовательской дерматологии . 127 (3): 514–525. дои : 10.1038/sj.jid.5700701 . ПМИД 17299434 .
- ^ Мезуар С., Меге Дж.Л. (июль 2020 г.). «Изменение парадигмы IFN-γ на стыке врожденного и адаптивного иммунитета: IFN-γ, полученный из макрофагов». Журнал биологии лейкоцитов . 108 (1): 419–426. дои : 10.1002/JLB.4MIR0420-619RR . ПМИД 32531848 . S2CID 219622032 .
- ^ Кресс Х., Стельцер Э.Х., Хольцер Д., Басс Ф., Гриффитс Г., Рорбах А. (июль 2007 г.). «Филоподии действуют как фагоцитарные щупальца и тянут дискретными шагами и со скоростью, зависящей от нагрузки» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (28): 11633–11638. Бибкод : 2007PNAS..10411633K . дои : 10.1073/pnas.0702449104 . ЧВК 1913848 . ПМИД 17620618 .
- ^ Jump up to: Перейти обратно: а б с Геррьеро Дж.Л. (2019). «Макрофаги: их нерассказанная история активации и функции Т-клеток». Международное обозрение клеточной и молекулярной биологии . 342 . Эльзевир: 73–93. дои : 10.1016/bs.ircmb.2018.07.001 . ISBN 978-0-12-815381-9 . ПМИД 30635094 .
- ^ Jump up to: Перейти обратно: а б с Итано А.А., Дженкинс М.К. (август 2003 г.). «Презентация антигена наивным CD4 Т-клеткам в лимфатическом узле». Природная иммунология . 4 (8): 733–739. дои : 10.1038/ni957 . ПМИД 12888794 . S2CID 10305140 .
- ^ Jump up to: Перейти обратно: а б с Мерфи К., Уивер С. (2016). Иммунобиология Джейнвей (9-е изд.). Нью-Йорк, Нью-Йорк: Garland Science. стр. 363–364. ISBN 978-0-8153-4505-3 .
- ^ Jump up to: Перейти обратно: а б Грей Э.Э., Цистер Дж.Г. (2012). «Макрофаги лимфатических узлов» . Журнал врожденного иммунитета . 4 (5–6): 424–436. дои : 10.1159/000337007 . ПМЦ 3574571 . ПМИД 22488251 .
- ^ Аббас АК (сентябрь 2020 г.). «Удивительная история Ил-2» . Американский журнал патологии . 190 (9): 1776–1781. doi : 10.1016/j.ajpath.2020.05.007 . ПМИД 32828360 . S2CID 221280663 .
- ^ Аннунциато Ф, Романьяни С, Романьяни С (март 2015 г.). «Три основных типа врожденного и адаптивного клеточно-опосредованного эффекторного иммунитета» . Журнал аллергии и клинической иммунологии . 135 (3): 626–635. дои : 10.1016/j.jaci.2014.11.001 . ПМИД 25528359 .
- ^ Jump up to: Перейти обратно: а б с Цай Х, Чжан Ю, Ван Дж, Гу Дж (23 июня 2021 г.). «Дефекты перепрограммирования макрофагов при терапии рака: негативное влияние PD-L1/PD-1» . Границы в иммунологии . 12 : 690869. дои : 10.3389/fimmu.2021.690869 . ПМЦ 8260839 . ПМИД 34248982 .
- ^ Jump up to: Перейти обратно: а б Хилхорст М., Шираи Т., Берри Дж., Горонзи Дж.Дж., Вейанд СМ (2014). «Взаимодействие Т-клеток и макрофагов и образование гранулем при васкулите» . Границы в иммунологии . 5 : 432. дои : 10.3389/fimmu.2014.00432 . ПМК 4162471 . ПМИД 25309534 .
- ^ Jump up to: Перейти обратно: а б с д Ролот М., Девалс Б.Г. (2 июля 2018 г.). «Активация макрофагов и функции во время заражения гельминтами: последние достижения лабораторных мышей» . Журнал иммунологических исследований . 2018 : 2790627. doi : 10.1155/2018/2790627 . ПМК 6051086 . ПМИД 30057915 .
- ^ Гордон С. (январь 2003 г.). «Альтернативная активация макрофагов». Обзоры природы. Иммунология . 3 (1): 23–35. дои : 10.1038/nri978 . ПМИД 12511873 . S2CID 23185583 .
- ^ Петерс В.А., Йостинг Дж.Дж., Фройнд Г.Г. (август 2013 г.). «Рецептор 2 IL-1 (IL-1R2) и его роль в иммунной регуляции» . Мозг, поведение и иммунитет . 32 : 1–8. дои : 10.1016/j.bbi.2012.11.006 . ПМЦ 3610842 . ПМИД 23195532 .
- ^ Мунтьеверфф Э.М., Меестерс Л.Д., ван ден Богаарт Г. (8 июля 2020 г.). «Перекрестная презентация антигена макрофагами» . Границы в иммунологии . 11 : 1276. дои : 10.3389/fimmu.2020.01276 . ПМЦ 7360722 . ПМИД 32733446 .
- ^ Сюй В., Баншеро Дж. (январь 2014 г.). «Антигенпрезентирующие клетки инструктируют дифференцировку плазматических клеток» . Границы в иммунологии . 4 : 504. дои : 10.3389/fimmu.2013.00504 . ПМЦ 3880943 . ПМИД 24432021 .
- ^ Котран Р.С., Кумар В., Коллинз Т. (1999). Роббинс Патологическая основа болезней . Филадельфия: Компания WB Saunders. ISBN 978-0-7216-7335-6 .
- ^ «История лимфоцитов» . Новый учёный (1605) . Проверено 13 сентября 2007 г.
- ^ Jump up to: Перейти обратно: а б с д Хескет М., Сахин КБ, Вест З.Э., Мюррей Р.З. (июль 2017 г.). «Фенотипы макрофагов регулируют образование рубцов и заживление хронических ран» . Международный журнал молекулярных наук . 18 (7): 1545. doi : 10.3390/ijms18071545 . ПМЦ 5536033 . ПМИД 28714933 .
- ^ Галдьеро М.Р., Гарланда С., Джайон С., Мароне Г., Мантовани А. (июль 2013 г.). «Макрофаги и нейтрофилы, связанные с опухолью, в прогрессировании опухоли». Журнал клеточной физиологии . 228 (7): 1404–1412. дои : 10.1002/jcp.24260 . ПМИД 23065796 . S2CID 41189572 .
- ^ Хотамислигил Г.С. (апрель 2010 г.). «Стресс эндоплазматической сети и атеросклероз» . Природная медицина . 16 (4): 396–399. дои : 10.1038/nm0410-396 . ПМК 2897068 . ПМИД 20376052 .
- ^ О Дж., Риек А.Е., Венг С., Петти М., Ким Д., Колонна М. и др. (апрель 2012 г.). «Стресс эндоплазматической сети контролирует дифференцировку макрофагов М2 и образование пенистых клеток» . Журнал биологической химии . 287 (15): 11629–11641. дои : 10.1074/jbc.M111.338673 . ПМК 3320912 . ПМИД 22356914 .
- ^ Криппендорф Б.Б., Райли Д.А. (январь 1993 г.). «Различие изменений в камбаловидной мышце крысы, вызванных разгрузкой и перезагрузкой». Мышцы и нервы . 16 (1): 99–108. дои : 10.1002/mus.880160116 . ПМИД 8423838 . S2CID 23012375 .
- ^ Jump up to: Перейти обратно: а б с Сен-Пьер, BA, Tidball JG (июль 1994 г.). «Дифференциальный ответ субпопуляций макрофагов на перезагрузку камбаловидной мышцы после подвешивания задних конечностей крысы». Журнал прикладной физиологии . 77 (1): 290–297. дои : 10.1152/яп.1994.77.1.290 . ПМИД 7961247 .
- ^ Тидболл Дж.Г., Берченко Э., Френетт Дж. (апрель 1999 г.). «Инвазия макрофагов не способствует повреждению мышечной мембраны во время воспаления» . Журнал биологии лейкоцитов . 65 (4): 492–498. дои : 10.1002/jlb.65.4.492 . ПМИД 10204578 . S2CID 23315528 .
- ^ Jump up to: Перейти обратно: а б Скьяффино С., Партридж Т. (2008). Восстановление и регенерация скелетных мышц . Достижения в исследованиях мышц. Том. 3.
- ^ Брешо Н., Гомес Э., Биньон М., Халлу-Лаше Дж., Дюссио М., Казес А. и др. (2008). «Модуляция состояния активации макрофагов защищает ткани от некроза во время критической ишемии конечностей у мышей с дефицитом тромбоспондина-1» . ПЛОС ОДИН . 3 (12): е3950. Бибкод : 2008PLoSO...3.3950B . дои : 10.1371/journal.pone.0003950 . ПМК 2597179 . ПМИД 19079608 .
- ^ Jump up to: Перейти обратно: а б де ла Торре Дж., Шолар А. (2006). Заживление ран: Хронические раны . Emedicine.com. По состоянию на 20 января 2008 г.
- ^ «Фазы заживления кожных ран» (PDF) . Обзоры экспертов в области молекулярной медицины . 5 . Издательство Кембриджского университета. 21 марта 2003 г. Архивировано из оригинала (PDF) 17 декабря 2008 г.
- ^ Лоренц Х.П., Лонгакер М.Т. (2003). «Раны: биология, патология и лечение». (PDF) . В Ли М., Нортон Дж.А., Боллинджер Р.Р., Чанг А.Э., Лоури С.Ф., Малвихилл С.Дж., Пасс Х.И., Томпсон Р.В. (ред.). Основная практика хирургии . Нью-Йорк, штат Нью-Йорк: Спрингер. стр. 77–88. ISBN 978-0-387-22744-3 . Архивировано из оригинала (PDF) 31 октября 2005 г.
- ^ Свирски Ф.К., Нарендорф М., Эцродт М., Вильдгрубер М., Кортес-Ретамозо В., Паницци П. и др. (июль 2009 г.). «Идентификация моноцитов-резервуаров селезенки и их размещение в очагах воспаления» . Наука . 325 (5940): 612–616. Бибкод : 2009Sci...325..612S . дои : 10.1126/science.1175202 . ПМК 2803111 . ПМИД 19644120 .
- ^ Цзя Т., Памер Э.Г. (июль 2009 г.). «Иммунология. Незаменима, но не неактуальна» . Наука . 325 (5940): 549–550. Бибкод : 2009Sci...325..549J . дои : 10.1126/science.1178329 . ПМК 2917045 . ПМИД 19644100 .
- ^ Деодхар АК, Рана РЭ (1997). «Хирургическая физиология заживления ран: обзор» . Журнал последипломной медицины . 43 (2): 52–56. ПМИД 10740722 .
- ^ Розенберг Л., де ла Торре Дж. (2006). Заживление ран, факторы роста . Emedicine.com. По состоянию на 20 января 2008 г.
- ^ Ньютон П.М., Уотсон Дж.А., Воловач Р.Г., Вуд Э.Дж. (август 2004 г.). «Макрофаги сдерживают сокращение модели заживления ран in vitro». Воспаление . 28 (4): 207–214. doi : 10.1023/B:IFLA.0000049045.41784.59 . ПМИД 15673162 . S2CID 9612298 .
- ^ Гринхал, Д.Г. (сентябрь 1998 г.). «Роль апоптоза в заживлении ран». Международный журнал биохимии и клеточной биологии . 30 (9): 1019–1030. дои : 10.1016/S1357-2725(98)00058-2 . ПМИД 9785465 .
- ^ Сташак Т.С., Фарстведт Э, Отик А (июнь 2004 г.). «Обновленная информация о повязках на раны: показания и наилучшее использование». Клинические методы в лошадиной практике . 3 (2): 148–163. дои : 10.1053/j.ctep.2004.08.006 .
- ^ Jump up to: Перейти обратно: а б Суппури А (23 мая 2013 г.). «Ученые идентифицировали клетку, которая может хранить секрет регенерации конечностей» . сайт verge.com.
Исследователи идентифицировали клетку, которая способствует отрастанию конечностей у саламандр. Макрофаги — это тип восстанавливающих клеток, которые пожирают мертвые клетки и патогены и заставляют другие иммунные клетки реагировать на патогены.
- ^ Jump up to: Перейти обратно: а б Годвин Дж.В., Пинто А.Р., Розенталь Н.А. (июнь 2013 г.). «Макрофаги необходимы для регенерации конечностей взрослой саламандры» . Труды Национальной академии наук Соединенных Штатов Америки . 110 (23): 9415–9420. Бибкод : 2013PNAS..110.9415G . дои : 10.1073/pnas.1300290110 . ПМЦ 3677454 . ПМИД 23690624 .
- ^ Мисима Ю. (октябрь 1967 г.). «Лизосомы в фагоцитозе и синтезе маланина» . Природа . 216 (5110): 67. Бибкод : 1967Natur.216...67M . дои : 10.1038/216067a0 . ПМИД 6050674 . S2CID 4285140 .
- ^ Мисима Ю. (январь 1966 г.). «Клеточная и субклеточная дифференциация фагоцитоза и синтеза меланина посредством лизосомальной и меланосомной активности» . Журнал исследовательской дерматологии . 46 (1): 70–75. дои : 10.1038/jid.1966.11 . ПМИД 5905254 .
- ^ Баранска А., Шокет А., Жув М., Баратин М., Малоссе С., Волузан О. и др. (апрель 2018 г.). «Выявление динамики кожных макрофагов объясняет как стойкость татуировки, так и трудоемкость ее удаления» . Журнал экспериментальной медицины . 215 (4): 1115–1133. дои : 10.1084/jem.20171608 . ПМЦ 5881467 . ПМИД 29511065 .
- ^ Окабе Ю., Меджитов Р. (май 2014 г.). «Тканеспецифические сигналы контролируют обратимую программу локализации и функциональной поляризации макрофагов» . Клетка . 157 (4): 832–844. дои : 10.1016/j.cell.2014.04.016 . ПМК 4137874 . ПМИД 24792964 .
- ^ Госселин Д., Линк В.М., Романоски С.Э., Фонсека Г.Дж., Эйхенфилд Д.З., Спанн, Нью-Джерси и др. (декабрь 2014 г.). «Окружающая среда управляет выбором и функцией энхансеров, контролирующих идентичность тканеспецифичных макрофагов» . Клетка . 159 (6): 1327–1340. дои : 10.1016/j.cell.2014.11.023 . ПМЦ 4364385 . ПМИД 25480297 .
- ^ Мюллер П.А., Коссо Б., Раджани Г.М., Стеванович К., Беррес М.Л., Хашимото Д. и др. (июль 2014 г.). «Перекрестное взаимодействие между мышечными макрофагами и кишечными нейронами регулирует моторику желудочно-кишечного тракта» . Клетка . 158 (2): 300–313. дои : 10.1016/j.cell.2014.04.050 . ПМК 4149228 . ПМИД 25036630 .
- ^ Удерхардт С., Мартинс А.Дж., Цанг Дж.С., Леммерманн Т., Жермен Р.Н. (апрель 2019 г.). «Резидентные макрофаги скрывают микроповреждения тканей, чтобы предотвратить воспалительное повреждение, вызванное нейтрофилами» . Клетка . 177 (3): 541–555.e17. дои : 10.1016/j.cell.2019.02.028 . ПМК 6474841 . ПМИД 30955887 .
- ^ Колтер Дж., Кирдорф К., Хеннеке П. (январь 2020 г.). «Происхождение и дифференциация нерв-ассоциированных макрофагов» . Журнал иммунологии . 204 (2): 271–279. doi : 10.4049/jimmunol.1901077 . ПМИД 31907269 . S2CID 210043405 .
- ^ Вольф Эй Джей, Андерхилл DM (2014). "Фагоцитоз". Макрофаги: биология и роль в патологии заболеваний . Спрингер Нью-Йорк. стр. 91–109. дои : 10.1007/978-1-4939-1311-4_5 . ISBN 978-1-4939-1310-7 .
- ^ Херб М., Шрамм М. (февраль 2021 г.). «Функции АФК в макрофагах и антимикробном иммунитете» . Антиоксиданты . 10 (2): 313. doi : 10.3390/antiox10020313 . ПМЦ 7923022 . PMID 33669824 .
- ^ Вайс Г., Schaible UE (март 2015 г.). «Механизмы защиты макрофагов от внутриклеточных бактерий» . Иммунологические обзоры . 264 (1): 182–203. дои : 10.1111/imr.12266 . ПМЦ 4368383 . ПМИД 25703560 .
- ^ Райан К.Дж., Рэй К.Г., ред. (2004). Медицинская микробиология Шерриса (4-е изд.). МакГроу Хилл. ISBN 978-0-8385-8529-0 .
- ^ Дюпюи-Магирага Л., Норе М., Брюн С., Ле Гранд Р., Гра Ж., Рокес П. (2012). «Болезнь Чикунгунья: инфекционно-ассоциированные маркеры от острой до хронической фазы артралгии, вызванной арбовирусом» . PLOS Забытые тропические болезни . 6 (3): e1446. дои : 10.1371/journal.pntd.0001446 . ПМЦ 3313943 . ПМИД 22479654 .
- ^ Лукас А.Д., Гривз Д.Р. (ноябрь 2001 г.). «Атеросклероз: роль хемокинов и макрофагов». Обзоры экспертов в области молекулярной медицины . 3 (25): 1–18. дои : 10.1017/S1462399401003696 . ПМИД 14585150 . S2CID 8952545 .
- ^ Франц С., Нарендорф М. (май 2014 г.). «Сердечные макрофаги и их роль при ишемической болезни сердца» . Сердечно-сосудистые исследования . 102 (2): 240–248. дои : 10.1093/cvr/cvu025 . ПМЦ 3989449 . ПМИД 24501331 .
- ^ Грюн Дж., Льюис А.Дж., Ямадзо М., Хульсманс М., Роде Д., Сяо Л. и др. (июль 2022 г.). «Нейтрофилы провоцируют, а макрофаги предотвращают грозу после инфаркта миокарда» . Природные сердечно-сосудистые исследования . 1 (7): 649–664. дои : 10.1038/s44161-022-00094-w . ПМЦ 9410341 . ПМИД 36034743 . S2CID 250475623 .
- ^ Бол С.М., Кобос-Хименес В., Кустра Н.А., Вант Ваут А.Б. (февраль 2011 г.). «Макрофаг». Будущая вирусология . 6 (2): 187–208. дои : 10.2217/fvl.10.93 .
- ^ Коппенштайнер Х., Брак-Вернер Р., Шиндлер М. (октябрь 2012 г.). «Макрофаги и их роль в инфекции вируса иммунодефицита человека I типа» . Ретровирусология . 9 (1): 82. дои : 10.1186/1742-4690-9-82 . ПМЦ 3484033 . ПМИД 23035819 .
- ^ Цянь Б.З., Поллард Дж.В. (апрель 2010 г.). «Разнообразие макрофагов усиливает прогрессирование опухоли и метастазирование» . Клетка . 141 (1): 39–51. дои : 10.1016/j.cell.2010.03.014 . ПМЦ 4994190 . ПМИД 20371344 .
- ^ Jump up to: Перейти обратно: а б Энгблом С., Пфиршке С., Питтет М.Дж. (июль 2016 г.). «Роль миелоидных клеток в терапии рака». Обзоры природы. Рак . 16 (7): 447–462. дои : 10.1038/nrc.2016.54 . ПМИД 27339708 . S2CID 21924175 .
- ^ Стикс Джи (июль 2007 г.). «Злокачественное пламя. Понимание хронического воспаления, которое способствует развитию сердечно-сосудистых заболеваний, болезни Альцгеймера и ряда других заболеваний, может стать ключом к разгадке тайн рака». Научный американец . 297 (1): 60–67. Бибкод : 2007SciAm.297a..60S . doi : 10.1038/scientificamerican0707-60 . ПМИД 17695843 .
- ^ Лин Э.Ю., Ли Дж.Ф., Гнатовский Л., Дэн Ю., Чжу Л., Гжесик Д.А. и др. (декабрь 2006 г.). «Макрофаги регулируют ангиогенный переключатель в мышиной модели рака молочной железы». Исследования рака . 66 (23): 11238–11246. дои : 10.1158/0008-5472.can-06-1278 . ПМИД 17114237 . S2CID 12722658 .
- ^ Бингл Л., Браун, Нью-Джерси, Льюис CE. Роль опухолеассоциированных макрофагов в прогрессировании опухоли: значение для новых противораковых методов лечения. Дж. Патол, 2002 г.; 196:254–65.
- ^ де Гроот А.Е. (июль 2018 г.). «Модель макрофагов, ассоциированных с опухолью человека, in vitro предполагает пролиферацию макрофагов как механизм поддержания популяций ассоциированных с опухолью макрофагов» . Исследования рака . 78 (13 Дополнение): 4060. doi : 10.1158/1538-7445.AM2018-4060 . S2CID 80769044 .
- ^ Лин Э.Ю., Нгуен А.В., Рассел Р.Г., Поллард Дж.В. (март 2001 г.). «Колониестимулирующий фактор 1 способствует прогрессированию опухолей молочной железы в злокачественные» . Журнал экспериментальной медицины . 193 (6): 727–740. дои : 10.1084/jem.193.6.727 . ПМК 2193412 . ПМИД 11257139 .
- ^ Цянь Б.З., Ли Дж., Чжан Х., Китамура Т., Чжан Дж., Кэмпион Л.Р. и др. (июнь 2011 г.). «CCL2 привлекает воспалительные моноциты, чтобы облегчить метастазирование опухоли молочной железы» . Природа . 475 (7355): 222–225. дои : 10.1038/nature10138 . ПМК 3208506 . ПМИД 21654748 .
- ^ Кортес-Ретамосо В., Эцродт М., Ньютон А., Райан Р., Пуччи Ф., Сио С.В. и др. (февраль 2013 г.). «Ангиотензин II стимулирует выработку макрофагов, способствующих развитию опухолей» . Иммунитет . 38 (2): 296–308. doi : 10.1016/j.immuni.2012.10.015 . ПМЦ 3582771 . ПМИД 23333075 .
- ^ Пуччи Ф., Гаррис С., Лай С.П., Ньютон А., Пфиршке С., Энгблом С. и др. (апрель 2016 г.). «Макрофаги SCS подавляют меланому, ограничивая взаимодействие опухолевых пузырьков и В-клеток» . Наука . 352 (6282): 242–246. Бибкод : 2016Sci...352..242P . дои : 10.1126/science.aaf1328 . ПМЦ 4960636 . ПМИД 26989197 .
- ^ Мантовани А., Аллавена П. (апрель 2015 г.). «Взаимодействие противораковой терапии с опухолеассоциированными макрофагами» . Журнал экспериментальной медицины . 212 (4): 435–445. дои : 10.1084/jem.20150295 . ПМЦ 4387285 . ПМИД 25753580 .
- ^ Де Пальма М., Льюис CE (март 2013 г.). «Макрофагальная регуляция реакции опухоли на противораковую терапию» . Раковая клетка . 23 (3): 277–286. дои : 10.1016/j.ccr.2013.02.013 . ПМИД 23518347 .
- ^ Миллер М.А., Чжэн Ю.Р., Гадде С., Пфиршке С., Зопе Х., Энгблом С. и др. (октябрь 2015 г.). «Макрофаги, ассоциированные с опухолью, действуют как резервуар медленного высвобождения нанотерапевтического пролекарства Pt(IV)» . Природные коммуникации . 6 : 8692. Бибкод : 2015NatCo...6.8692M . дои : 10.1038/ncomms9692 . ПМЦ 4711745 . ПМИД 26503691 .
- ^ Клуг Ф., Пракаш Х., Хубер П.Е., Сейбел Т., Бендер Н., Халама Н. и др. (ноябрь 2013 г.). «Низкие дозы облучения программируют дифференцировку макрофагов до фенотипа iNOS⁺/M1, что обеспечивает эффективную Т-клеточную иммунотерапию» . Раковая клетка . 24 (5): 589–602. дои : 10.1016/j.ccr.2013.09.014 . ПМИД 24209604 .
- ^ Раффелл Б., Чанг-Страчан Д., Чан В., Розенбуш А., Хо СМ, Прайер Н. и др. (ноябрь 2014 г.). «Макрофаг IL-10 блокирует CD8+ Т-клеточный ответ на химиотерапию путем подавления экспрессии IL-12 во внутриопухолевых дендритных клетках» . Раковая клетка . 26 (5): 623–637. дои : 10.1016/j.ccell.2014.09.006 . ПМК 4254570 . ПМИД 25446896 .
- ^ ДеНардо Д.Г., Бреннан Д.Д., Рексхепадж Э., Раффелл Б., Шиао С.Л., Мэдден С.Ф. и др. (июнь 2011 г.). «Сложность лейкоцитов предсказывает выживаемость при раке молочной железы и функционально регулирует реакцию на химиотерапию» . Открытие рака . 1 (1): 54–67. дои : 10.1158/2159-8274.CD-10-0028 . ПМК 3203524 . ПМИД 22039576 .
- ^ Шиао С.Л., Раффелл Б., ДеНардо Д.Г., Фаддегон Б.А., Парк CC, Куссенс Л.М. (май 2015 г.). «TH2-поляризованные CD4 (+) Т-клетки и макрофаги ограничивают эффективность лучевой терапии» . Исследования в области иммунологии рака . 3 (5): 518–525. doi : 10.1158/2326-6066.CIR-14-0232 . ПМЦ 4420686 . ПМИД 25716473 .
- ^ Козин С.В., Камун В.С., Хуан Й., Доусон М.Р., Джайн Р.К., Дуда Д.Г. (июль 2010 г.). «Привлечение миелоидных, но не эндотелиальных клеток-предшественников способствует возобновлению роста опухоли после местного облучения» . Исследования рака . 70 (14): 5679–5685. дои : 10.1158/0008-5472.CAN-09-4446 . ПМЦ 2918387 . ПМИД 20631066 .
- ^ Арлаукас С.П., Гаррис К.С., Колер Р.Х., Китаока М., Куккарезе М.Ф., Ян К.С. и др. (май 2017 г.). «Визуализация in vivo выявляет опухоль-ассоциированный путь резистентности, опосредованный макрофагами, при терапии анти-PD-1» . Наука трансляционной медицины . 9 (389): eaal3604. doi : 10.1126/scitranslmed.aal3604 . ПМЦ 5734617 . ПМИД 28490665 .
- ^ Чжу Ю., Кнолхофф Б.Л., Мейер М.А., Нювенинг Т.М., Вест Б.Л., Луо Дж. и др. (сентябрь 2014 г.). «Блокада CSF1/CSF1R перепрограммирует инфильтрирующие опухоль макрофаги и улучшает ответ на иммунотерапию контрольных точек Т-клеток на моделях рака поджелудочной железы» . Исследования рака . 74 (18): 5057–5069. дои : 10.1158/0008-5472.CAN-13-3723 . ПМК 4182950 . ПМИД 25082815 .
- ^ Райс Ч., Каннарил М.А., Ховес С., Бенц Дж., Варта К., Рунза В. и др. (июнь 2014 г.). «Нацеливание на опухолеассоциированные макрофаги с помощью антитела против CSF-1R открывает стратегию терапии рака» . Раковая клетка . 25 (6): 846–859. дои : 10.1016/j.ccr.2014.05.016 . ПМИД 24898549 .
- ^ Раффелл Б., Куссенс Л.М. (апрель 2015 г.). «Макрофаги и терапевтическая резистентность рака» . Раковая клетка . 27 (4): 462–472. дои : 10.1016/j.ccell.2015.02.015 . ПМК 4400235 . ПМИД 25858805 .
- ^ Шарма Н., Вашер Дж., Эллисон Дж. П. (май 2019 г.). «Лиганд TLR1/2 усиливает противоопухолевую эффективность блокады CTLA-4 за счет увеличения внутриопухолевого истощения Treg» . Труды Национальной академии наук Соединенных Штатов Америки . 116 (21): 10453–10462. Бибкод : 2019PNAS..11610453S . дои : 10.1073/pnas.1819004116 . ПМК 6534983 . ПМИД 31076558 .
- ^ Вайсберг С.П., Макканн Д., Десаи М., Розенбаум М., Лейбель Р.Л., Ферранте А.В. Ожирение связано с накоплением макрофагов в жировой ткани» Journal of Clinical Investigation 2003; 112:1796–808.
- ^ Гильерме А., Энрикес Ф., Бедард А.Х., член парламента Чехии (апрель 2019 г.). «Молекулярные пути, связывающие иннервацию жировой ткани с действием инсулина при ожирении и сахарном диабете» . Обзоры природы. Эндокринология . 15 (4): 207–225. дои : 10.1038/s41574-019-0165-y . ПМК 7073451 . ПМИД 30733616 .
- ^ Петкевичюс К., Бидо Дж., Вирчу С., Ньюленд С.А., Дейл М., Дюгурд А. и др. (июнь 2021 г.). «Макрофагальный бета2-адренергический рецептор необходим для воспаления и функционирования жировой ткани» . Молекулярный метаболизм . 48 : 101220. doi : 10.1016/j.molmet.2021.101220 . ПМК 8086137 . ПМИД 33774223 .
- ^ Болюс В.Р., Гутьеррес Д.А., Кеннеди А.Дж., Андерсон-Баукум Е.К., Хэсти А.Х. (октябрь 2015 г.). «Дефицит CCR2 приводит к увеличению количества эозинофилов, альтернативной активации макрофагов и экспрессии цитокинов 2 типа в жировой ткани» . Журнал биологии лейкоцитов . 98 (4): 467–477. дои : 10.1189/jlb.3HI0115-018R . ПМК 4763864 . ПМИД 25934927 .
- ^ Бутенс Л., Стиенстра Р. (май 2016 г.). «Макрофаги жировой ткани: сбиваются с пути при ожирении» . Диабетология . 59 (5): 879–894. дои : 10.1007/s00125-016-3904-9 . ПМЦ 4826424 . ПМИД 26940592 .
- ^ Синти С., Митчелл Г., Барбателли Г., Мурано И., Серези Е., Фалоя Е. и др. (ноябрь 2005 г.). «Смерть адипоцитов определяет локализацию и функцию макрофагов в жировой ткани мышей и людей с ожирением» . Журнал исследований липидов . 46 (11): 2347–2355. doi : 10.1194/jlr.M500294-JLR200 . ПМИД 16150820 .
- ^ Кюль А.А., Эрбен У, Кредель Л.И., Зигмунд Б. (7 декабря 2015 г.). «Разнообразие кишечных макрофагов при воспалительных заболеваниях кишечника» . Границы в иммунологии . 6 : 613. дои : 10.3389/fimmu.2015.00613 . ПМК 4670857 . ПМИД 26697009 .
- ^ Jump up to: Перейти обратно: а б с Смитис Л.Е., Селлерс М., Клементс Р.Х., Мостеллер-Барнум М., Менг Г., Бенджамин В.Х. и др. (январь 2005 г.). «Макрофаги кишечника человека проявляют глубокую воспалительную анергию, несмотря на активную фагоцитарную и бактерицидную активность» . Журнал клинических исследований . 115 (1): 66–75. дои : 10.1172/JCI19229 . ПМК 539188 . ПМИД 15630445 .
- ^ Jump up to: Перейти обратно: а б Моват А.М., Бейн CC (2011). «Макрофаги слизистой оболочки в гомеостазе и воспалении кишечника» . Журнал врожденного иммунитета . 3 (6): 550–564. дои : 10.1159/000329099 . ПМК 3224516 . ПМИД 22025201 .
- ^ Бейн CC, Моват AM (июль 2014 г.). «Макрофаги в кишечном гомеостазе и воспалении» . Иммунологические обзоры . 260 (1): 102–117. дои : 10.1111/imr.12192 . ПМЦ 4141699 . ПМИД 24942685 .
- ^ Вайс Дж. (январь 2023 г.). «Макрофагальные везикулы лишают бактерии железа». Природный метаболизм . 5 (1): 10–12. дои : 10.1038/s42255-022-00719-1 . ПМИД 36658401 . S2CID 256030791 .
- ^ Эпельман С., Лавин К.Дж., Рэндольф Г.Дж. (июль 2014 г.). «Происхождение и функции тканевых макрофагов» . Иммунитет . 41 (1): 21–35. doi : 10.1016/j.immuni.2014.06.013 . ПМЦ 4470379 . ПМИД 25035951 .
- ^ Масс Е, Лахманн Н (сентябрь 2021 г.). «От биологии макрофагов к клеточной иммунотерапии на основе макрофагов» . Генная терапия . 28 (9): 473–476. дои : 10.1038/s41434-021-00221-5 . ПМЦ 8455330 . ПМИД 33542457 .
- ^ Эпельман С., Лавин К.Дж., Рэндольф Г.Дж. (июль 2014 г.). «Происхождение и функции тканевых макрофагов» . Иммунитет . 41 (1): 21–35. doi : 10.1016/j.immuni.2014.06.013 . ПМЦ 4470379 . ПМИД 25035951 .
- ^ Итальани П., Бораски Д. (август 2015 г.). «Новый взгляд на тканевые макрофаги: от их происхождения до развития памяти» . Иммунная сеть . 15 (4): 167–176. дои : 10.4110/in.2015.15.4.167 . ПМЦ 4553254 . ПМИД 26330802 .
- ^ Лазаров Т., Хуарес-Карреньо С., Кокс Н., Гейссманн Ф. (июнь 2023 г.). «Физиология и болезни тканевых макрофагов» . Природа . 618 (7966): 698–707. Бибкод : 2023Natur.618..698L . дои : 10.1038/s41586-023-06002-x . ПМЦ 10649266 . ПМИД 37344646 .