Эозинофил
| Эозинофил | |
|---|---|
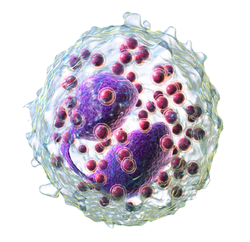 3D rendering of eosinophil | |
 Эозинофил под микроскопом (400×) в мазке периферической крови . Эритроциты окружают эозинофил, два тромбоцита в верхнем левом углу. | |
| Подробности | |
| Произношение | / ˌ iː oʊ ˈ s ɪ ə n f ɪ l / ) [1] |
| Система | Иммунная система |
| Идентификаторы | |
| МеШ | D004804 |
| ТД | Х2.00.04.1.02017 |
| ФМА | 62861 |
| Анатомические термины микроанатомии | |
Эозинофилы , иногда называемые эозинофилами или, реже, ацидофилами , представляют собой разновидность лейкоцитов и один из компонентов иммунной системы, ответственных за борьбу с многоклеточными паразитами и некоторыми инфекциями у позвоночных . [2] Наряду с тучными клетками и базофилами они также контролируют механизмы, связанные с аллергией и астмой . Они представляют собой гранулоциты , развивающиеся в процессе кроветворения в костном мозге перед миграцией в кровь, после чего окончательно дифференцируются и не размножаются. [3]
Эти клетки являются эозинофильными или « любящими кислоту » из-за их крупных ацидофильных цитоплазматических гранул, которые проявляют свое сродство к кислотам благодаря сродству к красителям каменноугольной смолы : обычно прозрачные , именно это сродство заставляет их казаться кирпично-красными окрашивания после эозин , красный краситель , по методу Романовского . [4] Окрашивание концентрируется в небольших гранулах внутри клеточной цитоплазмы , которые содержат множество химических медиаторов, таких как пероксидаза эозинофилов , рибонуклеаза (РНКаза), дезоксирибонуклеаза (ДНКаза), липаза , плазминоген и основной основной белок . Эти медиаторы высвобождаются в результате процесса, называемого дегрануляцией, после активации эозинофила, и токсичны как для паразитов, так и для тканей хозяина.
У нормальных людей эозинофилы составляют около 1–3% лейкоцитов, имеют около 12–17 микрометров и имеют двудольные ядра. размер [3] [5] Хотя эозинофилы попадают в кровоток, они остаются в тканях. [4] Они обнаруживаются в мозговом веществе и месте соединения коры и мозгового слоя тимуса , а также в нижних отделах желудочно-кишечного тракта, яичниках , матке , селезенке , предстательной железе и лимфатических узлах , но не в легких , коже , пищеводе или некоторых других органах. другие внутренние органы [ нечеткий ] в нормальных условиях. Присутствие эозинофилов в этих последних органах связано с заболеванием. Например, у пациентов с эозинофильной астмой наблюдается высокий уровень эозинофилов, что приводит к воспалению и повреждению тканей, что затрудняет дыхание пациентов. [6] [7] Эозинофилы сохраняются в кровообращении в течение 8–12 часов и могут выжить в тканях еще 8–12 дней при отсутствии стимуляции. [8] Новаторская работа 1980-х годов показала, что эозинофилы являются уникальными гранулоцитами, обладающими способностью выживать в течение длительных периодов времени после их созревания, что было продемонстрировано экспериментами с культурой ex-vivo. [9]
Разработка
[ редактировать ]
Клетки TH2 и ILC2 экспрессируют фактор транскрипции GATA-3 , который способствует выработке цитокинов TH2, включая интерлейкины (IL). [6] IL-5 контролирует развитие эозинофилов в костном мозге, поскольку они дифференцируются из миелоидных клеток-предшественников. [6] [10] [11] [12] Судьба их линии определяется факторами транскрипции, включая GATA и C/EBP. [3] Эозинофилы производят и хранят множество белков вторичных гранул до их выхода из костного мозга. После созревания эозинофилы циркулируют в крови и мигрируют к местам воспаления в тканях или к местам заражения гельминтами в ответ на хемокины , такие как CCL11 (эотаксин-1), CCL24 (эотаксин-2), CCL5 ( RANTES ), 5-гидроксиикозатетраеновая кислота и 5-оксо-эйкозатетраеновая кислота и некоторые лейкотриены , такие как лейкотриен B4 (LTB4) и MCP1/4. Интерлейкин-13 , еще один цитокин TH2, стимулирует выход эозинофилов из костного мозга, выстилая стенки сосудов молекулами адгезии, такими как VCAM-1 и ICAM-1. [6] Когда эозинофилы активируются, они подвергаются цитолизу, при котором при разрушении клетки высвобождаются эозинофильные гранулы, находящиеся во внеклеточных ловушках ДНК. [6] Известно, что высокие концентрации этих ДНК-ловушек вызывают повреждение клеток, поскольку содержащиеся в них гранулы ответственны за индуцированную лигандами секрецию эозинофильных токсинов, которые вызывают структурные повреждения. [6] Имеются данные, позволяющие предположить, что экспрессия белка гранул эозинофилов регулируется некодирующей РНК EGOT . [13]
Функция
[ редактировать ]
После активации эффекторные функции эозинофилов включают выработку следующих веществ:
- Катионные белки гранул и их высвобождение путем дегрануляции [14] [15] [16]
- Активные формы кислорода, такие как гипобромит , супероксид и пероксид ( бромноватистая кислота , которая преимущественно продуцируется эозинофильной пероксидазой ) [17]
- Липидные медиаторы, такие как эйкозаноиды из семейств лейкотриенов (например, LTC 4 , LTD 4 , LTE 4 ) и простагландинов (например, PGE 2 ). [18]
- Ферменты, такие как эластаза
- Факторы роста , такие как TGF бета , VEGF и PDGF. [19] [20]
- Цитокины, такие как IL-1 , IL-2 , IL-4 , IL-5 , IL-6 , IL-8 , IL-9 , IL-13 и TNF-альфа. [15] [21]
Существуют также эозинофилы, которые играют роль в борьбе с вирусными инфекциями, о чем свидетельствует обилие РНКаз , содержащихся в их гранулах, а также в фибрина удалении во время воспаления . Эозинофилы, наряду с базофилами и тучными клетками , являются важными медиаторами аллергических реакций и астмы патогенеза и связаны с тяжестью заболевания. Они также борются с колонизацией гельминтов (червей) и могут слегка повышаться в присутствии определенных паразитов. Эозинофилы также участвуют во многих других биологических процессах, включая постпубертатное развитие молочных желез , цикл эструса , отторжение аллотрансплантата и неоплазию . [21] Они также участвуют в презентации антигена Т -клеткам . [22]
Эозинофилы ответственны за повреждение тканей и воспаление при многих заболеваниях, включая астму. [6] [7] Было обнаружено, что высокие уровни интерлейкина-5 повышают экспрессию молекул адгезии, которые затем способствуют адгезии эозинофилов к эндотелиальным клеткам, тем самым вызывая воспаление и повреждение тканей. [7]
Накопление эозинофилов в слизистой оболочке носа считается основным диагностическим критерием аллергического ринита (назальной аллергии).
Гранулированные белки
[ редактировать ]После активации иммунным стимулом эозинофилы дегранулируются, высвобождая ряд цитотоксических катионных белков из гранул, которые способны вызывать повреждение и дисфункцию тканей. [23] К ним относятся:
- главный основной белок (MBP)
- катионный белок эозинофилов (ECP)
- эозинофильная пероксидаза (EPX)
- нейротоксин эозинофильного происхождения (EDN)
Главный основной белок, пероксидаза эозинофилов и катионный белок эозинофилов токсичны для многих тканей. [21] происходящий из эозинофилов, Катионный белок эозинофилов и нейротоксин, представляют собой рибонуклеазы с противовирусной активностью. [24] Основной основной белок индуцирует дегрануляцию тучных клеток и базофилов и участвует в ремоделировании периферических нервов . [25] [26] Катионный белок эозинофилов создает токсичные поры в мембранах клеток-мишеней, обеспечивая потенциальное проникновение в клетку других цитотоксических молекул. [27] может ингибировать пролиферацию Т -клеток , подавлять антител выработку В-клетками , вызывать дегрануляцию тучными клетками и стимулировать клетки фибробластов к секреции слизи и гликозаминогликанов . [28] Эозинофильная пероксидаза образует активные формы кислорода и активные промежуточные соединения азота , которые способствуют окислительному стрессу в мишени, вызывая гибель клеток путем апоптоза и некроза . [21]
Клиническое значение
[ редактировать ]Анализ крови
[ редактировать ]Убедительные доказательства указывают на то, что количество эозинофилов в крови может предсказать эффективность конкретных противовоспалительных препаратов. Несмотря на их все более широкое использование в клинической практике, данных о «нормальном» количестве эозинофилов в крови остается недостаточно. Из-за правостороннего распределения этих показателей медианные значения более информативны, чем средние значения, для определения нормальных уровней. В нескольких крупномасштабных исследованиях сообщалось о среднем количестве эозинофилов в крови: медиана для здоровых людей составляет 100 клеток/мкл, а 95-й процентиль — 420 клеток/мкл. Таким образом, теперь очевидно, что нормальное медианное количество эозинофилов в крови у здоровых взрослых составляет около 100 клеток/мкл, а количество выше 400 клеток/мкл считается выходом за пределы нормального диапазона. Текущие пороговые значения, такие как 150 или 300 клеток/мкл, используемые при лечении астмы или ХОБЛ, находятся в пределах нормы. [29]
Эозинофилия
[ редактировать ]Увеличение количества эозинофилов, т. е. наличие более 500 эозинофилов на микролитр крови, называется эозинофилией и обычно наблюдается у людей с паразитарным заражением кишечника ; аутоиммунные и коллагеновые сосудистые заболевания (такие как ревматоидный артрит ) и системная красная волчанка ; злокачественные заболевания, такие как эозинофильный лейкоз , клональная гиперэозинофилия и лимфома Ходжкина ; лимфоцитарный вариант гиперэозинофилии ; обширные кожные заболевания (например, эксфолиативный дерматит ); болезнь Аддисона и другие причины низкой выработки кортикостероидов (кортикостероиды подавляют уровень эозинофилов в крови); рефлюкс-эзофагит (при котором эозинофилы обнаруживаются в плоском эпителии пищевода) и эозинофильный эзофагит ; и при использовании некоторых лекарств, таких как пенициллин . Но, пожалуй, наиболее распространенной причиной эозинофилии является аллергическое заболевание, такое как астма. В 1989 году загрязненные добавки L-триптофана вызвали смертельную форму эозинофилии, известную как синдром эозинофилии-миалгии. , что напоминало синдром токсичной нефти в Испании в 1981 году.
Эозинофилы играют важную роль при астме, поскольку количество накопленных эозинофилов соответствует тяжести астматической реакции. [7] Показано, что эозинофилия на мышах связана с высокими уровнями интерлейкина-5. [7] Кроме того, было обнаружено, что биопсия слизистой оболочки бронхов, проведенная у пациентов с такими заболеваниями, как астма, имеет более высокий уровень интерлейкина-5, что приводит к более высокому уровню эозинофилов. [7] Инфильтрация эозинофилов в таких высоких концентрациях вызывает воспалительную реакцию. [7] В конечном итоге это приводит к ремоделированию дыхательных путей и затруднению дыхания. [7]
Эозинофилы также могут вызывать повреждение тканей легких у больных астмой. [7] Высокие концентрации основного основного белка эозинофилов и нейротоксина, происходящего из эозинофилов, приближающиеся к цитотоксическим уровням, наблюдаются в местах дегрануляции в легких, а также в астматической мокроте. [7]
Уход
[ редактировать ]Лечение, используемое для борьбы с аутоиммунными заболеваниями и состояниями, вызванными эозинофилами, включает:
- кортикостероиды – способствуют апоптозу . Количество эозинофилов в крови быстро снижается.
- терапия моноклональными антителами – например, меполизумаб или реслизумаб против IL-5 , предотвращающие эозинофилопоэз, или бенрализумаб против рецептора IL-5 , который уничтожает эозинофилы посредством ADCC
- антагонисты синтеза или рецепторов лейкотриенов
- иматиниб (STI571) – ингибирует PDGF-BB при гиперэозинофильном лейкозе.
Моноклональные антитела, такие как дупилумаб и лебрикизумаб, нацелены на IL-13 и его рецептор, что уменьшает эозинофильное воспаление у пациентов с астмой за счет снижения количества молекул адгезии, с которыми могут связываться эозинофилы, тем самым уменьшая воспаление. [30] [31] Меполизумаб и бенрализумаб являются другими вариантами лечения, которые нацелены на альфа-субъединицу рецептора IL-5 , тем самым ингибируя его функцию и уменьшая количество развивающихся эозинофилов, а также количество эозинофилов, что приводит к воспалению за счет антителозависимой клеточно-опосредованной цитотоксичности и эозинофильной активности. апоптоз. [32] [33]
Исследования на животных
[ редактировать ]В жировой ( жировой ) ткани CCR2 с дефицитом мышей наблюдается повышенное количество эозинофилов, большая активация альтернативных макрофагов и склонность к экспрессии цитокинов 2 типа . Более того, этот эффект был преувеличен, когда мыши страдали ожирением из-за диеты с высоким содержанием жиров. [34] Мышиные модели эозинофилии у мышей, инфицированных T. canis, показали увеличение мРНК IL-5 в селезенке мышей. [7] Мышиные модели астмы, полученные от OVA, демонстрируют более высокий ответ TH2 . [6] Когда мышам вводят IL-12 для индукции ответа TH1 , ответ TH2 подавляется, показывая, что мыши без цитокинов TH2 значительно менее склонны к проявлению симптомов астмы. [6]
См. также
[ редактировать ]- Эозинопения , снижение количества эозинофилов в крови
- Эозинофилия , увеличение (>500 клеток на микролитр) количества эозинофилов в крови.
- Гиперэозинофилия , резкое увеличение (> 1500 клеток на микролитр) количества эозинофилов в крови.
- Клональная гиперэозинофилия , наличие предракового или злокачественного клона эозинофилов в костном мозге и крови.
- Хронический эозинофильный лейкоз
- Ацидофил (гистология)
- Список различных типов клеток в организме взрослого человека
Ссылки
[ редактировать ]- ^ «Эозинофил - Определение эозинофила на английском языке в Оксфордских словарях» . Оксфордские словари — английский язык . Архивировано из оригинала 8 февраля 2018 года . Проверено 27 марта 2018 г.
- ^ «Что такое эозинофил? | Определение и функция | CCED» . www.cincinnatichildrens.org . Проверено 14 июня 2018 г.
- ^ Jump up to: а б с Ум Т.Г., Ким Б.С., Чунг И.Ю. (март 2012 г.). «Развитие эозинофилов, регуляция специфичных для эозинофилов генов и роль эозинофилов в патогенезе астмы» . Исследования аллергии, астмы и иммунологии . 4 (2): 68–79. дои : 10.4168/aair.2012.4.2.68 . ПМЦ 3283796 . ПМИД 22379601 .
- ^ Jump up to: а б Розенберг Х.Ф., Фиппс С., Фостер П.С. (июнь 2007 г.). «Торговля эозинофилами при аллергии и астме». Журнал аллергии и клинической иммунологии . 119 (6): 1303–10, викторина 1311–2. дои : 10.1016/j.jaci.2007.03.048 . hdl : 1885/30451 . ПМИД 17481712 .
- ^ Янг Б., Лоу Джо, Стивенс А., Хит Дж.В. (2006). Функциональная гистология Уитера (5-е изд.). Эльзевир Лимитед. ISBN 978-0-443-06850-8 .
- ^ Jump up to: а б с д и ж г час я Ламбрехт Б.Н., Хаммад Х. (январь 2015 г.). «Иммунология астмы». Природная иммунология . 16 (1): 45–56. дои : 10.1038/ni.3049 . ПМИД 25521684 . S2CID 5451867 .
- ^ Jump up to: а б с д и ж г час я дж к Сандерсон, Колин (1992). «Интерлейкин-5, эозинофилы и болезни» . Кровь . 79 (12): 3101–3109. doi : 10.1182/blood.V79.12.3101.bloodjournal79123101 . ПМИД 1596561 .
- ^ Янг Б., Лоу Дж.С., Стивенс А., Хит Дж.В. (2006). Функциональная гистология Уитера (5-е изд.). Эльзевир Лимитед. ISBN 978-0-443-06850-8 .
- ^ Парк Ю.М., Бохнер Б.С. (апрель 2010 г.). «Выживаемость эозинофилов и апоптоз в норме и болезни» . Исследования аллергии, астмы и иммунологии . 2 (2): 87–101. дои : 10.4168/aair.2010.2.2.87 . ПМЦ 2846745 . ПМИД 20358022 .
- ^ Меткалф Д., Бегли К.Г., Никола Н.А., Джонсон Г.Р. (март 1987 г.). «Количественная чувствительность мышиных гемопоэтических популяций in vitro и in vivo к рекомбинантному мульти-КСФ (IL-3)». Экспериментальная гематология . 15 (3): 288–95. ПМИД 3493174 .
- ^ Меткалф Д., Берджесс А.В., Джонсон Г.Р., Никола Н.А., Найс ЕС, ДеЛамартер Дж., Тэтчер Д.Р., Мермод Дж.Дж. (сентябрь 1986 г.). «Действие in vitro на кроветворные клетки рекомбинантного мышиного GM-CSF, очищенного после производства в Escherichia coli: сравнение с очищенным нативным GM-CSF». Журнал клеточной физиологии . 128 (3): 421–31. дои : 10.1002/jcp.1041280311 . ПМИД 3528176 . S2CID 515338 .
- ^ Ямагути Ю, Суда Т, Суда Дж, Эгучи М, Миура Ю, Харада Н, Томинага А, Такацу К (январь 1988 г.). «Очищенный интерлейкин 5 поддерживает терминальную дифференцировку и пролиферацию мышиных эозинофильных предшественников» . Журнал экспериментальной медицины . 167 (1): 43–56. дои : 10.1084/jem.167.1.43 . ПМК 2188821 . ПМИД 3257253 .
- ^ Вагнер Л.А., Кристенсен С.Дж., Данн Д.М., Спангруд Г.Дж., Джорджелас А., Келли Л., Эсплин М.С., Вайс Р.Б., Глейх Г.Дж. (июнь 2007 г.). «EGO, новый некодирующий ген РНК, регулирует экспрессию транскрипта белка эозинофильных гранул» . Кровь . 109 (12): 5191–8. дои : 10.1182/blood-2006-06-027987 . ПМК 1890841 . ПМИД 17351112 .
- ^ Трулсон А., Быстром Дж., Энгстрем А., Ларссон Р., Венге П. (февраль 2007 г.). «Функциональная гетерогенность катионного белка эозинофилов определяется полиморфизмом генов и посттрансляционными модификациями» . Клиническая и экспериментальная аллергия . 37 (2): 208–18. дои : 10.1111/j.1365-2222.2007.02644.x . ПМИД 17250693 . S2CID 45301814 .
- ^ Jump up to: а б Хоган С.П., Розенберг Х.Ф., Мокбель Р., Фиппс С., Фостер П.С., Лейси П., Кей А.Б., Ротенберг М.Е. (май 2008 г.). «Эозинофилы: биологические свойства и роль в здоровье и болезни». Клиническая и экспериментальная аллергия . 38 (5): 709–50. дои : 10.1111/j.1365-2222.2008.02958.x . ПМИД 18384431 . S2CID 25254034 .
- ^ Лейси П. (сентябрь 2005 г.). «Роль Rho GTPases и SNARE в высвобождении медиаторов из гранулоцитов». Фармакология и терапия . 107 (3): 358–76. doi : 10.1016/j.pharmthera.2005.03.008 . ПМИД 15951020 .
- ^ Сайто К., Нагата М., Кикучи И., Сакамото Ю. (декабрь 2004 г.). «Трансэндотелиальная миграция лейкотриена D4 и эозинофилов, образование супероксида и дегрануляция посредством бета2-интегрина». Анналы аллергии, астмы и иммунологии . 93 (6): 594–600. дои : 10.1016/S1081-1206(10)61269-0 . ПМИД 15609771 .
- ^ Бандейра-Мело С., Бозза П.Т., Веллер П.Ф. (март 2002 г.). «Клеточная биология образования и функции эйкозаноидов эозинофилов» . Журнал аллергии и клинической иммунологии . 109 (3): 393–400. дои : 10.1067/май.2002.121529 . ПМИД 11897981 .
- ^ Като Ю, Фудзисава Т, Нисимори Х, Кацумата Х, Ацута Дж, Игучи К, Камия Х (2005). «Лейкотриен D4 индуцирует выработку трансформирующего фактора роста бета1 эозинофилами». Международный архив аллергии и иммунологии . 137. 137 Приложение 1 (1): 17–20. дои : 10.1159/000085427 . ПМИД 15947480 . S2CID 23556551 .
- ^ Хориучи Т., Веллер П.Ф. (июль 1997 г.). «Экспрессия фактора роста эндотелия сосудов эозинофилами человека: усиление с помощью колониестимулирующего фактора гранулоцитов-макрофагов и интерлейкина-5». Американский журнал респираторной клеточной и молекулярной биологии . 17 (1): 70–7. дои : 10.1165/ajrcmb.17.1.2796 . ПМИД 9224211 .
- ^ Jump up to: а б с д Ротенберг М.Э., Хоган С.П. (2006). «Эозинофил». Ежегодный обзор иммунологии . 24 (1): 147–74. doi : 10.1146/annurev.immunol.24.021605.090720 . ПМИД 16551246 .
- ^ Ши Х.З. (сентябрь 2004 г.). «Эозинофилы функционируют как антигенпрезентирующие клетки». Журнал биологии лейкоцитов . 76 (3): 520–7. дои : 10.1189/jlb.0404228 . ПМИД 15218055 . S2CID 25152503 .
- ^ Глейх Г.Дж., Адольфсон Ч.Р. (1986). «Эозинофильный лейкоцит: строение и функции». Достижения иммунологии, том 39 . Достижения иммунологии. Том. 39. стр. 177–253. doi : 10.1016/S0065-2776(08)60351-X . ISBN 9780120224395 . ПМИД 3538819 .
- ^ Слифман Н.Р., Легеринг Д.А., Маккин DJ, Глейх Г.Дж. (ноябрь 1986 г.). «Активность рибонуклеазы, связанная с нейротоксином эозинофильного происхождения человека и катионным белком эозинофилов» . Журнал иммунологии . 137 (9): 2913–7. doi : 10.4049/jimmunol.137.9.2913 . ПМИД 3760576 . S2CID 33456907 .
- ^ Жутлин Л.М., Акерман С.Дж., Глейх Г.Дж., Томас Л.Л. (октябрь 1984 г.). «Стимуляция высвобождения гистамина базофилами и тучными клетками крысы катионными белками, полученными из эозинофильных гранул» . Журнал иммунологии . 133 (4): 2180–5. doi : 10.4049/jimmunol.133.4.2180 . ПМИД 6206154 . S2CID 12043171 .
- ^ Морган Р.К., Костелло Р.В., Дуркан Н., Кингхэм П.Дж., Глейх Г.Дж., Маклин В.Г., Уолш М.Т. (август 2005 г.). «Различные эффекты белков катионных гранул эозинофилов на передачу сигналов и выживаемость нервных клеток IMR-32». Американский журнал респираторной клеточной и молекулярной биологии . 33 (2): 169–77. CiteSeerX 10.1.1.335.4162 . дои : 10.1165/rcmb.2005-0056OC . ПМИД 15860794 .
- ^ Янг Д.Д., Петерсон К.Г., Вендж П., Кон З.А. (1986). «Механизм повреждения мембраны, опосредованный катионным белком эозинофилов человека». Природа . 321 (6070): 613–6. Бибкод : 1986Natur.321..613Y . дои : 10.1038/321613a0 . ПМИД 2423882 . S2CID 4322838 .
- ^ Венге П., Быстром Дж., Карлсон М., Хаканссон Л., Каравачик М., Петерсон С., Севеус Л., Трулсон А. (сентябрь 1999 г.). «Катионный белок эозинофилов (ECP): молекулярные и биологические свойства и использование ECP в качестве маркера активации эозинофилов при заболевании». Клиническая и экспериментальная аллергия . 29 (9): 1172–86. дои : 10.1046/j.1365-2222.1999.00542.x . ПМИД 10469025 . S2CID 11541968 .
- ^ Ломмач, Марек; Наир, Парамешваран; Вирхов, Иоганн Кристиан (2024). «Нормальное количество эозинофилов в крови у человека» . Дыхание . 103 (4): 214–216. дои : 10.1159/000537833 . ISSN 0025-7931 . ПМЦ 10997252 . ПМИД 38354723 .
- ^ Венцель С., Форд Л., Перлман Д., Спектор С., Шер Л., Скоберанда Ф., Ван Л., Киркесели С., Роклин Р., Бок Б., Хэмилтон Дж., Минг Дж.Э., Радин А., Шталь Н., Янкопулос Г.Д., Грэм Н., Пироцци Г. (июнь 2013 г.). «Дупилумаб при персистирующей астме с повышенным уровнем эозинофилов» . Медицинский журнал Новой Англии . 368 (26): 2455–66. дои : 10.1056/nejmoa1304048 . ПМИД 23688323 .
- ^ Коррен Дж., Леманске Р.Ф., Ханания Н.А., Коренблат П.Е., Парси М.В., Аррон Дж.Р., Харрис Дж.М., Ширенс Х., Ву Л.К., Су З., Мозесова С., Эйснер М.Д., Боэн С.П., Мэтьюз Дж.Г. (сентябрь 2011 г.). «Лебрикизумаб лечение у взрослых с астмой» . Медицинский журнал Новой Англии . 365 (12): 1088–98. дои : 10.1056/nejmoa1106469 . ПМИД 21812663 .
- ^ Лавиолетт М., Госсаж Д.Л., Говро Г., Ли Р., Оливенштейн Р., Катиал Р., Буссе В.В., Венцель С., Ву Ю, Датта В., Колбек Р., Молфино Н.А. (ноябрь 2013 г.). «Влияние бенрализумаба на эозинофилы дыхательных путей у больных астмой с эозинофилией мокроты» . Журнал аллергии и клинической иммунологии . 132 (5): 1086–1096.e5. дои : 10.1016/j.jaci.2013.05.020 . ПМЦ 4172321 . ПМИД 23866823 .
- ^ Ортега Х.Г., Лю М.К., Паворд И.Д., Брюссель Г.Г., Фитцджеральд Дж.М., Четта А., Умберт М., Кац Л.Е., Кин О.Н., Янси С.В., Чанес П. (сентябрь 2014 г.). «Лечение меполизумабом у больных тяжелой эозинофильной астмой» . Медицинский журнал Новой Англии . 371 (13): 1198–207. дои : 10.1056/nejmoa1403290 . hdl : 2268/176693 . ПМИД 25199059 .
- ^ Болюс В.Р., Гутьеррес Д.А., Кеннеди А.Дж., Андерсон-Баукум Е.К., Хэсти А.Х. (октябрь 2015 г.). «Дефицит CCR2 приводит к увеличению количества эозинофилов, альтернативной активации макрофагов и экспрессии цитокинов 2 типа в жировой ткани» . Журнал биологии лейкоцитов . 98 (4): 467–77. дои : 10.1189/jlb.3HI0115-018R . ПМЦ 4763864 . ПМИД 25934927 . Архивировано из оригинала 9 мая 2017 года . Проверено 8 сентября 2016 г.
Внешние ссылки
[ редактировать ]- Эозинофил [ мертвая ссылка ] - Система BioWeb в Университете Висконсина
- Гистология на ucsf.edu
- «Что такое эозинофил?» в Центре эозинофильных заболеваний Цинциннати