Клональное удаление
В иммунологии клональная делеция — это процесс удаления Т- и В- лимфоцитов из репертуара иммунной системы . [1] [2] Процесс клональной делеции помогает предотвратить распознавание и разрушение собственных клеток-хозяев, что делает его разновидностью негативного отбора . В конечном счете, клональная делеция играет роль в центральной толерантности . [3] Клональная делеция может помочь защитить людей от аутоиммунитета , когда организм производит иммунный ответ на свои собственные клетки. Это один из многих методов, используемых организмом для иммунной толерантности .
Открытие
[ редактировать ]Центральная толерантность и клональная делеция не привлекали особого внимания в первые годы иммунологии. [2] [4] Фрэнк Макфарлейн Бёрнет был первым, кто предложил идею удаления клонов. Несколько ключевых выводов помогли Бёрнету в этом открытии. В 1936 году Эрих Трауб продемонстрировал, что, когда развивающаяся в матке мышь заражается вирусом, после рождения она не вызывает реакции антител к тому же вирусу. В то время как мышь, которая развивается нормально без какого-либо заражения вирусом во время развития, разовьет иммунный ответ на тот же вирус при заражении после рождения. [5] [6] Затем, в 1945 году, Рэй Дэвид Оуэнс заметил, что неидентичные близнецы крупного рогатого скота не могли отвергнуть кровь друг друга, когда у крупного рогатого скота были разные группы крови. [4] [5] Сочетание доказательств Трауба и наблюдений Оуэнса помогло Бернету и его партнеру Фрэнку Феннеру предположить, что «собственные» маркеры клеток-хозяев определяются в эмбриональном состоянии. [5] Затем в 1959 году Бернет смог выдвинуть гипотезу клонального отбора. [2] [5] В рамках этой гипотезы Бёрнет заявил, что аутореактивные лимфоциты уничтожаются до созревания, чтобы предотвратить дальнейшую пролиферацию. [2] [7] Бёрнет и другие впоследствии получили Нобелевскую премию в 1960 году за вклад в иммунологическую толерантность. [4] В настоящее время клональная делеция является широко обсуждаемой темой в иммунологии и трансплантологии на протяжении последних десятилетий. [5]
Функция
[ редактировать ]
В иммунной системе имеются миллионы В- и Т-лимфоцитов. По мере развития Т- или В-лимфоцитов они могут перестраивать свой геном чтобы экспрессировать уникальный антиген , который распознает специфический эпитоп патогена , . [8] [9] Существует большое разнообразие распознаваемых эпитопов, и в результате некоторые В- и Т-лимфоциты могут развить способность распознавать себя. [10] Чтобы этого не произошло, каждый образующийся Т- и В-лимфоцит снабжается аутоантигеном. [2] [7] Если рецептор антигена, присутствующий на лимфоците, взаимодействует с высоким сродством к аутоантигену, то этот лимфоцит классифицируется как «аутореактивный». Эти «самореактивные» лимфоциты затем подвергаются процессу клональной делеции. Это достигается за счет апоптоза соответствующей клетки, в конечном итоге удаляющего клетку из иммунной системы. [2] Важно отметить, что не все лимфоциты, обладающие высоким сродством к аутоантигену, подвергаются клональной делеции. Если аутореактивные клетки избегают клональной делеции, на периферии существуют механизмы с участием Т-регуляторных клеток, предотвращающие развитие аутоиммунного заболевания у хозяина. [7] Однако как для В-, так и для Т-клеток в первичных лимфоидных органах клональная делеция является наиболее распространенной формой негативного отбора. Процесс клональной делеции помогает защитить хозяина от аутоиммунитета. [2] [7]
Расположение и механизм
[ редактировать ]В- и Т-лимфоциты проверяются на самореактивность в первичных лимфоидных органах перед попаданием на периферию. [2] Место, где это происходит, зависит от типа лимфоцита. [8] В-лимфоциты развиваются и созревают в костном мозге. В то время как Т-лимфоциты развиваются в костном мозге и позже созревают в тимусе, следовательно, T. [8] Механизмы центральной толерантности не являются полностью аффективными, и некоторые аутореактивные лимфоциты могут попасть в кровоток. Однако иммунная система имеет вторичную защиту на периферии для защиты от этого, называемую периферической толерантностью . [11] [12]
В-лимфоциты
[ редактировать ]Регуляция аутореактивных В-лимфоцитов может происходить на многих различных стадиях развития В-клеток. Первая линия защиты возникает в костном мозге, прежде чем аутореактивные клетки смогут достичь кровообращения. [8] [11] функционального рецептора B-клеток (BCR). Это происходит после сборки [3] Если BCR демонстрирует высокое сродство к аутоантигену, то на этом этапе может произойти клональная делеция. Однако некоторые аутореактивные В-лимфоциты могут проскользнуть через эту контрольную точку и попасть в кровоток. Если это происходит, то тогда вступает в силу периферическая толерантность. Это процесс удаления аутореактивных клеток из кровообращения после их полного созревания. Примеры механизмов, используемых для периферической толерантности к аутореактивным В-лимфоцитам, включают анергию и десенсибилизацию антигенных рецепторов. Как и центральная толерантность, периферическая толерантность не всегда является точной, что оставляет возможность аутореактивным лимфоцитам оставаться в кровообращении. [11]
Т-лимфоциты
[ редактировать ]Процесс удаления аутореактивных Т-лимфоцитов происходит в тимусе. [2] [8] [12] Тимус состоит из двух зон: внешней области, называемой корой тимуса , и внутренней области, называемой мозговым веществом тимуса . Внутри этих регионов Т-лимфоциты подвергнутся серии положительного или отрицательного отбора. [12] [13]
Кора тимуса
[ редактировать ]Т-лимфоциты сначала подвергаются положительному отбору в коре тимуса. Здесь Т-лимфоциты проверяются, чтобы увидеть, могут ли они распознавать собственный главный комплекс гистосовместимости класса I или II (MHC I/II). [12] Если Т-лимфоцит сможет распознать MHC I/II, он продолжит созревание и переместится в мозговое вещество тимуса. Если Т-лимфоцит не может распознать себя (MHC I/II), он подвергается игнорированию или апоптозу. [13] тимуса Дендритные клетки и макрофаги , по-видимому, ответственны за сигналы апоптоза, посылаемые аутореактивным Т-клеткам в коре тимуса. [3] [14]
Мозговой мозг тимуса
[ редактировать ]Т-клетки также имеют возможность подвергаться клональной делеции в мозговом веществе тимуса. Здесь Т-лимфоциты подвергаются негативному отбору. [12] [13] В этот момент они сталкиваются с комплексами MHC I/II, представляющими собственные антигены. [12] Если Т-лимфоцит взаимодействует с высоким сродством к комплексу, представляющему аутоантиген, то этот лимфоцит подвергается апоптозу или дифференцировке Treg . [13] Подобно регуляции В-лимфоцитов, Т-лимфоциты могут покинуть тимус и при этом оставаться аутореактивными. Однако иммунная система эволюционировала, чтобы бороться с этой периферической толерантностью. Механизмы периферической толерантности к аутореактивным Т-лимфоцитам включают клональный арест, клональную анергию и клональное редактирование после. [3]
Полное и неполное клональное удаление
[ редактировать ]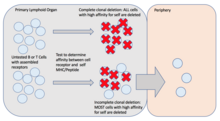
Полная клональная делеция приводит к апоптозу всех В- и Т-лимфоцитов, проявляющих высокое сродство к аутоантигену. [2] Неполная клональная делеция приводит к апоптозу большинства аутореактивных В- и Т-лимфоцитов. [2] Полная клональная делеция может открыть возможности для молекулярной мимикрии , что имеет неблагоприятные последствия для хозяина. [2] Следовательно, неполная клональная делеция обеспечивает баланс между способностью хозяина распознавать чужеродные антигены и собственные антигены. [2]
Методы эксплуатации
[ редактировать ]Молекулярная мимикрия
[ редактировать ]Клональная делеция стимулирует микроорганизмы к выработке эпитопов, сходных с белками, обнаруженными в организме хозяина. Поскольку большинство аутореактивных клеток подвергаются клональной делеции, это позволяет микроорганизмам с эпитопами, сходными с антигеном хозяина, избежать распознавания и обнаружения Т- и В-лимфоцитами. [2] Однако в случае обнаружения это может привести к аутоиммунному ответу из-за сходства эпитопов микроорганизма и антигена хозяина. Примеры этого наблюдаются у Streptococcus pyogenes и Borrelia burgdorferi . [2] Возможно, но редко, когда молекулярная мимикрия приводит к аутоиммунному заболеванию. [2]
Подавляющий
[ редактировать ]Суперантигены состоят из вирусных или бактериальных белков и могут блокировать процесс клональной делеции при экспрессии в тимусе, поскольку они напоминают Т-клеточного рецептора (TCR) с собственным MHC/пептидами. взаимодействие [1] Таким образом, благодаря этому процессу суперантигены могут эффективно предотвращать созревание родственных Т-клеток.
Ссылки
[ редактировать ]- ^ Jump up to: а б Рассел, Джон Х. (1998-01-01), Дельвес, Питер Дж. (редактор), «Клональная делеция» , Энциклопедия иммунологии (второе издание) , Оксфорд: Elsevier, стр. 569–573, ISBN 978-0-12-226765-9 , получено 23 апреля 2024 г.
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п Роуз НР (2015). Молекулярная мимикрия и клональная делеция: свежий взгляд. Журнал теоретической биологии , 375 , 71–76. https://doi.org/10.1016/j.jtbi.2014.08.034
- ^ Jump up to: а б с д Дженни, Пунт; А., Стрэнфорд, Шэрон; П., Джонс, Патрисия; Янис., Куби (01 января 2013 г.). Куби Иммунология . У. Х. Фриман. ISBN 978-1-4292-1919-8 ОСЛК 820117219
- ^ Jump up to: а б с Сильверстайн, Артур М. (март 2016 г.). «Любопытный случай с Нобелевской премией 1960 года Бёрнету и Медавару» . Иммунология . 147 (3): 269–274. дои : 10.1111/imm.12558 . ISSN 0019-2805 . ПМЦ 4754613 . ПМИД 26790994 .
- ^ Jump up to: а б с д и Холл, Б.М., Верма, Н.Д., Тран, Г.Т. и Ходжкинсон, С.Дж. (2022). Толерантность к трансплантации, а не только клональная делеция. Frontiers inimmunology , 13 , 810798. https://doi.org/10.3389/fimmu.2022.810798.
- ^ Трауб Э. (1936). ЭПИДЕМИЯ В КОЛОНИИ МЫШЕЙ, ВЫЗВАННАЯ ВИРУСОМ ОСТРУЕГО ЛИМФОЦИТАРНОГО ХОРИОМЕНИНГИТА. Журнал экспериментальной медицины , 63 (4), 533–546. https://doi.org/10.1084/jem.63.4.533
- ^ Jump up to: а б с д Э., Пол, Уильям (октябрь 2015 г.). Иммунитет . ISBN 978-1-4214-1802-5 ОСЛК 948563239
- ^ Jump up to: а б с д и Кано, Р. Луз Елена; Лопера, Х. Дамарис Э. (18 июля 2013 г.), «Введение в Т- и В-лимфоциты» , Аутоиммунитет: от скамьи до постели [Интернет] , El Rosario University Press , получено 12 марта 2024 г.
- ^ Чарльз Джейнвей-младший; Трэверс, Пол; Уолпорт, Марк; Шломчик, Марк Дж. (2001), «Перестройка сегментов генов антиген-рецептор контролирует развитие лимфоцитов» , Иммунобиология: Иммунная система в здоровье и болезни. 5-е издание , Garland Science , получено 23 апреля 2024 г.
- ^ Китц, Александра; Хафлер, Дэвид А. (2015). «Тимический отбор: будь верен самому себе». Иммунитет . 42 (5): 788–789. doi :10.1016/j.immuni.2015.05.007. ПМИД 25992854.
- ^ Jump up to: а б с Немази Д. (2017). Механизмы центральной толерантности к В-клеткам. Обзоры природы. Иммунология , 17 (5), 281–294. https://doi.org/10.1038/nri.2017.19
- ^ Jump up to: а б с д и ж «Развитие Т-клеток» . www2.nau.edu . Проверено 25 апреля 2024 г.
- ^ Jump up to: а б с д Син Ю. и Хогквист К.А. (2012). Т-клеточная толерантность: центральная и периферическая. Перспективы Колд-Спринг-Харбора в биологии , 4 (6), a006957. https://doi.org/10.1101/cshperspect.a006957
- ^ Кляйн, Людгер; Киевский, Бруно; Аллен, Пол М.; Хогквист, Кристин А. (2014). «Положительный и отрицательный отбор репертуара Т-клеток: что видят (и не видят) тимоциты». Обзоры природы Иммунология . 14 (6): 377–391. дои : 10.1038/nri3667. ПМЦ 4757912. ПМИД 24830344.
Внешние ссылки
[ редактировать ]- Клонирование + удаление Национальной медицинской библиотеки США в медицинских предметных рубриках (MeSH)