Тимус
| Тимус | |
|---|---|
 Положение тимуса | |
| Подробности | |
| Предшественник | Третий глоточный мешок |
| Система | Лимфатическая система , часть иммунной системы |
| Лимфа | Трахеобронхиальный , парастернальный |
| Функция | Поддержка развития функциональных Т-клеток |
| Идентификаторы | |
| латинский | тимус |
| МеШ | Д013950 |
| ТА98 | А13.1.02.001 |
| ТА2 | 5152 |
| ФМА | 9607 |
| Анатомическая терминология | |
Тимус тимус ( мн. ч .: тимус или ) является специализированным первичным лимфоидным органом иммунной системы . В тимусе тимуса лимфоциты или Т-клетки созревают . Т-клетки имеют решающее значение для адаптивной иммунной системы , где организм адаптируется к конкретным инородным захватчикам. Тимус расположен в верхней передней части грудной клетки, в переднем верхнем средостении , позади грудины и впереди сердца . Он состоит из двух долей, каждая из которых состоит из центрального мозгового вещества и внешней коры, окруженных капсулой.
Тимус состоит из незрелых Т-клеток, называемых тимоцитами , а также выстилающих клеток, называемых эпителиальными клетками , которые помогают тимоцитам развиваться. Т-клетки, которые успешно развиваются, реагируют соответствующим образом с иммунными рецепторами MHC организма (так называемый положительный отбор ), а не против белков организма (так называемый негативный отбор ). Тимус является самым крупным и наиболее активным в неонатальном и предподростковом периодах. К раннему подростковому возрасту тимус начинает уменьшаться в размерах и активности , а ткань тимуса постепенно заменяется жировой тканью . Тем не менее, развитие некоторых Т-клеток продолжается на протяжении всей взрослой жизни.
Аномалии тимуса могут привести к уменьшению количества Т-клеток и аутоиммунным заболеваниям, таким как аутоиммунный полиэндокринный синдром 1 типа и миастения гравис . Они часто связаны с раком ткани тимуса, называемого тимомой , или тканей, возникающих из незрелых лимфоцитов, таких как Т-клетки, называемых лимфомой . Удаление тимуса называется тимэктомией . Хотя тимус считался частью тела еще со времен древних греков , только с 1960-х годов функция тимуса в иммунной системе стала яснее.
Структура
[ редактировать ]Тимус — это орган, который расположен за грудиной в верхней передней части грудной клетки и тянется вверх к шее. У детей тимус розовато-серый, мягкий, дольчатой поверхности. [1] При рождении его длина составляет около 4–6 см, ширина 2,5–5 см и толщина около 1 см. [2] Он увеличивается в размерах до полового созревания, где может иметь размер около 40–50 г. [3] [4] после чего он уменьшается в размерах в процессе, известном как инволюция . [4]
Тимус расположен в переднем средостении . [5] Он состоит из двух долей, которые встречаются в верхней средней линии и простираются от нижней части щитовидной железы на шее до хряща четвертого ребра. [1] Доли покрыты капсулой. [3] Тимус лежит позади грудины, опирается на перикард и отделен от дуги аорты и магистральных сосудов слоем фасции . Левая брахиоцефальная вена может даже проникать в тимус. [1] В шее он лежит на передней и боковых сторонах трахеи , позади грудино-подъязычной и грудино-щитовидной мышц . [1]
Микроанатомия
[ редактировать ]Тимус состоит из двух долей, слившихся посередине, окруженных капсулой, простирающейся вместе с кровеносными сосудами внутрь. [2] Доли состоят из внешней коры, богатой клетками, и внутреннего менее плотного мозгового вещества . [4] Доли делятся на более мелкие дольки диаметром 0,5-2 мм, между которыми вдоль перегородок из капсулы выступают радиально отходящие вставки . [1]
Кора состоит в основном из тимоцитов и эпителиальных клеток. [3] Тимоциты, незрелые Т-клетки , поддерживаются сетью мелкоразветвленных эпителиальных ретикулярных клеток , которые переходят в аналогичную сеть в мозговом веществе. Эта сеть образует адвентицию кровеносных сосудов, которые входят в кору через перегородки вблизи места соединения с мозговым веществом. [1] В тимусе также присутствуют и другие клетки, включая макрофаги , дендритные клетки и небольшое количество В-клеток , нейтрофилов и эозинофилов . [3]
В мозговом веществе сеть эпителиальных клеток более грубая, чем в коре, а лимфоидных клеток относительно меньше. [1] Концентрические, похожие на гнезда тельца, называемые тельцами Гассаля (также называемые тельцами тимуса ), образуются скоплениями медуллярных эпителиальных клеток. [3] Это концентрические слоистые завитки эпителиальных клеток , количество которых увеличивается на протяжении всей жизни. [1] Они представляют собой остатки эпителиальных трубок, вырастающих из третьих глоточных мешков эмбриона и образующих тимус. [6]
- Микрофотография, показывающая дольку тимуса. Кора (более темно-фиолетовая область) окружает менее плотный и более светлый мозговой слой.
- Микрофотография, показывающая тельца Гассаля, обнаруженные в мозговом веществе тимуса.
Кровоснабжение и нервное снабжение
[ редактировать ]Артерии , кровоснабжающие вилочковую железу, представляют собой ветви внутренней грудной и нижней щитовидной артерий , иногда встречаются ветви верхней щитовидной артерии . [2] Ветви достигают тимуса и вместе с перегородками капсулы направляются в область между корковым и мозговым веществом, где входят в сам тимус; или, альтернативно, непосредственно вводить в капсулу. [2]
Вены левой тимуса, тимические вены , заканчиваются в плечеголовной вене , внутренней грудной вене и в нижних щитовидных венах . [2] Иногда вены заканчиваются непосредственно в верхней полой вене. [2]
Лимфатические сосуды отходят только от тимуса, сопровождая артерии и вены. Они дренируются в брахиоцефальные, трахеобронхиальные и парастернальные лимфатические узлы . [2]
Нервы , иннервирующие вилочковую железу, возникают из блуждающего нерва и шейной симпатической цепи . [2] Ветви от диафрагмальных нервов достигают капсулы тимуса, но не входят в сам тимус. [2]
Вариация
[ редактировать ]Две доли немного различаются по размеру: левая доля обычно выше правой. Ткань тимуса может быть разбросана по поверхности железы или вокруг нее, а иногда и внутри щитовидной железы. [2] Тимус у детей тянется вверх по-разному, иногда до уровня щитовидной железы. [2]
Разработка
[ редактировать ]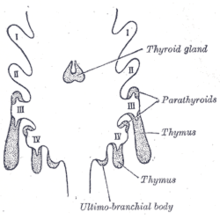
Тимоциты и эпителий тимуса имеют различное происхождение. [4] Эпителий тимуса развивается первым и представляет собой два выроста, по одному с каждой стороны, третьего глоточного мешка . [4] Иногда вовлекается также четвертый глоточный мешок. [3] Они простираются наружу и назад в окружающую мезодерму и нервного гребня, происходящую из мезенхиму, перед вентральной аортой . Здесь тимоциты и эпителий встречаются и соединяются соединительной тканью. Глоточное отверстие каждого дивертикула вскоре стирается, но шейка колбы некоторое время сохраняется в виде клеточного тяжа. В результате дальнейшей пролиферации клеток, выстилающих колбу, образуются зачатки клеток, которые окружаются и изолируются вторгающейся мезодермой. [7]
Эпителий образует мелкие дольки и превращается в губчатую структуру. На этом этапе гемопоэтические предшественники костного мозга мигрируют в тимус. [4] Нормальное развитие зависит от взаимодействия эпителия и гемопоэтических тимоцитов . Йод также необходим для развития и активности тимуса. [8]
Инволюция
[ редактировать ]Тимус продолжает расти после рождения, достигая относительного максимального размера к периоду полового созревания. [2] Он наиболее активен в жизни плода и новорожденного . [9] К моменту полового созревания его масса увеличивается до 20–50 граммов. [3] Затем он начинает уменьшаться в размере и активности в процессе, называемом инволюцией тимуса . [4] После первого года жизни количество вырабатываемых Т-клеток начинает падать. [4] Жир и соединительная ткань заполняют часть объема тимуса. [2] Во время инволюции тимус уменьшается в размерах и активности. [4] Жировые клетки присутствуют при рождении, но после полового созревания заметно увеличиваются в размерах и количестве, проникая в железу сначала со стенок между дольками, затем в кору и мозговой слой. [4] Этот процесс продолжается и в пожилом возрасте, когда тимус может быть трудно обнаружить, будь то с помощью микроскопа или человеческого глаза. [4] хотя обычно весит 5–15 граммов. [3] Кроме того, появляется все больше данных, показывающих, что возрастная инволюция тимуса обнаруживается у большинства, если не у всех, видов позвоночных, имеющих тимус, что позволяет предположить, что это эволюционный процесс, который сохранился. [40]
Атрофия происходит из-за повышенного уровня циркулирующих половых гормонов , а химическая или физическая кастрация взрослого человека приводит к увеличению размера и активности тимуса. [10] Тяжелая болезнь или заражение вирусом иммунодефицита человека также могут привести к инволюции. [3]
Функция
[ редактировать ]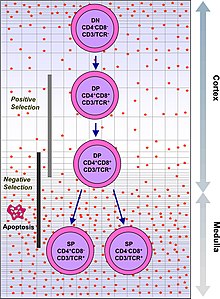
Созревание Т-клеток
[ редактировать ]Тимус способствует созреванию Т-клеток — важной части иммунной системы, обеспечивающей клеточный иммунитет . [11] Т-клетки начинаются как гемопоэтические предшественники из костного мозга и мигрируют в тимус, где их называют тимоцитами . В тимусе они подвергаются процессу созревания, который включает в себя обеспечение реакции клеток на антигены («положительный отбор»), но не на антигены, обнаруженные в тканях организма («негативный отбор»). [11] После созревания Т-клетки эмигрируют из тимуса, чтобы обеспечить жизненно важные функции иммунной системы. [11] [12]
Каждая Т-клетка имеет отдельный Т-клеточный рецептор , соответствующий определенному веществу, называемому антигеном . [12] Большинство рецепторов Т-клеток связываются с главным комплексом гистосовместимости клеток организма. MHC представляет антиген рецептору Т-клеток, который становится активным, если он соответствует специфическому рецептору Т-клеток. [12] Чтобы правильно функционировать, зрелые Т-клетки должны быть способны связываться с молекулой MHC («положительный отбор») и не реагировать на антигены, которые на самом деле находятся в тканях организма («негативный отбор»). [12] Положительный отбор происходит в коре головного мозга, а отрицательный — в мозговом веществе тимуса. [13] После этого процесса выжившие Т-клетки покидают тимус, регулируемый сфингозин-1-фосфатом . [13] Дальнейшее созревание происходит в периферическом кровообращении. [13] Частично это происходит из-за гормонов и цитокинов, секретируемых клетками тимуса, включая тимулин , тимопоэтин и тимозины . [4]
Положительный выбор
[ редактировать ]Т-клетки имеют отдельные рецепторы Т-клеток. Эти отдельные рецепторы образуются в результате реаранжировки генов рекомбинации V(D)J, стимулируемой генами RAG1 и RAG2 . [13] Этот процесс подвержен ошибкам: некоторые тимоциты не способны создавать функциональные рецепторы Т-клеток, тогда как другие тимоциты создают аутореактивные рецепторы Т-клеток. [14] Если образуется функциональный Т-клеточный рецептор, тимоцит начнет одновременно экспрессировать белки клеточной поверхности CD4 и CD8 . [13]
Выживание и природа Т-клетки зависят от ее взаимодействия с окружающими эпителиальными клетками тимуса. Здесь рецептор Т-клеток взаимодействует с молекулами MHC на поверхности эпителиальных клеток. [13] АТ-клетка с рецептором, который не реагирует или реагирует слабо, погибнет в результате апоптоза . AT-клетка, которая реагирует, выживет и размножится. [13] Зрелая Т-клетка экспрессирует только CD4 или CD8, но не то и другое. [12] Это зависит от силы связывания между TCR и MHC класса 1 или класса 2. [13] Рецептор AT-клеток, который связывается в основном с MHC класса I, имеет тенденцию продуцировать зрелые «цитотоксические» CD8-положительные Т-клетки; Рецептор Т-клеток, который связывается в основном с MHC класса II, имеет тенденцию продуцировать CD4-положительные Т-клетки. [14]
Отрицательный выбор
[ редактировать ]Т-клетки, атакующие собственные белки организма, удаляются в тимусе, что называется «негативным отбором». [12] Эпителиальные клетки мозгового вещества и дендритные клетки тимуса экспрессируют основные белки из других частей тела. [13] Ген, который стимулирует это, — AIRE . [12] [13] Тимоциты, которые сильно реагируют на аутоантигены, не выживают и погибают в результате апоптоза. [12] [13] Некоторые CD4-положительные Т-клетки, подвергшиеся воздействию аутоантигенов, сохраняются как Т-регуляторные клетки . [12]
Клиническое значение
[ редактировать ]Иммунодефицит
[ редактировать ]Поскольку в тимусе развиваются Т-клетки, врожденные проблемы с развитием тимуса могут привести к иммунодефициту , будь то из-за проблемы с развитием вилочковой железы или проблемы, специфичной для развития тимоцитов. Иммунодефицит может быть глубоким. [9] Потеря тимуса в раннем возрасте из-за генетической мутации (как при синдроме ДиДжорджа , синдроме CHARGE или очень редком «голом» тимусе, вызывающем отсутствие волос и тимуса). [15] ) приводит к тяжелому иммунодефициту и последующей высокой восприимчивости к инфекциям вирусами, простейшими и грибами . [16] Голые мыши с очень редким «голым» дефицитом в результате мутации FOXN1 представляют собой линию исследовательских мышей в качестве модели дефицита Т-клеток. [17]
Наиболее распространенной врожденной причиной иммунодефицита, связанного с тимусом, является делеция 22-й хромосомы , называемая синдромом ДиДжорджа . [15] [16] Это приводит к нарушению развития третьего и четвертого глоточных мешков, что приводит к нарушению развития тимуса и различным другим сопутствующим проблемам, таким как врожденные пороки сердца и аномалии рта (такие как расщелина неба и расщелина губы ). недостаточность развития паращитовидных желез и наличие свища между трахеей и пищеводом . [16] Наблюдается очень низкое количество циркулирующих Т-клеток. [16] Состояние диагностируется с помощью флуоресцентной гибридизации in situ и лечится трансплантацией тимуса . [15]
Тяжелый комбинированный иммунодефицит (ТКИД) представляет собой группу редких врожденных генетических заболеваний, которые могут приводить к комбинированному дефициту Т-, В- и NK-клеток . [16] Эти синдромы вызваны мутациями, которые влияют на созревание гемопоэтических клеток-предшественников , которые являются предшественниками как В-, так и Т-клеток. [16] Ряд генетических дефектов может вызвать SCID, включая рецептора IL-2 потерю функции гена и мутацию, приводящую к дефициту фермента адениндезаминазы . [16]
Аутоиммунное заболевание
[ редактировать ]Аутоиммунный полиэндокринный синдром
[ редактировать ]Аутоиммунный полиэндокринный синдром 1 типа — редкий генетический аутоиммунный синдром, возникающий в результате генетического дефекта тканей тимуса. [18] В частности, заболевание возникает в результате дефектов гена аутоиммунного регулятора (AIRE), который стимулирует экспрессию аутоантигенов в эпителиальных клетках мозгового вещества тимуса. Из-за дефектов этого состояния аутоантигены не экспрессируются, в результате чего Т-клетки не приспособлены переносить ткани организма и могут относиться к ним как к чужеродным, стимулируя иммунный ответ и приводя к аутоиммунитету. [18] людей с APECED развивается аутоиммунное заболевание, поражающее множество эндокринных тканей, причем обычно поражаются органы, такие как щитовидной железы , болезнь Аддисона надпочечников У и кандидозная инфекция поверхностей тела, включая внутреннюю оболочку рта и ногти . гипотиреоз к дисфункции клеток TH17 , а симптомы часто начинаются в детстве. Могут также возникнуть многие другие аутоиммунные заболевания. [18] Лечение направлено на пораженные органы. [18]
Мультиорганный аутоиммунитет, связанный с тимомой
[ редактировать ]мультиорганный аутоиммунитет, связанный с тимомой У людей с тимомой может возникнуть . В этом состоянии Т-клетки, развивающиеся в тимусе, направлены против тканей организма. Это связано с тем, что злокачественный тимус не способен соответствующим образом обучать развивающиеся тимоциты элиминации аутореактивных Т-клеток. Это состояние практически неотличимо от реакции «трансплантат против хозяина» . [19]
Миастения гравис
[ редактировать ]Миастения является аутоиммунным заболеванием, чаще всего вызываемым антителами, которые блокируют рецепторы ацетилхолина , участвующие в передаче сигналов между нервами и мышцами . [20] Это часто связано с гиперплазией тимуса или тимомой. [20] антитела вырабатываются, вероятно, из-за аномального развития Т-клеток. [21] Миастения чаще всего развивается в молодом и среднем возрасте, вызывая легкое утомление мышечных движений. [20] Исследования включают выявление антител (например, против рецепторов ацетилхолина или специфической для мышц киназы ) и компьютерную томографию для выявления тимомы или тимэктомию. [20] Что касается тимуса, в качестве лечения можно рассматривать удаление тимуса, называемое тимэктомией , особенно если обнаружена тимома. [20] Другие методы лечения включают увеличение продолжительности действия ацетилхолина на нервные синапсы за счет снижения скорости распада. Это осуществляется ингибиторами ацетилхолинэстеразы, такими как пиридостигмин . [20]
Рак
[ редактировать ]Тимомас
[ редактировать ]Опухоли, исходящие из эпителиальных клеток тимуса, называются тимомами . [3] Чаще всего они возникают у взрослых старше 40 лет. [3] Опухоли обычно выявляются, когда они вызывают такие симптомы, как образование в шее или поражают близлежащие структуры, такие как верхняя полая вена ; [21] обнаружен в результате скрининга у пациентов с миастенией, которая имеет сильную связь с тимомами и гиперплазией; [3] и обнаруживается как случайная находка при рентгенографии грудной клетки . [21] Гиперплазия и опухоли, исходящие из тимуса, связаны с другими аутоиммунными заболеваниями, такими как гипогаммаглобулинемия , болезнь Грейвса , чистая аплазия эритроцитов , пернициозная анемия и дерматомиозит , вероятно, из-за дефектов отрицательного отбора в пролиферирующих Т-клетках. [3] [22]
Тимомы могут быть доброкачественными; доброкачественная, но вследствие расширения, проникающая за пределы капсулы тимуса («инвазивная тимома»), или злокачественная ( карцинома ). [3] Эта классификация основана на внешнем виде клеток. [3] Классификация ВОЗ также существует, но не используется как часть стандартной клинической практики. [3] Наиболее распространены доброкачественные опухоли, ограниченные тимусом; за ними следуют локально инвазивные опухоли, а затем карциномы. [3] Сообщения различаются: некоторые источники сообщают, что злокачественные опухоли более распространены. [22] Инвазивные опухоли, хотя и не являются технически злокачественными, все же могут распространяться ( метастазировать ) в другие части тела. [3] Хотя тимомы состоят из эпителиальных клеток, они также могут содержать тимоциты. [3] Лечение тимомы часто требует хирургического вмешательства по удалению всего тимуса. [22] Это также может привести к временной ремиссии любых связанных с ним аутоиммунных заболеваний. [22]
Лимфомы
[ редактировать ]Опухоли, происходящие из Т-клеток тимуса, образуют разновидность острого лимфобластного лейкоза (ОЛЛ). [23] По симптомам, подходу к исследованию и лечению они схожи с другими формами ОЛЛ. [23] Развивающиеся симптомы, как и при других формах ОЛЛ, связаны с дефицитом тромбоцитов , что приводит к образованию синяков или кровотечений; иммуносупрессия, приводящая к инфекциям; или проникновение клеток в части тела, что приводит к увеличению печени , селезенки , лимфатических узлов или других участков. [23] Анализ крови может выявить большое количество лейкоцитов или лимфобластов , а также дефицит других клеточных линий, например низкий уровень тромбоцитов или анемию . [23] Иммунофенотипирование выявит клетки, которые являются CD3 , белком, обнаруженным в Т-клетках, и поможет дополнительно определить зрелость Т-клеток. Генетический анализ, включая кариотипирование, может выявить специфические аномалии, которые могут повлиять на прогноз или лечение, например, Филадельфийскую транслокацию . [23] Лечение может включать несколько курсов химиотерапии , трансплантацию стволовых клеток и решение сопутствующих проблем, таких как лечение инфекций антибиотиками и переливание крови . Очень высокое количество лейкоцитов может также потребовать циторедукции с помощью афереза . [23]
Опухоли, происходящие из небольшой популяции В-клеток, присутствующих в тимусе, приводят к первичным медиастинальным (тимическим) крупноклеточным В-клеточным лимфомам . [24] Это редкий подтип неходжкинской лимфомы , хотя по активности генов и иногда микроскопической форме они необычно также имеют характеристики лимфом Ходжкина . [25] Чаще всего они возникают у лиц молодого и среднего возраста, более выражены у женщин. [25] Чаще всего симптомы возникают из-за сдавления структур вблизи вилочковой железы, таких как верхняя полая вена или верхние дыхательные пути ; при поражении лимфатических узлов часто это происходит в средостении и группах шеи . [25] Такие опухоли часто выявляются с помощью биопсии , подлежащей иммуногистохимическому исследованию . Это покажет наличие кластеров дифференцировки белков клеточной поверхности – а именно CD30 , с CD19 , CD20 и CD22 , и с отсутствием CD15 . Для подтверждения диагноза также могут использоваться другие маркеры. [25] Лечение обычно включает типичные схемы CHOP или EPOCH или другие схемы; схемы лечения, обычно включающие циклофосфамид , антрациклин , преднизолон и другие химиотерапевтические средства; и, возможно, также трансплантация стволовых клеток . [25]
Кисты тимуса
[ редактировать ]Тимус может содержать кисты, обычно менее 4 см в диаметре. Кисты тимуса обычно обнаруживаются случайно и обычно не вызывают симптомов. [3] Кисты тимуса могут возникать на шее или в грудной клетке ( средостении ). [26] Кисты обычно содержат только жидкость и выстланы множеством слоев плоских клеток или столбчатых клеток . [26] Несмотря на это, наличие кисты может вызывать проблемы, аналогичные проблемам тимомы, поскольку сдавливает близлежащие структуры. [3] а некоторые могут контактировать с внутренними стенками ( перегородками ), и их трудно отличить от опухолей. [26] При обнаружении кист исследование может включать обследование на наличие опухолей, которое может включать КТ или МРТ области, в которой предположительно находится киста. [3] [26]
Хирургическое удаление
[ редактировать ]Тимэктомия – хирургическое удаление тимуса. [2] Обычной причиной удаления является получение доступа к сердцу для хирургической коррекции врожденных пороков сердца в неонатальном периоде. [27] Другие показания к тимэктомии включают удаление тимом и лечение миастении. [2] У новорожденных относительный размер тимуса затрудняет хирургический доступ к сердцу и окружающим его сосудам. [27]
Удаление тимуса в младенчестве часто приводит к фатальному иммунодефициту, поскольку функциональные Т-клетки не развились. [2] [28] У детей старшего возраста и взрослых, у которых имеется функционирующая лимфатическая система со зрелыми Т-клетками, также расположенными в других лимфоидных органах, эффект снижается, но включает неспособность сформировать иммунный ответ против новых антигенов, [2] рост заболеваемости раком и рост смертности от всех причин. [29]
Общество и культура
[ редактировать ]При использовании в пищу человека тимус животных известен как один из видов сладкого хлеба . [30]
История
[ редактировать ]Тимус был известен древним грекам , а его название происходит от греческого слова θυμός ( thumos ), означающего «гнев», или по-древнегречески «сердце, душа, желание, жизнь», возможно, из-за его расположения в груди. , рядом с местом, где субъективно ощущаются эмоции; [31] или же название происходит от травы тимьяна (также по-гречески θύμος или θυμάρι ), которое стало названием «бородавчатого нароста», возможно, из-за его сходства с пучком тимьяна. [32]
Гален первым заметил, что размеры органа меняются на протяжении жизни человека. [33]
В девятнадцатом веке состояние было идентифицировано как тимиколимфатический статус, определяемый увеличением лимфоидной ткани и увеличением тимуса. Считалось, что это причина синдрома внезапной детской смерти , но сейчас это устаревший термин. [34]
Важность тимуса в иммунной системе была открыта в 1961 году Жаком Миллером путем хирургического удаления тимуса у однодневных мышей и наблюдения последующего дефицита в популяции лимфоцитов, впоследствии названных Т-клетками в честь органа их происхождения. . [35] [36] До открытия своей иммунологической роли тимус считался «эволюционной случайностью», не имеющей функционального значения. [14] Роль тимуса в обеспечении толерантности зрелых Т-клеток к тканям организма была раскрыта в 1962 году, когда было обнаружено, что Т-клетки трансплантированного тимуса мышам демонстрируют толерантность к тканям мыши-донора. [14] В 1968 году В-клетки и Т-клетки были идентифицированы как разные типы лимфоцитов, и был понятен тот факт, что Т-клетки требуют созревания в тимусе. [14] Подтипы Т-клеток (CD8 и CD4) были идентифицированы к 1975 году. [14] Способ созревания этих подклассов Т-клеток – позитивный отбор клеток, функционально связанных с рецепторами MHC – был известен к 1990-м годам. [14] Важная роль гена AIRE и роль негативного отбора в предотвращении созревания аутореактивных Т-клеток была понята к 1994 году. [14]
Недавно достижения иммунологии позволили более полно понять функцию тимуса в созревании Т-клеток. [14]
Другие животные
[ редактировать ]Тимус присутствует у всех челюстных позвоночных , где он с возрастом подвергается такому же сокращению и выполняет ту же иммунологическую функцию, что и у других позвоночных. тимусоподобная лимфоэпителиальная структура, названная тимоидом Недавно, в 2011 году, в жабрах личинок миног была обнаружена дискретная . [37] У миксины есть прототимус, связанный с глоточными велярными мышцами, который отвечает за различные иммунные реакции. [38]
Тимус также присутствует у большинства других позвоночных животных и имеет структуру и функцию, сходную с тимусом человека. Сообщалось, что у мышей иногда возникает второй тимус на шее. [39] Как и у людей, тимус морской свинки естественным образом атрофируется по мере того, как животное достигает взрослой жизни. [40] но у атимической голой морской свинки (возникшей в результате спонтанной лабораторной мутации) ткань тимуса вообще отсутствует, а полость органа замещена кистозными пространствами. [41]
Дополнительные изображения
[ редактировать ]- Объяснение функции тимуса
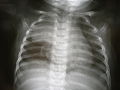
- Тимус плода
- На рентгенограмме грудной клетки тимус выглядит как рентгеноплотное (более яркое на этом изображении) образование в верхней доле правого (левого на изображении) легкого ребенка.
Ссылки
[ редактировать ]![]() В эту статью включен общедоступный текст со страницы 1273 20-го издания «Анатомии Грея» (1918 г.).
В эту статью включен общедоступный текст со страницы 1273 20-го издания «Анатомии Грея» (1918 г.).
- ^ Перейти обратно: а б с д и ж г час Стэндринг С. и др., ред. (2008). Анатомия Грея: анатомические основы клинической практики (40-е изд.). Лондон: Черчилль Ливингстон. ISBN 978-0-8089-2371-8 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д Стэндринг С., Грей Х., ред. (2016). Анатомия Грея: анатомические основы клинической практики (41-е изд.). Филадельфия. стр. 983–6. ISBN 9780702052309 . OCLC 920806541 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v Кумар В., Аббас А.К., Фаусто Н., Астер Дж.К. (27 августа 2014 г.). «Глава 13. Заболевания лейкоцитов, лимфатических узлов, селезенки и тимуса: Тимус.». Патологическая основа болезней Роббинса и Котрана (9-е (онлайн-издание)). Elsevier Науки о здоровье. ISBN 9780323296397 .
- ^ Перейти обратно: а б с д и ж г час я дж к л Янг Б., О'Дауд Дж., Вудфорд П. (2013). Функциональная гистология Уитера: текстовый и цветной атлас (6-е изд.). Филадельфия: Эльзевир. стр. 204–6. ISBN 9780702047473 .
- ^ Нассери, Фарбод; Эфтехари, Фарзин (март 2010 г.). «Клинический и радиологический обзор нормального и аномального тимуса: жемчужины и ловушки» . Радиографика . 30 (2): 413–428. дои : 10.1148/rg.302095131 . ISSN 0271-5333 . ПМИД 20228326 .
- ^ Ларсен В. (2001). Эмбриология человека (3-е изд.). Эльзевир. стр. 366–367. ISBN 978-0-443-06583-5 .
- ^ Швейцарская эмбриология (из UL , UB и UF ) qblood/lymphat03
- ^ Вентури С., Вентури М. (сентябрь 2009 г.). «Йод, тимус и иммунитет». Питание . 25 (9): 977–9. дои : 10.1016/j.nut.2009.06.002 . ПМИД 19647627 .
- ^ Перейти обратно: а б Дэвидсона, 2018 , с. 67.
- ^ Сазерленд Дж.С., Голдберг Г.Л., Хэмметт М.В., Ульдрих А.П., Берзиньш С.П., Хенг Т.С. и др. (август 2005 г.). «Активация регенерации тимуса у мышей и людей после андрогенной блокады» . Журнал иммунологии . 175 (4): 2741–53. дои : 10.4049/jimmunol.175.4.2741 . ПМИД 16081852 .
- ^ Перейти обратно: а б с Холл Дж.Э. (2016). Учебник Гайтона и Холла по медицинской физиологии (13-е изд.). Филадельфия: Эльзевир. стр. 466–7. ISBN 978-1-4557-7016-8 .
- ^ Перейти обратно: а б с д и ж г час я Кумар В., Аббас А.К., Фаусто Н., Астер Дж.К. (27 августа 2014 г.). «Глава 6. Болезни иммунной системы. Нормальная иммунная система». Патологическая основа болезней Роббинса и Котрана (9-е (онлайн-издание)). Elsevier Науки о здоровье. ISBN 9780323296397 .
- ^ Перейти обратно: а б с д и ж г час я дж к Холь ТМ (2019). «6. Клеточная защита от инфекции: тимическая селекция CD4+ и CD8+ Т-клеток». Беннетт Дж.Э., Долин Р., Блазер М.Дж. (ред.). Принципы и практика Манделла, Дугласа и Беннета в области инфекционных заболеваний (9-е (онлайн-издание)). Эльзевир. ISBN 9780323482554 .
- ^ Перейти обратно: а б с д и ж г час я Миллер Дж. Ф. (май 2011 г.). «Золотой юбилей тимуса». Обзоры природы. Иммунология . 11 (7): 489–95. дои : 10.1038/nri2993 . ПМИД 21617694 . S2CID 21191923 .
- ^ Перейти обратно: а б с Харрисона, 2015 , стр. 2493.
- ^ Перейти обратно: а б с д и ж г Дэвидсона, 2018 , стр. 79–80.
- ^ Фокс Дж.Г. (2006). Мышь в биомедицинских исследованиях: иммунология . Эльзевир. п. 277. ИСБН 978-0-08-046908-9 .
- ^ Перейти обратно: а б с д Харрисонс, 2015 , стр. 2756–7.
- ^ Вадхера А., Маверакис Э., Мициадес Н., Лара П.Н., Фунг М.А., Линч П.Дж. (октябрь 2007 г.). «Мультиорганный аутоиммунитет, связанный с тимомой: болезнь типа трансплантат против хозяина». Журнал Американской академии дерматологии . 57 (4): 683–9. дои : 10.1016/j.jaad.2007.02.027 . ПМИД 17433850 .
- ^ Перейти обратно: а б с д и ж Дэвидсона, 2018 , стр. 1141–43.
- ^ Перейти обратно: а б с Энгельс Е.А. (октябрь 2010 г.). «Эпидемиология тимомы и связанных с ней злокачественных новообразований» . Журнал торакальной онкологии . 5 (10 Приложение 4): S260-5. дои : 10.1097/JTO.0b013e3181f1f62d . ПМЦ 2951303 . ПМИД 20859116 .
- ^ Перейти обратно: а б с д Харрисона, 2015 , стр. 2759.
- ^ Перейти обратно: а б с д и ж Ларсон Р.А. (2015). «Глава 91: Острый лимфобластный лейкоз». Гематология Уильямса (онлайн) (9-е изд.). Макгроу-Хилл Образование. ISBN 978-0071833004 .
- ^ Домбровска-Иваницка А., Валевский Ю.А. (сентябрь 2014 г.). «Первичная медиастинальная крупноклеточная В-клеточная лимфома» . Текущие отчеты о гематологических злокачественных новообразованиях . 9 (3): 273–83. дои : 10.1007/s11899-014-0219-0 . ПМК 4180024 . ПМИД 24952250 .
- ^ Перейти обратно: а б с д и Смит С.Д., Press OW (2015). «Глава 98. Диффузная крупноклеточная В-клеточная лимфома и родственные заболевания». Гематология Уильямса (онлайн) (9-е изд.). Макгроу-Хилл Образование. ISBN 978-0071833004 .
- ^ Перейти обратно: а б с д Гольдштейн, Алан Дж.; Олива, Изабель; Хонарпише, Хедие; Рубиновиц, Ами (1 февраля 2015 г.). «Экскурсия по тимусу: обзор поражений тимуса с радиологической и патологической корреляцией» . Журнал Канадской ассоциации радиологов . 66 (1): 5–15. дои : 10.1016/j.carj.2013.09.003 . ПМИД 24736228 . S2CID 33986973 .
- ^ Перейти обратно: а б Эйстейнсдоттир Дж. Х., Фрейсдоттир Дж., Харальдссон А., Стефансдоттир Дж., Скафтадоттир И., Хельгасон Х., Огмундсдоттир Х. М. (май 2004 г.). «Влияние частичной или тотальной тимэктомии во время операции на открытом сердце у младенцев на иммунную функцию в более позднем возрасте» . Клиническая и экспериментальная иммунология . 136 (2): 349–55. дои : 10.1111/j.1365-2249.2004.02437.x . ПМК 1809033 . ПМИД 15086401 .
- ^ Прелог, Мартина; Уилк, Кордула; Келлер, Майкл; Каралл, Томас; Орт, Доротея; Гейгер, Ральф; Уолдер, Гернот; Лауфер, Гюнтер; Коттони, Марко; Циммерхакл Лотар, Бернд; Штейн, Йорг; Грубек-Лебенштайн, Беатрикс; Вюрцнер, Рейнхард (30 января 2008 г.). «Снижение реакции на вакцинацию против клещевого энцефалита у детей после тимэктомии» . Вакцина . 26 (5): 595–600. doi : 10.1016/j.vaccine.2007.11.074 . ISSN 0264-410X . ПМИД 18178293 .
- ^ Кушеш, Кэмерон А.; Фой, Броди Х.; Сайкс, Дэвид Б.; Густафссон, Карин; Скэдден, Дэвид Т. (3 августа 2023 г.). «Последствия для здоровья удаления тимуса у взрослых» . Медицинский журнал Новой Англии . 389 (5): 406–417. дои : 10.1056/NEJMoa2302892 . ISSN 0028-4793 . ПМЦ 10557034 . ПМИД 37530823 . S2CID 260377788 .
- ^ «Рецепты сладкого хлеба – BBC Food» . Би-би-си Еда . Проверено 12 декабря 2019 г.
- ^ Лидделл Х.Г., Скотт Р. «θυμός» . Греко-английский лексикон . Проверено 10 декабря 2019 г.
- ^ «тимус | Происхождение и значение тимуса в онлайн-этимологическом словаре» . www.etymonline.com . Проверено 10 декабря 2019 г.
- ^ Нишино М., Ашику С.К., Кохер О.Н., Тюрер Р.Л., Буазель П.М., Хатабу Х. (2006). «Тимус: всесторонний обзор». Рентгенография . 26 (2): 335–48. дои : 10.1148/rg.262045213 . ПМИД 16549602 .
- ^ Сапольский Р.М. (2004). Почему у зебр не бывает язв (3-е изд.). Нью-Йорк: Генри Холд и компания/Owl Books. стр. 182–185. ISBN 978-0805073690 .
- ^ Миллер Дж. Ф. (июль 2002 г.). «Открытие функции тимуса и лимфоцитов, происходящих из тимуса». Иммунологические обзоры . 185 (1): 7–14. дои : 10.1034/j.1600-065X.2002.18502.x . ПМИД 12190917 . S2CID 12108587 .
- ^ Миллер Дж. Ф. (июнь 2004 г.). «События, которые привели к открытию развития и функционирования Т-клеток - личные воспоминания». Тканевые антигены . 63 (6): 509–17. дои : 10.1111/j.0001-2815.2004.00255.x . ПМИД 15140026 .
- ^ Баджогли Б., Го П., Агааллаи Н., Хирано М., Стромайер С., МакКёрли Н. и др. (февраль 2011 г.). «Кандидат на тимус у миног». Природа 470 (7332): 90–4. Бибкод : 2011Природа.470…90Б . дои : 10.1038/nature09655 . ПМИД 21293377 . S2CID 4417477 .
- ^ Ривьер Х.Б., Купер Э.Л., Редди А.Л., Хильдеманн В.Х. (1975). «В поисках тимуса миксины» (PDF) . Американский зоолог . 15 (1): 39–49. дои : 10.1093/icb/15.1.39 . JSTOR 3882269 .
- ^ Тершовский Г., Мюллер С.М., Блеул С.С., Блюм С., Ширмбек Р., Рейманн Дж. и др. (апрель 2006 г.). «Доказательства функционального второго тимуса у мышей» . Наука . 312 (5771): 284–7. Бибкод : 2006Sci...312..284T . дои : 10.1126/science.1123497 . ПМИД 16513945 . S2CID 24553384 .
- ^ Суков, Марк А.; Стивенс, Карла А.; Уилсон, Рональд П. (2012). Лабораторный кролик, морская свинка, хомяк и другие грызуны . Академическая пресса. п. 583. ИСБН 978-0-12-380920-9 .
- ^ Гершвин, М. Эрик; Торговец, Брюс (2012). Иммунологические дефекты у лабораторных животных 1 . Springer Science & Business Media. п. 289. ИСБН 978-1-4757-0325-2 .
Книги
[ редактировать ]- Ралстон С.Х., Пенман И.Д., Страчан М.В., Хобсон Р.П., ред. (2018). Принципы и медицинская практика Дэвидсона (23-е изд.). Эльзевир. ISBN 978-0-7020-7028-0 .
- Каспер Д., Фаучи А., Хаузер С., Лонго Д., Джеймсон Дж., Лоскальцо Дж. (2015). Принципы внутренней медицины Харрисона (19-е изд.). МакГроу-Хилл Профессионал. ISBN 9780071802154 .
Внешние ссылки
[ редактировать ]- Развитие Т-клеток в тимусе. Видео Дженис Яу, описывающее стромальную передачу сигналов и толерантность. Кафедра иммунологии и биомедицинских коммуникаций Университета Торонто. Магистерский исследовательский проект, магистр наук в области биомедицинских коммуникаций. 2011.