Миастения гравис
| Миастения гравис | |
|---|---|
 | |
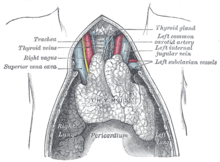
| Отклонение глаз и опущенное веко у человека с миастенией, пытающегося открыть глаза | |
| Специальность | Неврология |
| Симптомы | различной степени Мышечная слабость , двоение в глазах , опущение век , проблемы с речью, проблемы с ходьбой. [1] |
| Обычное начало | Женщины до 40 лет, мужчины старше 60 лет. [1] |
| Продолжительность | Долгосрочный [1] |
| Причины | Аутоиммунное заболевание [1] |
| Метод диагностики | Анализы крови на специфические антитела , эдрофониевый тест , исследования нервной проводимости. [1] |
| Дифференциальный диагноз | синдром Гийена-Барре , ботулизм , отравление фосфорорганическими соединениями , инсульт ствола мозга , [2] метаболические миопатии |
| Уход | Лекарственные препараты, хирургическое удаление тимуса , плазмаферез [1] |
| Медикамент | Ингибиторы ацетилхолинэстеразы ( неостигмин , пиридостигмин ), иммунодепрессанты [1] |
| Частота | От 50 до 200 на миллион [3] [4] |
Миастения гравис ( МГ ) — это хроническое заболевание нервно-мышечных соединений , которое приводит к различной степени слабости скелетных мышц . [1] Чаще всего поражаются мышцы глаз , лица и глотания. [1] [5] Это может привести к двоению в глазах , опущению век и трудностям при разговоре и ходьбе. [1] Начало может быть внезапным. [1] У больных часто наблюдается большой тимус или развивается тимома . [1]
Миастения гравис — аутоиммунное заболевание нервно-мышечного соединения, возникающее в результате действия антител , которые блокируют или разрушают никотиновые рецепторы ацетилхолина (АХР) в месте соединения нерва и мышцы . [6] [7] [1] Это не позволяет нервным импульсам вызывать мышечные сокращения. [1] Большинство случаев связано с антителами иммуноглобулина G1 (IgG1) и IgG3, которые атакуют AChR в постсинаптической мембране, вызывая опосредованное комплементом повреждение и мышечную слабость. [8] В редких случаях наследственный генетический дефект нервно -мышечного соединения приводит к аналогичному состоянию, известному как врожденная миастения . [9] [10] У детей, чьи матери страдают миастенией, в течение первых нескольких месяцев жизни могут наблюдаться симптомы, известные как неонатальная миастения. [1] или, более конкретно, преходящая неонатальная миастения . [11] Диагноз может быть подтвержден анализами крови на специфические антитела, тестом с эдрофонием , электромиографией (ЭМГ) или исследованием нервной проводимости . [1]
МГ обычно лечат препаратами, известными как ингибиторы ацетилхолинэстеразы , такими как неостигмин и пиридостигмин . [1] иммунодепрессанты , такие как преднизолон или азатиоприн . Также можно использовать [1] симптомы . В некоторых случаях хирургическое удаление тимуса может улучшить [1] Плазмаферез и высокие дозы внутривенного иммуноглобулина могут использоваться во время внезапных обострений заболевания. [1] Если дыхательные мышцы значительно ослабевают, искусственная вентиляция легких . может потребоваться [1] После интубации можно временно прекратить прием ингибиторов ацетилхолинэстеразы для уменьшения секреции в дыхательных путях. [12]
МГ поражает от 50 до 200 человек на миллион. [3] [4] Ежегодно его впервые диагностируют у 3–30 человек на миллион. [13] Диагноз стал более распространенным из-за возросшей осведомленности. [13] МГ чаще всего встречается у женщин в возрасте до 40 лет и у мужчин старше 60 лет. [1] [5] [14] У детей это редкость. [1] При лечении большинство из них живут до средней продолжительности жизни . [1] Это слово происходит от греческого mys — «мышца», astheneia — «слабость» и латинского gravis — «серьёзный». [15]
Признаки и симптомы
[ редактировать ]Начальным, основным симптомом МГ является безболезненная слабость определенных мышц, а не утомляемость. [16] Мышечная слабость прогрессивно усиливается ( утомляемость ) в периоды физической активности и уменьшается после периодов отдыха. Обычно слабость и утомляемость усиливаются к концу дня. [17] МГ обычно начинается со слабости глаз; затем оно может перейти в более тяжелую генерализованную форму, характеризующуюся слабостью конечностей или мышц, управляющих основными жизненными функциями. [18]
Глаза
[ редактировать ]Примерно у двух третей людей начальный симптом МГ связан с мышцами вокруг глаз. [16] Опущение век ( может возникнуть птоз из-за слабости мышцы, поднимающей верхнее веко ) [19] и двоение в глазах ( диплопия , [16] из-за слабости экстраокулярных мышц ). [17] Глазные симптомы имеют тенденцию ухудшаться при просмотре телевизора, чтении или вождении автомобиля, особенно при ярком освещении. [16] Следовательно, некоторые пострадавшие люди предпочитают носить солнцезащитные очки. [16] Термин «глазная миастения» описывает подтип МГ, при котором мышечная слабость ограничивается глазами, т.е. экстраокулярными мышцами, m. levator palpebrae Superioris и m. круговая мышца глаза . [19] Обычно этот подтип развивается в генерализованную МГ, обычно через несколько лет. [19]
Еда
[ редактировать ]Слабость мышц, участвующих в глотании, может привести к затруднению глотания ( дисфагии ). Обычно это означает, что некоторое количество пищи может остаться во рту после попытки проглотить. [20] или пища и жидкости могут срыгиваться в нос, а не в горло ( небно-глоточная недостаточность ). [17] Слабость мышц, которые двигают челюсть ( жевательные мышцы ), может вызывать затруднения при жевании. У людей с МГ жевание становится более утомительным при пережевывании жесткой, волокнистой пищи. [16] Трудности с глотанием, жеванием и речью являются первым симптомом примерно у одной шестой части людей. [16]
Говорящий
[ редактировать ]Слабость мышц, участвующих в разговоре, может привести к дизартрии и гипофонии . [16] Речь может быть медленной и невнятной, [21] или иметь гнусавость . [17] В некоторых случаях от певческого хобби или профессии приходится отказаться. [20]
Голова и шея
[ редактировать ]Из-за слабости мимики и жевательных мышц мимическая слабость может проявляться в виде невозможности держать рот закрытым. [16] («знак отвисшей челюсти») и как рычащее выражение лица при попытке улыбнуться. [17] При опущенных веках из-за слабости лица человек может выглядеть сонным или грустным. [16] Могут возникнуть трудности с удержанием головы в вертикальном положении. [21]
Другой
[ редактировать ]конечностей ; Также могут поражаться мышцы, контролирующие дыхание и движения они редко проявляются как первые симптомы МГ, но развиваются в течение месяцев или лет. [22] При миастеническом кризе возникает паралич дыхательных мышц, что требует вспомогательной вентиляции для поддержания жизни. [23] Кризы могут быть вызваны различными биологическими стрессорами, такими как инфекция, лихорадка, нежелательная реакция на лекарства или эмоциональный стресс. [23]
Причина
[ редактировать ]Лекарства, которые вызывают или ухудшают МГ
[ редактировать ]Антибиотики , который телитромицин ( больше из семейства антибиотиков макролидов азитромицин не доступен на рынке США) и эритромицин . Сообщается, что усугубляют МГ. Сообщается, что из семейства фторхинолоновых антибиотиков ципрофлоксацин , норфлоксацин , офлоксацин , моксифлоксацин и моксифлоксацин усугубляют МГ. [24] Сообщается , что из аминогликозидов семейства антибиотиков гентамицин , стрептомицин и неомицин усугубляют МГ. [25] аминогликозид тобрамицин усугубляет МГ, и его можно применять у пациентов, которым требуется лечение аминогликозидами. Не сообщалось о том, что [24] Из-за редкости или отсутствия сообщений об обострении МГ у больных МГ считаются безопасными для применения следующие антибиотики: препараты цефалоспоринового класса, сульфаниламидные препараты , препараты тетрациклиновой группы , клиндамицин , полимиксин В и нитрофурантоин . [24]
Ингибиторы иммунных контрольных точек . Ингибиторы иммунных контрольных точек стимулируют определенные типы аутоиммунных реакций, блокируя пути контрольных точек, которые ингибируют эти реакции. Они используются для лечения рака, который способствует собственному росту и распространению путем стимуляции контрольных точек. К этим ингибиторам контрольных точек относятся пембролизумаб , ниволумаб , ипилимумаб , авелумаб , атезолизумаб и дурвалумаб . Из общего числа 5898 пациентов, получавших эти препараты, у 52 развилась новая МГ, а у 11 - обострение уже существующей МГ. Симптомы МГ развивались в течение от 6 дней до 16 недель (среднее время 4 недели). Симптомы МГ, вызванные приемом лекарств, часто были тяжелыми: у 29 пациентов развилась дыхательная недостаточность , потребовавшая искусственной вентиляции легких . [26] Другие исследования показали, что эти ингибиторы контрольных точек вызывают дыхательную недостаточность у 45% и смерть у 25–40% пациентов. [24] [27] Предполагается, что этих препаратов лучше избегать у пациентов с МГ, особенно у пациентов, у которых ранее была опасная для жизни реакция на них. Если эти препараты необходимо использовать у пациентов с МГ, рекомендуется предварительное лечение пациентов глюкокортикоидами , плазмаферезом или внутривенным иммуноглобулином , чтобы снизить вероятность развития тяжелых симптомов. [24]
Статины : Статины — это препараты, снижающие уровень холестерина в крови . В обзоре 169 пациентов, у которых сообщалось о развитии МГ или ухудшении симптомов МГ при приеме статинов (т. е. симвастатина , аторвастатина , розувастатина , правастатина , ловастатина или флувастатина ), у 138 развилась генерализованная МГ, у 13 - глазная МГ, и у 18 наблюдалось ухудшение МГ. После прекращения приема статинов и лечения МГ 63 пациента полностью выздоровели, 27 пациентов выздоровели, 19 пациентов еще не выздоровели, 5 пациентов выздоровели, но симптомы сохранялись, 1 пациент умер, при этом данных последующего наблюдения не было. 54 пациента. Среди этих случаев 56% были признаны серьезными. [28] Нестатиновые препараты, снижающие уровень холестерина (например, ниацин и секвестрирующие желчные кислоты препараты, холестирамин , , колестипол , колесевелам , алирокумаб и эволокумаб ) применялись у пациентов, не вызывая и не ухудшая МГ. Рекомендуется прекратить прием статинов, а затем избегать приема всех статинов в тех редких случаях, когда статин вызывал развитие или ухудшение МГ. [24]
Антиаритмические средства Ia . Антиаритмические средства типа Ia (см. классификацию Воана Уильямса ), т. е. прокаинамид , который используется для лечения сердечных аритмий , вызывал дыхательную недостаточность у пациентов с МГ, у которых до начала лечения им не было респираторных симптомов. Кроме того, этот препарат вызывает симптомы, подобные МГ, у пациентов с почечной недостаточностью, но без МГ. А прокаинамид усугубил мышечную дисфункцию на крысиной модели человеческого MG. Эти исследования показывают, что прокаинамид, как и другие антиаритмические средства типа Ia, следует избегать или применять с особой осторожностью у пациентов с МГ. [24]
Деполяризующие нервно-мышечные блокаторы . Деполяризующие нервно-мышечные блокаторы подавляют передачу сигналов нейронами в нервно-мышечных соединениях, тем самым уменьшая сократимость пораженных скелетных мышц. Эти блокаторы используются в качестве миорелаксантов у пациентов, перенесших операцию. [29] Сукцинилхолин — единственный деполяризующий нервно-мышечный блокатор, доступный на рынке США. [24] Способность сукцинилхолина индуцировать или ухудшать МГ неясна. Было высказано предположение, что он вызывает опасные для жизни побочные эффекты, такие как рабдомиолиз , миотония и гиперкалиемия у пациентов с мышечными заболеваниями, хотя роль сукцинилхолина в возникновении этих побочных эффектов также остается неясной. [29] До тех пор, пока не станет доступно больше данных по этим вопросам и пока не появятся другие нервно-мышечные блокаторы без этих вредных побочных эффектов, использования сукцинилхолина при МГ (и других нервно-мышечных расстройствах), вероятно, следует избегать, где это возможно. [24] [29]
Ингаляционные анестетики : Ингаляционные анестетики — это общие анестетики , которые вводятся ингаляционно, как правило, пациентам, перенесшим операцию. У пациентов с МГ, перенесших операцию с применением ингаляционных анестетиков (т.е. галотана , изофлурана , энфлюрана и севофлурана ), может развиться нервно-мышечная блокада и увеличиться риск развития опасного для жизни криза миастении, который необходимо лечить длительной искусственной вентиляцией легких. В исследовании 795 пациентов с МГ, перенесших хирургическое удаление тимуса под общей анестезией, сугаммадекс , нервно-мышечный блокирующий препарат (т.е. препарат, который устраняет нервно-мышечную блокаду), значительно уменьшал развитие этого криза. [24] [30] Эти исследования показывают, что лучше избегать применения ингаляционных анестетиков у пациентов с МГ, но в случае их использования следует проводить тщательный послеоперационный мониторинг для пациентов с МГ, анестезируемых этими препаратами. [24] и сугаммадекс следует рассматривать для рутинного использования у пациентов с МГ, анестезированных этими препаратами, которым проводится тимэктомия. [31] или другие виды хирургического вмешательства. [24]
Глюкокортикоиды . Глюкокортикоиды представляют собой противовоспалительные средства, которые в первоначальных исследованиях использовались в высоких дозах и, как было обнаружено, ухудшали МГ в 25–75% случаев. [32] Однако дальнейшие исследования показали, что глюкокортикоиды оказывают благоприятное воздействие на МГ при длительном приеме. Два глюкокортикоида, пероральный преднизолон и преднизолон терапией первой линии , в настоящее время являются иммуносупрессивной при МГ. Чтобы избежать обострения МГ, рекомендуется начинать прием кортикостероидов с низкой дозы и постепенно увеличивать ее до дозы, обеспечивающей максимальный ответ. Для достижения более быстрого терапевтического ответа в случаях тяжелых симптомов МГ рекомендуется начинать с высоких доз пероральных или внутривенных глюкокортикоидов после первого лечения пациентов с помощью плазмафереза или внутривенной терапии иммуноглобулинами, каждый из которых снижает вероятность возникновения тяжелой реакции на кортикостероиды. [24] [33] [34]
Блокаторы кальциевых каналов . Блокаторы кальциевых каналов (например, фелодипин , нифедипин и верапамил ) представляют собой препараты, снижающие артериальное давление у пациентов с гипертонией . Сообщается, что фелодипин и нифедипин ухудшают МГ, а нифедипин и верапамил вызывают дыхательную недостаточность у пациентов с тяжелой генерализованной МГ. Пациентов с МГ, особенно тех, кто находится в стадии ремиссии или имеет хорошо контролируемое заболевание, обычно можно лечить этими блокаторами, используя их самые низкие эффективные дозы и тщательно контролируя ухудшение симптомов МГ. [24]
Пеницилламин : Пеницилламин представляет собой препарат хелатной терапии, используемый для лечения различных заболеваний (например, болезни Вильсона ). Примерно у 1-2% лиц, длительно получавших пеницилламин, развивается МГ и/или развиваются низкие концентрации антител к АХР. [35] Их МГ часто бывает легкой и преимущественно глазной МГ, становится очевидной обычно через 6–7 месяцев (от одного месяца до 8 лет) после начала приема препарата и переходит в полную ремиссию в 70% случаев в течение 6–10 месяцев после отмены препарата. . Рекомендуется прекратить прием пеницилламина и в дальнейшем избегать его применения у пациентов, у которых при лечении им развиваются симптомы МГ. [24]
Ботулинический токсин А : Ботулинический токсин А (продаваемый под торговыми марками Botox, Jeuveau и Xeomin) блокирует передачу в нервно-мышечных соединениях, парализуя мышцы, в которые он вводится. Местные инъекции ботулотоксина А в косметических целях иногда вызывали слабость отдаленных мышц, симптомы, напоминающие глазную или генерализованную МГ у лиц с субклинической МГ, а также обострения ранее контролируемой МГ. Ботулинический токсин А также использовался для лечения спазматической кривошеи (т. е. непроизвольного поворота шеи), блефароспазма (непроизвольного сокращения век) и других неконтролируемых спазмов лицевых мышц у пациентов с МГ без побочных эффектов или только с кратковременной дисфагией или диплопией. . Предполагается, что лечения ботулиническим токсином А лучше избегать у пациентов с МГ, но его можно предлагать с осторожностью пациентам с легкой или стабильной МГ, используя постепенное увеличение дозировок и тщательный мониторинг. [24]
Магний : Магний — это химический элемент , который блокирует сокращение скелетных мышц, ингибируя высвобождение ацетилхолина в нервно-мышечных соединениях, а также снижая чувствительность этих мышц к ацетилхолину. [24] Дыхательная недостаточность возникала после системного применения магния (в основном в виде внутривенных инъекций сульфата магния ) при преэклампсии и после заместительной терапии магнием во время госпитализации у пациентов с сопутствующей МГ. [24] [36] Предполагается, что магний при внутривенном введении или пероральном введении в высоких дозах следует применять пациентам с МГ с особой осторожностью. [24]
Местные анестетики : Местные анестетики вызывают отсутствие боли и всех других ощущений в определенной части тела без потери сознания. Существует два широких класса этих анестетиков: сложные эфиры (т.е. лидокаин , бупивакаин , этидокаин , левобупивакаин , мепивакаин , прилокаин и ропивакаин амиды (т.е. новокаин , кокаин , тетракаинбензокаин ) и и хлорпрокаин ). Эфирные местные анестетики метаболизируются псевдохолинэстеразами , что у пациентов с МГ, принимающих антихолинэстеразные препараты, может привести к чрезмерному повышению уровня этих эфирных анестетиков. Амидные местные анестетики не метаболизируются псевдохолинэстеразами. Исходя из этих соображений, у пациентов с МГ амидные местные анестетики предпочтительнее эфирных. [37] [38]
Другие лекарственные средства. Редкие случаи обострения МГ были зарегистрированы у пациентов, получавших: 1) пенициллины , т.е. ампициллин и амоксициллин ; 2) противораковые препараты, т.е. лорлатиниб , нилотиниб , иматиниб (эти три препарата являются ингибиторами тирозинкиназы , которые также могут вызывать МГ), дабрафениб и траметиниб ; 3) антипсихотические препараты, т.е. хлорпромазин , пимозид , тиоридазин , клозапин , оланзапин , галоперидол , кветиапин , рисперидон и оланзапин ; 4) ИФН-α (также может вызывать МГ); и 5) химический элемент литий . Эти препараты можно использовать у пациентов с МГ, поскольку сообщения об обострении (или индукции) МГ у них редки. [24]
Патофизиология
[ редактировать ]МГ — аутоиммунная синаптопатия . Заболевание возникает, когда иммунная система дает сбой и вырабатывает антитела, атакующие ткани организма. Антитела в MG атакуют нормальный человеческий белок, никотиновый рецептор ацетилхолина или родственный ему белок под названием MuSK , специфическую для мышц киназу. [39] [40] Другие, менее частые антитела обнаруживаются против белков LRP4 , агрина и титина . [8] [41]
Гаплотипы лейкоцитарного антигена человека связаны с повышенной восприимчивостью к миастении и другим аутоиммунным заболеваниям. У родственников людей с миастенией наблюдается более высокий процент других иммунных нарушений. [42] [43]
Клетки вилочковой железы являются частью иммунной системы организма. У больных миастенией вилочковая железа имеет большие размеры и имеет аномальную форму. Иногда он содержит скопления иммунных клеток, что указывает на лимфоидную гиперплазию, а вилочковая железа может давать неверные инструкции иммунным клеткам. [44]
- Нервно-мышечный переход: 1. Аксон 2. Мембрана мышечной клетки 3. Синаптический везикула 4. Никотиновый рецептор ацетилхолина 5. Митохондрия.
- Ювенильный тимус с возрастом уменьшается.
- Никотиновый рецептор ацетилхолина
Во время беременности
[ редактировать ]Известно, что у беременных женщин, уже имеющих МГ, в трети случаев наблюдается обострение симптомов, и в этих случаях это обычно происходит в первом триместре беременности. [45] Признаки и симптомы у беременных имеют тенденцию к улучшению во втором и третьем триместрах . полная ремиссия . У некоторых матерей может наблюдаться [46] Иммуносупрессивную терапию следует продолжать на протяжении всей беременности, поскольку она снижает вероятность мышечной слабости новорожденных и контролирует миастению у матери. [47]
Около 10–20% младенцев, матери которых страдают этим заболеванием, рождаются с преходящей неонатальной миастенией (ТНМГ), которая обычно вызывает с кормлением и дыханием , которые развиваются примерно от 12 часов до нескольких дней после рождения. трудности [45] [47] Ребенок с ТНМГ обычно очень хорошо реагирует на ингибиторы ацетилхолинэстеразы, и состояние обычно проходит в течение трех недель по мере уменьшения количества антител и обычно не приводит к каким-либо осложнениям. [45] Однако у небольшого процента плодов и новорожденных с TNMG, особенно у тех, у кого есть антитела, направленные против фетальной формы AChR (их заболевание представляет собой подтип TNMG, называемый «синдром инактивации ацетилхолиновых рецепторов»), наблюдается более тяжелая форма TNMG, которая включает слабость скелетных мышц, регулирующих дыхание, дыхательную недостаточность и различные деформации, такие как врожденный множественный артрогрипоз . В некоторых из этих случаев мать остается бессимптомной . [47] [48]
Диагностика
[ редактировать ]МГ может быть трудно диагностировать, поскольку симптомы могут быть едва заметными и их трудно отличить как от нормальных вариантов, так и от других неврологических расстройств. [20]
У детей можно выделить три типа миастенических симптомов: [49]
- Транзиторная неонатальная миастения встречается у 10–15% детей, рожденных от матерей, страдающих этим заболеванием, и исчезает через несколько недель.
- Врожденная миастения, самая редкая форма, возникает при наличии генов от обоих родителей.
- Ювенильная миастения чаще всего встречается у женщин.
Врожденные миастении вызывают мышечную слабость и утомляемость, сходные с таковыми при МГ. [50] Признаки врожденной миастении обычно присутствуют в первые годы детства, хотя их можно не распознать до взрослой жизни. [51]
Классификация подгрупп
[ редактировать ]| Сорт | Описание |
|---|---|
| я | Любая слабость глазных мышц, возможный птоз , отсутствие других признаков мышечной слабости в других местах. |
| II | Слабость глазных мышц любой степени тяжести, легкая слабость других мышц. |
| IIа | Преимущественно конечности или осевые мышцы |
| IIб | Преимущественно бульбарные и/или дыхательные мышцы |
| III | Слабость глазных мышц любой степени выраженности, умеренная слабость других мышц. |
| IIIа | Преимущественно конечности или осевые мышцы |
| IIIб | Преимущественно бульбарные и/или дыхательные мышцы |
| IV | Слабость глазных мышц любой степени тяжести, выраженная слабость других мышц. |
| IVа | Преимущественно конечности или осевые мышцы |
| IVб | Преимущественно бульбарные и/или дыхательные мышцы |
| V | Интубация необходима для поддержания проходимости дыхательных путей |
При диагнозе МГ пациента можно разделить на отдельные подгруппы на основе клинических особенностей и серологического статуса, например, пораженной группы мышц, возраста начала заболевания, нарушений тимуса и профиля аутоантител в сыворотке. [53]
В зависимости от пораженной группы мышц пациентов можно разделить на глазную МГ или генерализованную МГ. Глазная МГ характеризуется исключительно глазными симптомами, опущением век или двоением в глазах. Генерализованная МГ характеризуется мышечной слабостью с вариабельным сочетанием бульбарных, осевых мышц или мышц конечностей и дыхательных мышц. [54]
Пациентов также можно разделить на подгруппы по возрасту начала: ювенильный МГ (возраст начала ≤ 18 лет), ранний МГ (EOMG; 19–50 лет), поздний МГ (LOMG; начало > 50 лет) и с очень поздним началом (VLOMG; возраст начала ≥ 65 лет). [55]
Подгруппа профиля аутоантител включает серопозитивные по AChR, серопозитивные по MuSK, серопозитивные по LRP4 и серопозитивные по агрину. [56]
Физический осмотр
[ редактировать ]Во время медицинского осмотра на наличие МГ врач может попросить человека выполнить повторяющиеся движения. Например, врач может попросить человека смотреть в фиксированную точку в течение 30 секунд и расслабить мышцы лба, поскольку человек с МГ и птозом глаз может непроизвольно задействовать мышцы лба для компенсации слабости глаз. веки. [20] Клинический эксперт также может попытаться вызвать у человека «признак занавески», удерживая один глаз человека открытым, что в случае МГ приведет к закрытию другого глаза. [20]
Анализы крови
[ редактировать ]При подозрении на диагноз серологическое исследование можно провести :
- Один тест предназначен для выявления антител против рецептора ацетилхолина; [20] тест имеет разумную чувствительность 80–96%, но при глазной миастении чувствительность падает до 50%.
- У части людей, не имеющих антител к рецептору ацетилхолина, имеются антитела против белка MuSK. [57]
- В особых ситуациях проводится тестирование на синдром Ламберта-Итона . [58]
Электродиагностика
[ редактировать ]

Мышечные волокна людей с МГ легко утомляются, что может помочь диагностировать повторяющийся тест на стимуляцию нервов . При одноволоконной электромиографии , которая считается наиболее чувствительным (хотя и не самым специфичным) тестом на МГ, [20] тонкий игольчатый электрод вводится в разные области определенной мышцы для регистрации потенциалов действия из нескольких образцов разных отдельных мышечных волокон. Идентифицируются два мышечных волокна, принадлежащие к одной и той же двигательной единице, и измеряется временная изменчивость их паттернов активности. Частота и доля определенных аномальных паттернов потенциала действия, называемых «дрожанием» и «блокировкой», являются диагностическими. Джиттер – это аномальное изменение временного интервала между потенциалами действия соседних мышечных волокон в одной и той же двигательной единице. Блокировка означает неспособность нервных импульсов вызвать потенциалы действия в соседних мышечных волокнах одной и той же двигательной единицы. [59]
Ледяной тест
[ редактировать ]Сообщается, что прикладывание льда к мышцам на 2–5 минут имеет чувствительность и специфичность 76,9% и 98,3% соответственно для идентификации МГ. Считается, что ацетилхолинэстераза ингибируется при более низкой температуре, что является основой для этого диагностического теста. Обычно это делается на веках при наличии птоза и считается положительным, если после удаления льда происходит подъем века на ≥2 мм. [60]
Эдрофониевый тест
[ редактировать ]Этот тест требует внутривенного введения хлорида эдрофония или неостигмина — препаратов, которые блокируют расщепление ацетилхолина холинэстеразой (ингибиторы ацетилхолинэстеразы). [61] Этот тест обычно больше не проводится, поскольку его использование может привести к опасной для жизни брадикардии (замедлению сердечного ритма), которая требует немедленной неотложной помощи. [62] Производство эдрофония было прекращено в 2008 году. [23]
Визуализация
[ редактировать ]Рентгенография грудной клетки может выявить расширение средостения , свидетельствующее о тимоме, но компьютерная томография или магнитно-резонансная томография (МРТ) являются более чувствительными способами выявления тимом и обычно проводятся по этой причине. [63] МРТ черепа и орбит также можно проводить для исключения компрессионных и воспалительных поражений черепных нервов и глазных мышц. [64]
Легочный функциональный тест
[ редактировать ]Форсированную жизненную емкость можно контролировать через определенные промежутки времени, чтобы обнаружить нарастающую мышечную слабость. В остром периоде отрицательную силу вдоха для определения адекватности вентиляции можно использовать ; его проводят людям с MG. [65] [66]
Дифференциальный диагноз
[ редактировать ]Мышечная слабость, которая усиливается при физической активности (аномальная мышечная утомляемость ) при миастении гравис. [67] является симптомом, характерным для других нервно-мышечных заболеваний. Большинство метаболических миопатий , таких как болезнь МакАрдла (GSD-V), характеризуются аномальной мышечной утомляемостью, а не фиксированной мышечной слабостью. [68] [69] Также, как и при миастении, [67] непереносимость физических упражнений при болезни МакАрдла улучшается при регулярной физической активности (выполняемой безопасно с использованием таких адаптаций к активности, как открытие второго дыхания , «правило 30 из 80» и «правило шести секунд»). [70] [71] У небольшого меньшинства пациентов с болезнью МакАрдла также имеется сопутствующее заболевание птоз (опущение верхнего века). [72] GSD-II с поздним началом ( болезнь Помпе ) и GSD-XV также имеют мышечную слабость или утомляемость с сопутствующими заболеваниями, такими как птоз и офтальмоплегия; как и многие митохондриальные миопатии . [73]
Другие заболевания, сопровождающиеся аномальной мышечной усталостью (которую можно охарактеризовать как мышечную слабость, вызванную физической нагрузкой, обратимую мышечную слабость или мышечную слабость, которая проходит после отдыха), включают: эндокринные миопатии (такие как синдром Хоффмана ), тубулярную агрегатную миопатию (ТАМ), ишемию . (такие как перемежающаяся хромота , синдром ущемления подколенной артерии и хроническая венозная недостаточность ), а также неправильное питание или заболевания мальабсорбции, которые приводят к дефициту витамина D (остеомальная миопатия). Хотя поясно- конечностные мышечные дистрофии (LGMD) сопровождаются фиксированной мышечной слабостью, LGMDR8 также предполагает мышечную утомляемость; [74] как и некоторые мышечные дистрофии-дистрогликанопатии конечностей, такие как MDDGC3 (также известные как LGMDR15 и LGMD2O). [73] [75] Миофибриллярная миопатия 10, [76] дефицит диметилглициндегидрогеназы, [77] дефект транспортера лактата эритроцитов, [78] и миопатия с миалгией, повышением уровня креатинкиназы в сыворотке, с эпизодическим рабдомиолизом или без него (MMCKR) [79] также включают мышечную усталость.
Х-сцепленная эпизодическая мышечная слабость (ЭМСС) включает общую мышечную слабость, птоз и колебания силы. У некоторых людей была заметна утомляемость, фенотип имел черты, сравнимые с врожденными миастеническими синдромами и каналопатиями . [80]
Признаки и симптомы миастении, проявляющиеся с младенчества или детства, могут быть одним из врожденных миастенических синдромов , которые могут наследоваться как по аутосомно-доминантному, так и по рецессивному типу. В настоящее время известно более двух десятков типов врожденных миастенических синдромов. [81]
Конечностно-поясная миастения отличается от миастении. Это аутоиммунное заболевание, возникающее у взрослых, поражающее нервно-мышечные соединения. Однако при нем отсутствуют глазные аномалии, и он связан с аутоиммунными состояниями, такими как системная красная волчанка, тиреоидит Хашимото и тимома. [82]
Миастенический синдром Ламберта-Итона (LEMS) — это аутоиммунное заболевание, поражающее нервно-мышечные соединения, либо как паранеопластический синдром (обычно у пожилых пациентов), либо связанное с нераковым первичным аутоиммунным заболеванием (обычно у молодых пациентов). Обычно оно включает слабость нижних конечностей и утомляемость, вызванную физической нагрузкой, хотя могут также поражаться верхние конечности и глаза. Признак Ламберта — необычное улучшение силы хвата, которое следует после сжимания руки с максимальной интенсивностью в течение 2–3 секунд. [83]
Управление
[ редактировать ]Лечение заключается в приеме лекарств и/или хирургическом вмешательстве. Лекарства состоят в основном из ингибиторов ацетилхолинэстеразы для непосредственного улучшения мышечной функции и иммунодепрессантов для уменьшения аутоиммунного процесса. [5] [84] Тимэктомия – хирургический метод лечения МГ. [85]
Медикамент
[ редактировать ]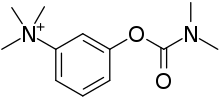
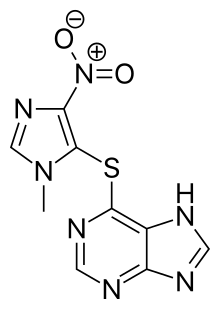
Около 10% людей с генерализованной МГ считаются резистентными к лечению . [86] Аутологичная трансплантация гемопоэтических стволовых клеток (ТГСК) иногда используется при тяжелой, резистентной к лечению МГ. Имеющиеся данные предоставляют предварительные доказательства того, что ТГСК может быть эффективным терапевтическим вариантом в тщательно отобранных случаях. [87]
Эфгартигимод альфа (Вивгарт) был одобрен для медицинского применения в США в декабре 2021 года. [88] [89] [90]
Эфгартигимод альфа/гиалуронидаза (Vyvgart Hytrulo) был одобрен для медицинского применения в США в июне 2023 года. [91] [92]
Розаноликизумаб (Ристигго) был одобрен для медицинского применения в США в июне 2023 года. [93] [94]
Ингибиторы ацетилхолинэстеразы
[ редактировать ]Ингибиторы ацетилхолинэстеразы могут принести симптоматическую пользу, но не могут полностью устранить слабость человека от MG. [95] Хотя они не могут полностью устранить все симптомы МГ, они все же могут позволить человеку выполнять нормальную повседневную деятельность. [95] Обычно прием ингибиторов ацетилхолинэстеразы начинают с низкой дозы и увеличивают ее до достижения желаемого результата. Если принять за 30 минут до еды, симптомы будут слабыми во время еды, что полезно для тех, у кого проблемы с глотанием из-за болезни. Другой препарат, используемый при МГ, атропин , может уменьшить мускариновые побочные эффекты ингибиторов ацетилхолинэстеразы. [96] Пиридостигмин является препаратом относительно длительного действия (по сравнению с другими холинергическими агонистами), с периодом полувыведения около четырех часов и относительно небольшим количеством побочных эффектов. [97] Обычно ее прекращают у тех, кто находится на искусственной вентиляции легких, поскольку известно, что она увеличивает количество слюнных выделений. [97] В нескольких высококачественных исследованиях ингибиторы холинэстеразы напрямую сравнивались с другими методами лечения (или плацебо); их практическая польза может быть настолько значительной, что проведение исследований, в которых они были бы скрыты от некоторых людей, было бы затруднительно. [84]
Иммунодепрессанты
[ редактировать ]Для достижения лучшего результата также можно использовать стероид преднизолон , но он может привести к ухудшению симптомов, и для достижения максимальной эффективности требуются недели. [97] Исследования показывают, что до 15% пациентов не реагируют положительно на иммуносупрессанты. [98] [99] [5] Из-за множества симптомов, которые может вызвать стероидное лечение, это не предпочтительный метод лечения. [97] Также могут использоваться другие иммуносупрессивные препараты, включая ритуксимаб. [100] или азатиоприн . [1]
Плазмаферез и ВВИГ
[ редактировать ]Если миастения серьезная (миастенический криз), можно использовать плазмаферез для удаления предполагаемых антител из кровообращения. Кроме того, внутривенные иммуноглобулины для связывания циркулирующих антител можно использовать (ВВИГ). Оба эти метода лечения имеют относительно кратковременный эффект, обычно измеряемый неделями, и часто связаны с высокими затратами, что делает их непомерно высокими; они обычно предназначены для случаев, когда MG требует госпитализации. [97] [101]
Операция
[ редактировать ]Поскольку тимомы наблюдаются у 10% всех людей с МГ, им часто делают рентгенографию грудной клетки и компьютерную томографию, чтобы оценить необходимость хирургического удаления вилочковой железы и любой раковой ткани, которая может присутствовать. [23] [62] Даже если проводится операция по удалению тимомы, она, как правило, не приводит к ремиссии МГ. [97] Хирургическое вмешательство в случае МГ включает удаление тимуса, хотя в 2013 году не было выявлено явных преимуществ, за исключением наличия тимомы. [102] Однако рандомизированное контролируемое исследование 2016 года выявило некоторые преимущества. [103]
Физические меры
[ редактировать ]Людей с МГ следует информировать о меняющемся характере их симптомов, включая слабость и утомляемость, вызванную физической нагрузкой. Участие в упражнениях следует поощрять частым отдыхом. [18] Некоторые данные указывают на то, что у людей с генерализованной МГ частичная домашняя программа, включающая обучение диафрагмальному дыханию , дыханию через поджатые губы и интервальную мышечную терапию, может улучшить силу дыхательных мышц, подвижность грудной клетки, характер дыхания и дыхательную выносливость. [104]
Медицинская визуализация
[ редактировать ]У людей с миастенией более старые формы йодсодержащего контраста, используемые для медицинской визуализации, вызывали повышенный риск обострения заболевания, но современные формы не имеют немедленного повышения риска. [105]
Прогноз
[ редактировать ]Прогноз для людей с МГ, как правило, хороший, как и качество жизни при очень хорошем лечении. [106] Мониторинг человека с МГ очень важен, поскольку по крайней мере у 20% людей с диагнозом МГ в течение двух лет после постановки диагноза возникает миастенический криз, требующий быстрого медицинского вмешательства. [97] Как правило, наиболее инвалидизирующий период МГ может длиться годы после первоначального диагноза. [95] Для облегчения передвижения могут потребоваться вспомогательные устройства. [1] В начале 1900-х годов 70% выявленных случаев умирали от проблем с легкими; теперь это число оценивается примерно в 3–5%, и это улучшение связано с повышением осведомленности и приемом лекарств для лечения симптомов. [97]
Эпидемиология
[ редактировать ]МГ встречается во всех этнических группах и обоих полах. Чаще всего от него страдают женщины до 40 лет и люди от 50 до 70 лет любого пола, но известно, что оно возникает в любом возрасте. У молодых людей тимома встречается редко. Распространенность в Соединенных Штатах оценивается от 0,5 до 20,4 случаев на 100 000, при этом, по оценкам, пострадало 60 000 американцев. [23] [107] В Соединенном Королевстве на 100 000 человек приходится примерно 15 случаев МГ. [62] Смертность от МГ составляет около 5-9%. [108]
История
[ редактировать ]Первыми о MG написали Томас Уиллис , Сэмюэл Уилкс , Эрб и Гольдфлам. [19] Термин «псевдопаралитическая миастения гравис» был предложен в 1895 году немецким врачом Жолли. [19] Мэри Уокер лечила человека с МГ физостигмином в 1934 году. [19] Симпсон и Настук подробно описали аутоиммунную природу заболевания. [19] В 1973 году Патрик и Линдстром на кроликах показали, что иммунизация очищенными мышечными рецепторами ацетилхолина вызывает развитие MG-подобных симптомов. [19]
Исследовать
[ редактировать ]В настоящее время исследуются иммуномодулирующие вещества, такие как препараты, которые предотвращают модуляцию рецептора ацетилхолина иммунной системой. [109] В последнее время некоторые исследования были посвящены ингибиторам анти-c5 в целях лечения, поскольку они безопасны и используются при лечении других заболеваний. [14] Кажется, что эфедрин приносит некоторым людям больше пользы, чем другие лекарства, но по состоянию на 2014 год он не был должным образом изучен. [10] [110] В лаборатории МГ преимущественно изучают на модельных организмах, например на грызунах. Кроме того, в 2015 году ученые разработали in vitro функциональный анализ нервно-мышечных соединений человека in vitro на основе эмбриональных стволовых клеток и стволовых клеток сомато-мышечных клеток. После добавления патогенных антител против рецептора ацетилхолина и активации системы комплемента нервно-мышечная совместная культура проявляет такие симптомы, как ослабление мышечных сокращений. [111] В последние годы ученые работают над поиском надежных биомаркеров МГ для мониторинга развития заболевания и оценки его тяжести.
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С «Информационный бюллетень по миастении гравис» . Национальный институт неврологических расстройств и инсульта . Архивировано из оригинала 16 сентября 2021 года . Проверено 22 сентября 2021 г.
- ^ Кахан С. (2005). На странице: Неврология . Липпинкотт Уильямс и Уилкинс. п. 118. ИСБН 978-1-4051-0432-6 . Архивировано из оригинала 8 сентября 2017 года.
- ^ Jump up to: а б Камински HJ (2009). Миастения Гравис и связанные с ней расстройства (2-е изд.). Springer Science & Business Media. п. 72. ИСБН 978-1-59745-156-7 . Архивировано из оригинала 8 сентября 2017 года.
- ^ Jump up to: а б Адамс Дж.Г. (2012). Неотложная медицина: Основы клинической помощи (2-е изд.). Elsevier Науки о здоровье. п. 844. ИСБН 978-1-4557-3394-1 . Архивировано из оригинала 8 сентября 2017 года.
- ^ Jump up to: а б с д Салари Н., Фатахи Б., Бартина Ю., Каземиния М., Фатахян Р., Мохаммади П. и др. (декабрь 2021 г.). «Глобальная распространенность миастении и эффективность распространенных лекарств при ее лечении: систематический обзор и метаанализ» . Журнал трансляционной медицины . 19 (1): 516. doi : 10.1186/s12967-021-03185-7 . ПМЦ 8686543 . ПМИД 34930325 .
- ^ Янг С., Макгилл, Южная Каролина (апрель 2021 г.). Ритуксимаб для лечения миастении гравис: обновленная информация на 2021 год [Интернет] (отчет). Оттава (Онтарио): Канадское агентство по лекарствам и технологиям в здравоохранении. PMID 34255447 . Архивировано из оригинала 7 июля 2022 года . Проверено 27 января 2022 г.
- ^ Даби А., Солиман Н., Курукумби М., Кальянам Дж. (2012). «Миастения Гравис: обзор» . Аутоиммунные заболевания . 2012 : 1–10. дои : 10.1155/2012/874680 . ПМК 3501798 . ПМИД 23193443 .
- ^ Jump up to: а б Филлипс В.Д., Винсент А. (1 января 2016 г.). «Патогенез миастении гравис: обновленная информация о типах заболеваний, моделях и механизмах» . F1000Исследования . 5 : 1513. doi : 10.12688/f1000research.8206.1 . ПМЦ 4926737 . ПМИД 27408701 .
- ^ Кандел Э., Шварц Дж., Джессел Т., Сигельбаум С., Хадспет А. (2012). Принципы нейронауки (5-е изд.). стр. 318–319.
- ^ Jump up to: а б Вринтен С., ван дер Цвааг А.М., Вайнрайх СС, Шолтен Р.Дж., Вершуурен Дж.Дж. (декабрь 2014 г.). «Эфедрин при миастении, неонатальной миастении и врожденных миастенических синдромах» . Кокрановская база данных систематических обзоров . 2014 (12): CD010028. дои : 10.1002/14651858.CD010028.pub2 . ПМЦ 7387729 . ПМИД 25515947 .
- ^ Линдроос Дж.Л., Бьорк М.Х., Гилхус Н.Е. (февраль 2024 г.). «Транзиторная неонатальная миастения гравис как частое осложнение редкого заболевания: систематический обзор» . Журнал клинической медицины . 13 (4): 1136. doi : 10.3390/jcm13041136 . ПМЦ 10889526 . ПМИД 38398450 .
- ^ Годой Д.А., Мелло Л.Дж., Масотти Л., Ди Наполи М. (сентябрь 2013 г.). «Миастенический пациент в кризисе: обновленная информация о ведении отделения нейрореанимации» . Arquivos de Neuro-Psiquiatria . 71 (9А): 627–39. дои : 10.1590/0004-282X20130108 . ПМИД 24141444 .
- ^ Jump up to: а б МакГроган А., Снеддон С., де Врис К.С. (2010). «Заболеваемость миастенией: систематический обзор литературы». Нейроэпидемиология . 34 (3): 171–183. дои : 10.1159/000279334 . ПМИД 20130418 . S2CID 34447321 .
- ^ Jump up to: а б Конти-Файн Б.М., Милани М., Камински Х.Дж. (ноябрь 2006 г.). «Миастения гравис: прошлое, настоящее и будущее» . Журнал клинических исследований . 116 (11): 2843–2854. дои : 10.1172/JCI29894 . ПМК 1626141 . ПМИД 17080188 .
- ^ Эрлих А., Шредер К.Л. (2014). Введение в медицинскую терминологию . Cengage Обучение. п. 87. ИСБН 978-1-133-95174-2 . Архивировано из оригинала 8 сентября 2017 года.
- ^ Jump up to: а б с д и ж г час я дж Энгель АГ (2012). Миастения Гравис и миастенические расстройства (2-е изд.). Издательство Оксфордского университета, США. стр. 109–110. ISBN 978-0-19-973867-0 . Архивировано из оригинала 8 сентября 2017 года.
- ^ Jump up to: а б с д и Скалли С. (2014). Медицинские проблемы Скалли в стоматологии . Elsevier Health Sciences UK. ISBN 978-0-7020-5963-6 . Архивировано из оригинала 8 сентября 2017 года.
- ^ Jump up to: а б Миастения Гравис в eMedicine
- ^ Jump up to: а б с д и ж г час Наир А.Г., Патил-Чхаблани П., Венкатрамани Д.В., Ганди Р.А. (октябрь 2014 г.). «Глазная миастения: обзор» . Индийский журнал офтальмологии . 62 (10): 985–991. дои : 10.4103/0301-4738.145987 . ПМЦ 4278125 . ПМИД 25449931 .
- ^ Jump up to: а б с д и ж г Шерер К., Бедлак Р.С., Симел Д.Л. (апрель 2005 г.). «Есть ли у этого пациента миастения?». ДЖАМА . 293 (15): 1906–1914. дои : 10.1001/jama.293.15.1906 . ПМИД 15840866 .
- ^ Jump up to: а б Раджендран А; Сундарам С. (2014). Учебник патологии полости рта Шафера (7-е изд.). Elsevier Health Sciences в Азиатско-Тихоокеанском регионе. п. 867. ИСБН 978-81-312-3800-4 . Архивировано из оригинала 2 апреля 2017 года.
- ^ Энциклопедия MedlinePlus : Миастения гравис
- ^ Jump up to: а б с д и Маркс Дж.А. (2014). Неотложная медицина Розена: концепции и клиническая практика (8-е изд.). Филадельфия: Эльзевир/Сондерс. стр. 1441–1444. ISBN 978-1-4557-0605-1 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т Шейх С., Алви У., Соливен Б., Резания К. (апрель 2021 г.). «Препараты, которые вызывают или вызывают ухудшение миастении гравис: обновленная информация» . Журнал клинической медицины . 10 (7): 1537. doi : 10.3390/jcm10071537 . ПМЦ 8038781 . ПМИД 33917535 .
- ^ Холл Д.Р., МакГиббон Д.Х., Эванс CC, Медоуз Джорджия (декабрь 1972 г.). «Гентамицин, тубокурарин, лигнокаин и нервно-мышечная блокада. Отчет о случае». Британский журнал анестезии . 44 (12): 1329–32. дои : 10.1093/бья/44.12.1329 . ПМИД 4568132 .
- ^ Сафа Х., Джонсон Д.Х., Трин В.А., Роджерс Т.Е., Лин Х., Суарес-Алмазор М.Э., Фаак Ф, Сабериан С., Йи К., Дэвис М.А., Туммала С., Вудман К., Абдель-Вахаб Н., Диаб А. (ноябрь 2019 г.) ). «Ингибиторы иммунных контрольных точек, связанные с миастенией гравис: опыт одного центра и систематический обзор литературы» . Журнал иммунотерапии рака . 7 (1): 319. doi : 10.1186/s40425-019-0774-y . ПМК 6868691 . ПМИД 31753014 .
- ^ Пуванант А., Исфорт М., Лакомис Д., Живкович С.А. (февраль 2019 г.). «Клинический спектр нервно-мышечных осложнений после ингибирования иммунных контрольных точек». Нервно-мышечные расстройства . 29 (2): 127–133. дои : 10.1016/j.nmd.2018.11.012 . ПМИД 30638612 .
- ^ Гра-Шампель В., Батте Б., Масмуди К., Лиабеф С. (октябрь 2019 г.). «Статиновая миастения: анализ диспропорции базы данных фармаконадзора VigiBase ВОЗ». Мышцы и нервы . 60 (4): 382–386. дои : 10.1002/mus.26637 . ПМИД 31298743 .
- ^ Jump up to: а б с ван ден Берселаар Л.Р., Губбельс М., Риази С., Хейтенс Л., Юнгблут Х., Фёрманс Н.К., Сноек М.М. (июнь 2022 г.). «Составление текущих данных об анестезиологическом лечении взрослых пациентов с нервно-мышечными расстройствами – обзорный обзор» . Канадский журнал анестезии = Journal Canadien d'Anesthesie . 69 (6): 756–773. дои : 10.1007/s12630-022-02230-3 . ПМЦ 9132812 . ПМИД 35322378 .
- ^ Моури Х, Джо Т, Мацуи Х, Фусими К, Ясунага Х (февраль 2020 г.). «Влияние сугаммадекса на послеоперационный миастенический криз у пациентов с миастенией гравис: анализ оценки склонности общенациональной базы данных Японии». Анестезия и анальгезия . 130 (2): 367–373. дои : 10.1213/ANE.0000000000004239 . ПМИД 31124838 .
- ^ Ката Дж.П., Ласала Дж.Д., Уильямс В., Мена Дж.Е. (сентябрь 2019 г.). «Хирургия миастении гравис и тимомы: обновленная клиническая информация для кардиоторакального анестезиолога». Журнал кардиоторакальной и сосудистой анестезии . 33 (9): 2537–2545. дои : 10.1053/j.jvca.2018.07.036 . ПМИД 30219643 .
- ^ Хоффманн С., Колер С., Циглер А., Майзель А. (октябрь 2014 г.). «Глюкокортикоиды при миастении – если, когда, как и сколько?» . Acta Neurologica Scandinavica . 130 (4): 211–21. дои : 10.1111/ane.12261 . ПМИД 25069701 .
- ^ Далакас MC, Майзель А. (апрель 2022 г.). «Иммуномодулирующее действие и клиническая польза внутривенного введения иммуноглобулина при миастении» . Экспертный обзор нейротерапии . 22 (4): 313–318. дои : 10.1080/14737175.2022.2057223 . ПМИД 35350948 .
- ^ Гимире А, Кунвар Б, Арьял Б, Гайре А, Бист А, Шах Б, Майнали А, Гимире Б, Гаджурел Б.П. (март 2024 г.). «Оценка сравнительной эффективности плазмафереза и внутривенного иммуноглобулина при лечении миастении: систематический обзор и метаанализ». Журнал клинической неврологии . 121 : 1–10. дои : 10.1016/j.jocn.2024.01.025 . ПМИД 38306763 .
- ^ Винсент А., Палас Дж., Хилтон-Джонс Д. (июнь 2001 г.). «Миастения гравис». Ланцет . 357 (9274): 2122–8. дои : 10.1016/S0140-6736(00)05186-2 . ПМИД 11445126 .
- ^ Петручелли Н., Барра М.Э., Кёль Дж.Л. (январь 2024 г.). «Оценка воздействия лекарств на обострение заболевания у пациентов с миастенией гравис». Нейрогоспиталист . 14 (1): 52–57. дои : 10.1177/19418744231206256 . ПМЦ 10790617. ПМИД 38235027 .
- ^ Маклер В.К., О'Брайен Дж.М., Мэтсон С.Е., Райс А.Н. (февраль 2019 г.). «Перианестетические последствия и соображения при миастении гравис». Журнал ухода за перианестезией . 34 (1): 4–15. дои : 10.1016/j.jopan.2018.03.009 . ПМИД 29980408 .
- ^ Прабху С.С., Хан С.А., Дудников А.Л., Рибай ООН (февраль 2019 г.). «Анестетические соображения для пациента с миастенией гравис, проходящего глубокую седацию в амбулаторных условиях челюстно-лицевой хирургии» . Журнал стоматологической анестезии и медицины боли . 19 (1): 67–72. дои : 10.17245/jdapm.2019.19.1.67 . ПМК 6405345 . ПМИД 30859135 .
- ^ Валенсуэла Д.М., Ститт Т.Н., ДиСтефано П.С., Рохас Э., Мэттссон К., Комптон Д.Л., Нуньес Л., Парк Дж.С., Старк Дж.Л., Гис Д.Р., Томас С., ЛеБо М.М., Фернальд А.А., Коупленд Н.Г., Дженкинс Н.А., Берден С.Дж., Glass DJ , Янкопулос Г.Д. (сентябрь 1995 г.). «Рецепторная тирозинкиназа, специфичная для скелетных мышц: экспрессия в эмбриональных мышцах, в нервно-мышечных соединениях и после травмы» . Нейрон . 15 (3): 573–584. дои : 10.1016/0896-6273(95)90146-9 . ПМИД 7546737 . S2CID 17575761 .
- ^ «Миастения гравис» . Домашний справочник по генетике . Архивировано из оригинала 11 июля 2015 года . Проверено 10 июля 2015 г.
- ^ Синмаз Н., Нгуен Т., Теа Ф., Дейл Р.К., Брилот Ф. (август 2016 г.). «Картирование эпитопов аутоантигенов: молекулярное понимание заболеваний нервной системы, связанных с аутоантителами» . Журнал нейровоспаления . 13 (1): 219. дои : 10.1186/s12974-016-0678-4 . ПМК 5006540 . ПМИД 27577085 .
- ^ Сатхасивам С. (январь 2014 г.). «Диагностика и лечение миастении» . Прогресс в неврологии и психиатрии . 18 (1): 6–14. дои : 10.1002/pnp.315 . S2CID 115659064 .
- ^ «Миастения Гравис» . ПабМед Здоровье . Бетесда, доктор медицины: Национальная медицинская библиотека США. Архивировано из оригинала 18 октября 2016 года . Проверено 9 июля 2015 г.
- ^ «Информационный бюллетень по миастении гравис» . www.ninds.nih.gov . Национальный институт неврологических расстройств и инсульта (NINDS). Архивировано из оригинала 11 июля 2015 года . Проверено 10 июля 2015 г.
- ^ Jump up to: а б с Варнер М. (июнь 2013 г.). «Миастения и беременность». Клиническая акушерство и гинекология . 56 (2): 372–81. дои : 10.1097/GRF.0b013e31828e92c0 . ПМИД 23563874 .
- ^ Тельес-Зентено Х.Ф., Эрнандес-Ронкильо Л., Салинас В., Эстанол Б., да Силва О (ноябрь 2004 г.). «Миастения и беременность: клинические последствия и исходы для новорожденных» . BMC Заболевания опорно-двигательного аппарата . 5 (1): 42. дои : 10.1186/1471-2474-5-42 . ПМК 534111 . ПМИД 15546494 .
- ^ Jump up to: а б с Уоррел Д.А., Кокс Т.М. и др. (2003). Оксфордский учебник медицины . Том. 3 (Четвертое изд.). Оксфорд. п. 1170. ИСБН 978-0-19-852787-9 .
- ^ Аллен Н.М., О'Рахелли М., Эймард Б., Шушан М., Хан А., Кирнс Дж., Ким Д.С., Бьюн С.Ю., Нгуен К.Э., Шара-Шмидт У., Колбель Х., Марина А.Д., Шнайдер-Голд С., Руфке К., Тиме А. , Ван ден Берг П., Авалос Г., Альварес-Веласко Р., Натера-де Бенито Д., Ченг М.Х., Чан В.К., Ван Х.С., Томас М.А., Борх Л., Лаузон Дж., Корнблюм С., Рейманн Дж., Мюллер А., Кунцер Т., Норвуд Ф., Рамдас С., Джейкобсон Л.В., Джи Икс, Фернандес-Гарсия М.А., Рэйдж Э., Лим М., Лин Дж.П., Клейс К.Г., Актас С., Оскуи М., Хакоэн Ю., Масуд А., Лейте М.И., Палас Дж., Де Виво Д. , Винсент А., Юнгблут Х. (октябрь 2023 г.). «Новый спектр нарушений, связанных с антителами к рецептору ацетилхолина плода (FARAD)» . Мозг: журнал неврологии . 146 (10): 4233–4246. дои : 10.1093/brain/awad153 . ПМЦ 10545502 . ПМИД 37186601 .
- ^ Радд К., Коциско Д. (2013). Педиатрический уход: важнейшие компоненты сестринского ухода . Ф.А. Дэвис. ISBN 978-0-8036-4053-5 . Архивировано из оригинала 3 июня 2016 года.
- ^ Энгель А.Г., Шен Х.М., Селцен Д., Сине С.М. (апрель 2015 г.). «Врожденные миастенические синдромы: патогенез, диагностика и лечение» . «Ланцет». Неврология . 14 (4): 420–434. дои : 10.1016/S1474-4422(14)70201-7 . ПМК 4520251 . ПМИД 25792100 .
- ^ «Информационная страница врожденной миастении: Национальный институт неврологических расстройств и инсульта (NINDS)» . www.ninds.nih.gov . Архивировано из оригинала 12 июля 2015 года . Проверено 11 июля 2015 г.
- ^ Вулф Дж.И., Барон Р.Дж. (2009). «Миастения Гравис: классификация и оценка результатов». Миастения Гравис и связанные с ней расстройства . стр. 293–302. дои : 10.1007/978-1-59745-156-7_18 . ISBN 978-1-58829-852-2 .
- ^ Мериджиоли, Мэтью Н; Сандерс, Дональд Б. (май 2009 г.). «Аутоиммунная миастения: возникающая клиническая и биологическая гетерогенность» . Ланцет Неврология . 8 (5): 475–490. дои : 10.1016/S1474-4422(09)70063-8 . ПМК 2730933 . ПМИД 19375665 .
- ^ Гилхус, Нильс Эрик; Вершуурен, Ян Дж (октябрь 2015 г.). «Миастения гравис: классификация подгрупп и терапевтические стратегии» . Ланцет Неврология . 14 (10): 1023–1036. дои : 10.1016/s1474-4422(15)00145-3 . ISSN 1474-4422 . ПМИД 26376969 .
- ^ Пунга, Анна Ростедт; Мэддисон, Пол; Хекманн, Жаннин М; Гуптилл, Джеффри Т; Эволи, Амелия (февраль 2022 г.). «Эпидемиология, диагностика и биомаркеры аутоиммунных нарушений нервно-мышечных соединений» . Ланцет Неврология . 21 (2): 176–188. дои : 10.1016/S1474-4422(21)00297-0 . ПМИД 35065040 .
- ^ Конечный, Инга; Хербст, Рут (2 июля 2019 г.). «Миастения Гравис: Патогенное воздействие аутоантител на нервно-мышечную архитектуру» . Клетки . 8 (7): 671. doi : 10.3390/cells8070671 . ISSN 2073-4409 . ПМК 6678492 . ПМИД 31269763 .
- ^ Лейте М.И., Джейкоб С., Вьегас С., Коссинс Дж., Клевер Л., Морган Б.П. и др. (июль 2008 г.). «Антитела IgG1 к рецепторам ацетилхолина при «серонегативной» миастении» . Мозг . 131 (Часть 7): 1940–52. дои : 10.1093/brain/awn092 . ПМЦ 2442426 . ПМИД 18515870 .
- ^ Энциклопедия MedlinePlus : синдром Ламберта-Итона
- ^ Сельван В.А. (январь 2011 г.). «Одноволоконная ЭМГ: обзор» . Анналы Индийской академии неврологии . 14 (1): 64–67. дои : 10.4103/0972-2327.78058 . ПМК 3108086 . ПМИД 21654930 .
- ^ Кирси С., Фернандо П., Д'Коста Д., Фердинанд П. (июнь 2010 г.). «Применение теста с пакетом льда при миастении» . Краткие отчеты JRSM . 1 (1): 14. дои : 10.1258/shorts.2009.090037 . ПМЦ 2984327 . ПМИД 21103106 .
- ^ Энциклопедия MedlinePlus : Тест на растяжение
- ^ Jump up to: а б с Спиллейн Дж., Хайэм Э., Куллманн Д.М. (декабрь 2012 г.). «Миастения гравис». БМЖ . 345 (21 декабря 3): e8497. дои : 10.1136/bmj.e8497 . ПМИД 23261848 . S2CID 13911967 .
- ^ де Кракер М., Клюин Дж., Ренкен Н., Маат А.П., Богерс А.Дж. (июнь 2005 г.). «КТ и миастения: корреляция между визуализацией средостения и гистопатологическими данными» . Интерактивная сердечно-сосудистая и торакальная хирургия . 4 (3): 267–271. дои : 10.1510/icvts.2004.097246 . ПМИД 17670406 .
- ^ Аллан Х. Роппер, Роберт Х. Браун Адамс и принципы неврологии Виктора McGraw-Hill Professional; 8-е издание (2005 г.)
- ^ Энциклопедия MedlinePlus : Функциональные тесты легких.
- ^ Неотложная помощь при миастении гравис в eMedicine
- ^ Jump up to: а б Гилхус, Нильс Эрик (1 марта 2021 г.). «Физическая тренировка и упражнения при миастении» . Нервно-мышечные расстройства . 31 (3): 169–173. дои : 10.1016/j.nmd.2020.12.004 . HDL : 11250/2767222 . ISSN 0960-8966 . ПМИД 33461846 . S2CID 229372884 .
- ^ Даррас, Британская Колумбия; Фридман, НР (февраль 2000 г.). «Метаболические миопатии: клинический подход; часть I» . Детская неврология . 22 (2): 87–97. дои : 10.1016/s0887-8994(99)00133-2 . ISSN 0887-8994 . ПМИД 10738913 . Архивировано из оригинала 24 мая 2023 года . Проверено 24 ноября 2023 г.
- ^ Тобон, Алехандро (декабрь 2013 г.). «Метаболические миопатии» . Континуум (Миннеаполис, Миннесота) . 19 (6 мышечных заболеваний): 1571–1597. дои : 10.1212/01.CON.0000440660.41675.06 . ISSN 1538-6899 . ПМЦ 10563931 . ПМИД 24305448 .
- ^ Вакелин, А. (2017). Жизнь с болезнью МакАрдла (PDF) . ЯGSD. Архивировано (PDF) из оригинала 5 марта 2023 года . Проверено 24 ноября 2023 г.
- ^ Причина, СЛ; Верманс, Н.; Люсия, А.; Виссинг, Дж.; Куинливан, Р.; Бхай, С.; Уэйклин, А. (июль 2023 г.). «Развитие непрерывного лечения болезни МакАрдла: практический инструмент для врачей и пациентов» . Нервно-мышечные расстройства . 33 (7): 575–579. дои : 10.1016/j.nmd.2023.05.006 . ISSN 1873-2364 . ПМИД 37354872 . S2CID 259141690 .
- ^ Скалько, Рената С.; Люсия, Алехандро; Санталла, Альфредо; Мартинуцци, Андреа; Вавла, Маринела; Рени, Джанлуиджи; Тоскано, Антонио; Мусумечи, Олимпия; Верманс, Никол К.; Кувенберг, Карлин В.; Форест, Паскаль; Сан-Мильян, Беатрис; Вьейтез, Ирен; Сицилиано, Габриэле; Кюнле, Энрико (24 ноября 2020 г.). «Данные Европейского регистра пациентов с болезнью МакАрдла и другими мышечными гликогенозами (EUROMAC)» . Сиротский журнал редких заболеваний . 15 (1): 330. doi : 10.1186/s13023-020-01562-x . ISSN 1750-1172 . ПМЦ 7687836 . ПМИД 33234167 .
- ^ Jump up to: а б Уртисбереа, Джон Андони; Севера, Джанмарко; Малфатти, Эдоардо (май 2023 г.). «Метаболические миопатии в эпоху секвенирования следующего поколения» . Гены . 14 (5): 954. doi : 10.3390/genes14050954 . ISSN 2073-4425 . ПМЦ 10217901 . ПМИД 37239314 .
- ^ «МЫШЕЧНАЯ ДИСТРОФИЯ, ПОЯС КОНЕЧНОСТИ, АУТОСОМНО-РЕЦЕССИВНЫЙ 8; LGMDR8» . www.omim.org . Архивировано из оригинала 31 мая 2024 года . Проверено 24 ноября 2023 г.
- ^ «МЫШЕЧНАЯ ДИСТРОФИЯ-ДИСТРОГЛИКАНОПАТИЯ (КОНЕЧНОСТИ-ПОЯС), ТИП C, 3; MDDGC3» . www.omim.org . Архивировано из оригинала 9 июня 2023 года . Проверено 24 ноября 2023 г.
- ^ «МИОФИБРИЛЛЯРНАЯ МИОПАТИЯ 10; МФМ10» . www.omim.org . Архивировано из оригинала 21 апреля 2024 года . Проверено 24 ноября 2023 г.
- ^ «ДЕФИЦИТ ДИМЕТИЛГЛИЦИНДЕГИДРОГЕНАЗЫ; DMGDHD» . www.omim.org . Архивировано из оригинала 14 октября 2022 года . Проверено 24 ноября 2023 г.
- ^ «ДЕФЕКТ ТРАНСПОРТЕРА ЭРИТРОЦИТОВ ЛАКТАТА» . www.omim.org . Архивировано из оригинала 13 мая 2024 года . Проверено 24 ноября 2023 г.
- ^ «МИОПАТИЯ С МИАЛГИЕЙ, ПОВЫШЕНИЕМ КРЕАТИНКИНАЗЫ В СЫВОРОТКЕ И С ЭПИЗОДИЧЕСКИМ РАБДОМИОЛИЗОМ ИЛИ БЕЗ ИЛИ БЕЗ; MMCKR» . www.omim.org . Архивировано из оригинала 3 июня 2024 года . Проверено 24 ноября 2023 г.
- ^ «ЭПИЗОДИЧЕСКАЯ МЫШЕЧНАЯ СЛАБОСТЬ, СВЯЗАННАЯ С Х-СВЯЗЬЮ; EMWX» . www.omim.org . Архивировано из оригинала 3 июля 2024 года . Проверено 24 ноября 2023 г.
- ^ «Фенотипическая серия – PS601462, PS610542 – Врожденные миастенические синдромы – ОМИМ» . www.omim.org . Архивировано из оригинала 3 июля 2024 года . Проверено 24 ноября 2023 г.
- ^ «159400 – МИАСТЕНИЯ, ПОЯСНО КОНЕЧНОСТИ, АУТОИММУННАЯ – ОМИМ» . www.omim.org . Архивировано из оригинала 2 июня 2023 года . Проверено 29 февраля 2024 г.
- ^ Паскуцци, Роберт М.; Бодкин, Синтия Л. (2022). «Миастения Гравис и миастенический синдром Ламберта-Итона: новые разработки в диагностике и лечении» . Нервно-психические заболевания и лечение . 18 : 3001–3022. дои : 10.2147/NDT.S296714 . ISSN 1176-6328 . ПМЦ 9792103 . ПМИД 36578903 .
- ^ Jump up to: а б Мендиратта М.М., Панди С., Кунцер Т. (октябрь 2014 г.). «Лечение миастении гравис ингибиторами ацетилхолинэстеразы» . Кокрановская база данных систематических обзоров . 2014 (10): CD006986. дои : 10.1002/14651858.CD006986.pub3 . ПМК 7390275 . ПМИД 25310725 .
- ^ Гронсет Г.С., барон Р.Дж. (июль 2000 г.). «Практический параметр: тимэктомия при аутоиммунной миастении гравис (обзор фактических данных): отчет Подкомитета по стандартам качества Американской академии неврологии» . Неврология . 55 (1): 7–15. дои : 10.1212/wnl.55.1.7 . ПМИД 10891896 .
- ^ Су Дж., Гольдштейн Дж. М., Новак Р. Дж. (июнь 2013 г.). «Клиническая характеристика больных рефрактерной миастенией» . Йельский журнал биологии и медицины . 86 (2): 255–60. ПМЦ 3670444 . ПМИД 23766745 .
- ^ Берман Дж., Тольф А., Хэгглунд Х., Аскмарк Х. (февраль 2018 г.). «Аутологичная трансплантация гемопоэтических стволовых клеток при неврологических заболеваниях» . Журнал неврологии, нейрохирургии и психиатрии . 89 (2): 147–155. дои : 10.1136/jnnp-2017-316271 . ПМК 5800332 . ПМИД 28866625 .
- ^
 В эту статью включен текст из этого источника, который находится в свободном доступе : «FDA одобрило новое лечение миастении гравис» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) (пресс-релиз). 17 декабря 2021 года. Архивировано из оригинала 20 декабря 2021 года . Проверено 21 декабря 2021 г.
В эту статью включен текст из этого источника, который находится в свободном доступе : «FDA одобрило новое лечение миастении гравис» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) (пресс-релиз). 17 декабря 2021 года. Архивировано из оригинала 20 декабря 2021 года . Проверено 21 декабря 2021 г. - ^ «Argenx объявляет об одобрении Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) препарата Вивгарт (эфгартигимод альфа-fcab) при генерализованной миастении гравис» . Аргенкс (Пресс-релиз). 17 декабря 2021 года. Архивировано из оригинала 20 декабря 2021 года . Проверено 21 декабря 2021 г.
- ^ «argenx объявляет об одобрении Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) препарата Вивгарт (эфгартигимод альфа-fcab) при генерализованной миастении гравис» (пресс-релиз). Аргенкс. 17 декабря 2021 года. Архивировано из оригинала 19 декабря 2021 года . Проверено 21 декабря 2021 г. - через Business Wire.
- ^ «Halozyme объявляет, что argenx получает одобрение FDA на Vyvgart Hytrulo With Enhanze для подкожного применения при генерализованной миастении гравис» (пресс-релиз). Галозимная терапия. 20 июня 2023 года. Архивировано из оригинала 24 июня 2023 года . Проверено 24 июня 2023 г. - через PR Newswire.
- ^ «Argenx объявляет об одобрении Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США инъекций Vyvgart Hytrulo (эфгартигимод альфа и гиалуронидаза-qvfc) для подкожного применения при генерализованной миастении гравис» . Аргенкс (Пресс-релиз). 20 июня 2023 года. Архивировано из оригинала 24 июня 2023 года . Проверено 24 июня 2023 г.
- ^ «Утверждения новых лекарственных препаратов на 2023 год» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 28 июня 2023 года. Архивировано из оригинала 21 января 2023 года . Проверено 28 июня 2023 г.
- ^ «UCB объявляет об одобрении FDA США препарата Ристигго (розаноликизумаб-ноли) для лечения взрослых с генерализованной миастенией» (пресс-релиз). ЮКБ. 27 июня 2023 года. Архивировано из оригинала 28 июня 2023 года . Проверено 28 июня 2023 г. - через PR Newswire.
- ^ Jump up to: а б с Мендиратта М.М., Панди С., Кунцер Т. (октябрь 2014 г.). «Лечение миастении гравис ингибиторами ацетилхолинэстеразы» . Кокрановская база данных систематических обзоров . 2014 (10): CD006986. дои : 10.1002/14651858.CD006986.pub3 . ПМК 7390275 . ПМИД 25310725 .
- ^ «Атропин – лекарственные средства и средства против миастении» . Выбор Национальной службы здравоохранения. 2014. Архивировано из оригинала 12 июля 2015 года . Проверено 11 июля 2015 г.
- ^ Jump up to: а б с д и ж г час Кумар В., Камински Х.Дж. (февраль 2011 г.). «Лечение миастении». Текущие отчеты по неврологии и нейробиологии . 11 (1): 89–96. дои : 10.1007/s11910-010-0151-1 . ПМИД 20927659 . S2CID 41052495 .
- ^ Драхман Д.Б., Адамс Р.Н., Ху Р., Джонс Р.Дж., Бродский Р.А. (1 июня 2008 г.). «Перезагрузка иммунной системы с помощью высоких доз циклофосфамида для лечения рефрактерной миастении» . Анналы Нью-Йоркской академии наук . 1132 (1): 305–314. Бибкод : 2008NYASA1132..305D . дои : 10.1196/анналы.1405.033 . ПМК 3390145 . ПМИД 18567882 .
- ^ Су Дж., Гольдштейн Дж. М., Новак Р. Дж. (июнь 2013 г.). «Клиническая характеристика больных рефрактерной миастенией» . Йельский журнал биологии и медицины . 86 (2): 255–260. ПМЦ 3670444 . ПМИД 23766745 .
- ^ Тандан Р., Хехир М.К., Вахид В., Ховард Д.Б. (август 2017 г.). «Лечение миастении гравис ритуксимабом: систематический обзор». Мышцы и нервы . 56 (2): 185–196. дои : 10.1002/mus.25597 . ПМИД 28164324 . S2CID 19504332 .
- ^ Джуэль ВК (март 2004 г.). «Миастения гравис: ведение миастенического криза и периоперационный уход». Семинары по неврологии . 24 (1): 75–81. дои : 10.1055/s-2004-829595 . ПМИД 15229794 . S2CID 260320936 .
- ^ Сеа Дж., Бенатар М., Вердуго Р.Дж., Салинас Р.А. (октябрь 2013 г.). «Тимэктомия при нетимоматозной миастении». Кокрейновская база данных систематических обзоров (10): CD008111. дои : 10.1002/14651858.CD008111.pub2 . ПМИД 24122674 .
- ^ Вулф Г.И., Камински Х.Дж., Абан И.Б., Минисман Г., Куо Х.К., Маркс А. и др. (август 2016 г.). «Рандомизированное исследование тимэктомии при миастении гравис» . Медицинский журнал Новой Англии . 375 (6): 511–522. дои : 10.1056/NEJMoa1602489 . HDL : 2318/1601939 . ПМК 5189669 . ПМИД 27509100 . (Ошибка: два : 10.1056/NEJMx170003 , PMID 28471717 , часы втягивания )
- ^ Cup EH, Питерс А.Дж., Тен Брук-Пастур Дж.М., Муннеке М., ван Энгелен Б.Г., Хендрикс Х.Т., ван дер Вилт Г.Дж., Остендорп Р.А. (ноябрь 2007 г.). «ЛФК и другие виды физиотерапии больных нервно-мышечными заболеваниями: систематический обзор». Архив физической медицины и реабилитации . 88 (11): 1452–1464. дои : 10.1016/j.apmr.2007.07.024 . ПМИД 17964887 .
- ^ Мехризи М., Паскуцци Р.М. (сентябрь 2014 г.). «Осложнения рентгенологического контрастирования у больных миастенией». Мышцы и нервы . 50 (3): 443–4. дои : 10.1002/mus.24254 . ПМИД 24677227 . S2CID 206295540 .
- ^ Sieb JP (март 2014 г.). «Миастения гравис: информация для врача» . Клиническая и экспериментальная иммунология . 175 (3): 408–418. дои : 10.1111/cei.12217 . ПМЦ 3927901 . ПМИД 24117026 .
- ^ Сеа Дж., Бенатар М., Вердуго Р.Дж., Салинас Р.А. (октябрь 2013 г.). «Тимэктомия при нетимоматозной миастении». Кокрейновская база данных систематических обзоров (10): CD008111. дои : 10.1002/14651858.CD008111.pub2 . ПМИД 24122674 .
- ^ Дрессер, Лаура; Влодарски, Ричард; Резания, Курош; Соливен, Бетти (21 мая 2021 г.). «Миастения Гравис: эпидемиология, патофизиология и клинические проявления» . Журнал клинической медицины . 10 (11): 2235. doi : 10.3390/jcm10112235 . ISSN 2077-0383 . ПМЦ 8196750 . ПМИД 34064035 .
- ^ Лосен М., Мартинес-Мартинес П., Фернамбук М., Шуурман Дж., Паррен П.В., Де Баетс М.Х. (2008). «Лечение миастении путем предотвращения модуляции рецепторов ацетилхолина». Анналы Нью-Йоркской академии наук . 1132 (1): 174–179. Бибкод : 2008NYASA1132..174L . дои : 10.1196/анналы.1405.034 . ПМИД 18567867 . S2CID 3206109 .
- ^ Вринтен С., ван дер Цвааг А.М., Вайнрайх СС, Шолтен Р.Дж., Вершуурен Дж.Дж. (декабрь 2014 г.). «Эфедрин при миастении, неонатальной миастении и врожденных миастенических синдромах» . Кокрановская база данных систематических обзоров . 2014 (12): CD010028. дои : 10.1002/14651858.CD010028.pub2 . ПМЦ 7387729 . ПМИД 25515947 .
- ^ Стейнбек Дж.А., Джайсвал М.К., Колдер Э.Л., Кишиневский С., Вейсхаупт А., Тойка К.В., Гольдштейн П.А., Студер Л. (январь 2016 г.). «Функциональная связность под оптогенетическим контролем позволяет моделировать нервно-мышечные заболевания человека» . Клеточная стволовая клетка . 18 (1): 134–143. дои : 10.1016/j.stem.2015.10.002 . ПМК 4707991 . ПМИД 26549107 .
Дальнейшее чтение
[ редактировать ]- Чжан Цз, Го Дж, Су Г, Ли Дж, У Х, Се Икс (17 ноября 2014 г.). «Оценка качества рекомендаций по миастении с помощью инструмента AGREE II» . ПЛОС ОДИН . 9 (11): e111796. Бибкод : 2014PLoSO...9k1796Z . дои : 10.1371/journal.pone.0111796 . ПМК 4234220 . ПМИД 25402504 .
- «Диагноз: Миастения гравис» . Национальный центр биотехнологической информации (NCBI) . Национальная медицинская библиотека США. Архивировано из оригинала 10 декабря 2017 года . Проверено 11 июля 2015 г.