Ловастатин
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Мевакор, Альтокор и другие. |
| Другие имена | Монаколин К, Мевинолин |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а688006 |
| Данные лицензии |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | <5% [1] |
| Связывание с белками | >98% [1] |
| Метаболизм | Печень (субстрат CYP3A и CYP2C8 ) [1] |
| Период полувыведения | 2–5 часов [1] |
| Экскреция | Фекалии (83%), моча (10%) [1] |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.115.931 |
| Химические и физические данные | |
| Формула | С 24 Н 36 О 5 |
| Молярная масса | 404.547 g·mol −1 |
| 3D model ( JSmol ) | |
| (проверять) | |
Ловастатин под торговой маркой Мевакор , продаваемый, среди прочего, , представляет собой статиновый препарат , предназначенный для лечения высокого уровня холестерина в крови и снижения риска сердечно-сосудистых заболеваний . [2] Его использование рекомендуется вместе с изменением образа жизни. [2] Его принимают внутрь. [2]
Общие побочные эффекты включают диарею, запор, головную боль, мышечные боли, сыпь и проблемы со сном. [2] Серьезные побочные эффекты могут включать проблемы с печенью , распад мышц и почечную недостаточность . [2] Использование во время беременности может нанести вред ребенку, поэтому использование во время грудного вскармливания не рекомендуется. [3] Он действует путем снижения способности печени вырабатывать холестерин путем блокирования фермента ГМГ-КоА-редуктазы . [2]
Ловастатин был запатентован в 1979 году и одобрен для медицинского применения в 1987 году. [4] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [5] Он доступен в виде непатентованного лекарства . [2] В 2021 году это было 100-е место среди наиболее часто назначаемых лекарств в США: на него было выписано более 6 миллионов рецептов. [6] [7]
Медицинское использование
[ редактировать ]Основное применение ловастатина — лечение дислипидемии и профилактика сердечно-сосудистых заболеваний . [8] Его рекомендуется использовать только после того, как другие меры, такие как диета, физические упражнения и снижение веса, не привели к улучшению уровня холестерина. [8]
Побочные эффекты
[ редактировать ]Ловастатин обычно хорошо переносится, при этом наиболее распространенными побочными эффектами, примерно в порядке убывания частоты, являются: креатинфосфокиназы повышение уровня , метеоризм , боли в животе, запор, диарея , мышечные боли или боли , тошнота, расстройство желудка , слабость, нечеткость зрения, сыпь, головокружение и мышечные судороги. [9] Как и все статины, он может иногда вызывать миопатию , гепатотоксичность (поражение печени), дерматомиозит или рабдомиолиз . [9] Это может быть опасным для жизни, если его не распознать и не начать лечение вовремя, поэтому о любой необъяснимой мышечной боли или слабости во время приема ловастатина следует немедленно сообщать врачу, назначившему препарат. Другие необычные побочные эффекты, о которых следует немедленно сообщить врачу, выписавшему рецепт, или в службу неотложной медицинской помощи, включают: [10]
- мышечная боль, нежность или слабость
- недостаток энергии
- слабость
- высокая температура
- моча темного цвета
- желтуха : пожелтение кожи или глаз
- боль в верхней правой части желудка
- тошнота
- необычное кровотечение или синяки
- потеря аппетита
- гриппоподобные симптомы
- сыпь
- крапивница
- зуд
- затрудненное дыхание или глотание
- отек лица, горла, языка, губ, глаз, рук, ног, лодыжек или голеней
- охриплость
Об этих менее серьезных побочных эффектах все равно следует сообщать, если они сохраняются или усиливаются: [10]
- запор
- потеря памяти или забывчивость
- путаница
Противопоказания
[ редактировать ]Противопоказания и состояния, при которых следует отказаться от лечения ловастатином, включают беременность, кормление грудью и заболевания печени. Ловастатин противопоказан во время беременности (категория беременности X); это может вызвать врожденные дефекты, такие как деформации скелета или неспособность к обучению. Из-за способности нарушать липидный обмен у детей ловастатин не следует принимать во время грудного вскармливания. [11] Пациентам с заболеваниями печени не следует принимать ловастатин. [12]
Взаимодействия
[ редактировать ]Как и в случае с аторвастатином , симвастатином и другими статиновыми препаратами, метаболизирующимися через CYP3A4 , употребление грейпфрутового сока во время терапии ловастатином может увеличить риск побочных эффектов. Компоненты грейпфрутового сока, флавоноид нарингин или фуранокумарин бергамоттин ингибируют CYP3A4 in vitro . [13] и может быть причиной эффекта in vivo концентрата грейпфрутового сока, снижающего метаболический клиренс ловастатина и повышающего его концентрацию в плазме. [14]
Механизм действия
[ редактировать ]Ловастатин является ингибитором 3-гидрокси-3-метилглутарил-кофермента А-редуктазы (ГМГ-КоА-редуктазы), фермента, который катализирует превращение ГМГ-КоА в мевалонат. [15] Мевалонат является необходимым строительным блоком для биосинтеза холестерина, а ловастатин препятствует его производству, действуя как обратимый конкурентный ингибитор ГМГ-КоА, который связывается с ГМГ-КоА-редуктазой. Ловастатин представляет собой пролекарство , неактивный лактон в своей нативной форме, форма закрытого кольца гамма-лактона, в которой его вводят, гидролизуется in vivo до формы открытого кольца β-гидроксикислоты; что является активной формой.
Ловастатин и другие статины изучались на предмет их химиопрофилактического и химиотерапевтического действия. В ранних исследованиях подобных эффектов не наблюдалось. [16] Более поздние исследования выявили некоторые химиопрофилактические и терапевтические эффекты при определенных типах рака, особенно в сочетании статинов с другими противораковыми препаратами. [17] Вероятно, эти эффекты опосредованы свойствами статинов снижать активность протеасом , что приводит к накоплению циклин-зависимых киназ ингибиторов р21 и р27 и последующей остановке G1 - фазы, что наблюдается в клетках различных раковых линий. [18] [19]
История
[ редактировать ]
Компактин и ловастатин, натуральные продукты с мощным ингибирующим действием на ГМГ-КоА-редуктазу , были открыты в 1970-х годах и введены в клиническую разработку в качестве потенциальных препаратов для снижения уровня холестерина ЛПНП . [21] [22]
В 1982 году были предприняты небольшие клинические исследования ловастатина, природного продукта, полученного из поликетида, выделенного из Aspergillus terreus , у пациентов с очень высоким риском, в ходе которых наблюдалось резкое снижение уровня холестерина ЛПНП с очень небольшим количеством побочных эффектов. После того как дополнительные исследования безопасности ловастатина на животных не выявили токсичности, связанной с компактином, клинические исследования были продолжены.
Масштабные исследования подтвердили эффективность ловастатина. Наблюдаемая переносимость оставалась превосходной, и ловастатин был одобрен FDA США в 1987 году. [23] Это был первый статин, одобренный FDA. [24]
Ловастатин также естественным образом продуцируется некоторыми высшими грибами , такими как Pleurotus ostreatus (вешенка) и близкородственными Pleurotus spp. [25] Исследования влияния вешенок и их экстрактов на уровень холестерина у лабораторных животных были обширными. [26] [27] [25] [28] [29] [30] [31] [32] [33] [34] [35] [36] хотя эффект был продемонстрирован у очень ограниченного числа людей. [37]
В 1998 году FDA наложило запрет на продажу пищевых добавок, полученных из красного дрожжевого риса , который естественным образом содержит ловастатин, утверждая, что продукты, содержащие рецептурные агенты, требуют одобрения лекарств. [38] Судья Дейл А. Кимбалл из Окружного суда США по округу Юта удовлетворил ходатайство производителя Cholestin, Pharmanex, о том, что запрет агентства был незаконным в соответствии с Законом о пищевых добавках, здравоохранении и образовании 1994 года , поскольку продукт продавался как пищевая добавка. , а не наркотик. [39]
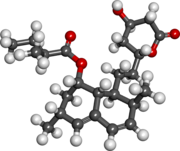
Цель состоит в том, чтобы снизить избыточный уровень холестерина до уровня, соответствующего поддержанию нормальной функции организма. Холестерин биосинтезируется в серии из более чем 25 отдельных ферментативных реакций, которые первоначально включают три последовательные конденсации звеньев ацетил-КоА с образованием шестиуглеродного соединения 3-гидрокси-3-метилглутарил-кофермента А (HMG-КоА). Он восстанавливается до мевалоната, а затем в ходе серии реакций превращается в изопрены , которые являются строительными блоками сквалена , непосредственного предшественника стеринов, который циклизуется в ланостерин (метилированный стерол) и далее метаболизируется до холестерина. Ряд ранних попыток блокировать синтез холестерина привели к созданию агентов, которые ингибировали поздние этапы пути биосинтеза ланостерола и холестерина. Основной этап, ограничивающий скорость, находится на уровне микросомального фермента, который катализирует превращение ГМГ-КоА в мевалоновую кислоту и который в течение нескольких лет считается основной мишенью фармакологического вмешательства. [15]
HMG-CoA-редуктаза возникает на ранних стадиях биосинтетического пути и является одним из первых шагов к созданию холестерина. Ингибирование этого фермента может привести к накоплению HMG-CoA, водорастворимого промежуточного продукта, который затем может легко метаболизироваться до более простых молекул. Это ингибирование редуктазы приведет к накоплению липофильных промежуточных продуктов с формальным стероловым кольцом.
Ловастатин был первым специфическим ингибитором ГМГ-КоА-редуктазы, получившим одобрение для лечения гиперхолестеринемии. Первый прорыв в попытках найти мощный, специфический и конкурентоспособный ингибитор HMG-CoA-редуктазы произошел в 1976 году, когда Endo et al. сообщили об открытии мевастатина , высокофункционализированного грибкового метаболита, выделенного из культур Penicillium citrium . [40]
Биосинтез
[ редактировать ]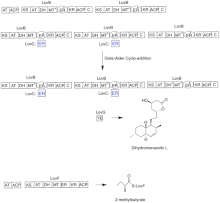
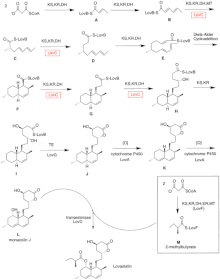
Биосинтез ловастатина происходит по итеративному пути поликетидсинтазы I типа (PKS). Шесть генов, которые кодируют ферменты, необходимые для биосинтеза ловастатина, — это lovB, lovC, lovA, lovD, lovG и lovF. [41] [42] Для синтеза дигидромонаколина L требуется всего 9-малонил-Коа. [41] Он протекает по пути PKS до тех пор, пока не достигнет (E) гексакетида, где он подвергается циклоприсоединению Дильса-Альдера с образованием конденсированных колец. После циклизации он продолжает идти по пути PKS до тех пор, пока не достигнет (I) нонакетида, который затем высвобождается из LovB посредством тиоэстеразы, кодируемой LovG. Дигидромонаколин L, (J), затем подвергается окислению и дегидратации с помощью оксигеназы цитохрома P450, кодируемой LovA, с получением монаколина J, (L) .
Домен MT из lovB активен в превращении ( B) в ( C) , когда он переносит метильную группу от S-аденозил-L-метионина (SAM) к тетракетиду (C) . [41] В связи с тем, что LovB содержит неактивный домен ER, LovC требуется на определенных этапах для получения полностью восстановленных продуктов. Доменная организация LovB, LovC, LovG и LovF показана на рисунке 2. Неактивный ER-домен lovB показан овалом, а место, где LovC действует в трансе к LovB, показано красным прямоугольником.
Параллельным путем дикетидная боковая цепь ловастатина синтезируется другим высоковосстанавливающим ферментом поликетидсинтазой I типа, кодируемым LovF. Наконец, боковая цепь, 2-метилбутират (M), ковалентно присоединяется к гидроксильной группе C-8 монаколина J (L) с помощью трансэстеразы, кодируемой LovD, с образованием ловастатина.
Полный синтез
[ редактировать ]Основная часть работ по синтезу ловастатина была проделана М. Хирамой в 1980-е гг. [43] [44] Хирама синтезировал компактин и использовал один из промежуточных продуктов, чтобы пойти по другому пути, чтобы получить ловастатин. Синтетическая последовательность показана на схемах ниже. γ-лактон синтезировали по методологии Ямады, начиная с глутаминовой кислоты. Вскрытие лактона осуществляли с использованием метоксида лития в метаноле и затем силилирования с получением разделяющейся смеси исходного лактона и силилового эфира . Силиловый эфир при гидрогенолизе с последующим окислением по Коллинзу дал альдегид. Стереоселективное получение (E,E)-диена осуществляли добавлением аниона транс-кротилфенилсульфона с последующим гашением Ac 2 O и последующим восстановительным удалением ацетата сульфона. Конденсация его с анионом лития диметилметилфосфоната дала соединение 1. Соединение 2 синтезировали, как показано на схеме в методике синтеза. Затем соединения 1 и 2 объединяли, используя 1,3 экв. гидрида натрия в ТГФ, с последующим кипячением с обратным холодильником в хлорбензоле в течение 82 часов под азотом, чтобы получить енон 3.
Для получения ловастатина использовали простые органические реакции, как показано на схеме.
- Путь биосинтеза холестерина
- HMG-CoA-редуктазная реакция
- Биосинтез с использованием циклизации, катализируемой Дильсом-Альдером.
- Биосинтез с использованием ацилтрансферазы широкой специфичности.
- Синтез соединений 1 и 2
- Полный синтез ловастатина
Общество и культура
[ редактировать ]Природные источники
[ редактировать ]Ловастатин — это природное соединение, которое в низких концентрациях содержится в пищевых продуктах, таких как вешенки , [45] красный дрожжевой рис , [46] и Пуэр . [47]
Названия брендов
[ редактировать ]Мевакор, Адвикор (в сочетании с никотиновой кислотой ), Альтокор, Альтопрев.
Другие приложения
[ редактировать ]В физиологии растений ловастатин иногда используется в качестве ингибитора биосинтеза цитокининов . [48]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и Неувонен П.Дж., Бэкман Дж.Т., Ниеми М. (2008). «Фармакокинетическое сравнение потенциальных статинов, отпускаемых без рецепта, симвастатина, ловастатина, флувастатина и правастатина». Клиническая фармакокинетика . 47 (7): 463–474. дои : 10.2165/00003088-200847070-00003 . ПМИД 18563955 . S2CID 11716425 .
- ^ Перейти обратно: а б с д и ж г «Монография Ловастатина для профессионалов» . Наркотики.com . Американское общество фармацевтов систем здравоохранения . Проверено 3 марта 2019 г.
- ^ «Предупреждения о ловастатине при беременности и грудном вскармливании» . Наркотики.com . Проверено 3 марта 2019 г.
- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 472. ИСБН 9783527607495 .
- ^ Всемирная организация здравоохранения (2021 г.). Примерный список основных лекарственных средств Всемирной организации здравоохранения: 22-й список (2021 г.) . Женева: Всемирная организация здравоохранения. hdl : 10665/345533 . ВОЗ/MHP/HPS/EML/2021.02.
- ^ «Топ-300 2021 года» . КлинКальк . Архивировано из оригинала 15 января 2024 года . Проверено 14 января 2024 г.
- ^ «Ловастатин – статистика применения препарата» . КлинКальк . Проверено 14 января 2024 г.
- ^ Перейти обратно: а б «Ловастатин» . Американское общество фармацевтов систем здравоохранения . Проверено 3 апреля 2011 г.
- ^ Перейти обратно: а б «Дозировка Мевакора, Алтопрева (ловастатина), показания, взаимодействие, побочные эффекты и многое другое» . Справочник Медскейп . ВебМД . Проверено 17 марта 2014 г.
- ^ Перейти обратно: а б «Ловастатин» . МедлайнПлюс . Национальная медицинская библиотека США. 15 июня 2012 года . Проверено 1 декабря 2012 г.
- ^ «Ловастатин» . ЛактМед . Национальная медицинская библиотека США . Проверено 1 декабря 2012 г.
- ^ Степплер М. «Центр побочных эффектов Мевакора» . RxList . Проверено 1 декабря 2012 г.
- ^ Бэйли Д.Г., Малкольм Дж., Арнольд О., Спенс Дж.Д. (август 1998 г.). «Взаимодействие грейпфрутового сока с лекарствами» . Британский журнал клинической фармакологии . 46 (2): 101–110. дои : 10.1046/j.1365-2125.1998.00764.x . ПМЦ 1873672 . ПМИД 9723817 .
- ^ Кантола Т., Кивистё К.Т., Неувонен П.Дж. (апрель 1998 г.). «Грейпфрутовый сок значительно увеличивает концентрацию ловастатина и ловастатиновой кислоты в сыворотке крови». Клиническая фармакология и терапия . 63 (4): 397–402. дои : 10.1016/S0009-9236(98)90034-0 . ПМИД 9585793 . S2CID 31911751 .
- ^ Перейти обратно: а б Альбертс А.В. (ноябрь 1988 г.). «Открытие, биохимия и биология ловастатина». Американский журнал кардиологии . 62 (15): 10Дж–15Дж. дои : 10.1016/0002-9149(88)90002-1 . ПМИД 3055919 .
- ^ Кац М.С. (февраль 2005 г.). «Терапевтическое понимание: потенциал статинов для химиопрофилактики и терапии рака». Природная клиническая практика. Онкология . 2 (2): 82–89. дои : 10.1038/ncponc0097 . ПМИД 16264880 . S2CID 9766310 .
- ^ Чае Ю.К., Юсуф М., Малечек М.К., Карнейро Б., Чандра С., Каплан Дж. и др. (декабрь 2015 г.). «Статины как противораковая терапия; можем ли мы перевести доклинические и эпидемиологические данные в клиническую пользу?». Медицина открытий . 20 (112): 413–427. ПМИД 26760985 .
- ^ Якобисяк М., Бруно С., Скиерски Й.С., Дажинкевич З. (май 1991 г.). «Эффекты ловастатина, специфичные для клеточного цикла» . Труды Национальной академии наук Соединенных Штатов Америки . 88 (9): 3628–3632. Бибкод : 1991PNAS...88.3628J . дои : 10.1073/pnas.88.9.3628 . ПМК 51505 . ПМИД 1673788 .
- ^ Рао С., Портер Д.С., Чен X, Херличек Т., Лоу М., Кейомарси К. (июль 1999 г.). «Опосредованный ловастатином арест G1 происходит за счет ингибирования протеасомы, независимо от гидроксиметилглутарил-КоА-редуктазы» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (14): 7797–7802. Бибкод : 1999PNAS...96.7797R . дои : 10.1073/pnas.96.14.7797 . ПМК 22141 . ПМИД 10393901 .
- ^ Аларкон Х., Агила С., Арансибия-Авила П., Фуэнтес О., Саморано-Понсе Э., Эрнандес М. (январь – февраль 2003 г.). «Производство и очистка статинов из штаммов Pleurotus ostreatus (Basidiomycetes)» . Журнал естественных исследований C. 58 (1–2): 62–64. дои : 10.1515/znc-2003-1-211 . ПМИД 12622228 . S2CID 29392568 .
- ^ Ведерас Дж.К., Мур Р.Н., Бигам Дж., Чан К.Дж. (1985). «Биосинтез гипохолестеринемического агента мевинолина Aspergillus terreus. Определение происхождения углерода, водорода и кислорода методами ЯМР 13С и масс-спектрометрии». J Am Chem Soc . 107 (12): 3694–701. дои : 10.1021/ja00298a046 .
- ^ Альбертс А.В., Чен Дж., Курон Г., Хант В., Хафф Дж., Хоффман С. и др. (июль 1980 г.). «Мевинолин: высокоэффективный конкурентный ингибитор гидроксиметилглутарил-кофермента А-редуктазы и средство, снижающее уровень холестерина» . Труды Национальной академии наук Соединенных Штатов Америки . 77 (7): 3957–3961. Бибкод : 1980PNAS...77.3957A . дои : 10.1073/pnas.77.7.3957 . ПМЦ 349746 . ПМИД 6933445 .
- ^ Подробности Оранжевой книги FDA для заявки N019643, показывающие одобрение таблеток по 20 мг 31 августа 1987 г. и таблеток по 40 мг 14 декабря 1988 г.
- ^ Эндо А (октябрь 2004 г.). «Происхождение статинов. 2004». Атеросклероз. Дополнения . 5 (3): 125–130. doi : 10.1016/j.atherosclerosissup.2004.08.033 . ПМИД 15531285 .
- ^ Перейти обратно: а б Бобек П., Оздин Л., Гальбави С. (март 1998 г.). «Дозозависимый и зависимый от времени гипохолестеролемический эффект вешенки (Pleurotus ostreatus) у крыс». Питание . 14 (3): 282–286. дои : 10.1016/S0899-9007(97)00471-1 . ПМИД 9583372 .
- ^ Хоссейн С., Хашимото М., Чоудхури Е.К., Алам Н., Хуссейн С., Хасан М. и др. (июль 2003 г.). «Диетический гриб (Pleurotus ostreatus) улучшает уровень атерогенных липидов у крыс с гиперхолестеринемией». Клиническая и экспериментальная фармакология и физиология . 30 (7): 470–475. дои : 10.1046/j.1440-1681.2003.03857.x . ПМИД 12823261 . S2CID 39632962 .
- ^ Бобек П., Гальбавы С. (октябрь 1999 г.). «Гипохолестеринемическое и антиатерогенное действие вешенки (Pleurotus ostreatus) у кроликов». Ди Нарунг . 43 (5): 339–342. doi : 10.1002/(SICI)1521-3803(19991001)43:5<339::AID-FOOD339>3.0.CO;2-5 . ПМИД 10555301 .
- ^ Оплетал Л., Яходар Л., Чобот В., Зданский П., Люкес Дж., Братова М. и др. (декабрь 1997 г.). «Доказательства антигиперлипидемической активности съедобного гриба Pleurotus ostreatus». Британский журнал биомедицинской науки . 54 (4): 240–243. ПМИД 9624732 .
- ^ Баджадж М., Вадхера С., Брар А.П., Сони Г.Л. (октябрь 1997 г.). «Роль вешенки (Pleurotus florida) как гипохолестеринемического/антиатерогенного средства». Индийский журнал экспериментальной биологии . 35 (10): 1070–1075. ПМИД 9475042 .
- ^ Бобек П., Оздин Л., Куняк Л., Громадова М. (март 1997 г.). «[Регуляция обмена холестерина с помощью диетического добавления вешенок (Pleurotus ostreatus) у крыс с гиперхолестеринемией]». Casopis Lekaru Ceskych (на словацком языке). 136 (6): 186–190. ПМИД 9221192 .
- ^ Бобек П., Оздин Л., Куниак Л. (август 1996 г.). «Влияние вешенки (Pleurotus Ostreatus) и его спиртового экстракта в рационе на всасывание и обмен холестерина у крыс с гиперхолестеринемией». Ди Нарунг . 40 (4): 222–224. дои : 10.1002/food.19960400413 . ПМИД 8810086 .
- ^ Бобек П., Оздин О., Микус М. (1995). «Диетическая вешенка (Pleurotus ostreatus) ускоряет обмен холестерина в плазме у крыс с гиперхолестеринемией». Физиологические исследования . 44 (5): 287–291. ПМИД 8869262 .
- ^ Бобек П., Оздин Л., Куняк Л. (1995). «Влияние вешенки (Pleurotus ostreatus), ее спиртового экстракта и остатков экстракции на уровень холестерина в сыворотке, липопротеинах и печени крыс». Ди Нарунг . 39 (1): 98–99. дои : 10.1002/food.19950390113 . ПМИД 7898579 .
- ^ Бобек П., Оздин Л., Куняк Л. (март 1994 г.). «Механизм гипохолестеринемического действия вешенки (Pleurotus ostreatus) у крыс: снижение всасывания холестерина и увеличение выведения холестерина из плазмы». Журнал диетологии . 33 (1): 44–50. дои : 10.1007/BF01610577 . ПМИД 8197787 . S2CID 41820928 .
- ^ Хорватова В, Бобек П, Гинтер Э, Клванова Ю (1993). «Влияние вешенки на гликемию и холестеринемию у крыс с инсулинозависимым диабетом». Физиологические исследования . 42 (3): 175–179. ПМИД 8218150 .
- ^ Бобек П., Гинтер Э., Юрковикова М., Куняк Л. (1991). «Снижающий уровень холестерина эффект гриба Pleurotus ostreatus у крыс с наследственной гиперхолестеринемией». Анналы питания и обмена веществ . 35 (4): 191–195. дои : 10.1159/000177644 . ПМИД 1897899 .
- ^ Хатун К., Махтаб Х., Ханам П.А., Саид М.А., Хан К.А. (январь 2007 г.). «Вешенка снижает уровень глюкозы и холестерина в крови у больных диабетом». Медицинский журнал Майменсингха . 16 (1): 94–99. doi : 10.3329/mmj.v16i1.261 (неактивен 7 февраля 2024 г.). ПМИД 17344789 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на февраль 2024 г. ( ссылка ) - ^ Маккарти М. (1998). «FDA запрещает продукт из красного дрожжевого риса» . Ланцет . 351 (9116): 1637. doi : 10.1016/s0140-6736(05)77698-4 . S2CID 54229753 .
- ↑ Лечение холестерина поддержано , The New York Times, 18 февраля 1999 г.
- ^ Эндо А., Курода М., Цуджита Ю. (декабрь 1976 г.). «ML-236A, ML-236B и ML-236C, новые ингибиторы холестерогенеза, продуцируемые Penicillium citrinium» . Журнал антибиотиков . 29 (12): 1346–1348. дои : 10.7164/антибиотики.29.1346 . ПМИД 1010803 .
- ^ Перейти обратно: а б с Кэмпбелл CD, Ведерас JC (сентябрь 2010 г.). «Биосинтез ловастатина и родственных метаболитов, образуемых грибковыми итеративными ферментами ПКС» . Биополимеры . 93 (9): 755–763. дои : 10.1002/bip.21428 . ПМИД 20577995 .
- ^ Сюй В., Чой Ю.Х., Чой Дж.В., Ли С., Ведерас Дж.К., Да Силва Н.А., Тан Ю. (июнь 2013 г.). «LovG: тиоэстераза, необходимая для высвобождения дигидромонаколина L и оборота ловастатиннонакетидсинтазы в биосинтезе ловастатина» . Ангеванде Хеми . 52 (25): 6472–6475. дои : 10.1002/anie.201302406 . ПМЦ 3844545 . ПМИД 23653178 .
- ^ Хирама М., Ветеринар М. (1982). «Хиральный полный синтез компактина». Дж. Ам. хим. Соц . 104 (15): 4251–4253. дои : 10.1021/ja00379a037 .
- ^ Хирама М., Ивашита М. (1983). «Синтез (+)-мевинолина на основе природных строительных блоков и с использованием реакции, вызывающей асимметрию». Тетраэдр Летт . 24 (17): 1811–1812. дои : 10.1016/S0040-4039(00)81777-3 .
- ^ Гунде-Цимерман Н., Цимерман А. (март 1995 г.). «Плодовые тела плевротуса содержат ингибитор 3-гидрокси-3-метилглутарил-коэнзима А-редуктазы - ловастатин». Экспериментальная микология . 19 (1): 1–6. дои : 10.1006/emyc.1995.1001 . ПМИД 7614366 .
- ^ Лю Дж., Чжан Дж., Ши Ю., Гримсгаард С., Альрак Т., Фоннебё В. (ноябрь 2006 г.). «Китайский красный дрожжевой рис (Monascus purpureus) при первичной гиперлипидемии: метаанализ рандомизированных контролируемых исследований» . Китайская медицина . 1 (1): 4. дои : 10.1186/1749-8546-1-4 . ПМК 1761143 . ПМИД 17302963 .
- ^ Чжао ZJ, Пан YZ, Лю QJ, Ли XH (июнь 2013 г.). «Оценка воздействия ловастатина в чае Пуэр». Международный журнал пищевой микробиологии . 164 (1): 26–31. doi : 10.1016/j.ijfoodmicro.2013.03.018 . ПМИД 23587710 .
- ^ Хартиг К., Бек Э. (2005). «Оценка применения ловастатина в качестве инструмента для исследования цитокинин-опосредованной регуляции клеточного цикла». Физиология Плантарум . 125 (2): 260–267. дои : 10.1111/j.1399-3054.2005.00556.x .