Аллергический бронхолегочный аспергиллез
| Аллергический бронхолегочный аспергиллез | |
|---|---|
| Другие имена | АБЛА, болезнь Хинсона-Пеписа. |
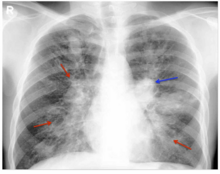 | |
| На рентгенограмме грудной клетки больного аллергическим бронхолегочным аспергиллезом видно левостороннее перихилярное затемнение (синяя стрелка) и неоднородные инфильтраты (транзиторные легочные инфильтраты, обозначены красными стрелками) во всех зонах обоих легочных полей. | |
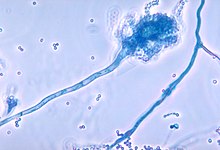 | |
| Конидиефор . грибного организма fumigatus Aspergillus | |
| Специальность | Пульмонология , Инфекционные болезни |
| Симптомы | свистящее дыхание , кашель , одышка и непереносимость физической нагрузки . [1] |
| Осложнения | астмы Обострения , аспергиллома , хронический аспергиллез легких , кавитация , локальная эмфизема , хронический или рецидивирующий ателектаз и сотовый фиброз . [2] |
| Причины | Воздействие аспергилл . |
| Факторы риска | Астма или муковисцидоз . [1] |
| Метод диагностики | Рентгенография грудной клетки , компьютерная томография , анализы крови , иммунологические тесты и посев мокроты . [2] |
| Дифференциальный диагноз | Астма с грибковой чувствительностью, муковисцидоз , бронхоэктатическая болезнь , эозинофильная пневмония , синдром Черджа-Штрауса , бронхоцентрический гранулематоз , туберкулез и саркоидоз . [2] |
| Профилактика | Кортикостероиды и противогрибковые препараты . [2] |
| Медикамент | Преднизолон и Итраконазол . [2] |
| Частота | 1–15% больных муковисцидозом и 2,5% взрослых с тяжелой астмой . [3] |
Аллергический бронхолегочный аспергиллез ( АБЛА ) — состояние, характеризующееся усиленной реакцией иммунной системы ( реакция гиперчувствительности ) на грибок Aspergillus (чаще всего Aspergillus fumigatus ). Чаще всего это происходит у людей, страдающих астмой или муковисцидозом . [1] Aspergillus Споры повсеместно распространены в почве и обычно обнаруживаются в мокроте здоровых людей. A. fumigatus вызывает целый ряд легочных заболеваний, известных как аспергиллез . [4]
АБЛА вызывает дыхательных путей воспаление , приводящее к бронхоэктазам — состоянию, характеризующемуся аномальным расширением дыхательных путей. При отсутствии лечения иммунная система и споры грибков могут повредить чувствительные ткани легких и привести к образованию рубцов. [5]
Точные критерии диагностики АБЛА не согласованы. рентгенография грудной клетки и компьютерная томография , повышение уровня IgE и эозинофилов в крови , иммунологические тесты на аспергиллы вместе с окрашиванием мокроты и посевом мокроты Могут быть полезны . Лечение состоит из кортикостероидов и противогрибковых препаратов . [2]
Признаки и симптомы
[ редактировать ]Практически у всех пациентов клинически диагностирована астма . [1] и проявляется свистящим дыханием (обычно эпизодическим по своей природе), кашлем , одышкой и непереносимостью физической нагрузки (особенно у пациентов с муковисцидозом ). [1] [6] В умеренных и тяжелых случаях наблюдаются симптомы, указывающие на бронхоэктазы , в частности выделение густой мокроты (часто содержащей коричневые слизистые пробки ), а также симптомы, отражающие рецидивирующую инфекцию, такие как плевритная боль в груди и лихорадка . Пациентов с астмой и симптомами продолжающейся инфекции, не реагирующих на лечение антибиотиками, следует подозревать в АБЛА. [1]
Патофизиология
[ редактировать ]Aspergillus Споры имеют небольшие размеры (2–3 мкм в диаметре) и могут проникать глубоко в дыхательную систему до альвеолярного уровня. [7] [8] У здоровых людей врожденные и адаптивные иммунные реакции запускаются различными иммунными клетками (особенно нейтрофилами , резидентными альвеолярными макрофагами и дендритными клетками ), привлеченными к месту инфекции многочисленными воспалительными цитокинами и нейтрофильными аттрактантами (такими как CXCR2 ). лиганды рецептора [9] В этой ситуации мукоцилиарный клиренс инициируется , и споры успешно фагоцитируются , очищая инфекцию от хозяина. [7] [10]
У людей с предрасполагающими заболеваниями легких, такими как персистирующая астма или муковисцидоз (или более редкими заболеваниями, такими как хроническая гранулематозная болезнь или синдром гипер-IgE ), несколько факторов приводят к повышенному риску АБЛА. [11] К ним относятся иммунные факторы (такие как атопия или иммуногенные HLA -ограниченные фенотипы ), [12] [13] а также генетические факторы (такие как мутации гена CFTR у астматиков и пациентов с муковисцидозом и мутация ZNF77, приводящая к преждевременному стоп-кодону у астматиков и пациентов с ABPA). [14] [10] [15] Позволяя спорам Aspergillus сохраняться в легочных тканях, они способствуют успешному прорастанию , что приводит к росту гиф в пробках слизи.
Существуют реакции гиперчувствительности как реакции I типа (атопические, с образованием иммуноглобулина Е, или IgE), так и реакции гиперчувствительности III типа (с образованием иммуноглобулина G , или IgG). [10] [16] Реакция IgE с Aspergillus антигенами приводит к дегрануляции тучных клеток с бронхоспазмом и увеличением проницаемости капилляров . [17] Иммунные комплексы (реакция III типа) и воспалительные клетки откладываются на слизистых оболочках дыхательных путей, что приводит к некрозу (гибель тканей) и эозинофильной инфильтрации. [10] типа 2 Т-хелперные клетки , по-видимому, играют важную роль при АБЛА из-за повышенной чувствительности к интерлейкину (IL) 4 и IL-5 . Эти цитокины усиливают дегрануляцию тучных клеток, усугубляя дыхательную недостаточность. [18] [19] [20]
Aspergillus также использует ряд факторов, чтобы продолжать уклоняться от реакции хозяина, в частности, использование протеолитических ферментов , которые прерывают направленные против него антитела IgG. Другой важной особенностью является его способность взаимодействовать и интегрироваться с эпителиальными поверхностями, что приводит к массивному провоспалительному ответу иммунной системы с участием IL-6 , IL-8 и MCP-1 ( лиганд рецептора CCL2 ). Протеазы, выделяемые как грибом, так и нейтрофилами, вызывают дальнейшее повреждение респираторного эпителия, что приводит к инициированию механизмов восстановления (таких как приток белков сыворотки и внеклеточного матрикса (ECM)) в месте инфекции. Споры и гифы Aspergillus могут взаимодействовать с белками ЕСМ, и предполагается, что этот процесс облегчает связывание спор с поврежденными участками дыхания. [10] [21]
По мере увеличения концентрации протеаз Aspergillus иммунологический эффект переключается с провоспалительного на ингибирующий и еще больше снижает способность фагоцитов уничтожать Aspergillus . В конечном итоге повторные острые эпизоды приводят к более масштабному повреждению легочных структур ( паренхимы ) и функции путем необратимого ремоделирования легких. При отсутствии лечения это проявляется прогрессирующими бронхоэктазами и фиброзом легких , которые часто наблюдаются в верхних долях и могут привести к рентгенологической картине, сходной с таковой при туберкулезе . [21] [22]
Диагностика
[ редактировать ]Точные критерии диагностики АБЛА еще не являются общепризнанными, хотя рабочие группы предложили конкретные рекомендации. [11] [23] Минимальные критерии включают пять факторов: наличие астмы и/или муковисцидоза, положительная кожная проба на Aspergillus sp., общий уровень IgE в сыворотке > 416 МЕ/мл (или кЕд/л), повышенное содержание к Aspergillus. видоспецифичных антител IgE и IgG и наличие инфильтратов на рентгенограмме грудной клетки. [24] [25]
АБЛА следует подозревать у пациентов с предрасполагающим заболеванием легких — чаще всего астмой или муковисцидозом — и часто связано с хроническим ограничением проходимости дыхательных путей (ХОЛ). У пациентов обычно наблюдаются симптомы рецидивирующей инфекции, такие как лихорадка , но они не реагируют на традиционную антибиотикотерапию. Плохо контролируемая астма является распространенным явлением: в серии случаев только у 19% пациентов с АБЛА наблюдалась хорошо контролируемая астма. Распространенными признаками являются свистящее дыхание и кровохарканье (кашель с кровью), а закупорка слизью наблюдается у 31–69% пациентов. [11]
Анализы крови и серология
[ редактировать ]Первый этап включает воздействие на кожу антигенов Aspergillus fumigatus; немедленная реакция – отличительная черта ABPA. [26] Тест следует проводить сначала путем кожного прик-теста, а в случае отрицательного результата – внутрикожной инъекции. Общая чувствительность процедуры составляет около 90%, хотя до 40% пациентов с астмой без АБЛА все еще могут проявлять некоторую чувствительность к антигенам Aspergillus (феномен, вероятно, связанный с менее тяжелой формой АБЛА, называемой тяжелой астмой с грибковой сенсибилизацией (SAFS). ). [11]
Анализы сыворотки крови являются важным маркером тяжести заболевания, а также полезны для первичной диагностики АБЛА. Когда сывороточный IgE в норме (и пациенты не лечатся глюкокортикоидами ), АБЛА исключается как причина симптомов. Повышенный уровень IgE увеличивает подозрения, хотя общепринятого порогового значения не существует. Значения могут быть указаны в международных единицах (МЕ/мл) или нг/мл, где 1 МЕ равна 2,4 нг/мл. С тех пор, как в 1970-х годах начались исследования, документирующие уровни IgE при АБЛА, использовались различные пороговые значения от 833 до 1000 МЕ/мл, чтобы исключить АБЛА и гарантировать дальнейшее серологическое тестирование. В настоящее время принято мнение, что следует использовать пороговую дозу 1000 МЕ/мл, поскольку более низкие значения встречаются при SAFS и астматической сенсибилизации . [11]
антител IgG Тест на преципитацию из сыворотки полезен, поскольку положительные результаты обнаруживаются у 69–90% пациентов, а также у 10% астматиков с SAFS и без него. Поэтому его необходимо использовать в сочетании с другими тестами. Существуют различные формы, включая иммуноферментный анализ (ELISA) и флуоресцентный иммуноферментный анализ (FEIA). Оба более чувствительны, чем обычный контриммуноэлектрофорез . IgG может быть не полностью специфичным для АБЛА, поскольку высокие уровни также обнаруживаются при хроническом аспергиллезе легких (ХЛА) наряду с более тяжелыми радиологическими данными. [11] [27]
До недавнего времени периферическая эозинофилия (высокое количество эозинофилов ) считалась отчасти признаком АБЛА. Более поздние исследования показывают, что только у 40% людей с АБЛА наблюдается эозинофилия, и, следовательно, низкое количество эозинофилов не обязательно исключает АБЛА; например, у пациентов, проходящих стероидную терапию, количество эозинофилов ниже. [11]
Радиологическое исследование
[ редактировать ]Консолидация и закупорка слизистой оболочки являются наиболее часто описываемыми радиологическими признаками, описанными в литературе ABPA, хотя большая часть доказательств консолидации возникла еще до разработки компьютерной томографии (КТ). Также распространены затенения трамвайных путей, помутнение пальцев в перчатках и «тени от зубной пасты». [28]
При использовании компьютерной томографии высокого разрешения можно лучше оценить распределение и характер бронхоэктазов в легких, и, следовательно, это инструмент выбора при радиологической диагностике АБЛА. Центральные (ограниченные двумя третями медиальной половины легкого) бронхоэктазы, сужающиеся по периферии бронхов, считаются обязательным условием патофизиологии АБЛА, хотя до 43% случаев наблюдается значительное распространение на периферию легкого. [1]
Часто встречается слизистое поражение верхних и нижних дыхательных путей. [1] Пробки гипоплотные, но на КТ появляются с высоким затуханием (более 70 единиц Хаунсфилда). [29] ) у до 20% пациентов. Там, где он присутствует, он является сильным диагностическим фактором АБЛА и отличает симптомы от других причин бронхоэктатической болезни. [11]
КТ может реже выявлять мозаичное затухание , центрилобулярные узелки в легких , помутнения типа «дерево в почке» и плевропульмональный фиброз (данные, согласующиеся с CPA, заболеванием с ABPA в качестве известного предшественника). [1] Редко на компьютерной томографии можно увидеть другие проявления, включая военные узелковые помутнения, перихилярные помутнения (которые имитируют внутригрудную лимфаденопатию ), плевральные выпоты и легочные массы. Кавитация и аспергиллома являются более редкими проявлениями, не превышающими 20% пациентов, и, вероятно, представляют собой переход от ABPA к CPA, если сопровождаются утолщением плевры или фиброзно-кавернозным заболеванием. [11]
Культура
[ редактировать ]Культивирование грибов из мокроты является вспомогательным тестом в диагностике АБЛА, но не является на 100% специфичным для АБЛА, поскольку A. fumigatus встречается повсеместно и обычно выделяется из отхаркивающих средств легких при других заболеваниях. Тем не менее, от 40 до 60% пациентов имеют положительные результаты посева в зависимости от количества взятых образцов. [11]
Постановка
[ редактировать ]Новые критерии, разработанные рабочей группой ISHAM по осложненной астме ABPA, предлагают 6-этапные критерии диагностики ABPA, хотя это еще не оформлено в официальных рекомендациях. [11] Это заменит нынешний золотой стандарт протокола постановки диагноза, разработанный Паттерсоном и его коллегами. [23] Стадия 0 представляет собой бессимптомную форму АБЛА с контролируемой астмой, но все еще отвечающую основным диагностическим требованиям положительной кожной пробы с повышенным уровнем общего IgE (> 1000 МЕ/мл). Стадия 6 представляет собой развитую АБЛА с наличием дыхательной недостаточности II типа или легочно-сердечной недостаточности с рентгенологическими признаками тяжелого фиброза, соответствующими АБЛА на КТ высокого разрешения. Диагноз необходимо ставить после исключения других, обратимых причин острой дыхательной недостаточности . [11]
Уход
[ редактировать ]Основное заболевание необходимо контролировать, чтобы предотвратить обострение и ухудшение АБЛА, и у большинства пациентов это заключается в лечении астмы или МВ. Также следует учитывать любые другие сопутствующие заболевания, такие как синусит или ринит. [30]
гиперчувствительности Механизмы , описанные выше , способствуют прогрессированию заболевания с течением времени и, если его не лечить, приводят к обширному фиброзу легочной ткани. Чтобы уменьшить это явление, основным методом лечения является терапия кортикостероидами (например, преднизолоном ); однако исследования кортикостероидов при АБЛА ограничены небольшими когортами и часто не являются двойными слепыми . Несмотря на это, есть доказательства того, что острое АБЛА улучшается при лечении кортикостероидами, поскольку оно уменьшает количество эпизодов консолидации . Существуют проблемы, связанные с длительной терапией кортикостероидами, которые могут вызывать тяжелую иммунную дисфункцию при хроническом использовании, а также метаболические нарушения, и были разработаны подходы для лечения АБЛА наряду с потенциальными побочными эффектами кортикостероидов. [30] [31]
Наиболее часто описываемый метод, известный как щадящий, включает использование противогрибкового средства для удаления спор из дыхательных путей, прилегающих к месту лечения кортикостероидами. Противогрибковый аспект направлен на уменьшение грибковых причин воспаления бронхов, а также на минимизацию дозы кортикостероидов, необходимой для уменьшения вклада иммунной системы в прогрессирование заболевания. Наиболее убедительные доказательства (двойные слепые рандомизированные - плацебо контролируемые исследования) получены для итраконазола два раза в день в течение четырех месяцев, что привело к значительному клиническому улучшению по сравнению с плацебо и было отражено у пациентов с МВ. Использование итраконазола, по-видимому, перевешивает риск от длительного приема высоких доз преднизолона. Новые триазольные препараты, такие как позаконазол или вориконазол , еще не изучались в ходе клинических испытаний в этом контексте. [30] [31]
Хотя польза от применения кортикостероидов в краткосрочной перспективе заметна и улучшает показатели качества жизни , существуют случаи, когда АБЛА перерастает в инвазивный аспергиллез во время лечения кортикостероидами. Кроме того, при одновременном применении с итраконазолом существует вероятность лекарственного взаимодействия индукции синдрома Кушинга и в редких случаях . Также могут быть вызваны метаболические расстройства, такие как сахарный диабет и остеопороз . [30] [31]
Чтобы смягчить эти риски, дозы кортикостероидов уменьшают раз в две недели, при условии отсутствия дальнейшего прогрессирования заболевания после каждого снижения. Если в течение трех месяцев после прекращения приема кортикостероидов не наблюдается обострений заболевания, считается, что у пациента наблюдается полная ремиссия . Исключением из этого правила являются пациенты, у которых диагностирована прогрессирующая АБЛА; в этом случае отмена кортикостероидов почти всегда приводит к обострению, и этим пациентам продолжают прием низких доз кортикостероидов (предпочтительно через день). [30] [31]
Сывороточный IgE можно использовать для определения лечения, его уровень проверяют каждые 6–8 недель после начала лечения стероидами, а затем каждые 8 недель в течение одного года. Это позволяет определить исходные уровни IgE, хотя важно отметить, что у большинства пациентов уровни IgE не полностью снижаются до исходного уровня. Рентгенография грудной клетки или КТ проводятся через 1–2 месяца лечения, чтобы убедиться инфильтратов . в рассасывании [30] [31]
Эпидемиология
[ редактировать ]Национальные и международные исследования бремени АБЛА ограничены, что усложняется нестандартизированными диагностическими критериями. По оценкам, бремя ABPA при астме составляет от 0,5 до 3,5%. [32] [33] и 1–17,7% при МВ. [32] [34] Пять национальных когорт, выявляющих распространенность АБЛА при астме (по оценкам GINA ), [35] были использованы в недавнем метаанализе для оценки глобального бремени ABPA, осложняющего астму. Из 193 миллионов человек, страдающих астмой во всем мире, распространенность ABPA при астме, по оценкам, составляет от 1,35 до 6,77 миллиона человек, при коэффициенте сокращения 0,7–3,5%. Также был предложен компромиссный вариант сокращения численности населения на 2,5%, в результате чего глобальное бремя составит около 4,8 миллиона пострадавших. В регионе Восточного Средиземноморья наблюдался самый низкий расчетный показатель распространенности: прогнозируемое бремя случаев составило 351 000; В совокупности в Америке было самое высокое прогнозируемое бремя - 1 461 000 случаев. Вероятно, это заниженная оценка общей распространенности, учитывая исключение пациентов с МВ и детей из исследования, а также ограниченность диагностического тестирования в менее развитых регионах. [33]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я Куша, М.; Тади, Р.; Субани, АО (1 сентября 2011 г.). «Легочный аспергиллез: клинический обзор» . Европейский респираторный обзор . 20 (121): 156–174. дои : 10.1183/09059180.00001011 . ПМЦ 9584108 . ПМИД 21881144 .
- ^ Jump up to: а б с д и ж Сисодия, Джитендра; Баджадж, Тушар (8 августа 2023 г.). «Аллергический бронхолегочный аспергиллез» . Издательство StatPearls. ПМИД 31194469 . Проверено 14 октября 2023 г.
- ^ «Статистика аспергиллеза — Аспергиллез — Виды грибковых заболеваний — Грибковые заболевания» . CDC . 5 декабря 2019 года . Проверено 14 октября 2023 г.
- ^ Бандрес, Мария В.; Моди, Пранав; Шарма, Сандип (8 августа 2023 г.). «Аспергиллус Фумигатус» . Издательство StatPearls. ПМИД 29494071 . Проверено 14 октября 2023 г.
- ^ Абузнейд, Юсеф С.; Яги, Ясмин; Мадия, Арейн; Салхаб, Наталья; Амро, Насер; Абухалаф, Сади А.; Харраз, Мохаммед (2021). «Ошибочный диагноз персистирующей астмы у пациента, страдающего острым бронхолегочным аспергиллезом (АБЛА)» . Анналы медицины и хирургии . 68 . Ovid Technologies (Wolters Kluwer Health). дои : 10.1016/j.amsu.2021.102696 . ISSN 2049-0801 . ПМЦ 8361028 .
- ^ Гринбергер, Пол А. (ноябрь 2002 г.). «Аллергический бронхолегочный аспергиллез» . Журнал аллергии и клинической иммунологии . 110 (5): 685–692. дои : 10.1067/май.2002.130179 . ПМИД 12417875 .
- ^ Jump up to: а б Холь, Тобиас М.; Фельдмессер, Марта (ноябрь 2007 г.). «Aspergillus fumigatus: принципы патогенеза и защиты хозяина» . Эукариотическая клетка . 6 (11): 1953–1963. дои : 10.1128/EC.00274-07 . ПМК 2168400 . ПМИД 17890370 .
- ^ Дьякон, ЖЖ; Панкхерст, LJ; Дрю, GH; Хейс, ET; Джексон, С.; Лонгхерст, Пи Джей; Лонгхерст, JWS; Лю, Дж.; Поллард, SJT; Тиррел, Сан-Франциско (ноябрь 2009 г.). «Распределение частиц по размерам переносимых по воздуху спор Aspergillus fumigatus, выделяемых из компоста с использованием мембранной фильтрации». Атмосферная среда . 43 (35): 5698–5701. Бибкод : 2009AtmEn..43.5698D . дои : 10.1016/j.atmosenv.2009.07.042 .
- ^ Докрелл, Дэвид Х.; МакГрат, Эммет Э.; Уайт, Мория КБ; Сабро, Ян (2007). «Нейтрофил». Иммунология грибковых инфекций . стр. 51–73. дои : 10.1007/1-4020-5492-0_3 . ISBN 978-1-4020-5491-4 . S2CID 215264748 .
- ^ Jump up to: а б с д и Мосс, РБ (январь 2005 г.). «Патофизиология и иммунология аллергического бронхолегочного аспергиллеза». Медицинская микология . 43 (с1): 203–206. CiteSeerX 10.1.1.585.3463 . дои : 10.1080/13693780500052255 . ПМИД 16110813 . S2CID 35301840 .
- ^ Jump up to: а б с д и ж г час я дж к л Агарвал, Р.; Чакрабарти, А.; Шах, А.; Гупта, Д.; Мейс, Дж. Ф.; Гулерия, Р.; Мосс, Р.; Деннинг, Д.В.; Рабочая группа ISHAM по ABPA, осложняющая астму (август 2013 г.). «Аллергический бронхолегочный аспергиллез: обзор литературы и предложение новых диагностических и классификационных критериев». Клиническая и экспериментальная аллергия . 43 (8): 850–873. дои : 10.1111/cea.12141 . ПМИД 23889240 . S2CID 24077597 .
- ^ Антунес, Дж.; Фернандес, А.; Мигель Боррего, Л.; Лейрия-Пинто, П.; Кавако, Дж. (1 сентября 2010 г.). «Муковисцидоз, атопия, астма и АБЛА». Аллергология и иммунопатология . 38 (5): 278–284. дои : 10.1016/j.aller.2010.06.002 . hdl : 10400.17/1668 . ПМИД 20675033 .
- ^ Уолл, Мануэль; Мондехар-Лопес, Педро; Мойя-Килес, Мария Роза; Сальгадо, Хема; Пастор-питомник Мария Долорес; Лопес-Эрнандес, Рут; Буа, Франциско; Кампильо, Хосе Антонио; Мингела, Альфредо; Гарсия-Алонсо, Ана; Санчес-Солис, Мануэль; Альварес-Лопес, Мария Росио (март 2013 г.). «Гены HLA-DRB1 и HLA-DQB1 на восприимчивость и защиту от аллергического бронхолегочного аспергиллеза у больных муковисцидозом: HLA и ABPA при муковисцидозе» . Микробиология и иммунология . 57 (3): 193–197. дои : 10.1111/1348-0421.12020 . ПМИД 23278646 .
- ^ Маршан, Эрик; Делонуа, Люк; Бранкалеоне, Пьер; Ванденплас, Оливье; Мерес, Мишель; Вереллен-Дюмулен, Кристина; Рахье, Жан-Франсуа (март 2001 г.). «Частота мутаций гена регулятора трансмембранной проводимости при муковисцидозе и аллеля 5T у пациентов с аллергическим бронхолегочным аспергиллезом». Грудь . 119 (3): 762–767. дои : 10.1378/сундук.119.3.762 . ПМИД 11243954 . S2CID 25448045 .
- ^ Гаго, Сара; Овертон, Никола Л.Д.; Бен-Газзи, Нагва; Новак-Фрейзер, Лилианн; Прочтите, Ник Д.; Деннинг, Дэвид В.; Бойер, Пол (декабрь 2018 г.). «Колонизация легких Aspergillus fumigatus контролируется ZNF77» . Природные коммуникации . 9 (1): 3835. Бибкод : 2018NatCo...9.3835G . дои : 10.1038/s41467-018-06148-7 . ПМК 6147781 . ПМИД 30237437 .
- ^ Читкара, РК; Саринас, П.С.; Фик Р.Б., младший (декабрь 2001 г.). «Лечение иммуноглобулином Е и анти-IgE при заболеваниях легких». Архив Мональди по заболеваниям грудной клетки 56 (6): 514–20. ПМИД 11980283 .
- ^ Матиас, Клинтон Б.; Фрейшмидт, Ева-Жасмин; Каплан, Бенджамин; Джонс, Татьяна; Поддиге, Дмитрий; Син, Вэй; Харрисон, Криста Л.; Гуриш, Майкл Ф.; Эттген, Ханс К. (15 февраля 2009 г.). «IgE влияет на количество и функцию зрелых тучных клеток, но не на рекрутирование предшественников при аллергическом воспалении легких» . Журнал иммунологии . 182 (4): 2416–2424. doi : 10.4049/jimmunol.0801569 . ПМЦ 2653867 . ПМИД 19201896 .
- ^ Кнутсен, АП; Хатчинсон, PS; Альберс, генеральный менеджер; Консолино, Дж.; Смик, Дж.; Куруп, вице-президент (январь 2004 г.). «Повышенная чувствительность к IL-4 у больных муковисцидозом с аллергическим бронхолегочным аспергиллезом». Аллергия . 59 (1): 81–87. дои : 10.1046/j.1398-9995.2003.00129.x . ПМИД 14674938 . S2CID 72623230 .
- ^ Мюллер, Ю; Пилер, Д; Стенцель, В; Келер, Г; Фрей, О; Хелд, Дж; Гранерт, А; Рихтер, Т; Эшке, М; Камрадт, Т; Бромбахер, Ф; Альбер, Г. (май 2012 г.). «Отсутствие экспрессии рецептора IL-4 на Т-хелперных клетках снижает полифункциональность Т-хелперов-2 и придает устойчивость к аллергическому бронхолегочному микозу» . Иммунология слизистой оболочки . 5 (3): 299–310. дои : 10.1038/ми.2012.9 . ПМИД 22333910 .
- ^ Сков, М; Поульсен, ЛК; Кох, К. (февраль 1999 г.). «Повышение антигенспецифического ответа Th-2 при аллергическом бронхолегочном аспергиллезе (АБЛА) у пациентов с муковисцидозом». Детская пульмонология . 27 (2): 74–9. doi : 10.1002/(sici)1099-0496(199902)27:2<74::aid-ppul2>3.0.co;2-l . ПМИД 10088929 . S2CID 27657458 .
- ^ Jump up to: а б Кауфман, Хенк Ф (2003). «Иммунопатогенез аллергического бронхолегочного аспергиллеза и ремоделирования дыхательных путей» (PDF) . Границы бионауки . 8 (5): е190–196. дои : 10.2741/990 . ПМИД 12456379 . S2CID 25768595 . Архивировано из оригинала (PDF) 5 марта 2019 г.
- ^ Коллинз, Дж (ноябрь 2001 г.). «КТ-признаки и закономерности заболеваний легких». Радиологические клиники Северной Америки . 39 (6): 1115–35. дои : 10.1016/s0033-8389(05)70334-1 . ПМИД 11699664 .
- ^ Jump up to: а б Паттерсон, Рой; Гринбергер, Пенсильвания; Радин, Р.К.; Робертс, М. (1 марта 1982 г.). «Аллергический бронхолегочный аспергиллез: стадирование как помощь в лечении». Анналы внутренней медицины . 96 (3): 286–291. CiteSeerX 10.1.1.1001.9839 . дои : 10.7326/0003-4819-96-3-286 . ПМИД 7059089 .
- ^ Редди, Ашвини; Гринбергер, Пол А. (май 2017 г.). «Аллергический бронхолегочный аспергиллез». Журнал аллергии и клинической иммунологии: на практике . 5 (3): 866–867. дои : 10.1016/j.jaip.2016.08.019 . ПМИД 28483324 .
- ^ Кнутсен, Алан П.; Буш, Роберт К.; Демейн, Джеффри Г.; Деннинг, Дэвид В.; Диксит, Анупма; Ярмарки, Эбби; Гринбергер, Пол А.; Кариуки, Барбара; Кита, Хирохито; Куруп, Вишванат П.; Мосс, Ричард Б.; Нивен, Роберт М.; Пэшли, Кэтрин Х.; Славин, Раймонд Г.; Виджай, Хари М.; Уордлоу, Эндрю Дж. (февраль 2012 г.). «Грибки и аллергические заболевания нижних дыхательных путей» . Журнал аллергии и клинической иммунологии . 129 (2): 280–291. дои : 10.1016/j.jaci.2011.12.970 . ПМИД 22284927 .
- ^ Хоган, Селия; Деннинг, Дэвид (декабрь 2011 г.). «Аллергический бронхолегочный аспергиллез и связанные с ним аллергические синдромы». Семинары по респираторной медицине и медицине интенсивной терапии . 32 (6): 682–692. дои : 10.1055/s-0031-1295716 . ПМИД 22167396 . S2CID 260319453 .
- ^ Бэйнс, Соня Н.; Джадсон, Марк А. (июнь 2012 г.). «Аллергический бронхолегочный аспергиллез». Клиники грудной медицины . 33 (2): 265–281. дои : 10.1016/j.ccm.2012.02.003 . ПМИД 22640845 .
- ^ Гринбергер, Пенсильвания (май – июнь 2012 г.). «Глава 18: Аллергический бронхолегочный аспергиллез». Труды по аллергии и астме . 33 Приложение 1 (3): S61–3. дои : 10.2500/aap.2012.33.3551 . ПМИД 22794691 .
- ^ Агарвал, Ритеш; Сегал, Индерпол Сингх; Дхурия, Сахаджал; Аггарвал, Ашутош (2016). «Рентгенологические критерии диагностики слизи высокого затухания при аллергическом бронхолегочном аспергиллезе» . Грудь . 149 (4): 1109–1110. дои : 10.1016/j.chest.2015.12.043 . ISSN 0012-3692 . ПМИД 27055707 .
- ^ Jump up to: а б с д и ж Уолш, Томас Дж.; Анаисси, Элиас Дж.; Деннинг, Дэвид В.; Хербрехт, Рауль; Контояннис, Димитриос П.; Марр, Кирен А.; Моррисон, Вики А.; Сигал, Брам Х; Стейнбах, Уильям Дж.; Стивенс, Дэвид А.; ван Бурик, Джо-Энн; Вингард, Джон Р.; Паттерсон, Томас Ф.; Американское общество инфекционистов (1 февраля 2008 г.). «Лечение аспергиллеза: Рекомендации по клинической практике Американского общества инфекционистов» (PDF) . Клинические инфекционные болезни . 46 (3): 327–360. дои : 10.1086/525258 . ПМИД 18177225 .
- ^ Jump up to: а б с д и Махадавиния, Махбубе; Грэммер, Лесли К. (июнь 2012 г.). «Лечение аллергического бронхолегочного аспергиллеза: обзор и обновление» . Терапевтические достижения в области респираторных заболеваний . 6 (3): 173–187. дои : 10.1177/1753465812443094 . ПМИД 22547692 . S2CID 20436079 .
- ^ Jump up to: а б Стивенс, Дэвид А.; Мосс, Ричард Б.; Куруп, Вишванат П.; Кнутсен, Алан П.; Гринбергер, Пол; Джадсон, Марк А.; Деннинг, Дэвид В.; Крамери, Рето; Броуди, Алан С.; Лайт, Майкл; Сков, Марианна; Мейш, Уильям; Мастелла, Джанни; Участники согласительной конференции Фонда муковисцидоза (октябрь 2003 г.). «Аллергический бронхолегочный аспергиллез при муковисцидозе — современное состояние: Консенсусная конференция Фонда муковисцидоза» . Клинические инфекционные болезни . 37 (с3): С225–С264. дои : 10.1086/376525 . ПМИД 12975753 .
- ^ Jump up to: а б Деннинг, Дэвид В.; Плеври, Алекс; Коул, Дональд К. (май 2013 г.). «Глобальное бремя аллергического бронхолегочного аспергиллеза с астмой и его осложнением хронического легочного аспергиллеза у взрослых» . Медицинская микология . 51 (4): 361–370. дои : 10.3109/13693786.2012.738312 . ПМИД 23210682 .
- ^ Армстед, Джоан; Моррис, Джули; Деннинг, Дэвид В. (10 июня 2014 г.). «Многострановая оценка различных проявлений аспергиллеза при муковисцидозе» . ПЛОС ОДИН . 9 (6): е98502. Бибкод : 2014PLoSO...998502A . дои : 10.1371/journal.pone.0098502 . ПМК 4051580 . ПМИД 24914809 .
- ^ «ДЖИНА» (PDF) . Глобальное бремя астмы . Архивировано из оригинала (PDF) 9 мая 2013 г. Проверено 5 февраля 2014 г. [ нужна страница ]
Внешние ссылки
[ редактировать ]- Фонд исследований грибков
- Веб-сайт Аспергилла
- Аллергический бронхолегочный аспергиллез — Тетрадь врача общей практики
- Медпикс. Рентгенологические снимки ABPA