Грипп
| Грипп | |
|---|---|
| Другие имена | грипп, грипп, грипп (по-французски грипп) |
 | |
| Вирус гриппа | |
| Специальность | Инфекционное заболевание |
| Симптомы | Лихорадка , насморк , боль в горле , мышечная боль , головная боль , кашель , усталость. |
| Обычное начало | 1–4 дня после заражения |
| Продолжительность | 2–8 дней |
| Причины | Вирусы гриппа |
| Профилактика | Мытье рук , вакцинация от гриппа |
| Медикамент | Противовирусные препараты, такие как осельтамивир |
| Частота | 3–5 миллионов тяжелых случаев в год [1] [2] |
| Летальные исходы | >290 000–650 000 смертей в год [3] [4] |
Грипп , широко известный как « грипп » или просто « грипп », представляет собой инфекционное заболевание, вызываемое вирусами гриппа . Симптомы варьируются от легких до тяжелых и часто включают лихорадку , насморк , боль в горле , мышечную боль , головную боль , кашель и усталость . Эти симптомы начинаются через один-четыре (обычно два) дня после контакта с вирусом и длятся от двух до восьми дней. Могут возникнуть диарея и рвота , особенно у детей. Грипп может перерасти в пневмонию из-за вируса или последующей бактериальной инфекции . Другие осложнения включают острый респираторный дистресс-синдром , менингит , энцефалит и ухудшение ранее существовавших проблем со здоровьем, таких как астма и сердечно-сосудистые заболевания .
Существует четыре типа вируса гриппа: типы А, В, С и D. Водоплавающие птицы являются основным источником вируса гриппа А (IAV), который также широко распространен у различных млекопитающих, включая человека и свиней. Вирус гриппа B (IBV) и вирус гриппа C (ICV) преимущественно поражают людей, а вирус гриппа D (IDV) обнаруживается у крупного рогатого скота и свиней. Вирус гриппа А и вирус гриппа В циркулируют у человека и вызывают сезонные эпидемии , а вирус гриппа С вызывает легкую инфекцию, преимущественно у детей. Вирус гриппа D может заразить человека, но неизвестно, вызывает ли он заболевание. У человека вирусы гриппа в основном передаются при воздушно-капельным путем кашле и чихании. Также происходит передача через аэрозоли и поверхности, загрязненные вирусом.
Частое мытье рук и прикрытие рта и носа при кашле и чихании снижают передачу инфекции. Ежегодная вакцинация может помочь обеспечить защиту от гриппа. Вирусы гриппа, особенно вирус гриппа А, быстро эволюционируют, поэтому вакцины против гриппа регулярно обновляются, чтобы соответствовать штаммам гриппа, которые находятся в обращении. Вакцины обеспечивают защиту от вируса гриппа А подтипов H1N1 и H3N2 и одного или двух подтипов вируса гриппа В. Инфекция гриппа диагностируется с помощью лабораторных методов, таких как тесты на антитела или антигены и полимеразная цепная реакция ( ПЦР ) для идентификации нуклеиновой кислоты вируса . Заболевание можно лечить поддерживающими мерами , а в тяжелых случаях — противовирусными препаратами , такими как осельтамивир . У здоровых людей грипп обычно проходит самостоятельно и редко приводит к летальному исходу, но в группах высокого риска он может быть смертельным.
В обычный год от пяти до 15 процентов населения заболевают гриппом. Ежегодно в мире регистрируется от 3 до 5 миллионов тяжелых случаев, при этом ежегодно во всем мире происходит до 650 000 случаев смерти от респираторных заболеваний. Смертельные случаи чаще всего происходят в группах высокого риска, включая маленьких детей, пожилых людей и людей с хроническими заболеваниями. В регионах с умеренным климатом пик числа случаев гриппа приходится на зиму, тогда как в тропиках грипп может возникать круглый год. С конца 1800-х годов пандемические вспышки новых штаммов гриппа происходили каждые 10–50 лет. пять пандемий гриппа С 1900 года произошло : испанский грипп с 1918 по 1920 год, который был самым тяжелым; азиатский грипп в 1957 году; гонконгский грипп в 1968 году; русский грипп в 1977 году; и пандемия свиного гриппа в 2009 году.
Признаки и симптомы

Симптомы гриппа аналогичны симптомам простуды, но обычно более выражены и реже сопровождаются насморком . [8] [9] Время между контактом с вирусом и развитием симптомов ( инкубационный период ) составляет от одного до четырех дней, чаще всего от одного до двух дней. Многие инфекции протекают бессимптомно. [10] Симптомы появляются внезапно, и начальные симптомы преимущественно неспецифичны, включая лихорадку, озноб, головные боли, мышечные боли , недомогание , потерю аппетита , недостаток энергии и спутанность сознания. Они обычно сопровождаются респираторными симптомами, такими как сухой кашель , боль или сухость в горле , хриплый голос , заложенность или насморк . Кашель является наиболее частым симптомом. [1] Также могут возникнуть желудочно-кишечные симптомы, включая тошноту, рвоту, диарею, [11] и гастроэнтерит, [12] особенно у детей. Стандартные симптомы гриппа обычно длятся от двух до восьми дней. [13] Некоторые исследования показывают, что грипп может вызывать длительные симптомы, подобно длительному COVID . [14] [15] [16]
Симптоматические инфекции обычно легкие и ограничиваются верхними дыхательными путями , но прогрессирование до пневмонии встречается относительно часто. Пневмония может быть вызвана первичной вирусной инфекцией или вторичной бактериальной инфекцией . Первичная пневмония характеризуется быстрым прогрессированием лихорадки, кашлем, затрудненным дыханием и низким уровнем кислорода , что вызывает синюшность кожи . Это особенно распространено среди тех, у кого есть основное сердечно-сосудистое заболевание, такое как ревматическая болезнь сердца . Вторичная пневмония обычно имеет период улучшения симптомов в течение одной-трех недель. [17] с последующим рецидивирующим повышением температуры, выделением мокроты и накоплением жидкости в легких , [1] но может возникнуть и через несколько дней после появления симптомов гриппа. [17] Около трети случаев первичной пневмонии сопровождается вторичной пневмонией, которую чаще всего вызывают бактерии Streptococcus pneumoniae и Staphylococcus aureus . [10] [1]
Вирусология
Типы вирусов

Вирусы гриппа включают четыре вида, каждый из которых является единственным представителем своего рода. Четыре рода гриппа включают четыре из семи родов семейства Orthomyxoviridae . Они есть: [1] [18]
- Вирус гриппа А (IAV), род Alphainfluenzavirus
- Вирус гриппа B (IBV), род Betainfluenzavirus
- Вирус гриппа С (ICV), род Gammainfluenzavirus
- Вирус гриппа D (IDV), род Deltainfluenzavirus
Вирус гриппа А является причиной большинства случаев тяжелых заболеваний, а также сезонных эпидемий и периодических пандемий. Он заражает людей всех возрастов, но имеет тенденцию непропорционально вызывать тяжелые заболевания у пожилых людей, очень молодых людей и людей с хроническими проблемами со здоровьем. Птицы являются основным резервуаром вируса гриппа А, особенно водоплавающие птицы, такие как утки, гуси, кулики и чайки. [19] [20] но вирус также циркулирует среди млекопитающих, включая свиней, лошадей и морских млекопитающих. Вирус гриппа А классифицируется на подтипы на основе вирусных белков гемагглютинина (H) и нейраминидазы (N). [21] По состоянию на 2019 год идентифицировано 18 подтипов H и 11 подтипов N. Большинство потенциальных комбинаций зарегистрировано у птиц, но H17-18 и N10-11 обнаружены только у летучих мышей. Известно, что у людей циркулируют только H-подтипы H1-3 и N-подтипы N1-2. [21] Подтипы вируса гриппа А, находящиеся в обращении по состоянию на 2018 г. [update] являются H1N1 и H3N2. [2] гриппа А Образцы вируса идентифицируются по номенклатуре, которая указывает вид хозяина, место сбора, номер штамма и год. [22] - такой как A/swine/South Dakota/152B/2009 (H1N2) . [23]
Вирус гриппа B в основном заражает людей, но был идентифицирован у тюленей, лошадей, собак и свиней. [21] Вирус гриппа B не имеет подтипов, подобных вирусу гриппа A, но имеет две антигенно различные линии, называемые B/Victoria/2/1987-подобной и B/Yamagata/16/1988-подобной линией. [1] или просто (B/)Виктория(-подобно) и (Б/)Ямагата(-подобно). [21] [2] Обе линии циркулируют у человека. [1] непропорционально сильно влияет на детей. [11] Вирусы гриппа В способствуют сезонным эпидемиям наряду с вирусами гриппа А, но никогда не были связаны с пандемией. [21]
Вирус гриппа С, как и вирус гриппа В, в основном обнаруживается у людей, хотя его обнаруживают у свиней, одичавших собак, дромадеров , крупного рогатого скота и собак. [12] [21] Инфекция, вызванная вирусом гриппа С, в первую очередь поражает детей и обычно протекает бессимптомно. [1] [11] или имеет легкие симптомы, похожие на простуду, хотя могут возникнуть и более серьезные симптомы, такие как гастроэнтерит и пневмония. [12] В отличие от вируса гриппа А и вируса гриппа В, вирус гриппа С не был в центре внимания исследований, касающихся противовирусных препаратов, вакцин и других мер против гриппа. [21] Вирус гриппа С подразделяется на шесть генетических/антигенных линий. [12] [24]
Вирус гриппа D был выделен от свиней и крупного рогатого скота, причем последний является естественным резервуаром. Инфекция также наблюдалась у людей, лошадей, верблюдов и мелких жвачных животных, таких как козы и овцы. [21] [24] Вирус гриппа D имеет отдаленное родство с вирусом гриппа С. Хотя работники крупного рогатого скота иногда получали положительный результат на предыдущую инфекцию вируса гриппа D, неизвестно, вызывает ли он заболевание у людей. [1] [11] [12] Вирус гриппа С и вирус гриппа D подвергаются более медленной антигенной эволюции, чем вирусы гриппа А и вирус гриппа В. Из-за этой антигенной стабильности появляется относительно мало новых линий. [24]
Геном и структура

Вирусы гриппа имеют отрицательным смыслом сегментированный одноцепочечный РНК-геном с . Отрицательный смысл генома означает, что его можно использовать в качестве матрицы для синтеза информационной РНК (мРНК). [10] Вирус гриппа А и вирус гриппа В имеют восемь сегментов генома, которые кодируют 10 основных белков. Вирус гриппа C и вирус гриппа D имеют семь сегментов генома, которые кодируют девять основных белков. [12] Три сегмента кодируют три субъединицы РНК-зависимого комплекса РНК-полимеразы (RdRp): PB1, транскриптазу, PB2, которая распознает 5'-кэпы, и PA (P3 для вируса гриппа C и вируса гриппа D), эндонуклеазу. [25] Матриксный белок (М1) и мембранный белок (М2) имеют общий сегмент, как и неструктурный белок (NS1) и белок ядерного экспорта (NEP). [1] Для вируса гриппа A и вируса гриппа B гемагглютинин (HA) и нейраминидаза (NA) кодируются по одному сегменту каждый, тогда как вирусы гриппа C и вирус гриппа D кодируют слитый белок гемагглютинин-эстераза (HEF) в одном сегменте, который объединяет функции ХА и NA. Последний сегмент генома кодирует вирусный нуклеопротеин (NP). [25] Вирусы гриппа также кодируют различные дополнительные белки, такие как PB1-F2 и PA-X, которые экспрессируются через альтернативные открытые рамки считывания. [1] [26] и которые важны для подавления защиты хозяина, вирулентности и патогенности. [27]
Вирусная частица, называемая вирионом, является плеоморфной и имеет нитевидную, палочковидную или сферическую форму. Клинические изоляты имеют тенденцию быть плеоморфными, тогда как штаммы, адаптированные к лабораторному росту, обычно производят сферические вирионы. Нитчатые вирионы имеют размер около 250 нанометров (нм) на 80 нм, палочковидные - 120–250 на 95 нм и сферические - 120 нм в диаметре. [28] Вирион состоит из каждого сегмента генома, связанного с нуклеопротеинами в отдельных рибонуклеопротеиновых (РНП) комплексах для каждого сегмента, каждый из которых окружен липидной двухслойной мембраной, называемой вирусной оболочкой . Существует копия RdRp, включая все субъединицы, привязанная к каждому RNP. Оболочка структурно усилена матриксными белками внутри, которые окружают РНП. [3] а конверт содержит HA и NA (или HEF [24] ) белки, выступающие наружу от внешней поверхности оболочки. ХА и ХЭФ [24] белки имеют четкую структуру «головки» и «ножки». Белки М2 образуют протон-ионные каналы через вирусную оболочку, необходимые для входа и выхода вируса. Вирусы гриппа B содержат поверхностный белок NB, который закреплен в оболочке, но его функция неизвестна. [1]
Жизненный цикл

Жизненный цикл вируса начинается со связывания с клеткой-мишенью. Связывание опосредуется вирусными белками НА на поверхности оболочки, которые связываются с клетками, содержащими рецепторы сиаловой кислоты на поверхности клеточной мембраны. [1] [19] [3] Для подтипов N1 с мутацией «G147R» и подтипов N2 белок NA может инициировать проникновение. Перед связыванием белки NA способствуют доступу к клеткам-мишеням путем разложения слизи, что помогает удалить внеклеточные рецепторы-ловушки, которые могут препятствовать доступу к клеткам-мишеням. [3] После связывания вирус интернализуется в клетку эндосомой , содержащей внутри себя вирион. Эндосома подкисляется клеточной вАТФазой. [26] иметь более низкий pH, что вызывает конформационные изменения HA, которые позволяют слиянию вирусной оболочки с эндосомальной мембраной. [27] В то же время ионы водорода диффундируют в вирион через ионные каналы М2, нарушая внутренние межбелковые взаимодействия и высвобождая РНП в цитозоль клетки-хозяина . Оболочка белка M1, окружающая РНП, разрушается, полностью снимая покрытие с РНП в цитозоле. [26] [3]
Затем РНП импортируются в ядро с помощью сигналов вирусной локализации. Там вирусная РНК-полимераза транскрибирует мРНК, используя геномную цепь с отрицательным смыслом в качестве матрицы. Полимераза захватывает 5'-конец вирусной мРНК из клеточной РНК для первичного синтеза мРНК, а 3'-конец мРНК полиаденилируется в конце транскрипции. [25] После транскрипции вирусной мРНК она экспортируется из ядра и транслируется рибосомами хозяина кэп-зависимым образом для синтеза вирусных белков. [26] RdRp также синтезирует комплементарные цепи вирусного генома с положительным смыслом в комплементарном комплексе RNP, которые затем используются вирусными полимеразами в качестве матриц для синтеза копий генома с отрицательным смыслом. [1] [3] Во время этих процессов RdRps вирусов птичьего гриппа (AIV) оптимально функционируют при более высокой температуре, чем вирусы гриппа млекопитающих. [13]
Недавно синтезированные субъединицы вирусной полимеразы и белки NP импортируются в ядро для дальнейшего увеличения скорости репликации вируса и формирования РНП. [25] Белки HA, NA и M2 передаются с помощью белков M1 и NEP. [27] к клеточной мембране через аппарат Гольджи [25] и внедряется в клеточную мембрану. Вирусные неструктурные белки, включая NS1, PB1-F2 и PA-X, регулируют клеточные процессы хозяина, отключая противовирусные реакции. [1] [27] [3] PB1-F2 также взаимодействует с PB1, чтобы дольше удерживать полимеразы в ядре. [20] Белки M1 и NEP локализуются в ядре на более поздних стадиях инфекции, связываются с вирусными РНП и опосредуют их экспорт в цитоплазму, где они мигрируют к клеточной мембране с помощью переработанных эндосом и объединяются в сегменты генома. [1] [3]
Вирусы-потомки покидают клетку путем отпочкования от клеточной мембраны, что инициируется накоплением белков М1 на цитоплазматической стороне мембраны. Вирусный геном встроен в вирусную оболочку, полученную из частей клеточной мембраны, которые содержат белки HA, NA и M2. В конце отпочкования белки HA остаются прикрепленными к клеточной сиаловой кислоте до тех пор, пока они не будут расщеплены сиалидазной активностью белков NA. Затем вирион высвобождается из клетки. Сиалидазная активность NA также расщепляет любые остатки сиаловой кислоты с поверхности вируса, что помогает предотвратить агрегацию вновь собранных вирусов вблизи поверхности клетки и повысить инфекционность. [1] [3] Подобно другим аспектам репликации гриппа, оптимальная активность NA зависит от температуры и pH. [13] В конечном итоге присутствие большого количества вирусной РНК в клетке запускает апоптоз (запрограммированную смерть клетки), который инициируется клеточными факторами, ограничивающими репликацию вируса. [26]
Антигенный дрейф и сдвиг

Двумя ключевыми процессами, посредством которых развиваются вирусы гриппа, являются антигенный дрейф и антигенный сдвиг . Антигенный дрейф – это когда антигены вируса гриппа изменяются из-за постепенного накопления мутаций в гене антигена (HA или NA). [19] Это может произойти в ответ на эволюционное давление , оказываемое иммунным ответом хозяина. Антигенный дрейф особенно характерен для белка НА, у которого всего несколько аминокислотных изменений в головной области могут представлять собой антигенный дрейф. [2] [24] Результатом является производство новых штаммов, которые могут уклоняться от ранее существовавшего иммунитета, опосредованного антителами. [1] [11] Антигенный дрейф происходит у всех видов гриппа, но медленнее у B, чем у A, и наиболее медленным у C и D. [24] Антигенный дрейф является основной причиной сезонного гриппа. [30] и требует ежегодного обновления вакцин против гриппа. ГК является основным компонентом инактивированных вакцин, поэтому надзор отслеживает антигенный дрейф этого антигена среди циркулирующих штаммов. Антигенная эволюция вирусов гриппа человека происходит быстрее, чем у свиней и лошадей. У диких птиц антигенные вариации внутри подтипа , по-видимому, ограничены, но наблюдались у домашней птицы. [1] [11]
Антигенный сдвиг – это внезапное и резкое изменение антигена вируса гриппа, обычно НА. Во время антигенного сдвига антигенно разные штаммы, инфицирующие одну и ту же клетку, могут реассоциировать сегменты генома друг с другом, производя гибридное потомство. Поскольку все вирусы гриппа имеют сегментированный геном, все они способны к реассортации. [12] [24] Антигенный сдвиг происходит только среди вирусов гриппа одного и того же рода. [25] и чаще всего встречается среди вирусов гриппа А. В частности, рекомбинация очень распространена при вирусах гриппа AIV, создавая большое разнообразие вирусов гриппа у птиц, но редко встречается у людей, лошадей и собак. [31] Свиньи, летучие мыши и перепела имеют рецепторы как для вирусов гриппа А млекопитающих, так и для птиц, поэтому они являются потенциальными «смесительными сосудами» для рекомбинации. [21] Если животный штамм реассортируется с человеческим штаммом, [2] тогда может появиться новый штамм, способный передаваться от человека к человеку. Это вызвало пандемии, но лишь в ограниченном количестве, поэтому трудно предсказать, когда произойдет следующая. [1] [11]
Механизм
Передача инфекции
Инфицированные люди могут передавать вирусы гриппа через дыхание, разговор, кашель и чихание, в результате чего попадают дыхательные капли и аэрозоли в воздух , содержащие вирусные частицы. Человек, восприимчивый к инфекции, может заразиться гриппом при контакте с этими частицами. [17] [32] Респираторные капли относительно велики и перемещаются менее двух метров, прежде чем упасть на близлежащие поверхности. Аэрозоли меньше по размеру и дольше остаются во взвешенном состоянии в воздухе, поэтому им требуется больше времени для оседания и они могут перемещаться дальше. [32] [4] Вдыхание аэрозолей может привести к заражению. [33] но большая часть передачи происходит в зоне около двух метров вокруг инфицированного человека воздушно-капельным путем. [10] которые контактируют со слизистой оболочкой верхних дыхательных путей. [33] передача инфекции через контакт с человеком, биологическими жидкостями или промежуточными объектами ( фомитами ). Также может произойти [10] [32] поскольку вирусы гриппа могут сохраняться часами на непористых поверхностях. [4] Если руки загрязнены, то прикосновение к лицу может вызвать инфекцию. [34]
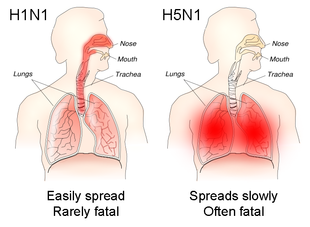
Грипп обычно передается от одного дня до появления симптомов до 5–7 дней после него. [11] У здоровых взрослых вирус выделяется до 3–5 дней. У детей и людей с ослабленным иммунитетом вирус может передаваться в течение нескольких недель. [10] Дети в возрасте от 2 до 17 лет считаются основными и наиболее эффективными распространителями гриппа. [1] [11] Дети, которые ранее не подвергались многократному контакту с вирусами гриппа, выделяют вирус в больших количествах и в течение более длительного времени, чем другие дети. [1] К людям, подверженным риску заражения гриппом, относятся работники здравоохранения, социальные работники, а также те, кто живет с людьми, уязвимыми к гриппу, или ухаживает за ними. В учреждениях длительного ухода грипп может распространяться быстро. [11] Передаче гриппа могут способствовать различные факторы, в том числе более низкая температура, более низкая абсолютная и относительная влажность , меньшее ультрафиолетовое излучение солнца, [33] [35] и скученность. [32] Вирусы гриппа, поражающие верхние дыхательные пути, такие как H1N1, обычно более легкие, но более заразные, тогда как вирусы, поражающие нижние дыхательные пути, такие как H5N1, обычно вызывают более тяжелое заболевание, но менее заразны. [10]
Патофизиология
У человека вирусы гриппа сначала вызывают инфекцию, заражая эпителиальные клетки дыхательных путей. Заболевание во время инфекции является, прежде всего, результатом воспаления легких и поражения, вызванного инфекцией и гибелью эпителиальных клеток, в сочетании с воспалением, вызванным реакцией иммунной системы на инфекцию. Могут вовлекаться и нереспираторные органы, однако механизмы поражения гриппа в этих случаях неизвестны. Тяжелое респираторное заболевание может быть вызвано множеством неисключительных механизмов, включая обструкцию дыхательных путей, потерю альвеолярной структуры, потерю целостности эпителия легких из-за инфекции и гибели эпителиальных клеток, а также деградацию внеклеточного матрикса, поддерживающего структуру легких. В частности, инфекция альвеолярных клеток, по-видимому, приводит к тяжелым симптомам, поскольку это приводит к нарушению газообмена и позволяет вирусам инфицировать эндотелиальные клетки, которые производят большое количество провоспалительных цитокинов . [17]
Пневмония, вызванная вирусами гриппа, характеризуется высоким уровнем репликации вируса в нижних дыхательных путях, что сопровождается сильной провоспалительной реакцией, называемой цитокиновым штормом . [1] Инфекция H5N1 или H7N9 особенно приводит к образованию высоких уровней провоспалительных цитокинов. [19] При бактериальных инфекциях раннее истощение макрофагов во время гриппа создает в легких благоприятную среду для роста бактерий, поскольку эти лейкоциты играют важную роль в ответе на бактериальную инфекцию. Механизмы хозяина, стимулирующие восстановление тканей, могут непреднамеренно привести к бактериальной инфекции. Инфекция также индуцирует выработку системных глюкокортикоидов , которые могут уменьшить воспаление и сохранить целостность тканей, но способствуют увеличению роста бактерий. [17]
На патофизиологию гриппа существенное влияние оказывает то, с какими рецепторами связываются вирусы гриппа при проникновении в клетки. Вирусы гриппа млекопитающих преимущественно связываются с сиаловыми кислотами, связанными с остальной частью олигосахарида посредством связи α-2,6, наиболее часто встречающейся в различных респираторных клетках. [1] [19] [3] такие как респираторные и эпителиальные клетки сетчатки. [26] AIV предпочитают сиаловые кислоты с α-2,3-связью, которые наиболее распространены у птиц в эпителиальных клетках желудочно-кишечного тракта. [1] [19] [3] и у человека в нижних дыхательных путях. [36] Расщепление белка НА на НА 1 , связывающую субъединицу, и НА 2 , слитую субъединицу, осуществляется различными протеазами, влияющими на то, какие клетки могут быть инфицированы. Для вирусов гриппа млекопитающих и низкопатогенных AIV расщепление является внеклеточным, что ограничивает инфицирование клетками, имеющими соответствующие протеазы, тогда как для высокопатогенных AIV расщепление является внутриклеточным и осуществляется вездесущими протеазами, что позволяет заразить большее разнообразие клеток. тем самым способствуя более тяжелому заболеванию. [1] [31] [37]
Иммунология
Клетки обладают сенсорами для обнаружения вирусной РНК, которая затем может индуцировать выработку интерферона . Интерфероны опосредуют экспрессию противовирусных белков и белков, которые привлекают иммунные клетки к очагу инфекции, а также уведомляют близлежащие неинфицированные клетки об инфекции. Некоторые инфицированные клетки выделяют провоспалительные цитокины, которые привлекают иммунные клетки к месту инфекции. Иммунные клетки контролируют вирусную инфекцию, убивая инфицированные клетки и фагоцитируя вирусные частицы и апоптотические клетки. Обостренный иммунный ответ может нанести вред организму хозяина посредством цитокинового шторма. [1] [13] [26] Чтобы противостоять иммунному ответу, вирусы гриппа кодируют различные неструктурные белки, включая NS1, NEP, PB1-F2 и PA-X, которые участвуют в подавлении иммунного ответа хозяина путем подавления продукции интерферона и экспрессии генов хозяина. [1] [27]
В-клетки , тип лейкоцитов, вырабатывают антитела, которые связываются с антигенами гриппа HA и NA (или HEF). [24] ) и другие белки в меньшей степени. Связавшись с этими белками, антитела блокируют связывание вирионов с клеточными рецепторами, нейтрализуя вирус. У людей значительная реакция антител возникает примерно через неделю после заражения вирусом. [38] Этот ответ антител обычно устойчивый и продолжительный, особенно в отношении вируса гриппа C и вируса гриппа D. [1] [24] Люди, подвергшиеся воздействию определенного штамма в детстве, все еще обладают антителами к этому штамму на разумном уровне в более позднем возрасте, что может обеспечить некоторую защиту от родственных штаммов. [1] Однако существует « первородный антигенный грех », при котором первый подтип НА, которому подвергается человек, влияет на основанный на антителах иммунный ответ на будущие инфекции и вакцины. [2]
Профилактика
Вакцинация

Ежегодная вакцинация является основным и наиболее эффективным способом профилактики гриппа и связанных с ним осложнений, особенно для групп высокого риска. [10] [1] [39] Вакцины против гриппа являются трехвалентными или четырехвалентными и обеспечивают защиту от штамма H1N1, штамма H3N2 и одного или двух штаммов вируса гриппа B, соответствующих двум линиям вируса гриппа B. [10] [2] Используются два типа вакцин: инактивированные вакцины, содержащие «убитые» (т.е. инактивированные) вирусы, и живые аттенуированные вакцины против гриппа (ЖГВ), содержащие ослабленные вирусы. [1] Существует три типа инактивированных вакцин: цельновирусные, расщепленные вирусы, в которых вирус разрушается детергентом, и субъединичные, содержащие только вирусные антигены HA и NA. [40] Большинство вакцин против гриппа инактивированы и вводятся внутримышечно. LAIV впрыскиваются в полость носа. [1]
Рекомендации по вакцинации различаются в зависимости от страны. Некоторые рекомендуют вакцинацию всем людям старше определенного возраста, например, 6 месяцев, [39] тогда как другие страны ограничивают рекомендации группами высокого риска. [1] [11] Младенцы раннего возраста не могут получать вакцины против гриппа по соображениям безопасности, но они могут унаследовать пассивный иммунитет от своей матери, если их вакцинируют во время беременности. [41] Вакцинация против гриппа помогает снизить вероятность рекомбинации. [13]

В целом, вакцины против гриппа эффективны только в том случае, если существует антигенное соответствие между вакцинными штаммами и циркулирующими штаммами. [10] [2] Большинство коммерчески доступных вакцин против гриппа производятся путем размножения вирусов гриппа в куриных яйцах с эмбрионами, что занимает 6–8 месяцев. [2] Сезоны гриппа в северном и южном полушарии различаются, поэтому ВОЗ собирается дважды в год, по одному для каждого полушария, чтобы обсудить, какие штаммы следует включить на основании результатов исследований ингибирования ГК. [10] [3] Другие методы производства включают инактивированную вакцину на основе культуры клеток MDCK и рекомбинантную субъединичную вакцину, полученную из сверхэкспрессии бакуловируса в клетках насекомых. [2] [42]
Противовирусная химиопрофилактика
Грипп можно предотвратить или уменьшить его тяжесть с помощью постконтактной профилактики противовирусными препаратами осельтамивиром , который можно принимать перорально детям в возрасте не менее трех месяцев, и занамивиром , который можно вдыхать детям старше семи лет. Химиопрофилактика наиболее полезна для лиц с высоким риском осложнений и тех, кто не может получить вакцину против гриппа. [10] Постконтактная химиопрофилактика рекомендуется только в том случае, если осельтамивир принят в течение 48 часов после контакта с подтвержденным или подозреваемым случаем заболевания, а занамивир - в течение 36 часов. [10] [11] Рекомендуется для людей, которые еще не получили вакцину от текущего сезона гриппа, которые были вакцинированы менее двух недель с момента контакта, если существует значительное несоответствие между вакциной и циркулирующими штаммами или во время вспышки в закрытом помещении, независимо от этого. истории вакцинации. [11]
Инфекционный контроль
Гигиена рук важна для снижения распространения гриппа. Это включает в себя частое мытье рук с мылом и водой, использование на спиртовой основе дезинфицирующих средств для рук и отказ от прикосновения руками к глазам, носу и рту. Важно прикрывать нос и рот при кашле или чихании. [43] Другие методы ограничения передачи гриппа включают в себя пребывание дома во время болезни, [1] избегать контактов с другими людьми в течение одного дня после исчезновения симптомов, [11] и дезинфекция поверхностей, которые могут быть заражены вирусом. [1]
Исследования до сих пор не показали значительного снижения заболеваемости сезонным гриппом при использовании масок. Эффективность проверки в пунктах въезда в страны недостаточно изучена. [43] Меры социального дистанцирования , такие как закрытие школ, изоляция или карантин, а также ограничение массовых собраний, могут снизить передачу вируса. [1] [43] но эти меры часто являются дорогостоящими, непопулярными и трудными для реализации. Следовательно, обычно рекомендуемыми методами инфекционного контроля являются респираторный этикет, гигиена рук и ношение масок, которые недороги и просты. Фармацевтические меры эффективны, но могут быть недоступны на ранних стадиях вспышки. [44]
В медицинских учреждениях инфицированные люди могут быть объединены в группы или помещены в отдельные палаты. При контакте с инфицированными людьми рекомендуется использовать защитную одежду, такую как маски, перчатки и халаты, если существует риск контакта с инфицированными биологическими жидкостями. Может помочь содержание пациентов в палатах с отрицательным давлением и избегание деятельности, связанной с образованием аэрозолей. [10] однако специальные системы обработки воздуха и вентиляции не считаются необходимыми для предотвращения распространения гриппа в воздухе. [4] В домах престарелых, возможно, придется закрыть прием новых пациентов до тех пор, пока распространение гриппа не будет взято под контроль. [11]
Поскольку вирусы гриппа циркулируют среди животных, таких как птицы и свиньи, важно предотвратить передачу инфекции от этих животных. Очистка воды , содержание животных в закрытых помещениях, карантин больных животных, вакцинация и биобезопасность являются основными используемыми мерами. Размещение птичников и свинарников на возвышенности вдали от ферм с высокой плотностью населения, приусадебных ферм, рынков живой птицы и водоемов помогает свести к минимуму контакт с дикими птицами. [1] Закрытие рынков живой птицы кажется наиболее эффективной мерой [19] и доказал свою эффективность в борьбе с распространением H5N1, H7N9 и H9N2 . [20] Другие меры биобезопасности включают очистку и дезинфекцию помещений и транспортных средств, запрет на посещение птицефабрик, невозвращение обратно на фермы птиц, предназначенных для убоя, [45] переодевание, дезинфекция ванночек для ног, обработка еды и воды. [1]
Если рынки живой птицы не закрыты, то для сокращения распространения вирусов гриппа можно использовать «чистые дни», когда непроданную домашнюю птицу удаляют, а помещения дезинфицируют, а политику «непереноса» для уничтожения инфекционного материала до прибытия новой птицы можно использовать. Если новый вирус гриппа нарушил вышеупомянутые меры биобезопасности, то для предотвращения эндемизации вируса может потребоваться его быстрое обнаружение с целью его ликвидации посредством карантина, обеззараживания и выбраковки. [1] Существуют вакцины против подтипов птиц H5, H7 и H9, которые используются в некоторых странах. [19] В Китае, например, вакцинация домашних птиц против H7N9 успешно ограничила его распространение, что указывает на то, что вакцинация может быть эффективной стратегией. [31] если они используются в сочетании с другими мерами по ограничению передачи. [1] У свиней и лошадей борьба с гриппом зависит от вакцинации с биозащитой. [1]
Диагностика

Диагноз, основанный на симптомах, достаточно точен у здоровых людей во время сезонных эпидемий, и его следует подозревать в случаях пневмонии, острого респираторного дистресс-синдрома (ОРДС), сепсиса или при возникновении энцефалита, миокардита или разрушения мышечной ткани . [17] Поскольку грипп похож на другие вирусные заболевания дыхательных путей, для подтверждения необходима лабораторная диагностика. Распространенные методы сбора образцов для тестирования включают мазки из носа и горла. [1] Пробы можно брать из нижних дыхательных путей, если инфекция поразила верхние, но не нижние дыхательные пути. Тестирование на грипп рекомендуется всем, кто госпитализирован с симптомами, напоминающими грипп, во время сезона гриппа или кто связан со случаем гриппа. В тяжелых случаях более ранняя диагностика улучшает исход заболевания. [39] Диагностические методы, которые могут идентифицировать грипп, включают вирусные культуры , тесты на выявление антител и антигенов, а также тесты на основе нуклеиновых кислот. [46]
Вирусы можно выращивать в культуре клеток млекопитающих или яйцах с эмбрионами в течение 3–10 дней для мониторинга цитопатического эффекта. Окончательное подтверждение затем может быть сделано с помощью окрашивания антителами, гемадсорбции с использованием эритроцитов или иммунофлуоресцентной микроскопии. Культуры из флаконов с оболочкой, которые могут идентифицировать инфекцию с помощью иммуноокрашивания до появления цитопатического эффекта, более чувствительны, чем традиционные культуры, и дают результаты через 1–3 дня. [1] [39] [46] Культуры можно использовать для характеристики новых вирусов, наблюдения за чувствительностью к противовирусным препаратам и мониторинга антигенного дрейфа, но они относительно медленны и требуют специальных навыков и оборудования. [1]
Серологические анализы можно использовать для выявления гуморальной реакции на грипп после естественного инфицирования или вакцинации. Общие серологические анализы включают анализы ингибирования гемагглютинации, которые выявляют HA-специфические антитела, анализы нейтрализации вируса, которые проверяют, нейтрализовали ли антитела вирус, и иммуноферментные анализы. Эти методы, как правило, относительно недороги и быстры, но менее надежны, чем тесты на основе нуклеиновых кислот. [1] [46]
Прямые флуоресцентные или иммунофлуоресцентные тесты на антитела (DFA/IFA) включают окрашивание респираторных эпителиальных клеток в образцах флуоресцентно-меченными антителами, специфичными для гриппа, с последующим исследованием под флуоресцентным микроскопом. Они могут различать вирус гриппа А и вирус гриппа В, но не могут подтипировать вирус гриппа А. [46] Экспресс-тесты для диагностики гриппа (RIDT) представляют собой простой способ получения результатов анализа, они недороги и дают результаты менее чем за 30 минут, поэтому они широко используются, но они не позволяют отличить вирус гриппа А от вируса гриппа В или между ними. подтипы вируса гриппа А и не так чувствительны, как тесты на основе нуклеиновых кислот. [1] [46]
Тесты на основе нуклеиновых кислот (NAT) усиливают и обнаруживают вирусную нуклеиновую кислоту. Большинство этих тестов занимают несколько часов. [46] но быстрые молекулярные анализы столь же быстры, как и RIDT. [39] Среди NAT полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) является наиболее традиционной и считается золотым стандартом диагностики гриппа. [46] потому что он быстрый и может подтипировать вирус гриппа А, но он относительно дорог и более склонен к ложноположительным результатам, чем посев. [1] Другие использованные NAT включают анализы на основе изотермической амплификации, опосредованные петлей , простые анализы на основе амплификации и амплификацию на основе последовательностей нуклеиновых кислот. Методы секвенирования нуклеиновых кислот позволяют идентифицировать инфекцию путем получения последовательности нуклеиновых кислот из вирусных образцов для выявления устойчивости вируса и противовирусных препаратов. Традиционным методом является секвенирование по Сэнгеру , но он в значительной степени заменен методами следующего поколения , которые имеют большую скорость и производительность секвенирования. [46]
Управление
Лечение в случаях легкого или умеренного заболевания является поддерживающим и включает жаропонижающие препараты, такие как ацетаминофен и ибупрофен . [47] достаточное потребление жидкости во избежание обезвоживания и отдых. [11] Лекарства от кашля и спреи для горла могут быть полезны при боли в горле. Во время болезни рекомендуется избегать употребления алкоголя и табака. [47] Аспирин не рекомендуется применять для лечения гриппа у детей из-за повышенного риска развития синдрома Рея . [48] Кортикостероиды не рекомендуются, за исключением случаев лечения септического шока или основного заболевания, такого как хроническая обструктивная болезнь легких или обострение астмы, поскольку они связаны с повышенной смертностью. [39] Если возникает вторичная бактериальная инфекция, может потребоваться применение антибиотиков. [11]
Противовирусные препараты
| Лекарство | Путь введения | Утвержденный возраст использования |
|---|---|---|
| Осельтамивир | Оральный | Минимум две недели |
| Занамивир | Вдыхание | Минимум пять лет |
| Перамивир | Внутривенная инъекция | По крайней мере 18 лет |
| Ланинамивир | Вдыхание [1] | Доза 40 миллиграммов (мг) для людей старше 10 лет, 20 мг для детей младше 10 лет [49] |
| Балоксавир марбоксил | Оральный [4] | По крайней мере 12 лет [39] |
Противовирусные препараты в основном используются для лечения тяжелобольных пациентов, особенно с ослабленной иммунной системой. Противовирусные препараты наиболее эффективны, если их начать в первые 48 часов после появления симптомов. Более позднее введение может быть полезным для тех, у кого есть основные иммунные дефекты, для людей с более тяжелыми симптомами или для тех, у кого более высокий риск развития осложнений, если эти люди все еще выделяют вирус. Противовирусное лечение также рекомендуется, если человек госпитализирован с подозрением на грипп вместо того, чтобы ждать результатов анализов, и если симптомы ухудшаются. [1] [39] Большинство противовирусных препаратов против гриппа делятся на две категории: ингибиторы нейраминидазы (НА) и ингибиторы М2. [13] Балоксавир марбоксил является заметным исключением, он нацелен на эндонуклеазную активность вирусной РНК-полимеразы и может использоваться в качестве альтернативы ингибиторам NA и M2 для вируса гриппа А и вируса гриппа B. [10] [19] [4]
Ингибиторы NA воздействуют на ферментативную активность рецепторов NA, имитируя связывание сиаловой кислоты в активном центре NA на вирионах вируса гриппа A и вируса гриппа B. [1] так что высвобождение вируса из инфицированных клеток и скорость репликации вируса нарушаются. [11] Ингибиторы NA включают осельтамивир, который принимают перорально в форме пролекарства и преобразуются в активную форму в печени, и занамивир, который представляет собой порошок, который вдыхают назально. Осельтамивир и занамивир эффективны для профилактики и постконтактной профилактики, а исследования в целом показывают, что ингибиторы NA эффективны в снижении частоты осложнений, госпитализации и смертности. [1] и продолжительность болезни. [13] [39] [4] Кроме того, чем раньше будут назначены ингибиторы NA, тем лучше результат. [4] хотя позднее введение все же может быть полезным в тяжелых случаях. [1] [39] Другие ингибиторы NA включают ланинамивир. [1] и перамивир, последний из которых может использоваться в качестве альтернативы осельтамивиру для людей, которые не могут его переносить или усваивать. [39]
Адамантаны представляют собой амантадин и римантадин препараты для перорального применения, которые блокируют ионный канал М2 вируса гриппа. [1] предотвращение вирусного разоблачения. [4] Эти препараты эффективны только против вируса гриппа А. [39] но больше не рекомендуются к использованию из-за широко распространенной устойчивости к ним среди вирусов гриппа А. [4] Устойчивость к адамантану впервые возникла у H3N2 в 2003 году, а к 2008 году она стала всемирной. Устойчивость к осельтамивиру больше не широко распространена, поскольку пандемический штамм H1N1 2009 года (H1N1 pdm09), устойчивый к адамантану, по-видимому, заменил устойчивые штаммы в обращении. После пандемии 2009 года резистентность к осельтамивиру наблюдалась в основном у пациентов, проходящих терапию. [1] особенно дети с ослабленным иммунитетом и маленькие дети. [4] Устойчивость к осельтамивиру обычно отмечается при вирусе H1N1, но реже сообщается о вирусах H3N2 и гриппа B. [1] По этой причине осельтамивир рекомендуется в качестве препарата первого выбора для иммунокомпетентных людей, тогда как для людей с ослабленным иммунитетом осельтамивир рекомендуется против вируса H3N2 и гриппа B, а занамивир против H1N1 pdm09. Резистентность к занамивиру наблюдается реже, возможна устойчивость к перамивиру и балоксавиру марбоксилу. [4]
Прогноз
У здоровых людей инфекция гриппа обычно проходит самостоятельно и редко приводит к летальному исходу. [10] [11] Симптомы обычно длятся 2–8 дней. [13] Грипп может привести к тому, что люди пропустят работу или учебу, он связан со снижением производительности труда, а у пожилых людей – с уменьшением независимости. Усталость и недомогание могут сохраняться в течение нескольких недель после выздоровления, а у здоровых взрослых могут возникнуть легочные нарушения, на устранение которых может потребоваться несколько недель. Осложнения и смертность в первую очередь возникают в группах высокого риска и у госпитализированных. Тяжелое заболевание и смертность обычно связаны с пневмонией, вызванной первичной вирусной инфекцией или вторичной бактериальной инфекцией. [1] [11] который может перейти в ОРДС. [13]
Другие респираторные осложнения, которые могут возникнуть, включают синусит , бронхит , бронхиолит , избыточное накопление жидкости в легких и обострение хронического бронхита и астмы. Могут возникнуть инфекция среднего уха и круп , чаще всего у детей. [10] [1] Вторичная инфекция S. aureus наблюдалась, прежде всего у детей, и вызывала синдром токсического шока после гриппа с гипотонией, лихорадкой, покраснением и шелушением кожи. [1] Осложнения, поражающие сердечно-сосудистую систему, встречаются редко и включают перикардит, молниеносный миокардит с учащенным, замедленным или нерегулярным сердцебиением , а также обострение ранее существовавшего сердечно-сосудистого заболевания. [10] [11] Воспаление или отек мышц, сопровождающееся разрушением мышечной ткани, встречается редко, обычно у детей, что проявляется сильной болезненностью и болью в мышцах ног, а также нежеланием ходить в течение 2–3 дней. [1] [11] [17]
Грипп может влиять на беременность, в том числе вызывать меньшие размеры новорожденных, повышенный риск преждевременных родов и повышенный риск детской смертности незадолго до или после рождения. [11] В редких случаях с гриппом были связаны неврологические осложнения, включая асептический менингит, энцефалит, диссеминированный энцефаломиелит, поперечный миелит и синдром Гийена-Барре . [17] Кроме того, могут возникать фебрильные судороги и синдром Рея, чаще всего у детей. [1] [11] Грипп-ассоциированная энцефалопатия может возникать непосредственно в результате инфекции центральной нервной системы из-за присутствия вируса в крови и проявляться внезапным началом лихорадки с судорогами с последующим быстрым прогрессированием до комы. [10] Атипичная форма энцефалита, называемая летаргическим энцефалитом, характеризующаяся головной болью, сонливостью и комой, в редких случаях может возникнуть через некоторое время после заражения. [1] У людей, переживших грипп-ассоциированную энцефалопатию, могут возникнуть неврологические дефекты. [10] В первую очередь у детей, в тяжелых случаях иммунная система редко может значительно перепроизводить лейкоциты , которые выделяют цитокины, вызывая тяжелое воспаление. [10]
Люди, достигшие возраста 65 лет, [11] из-за ослабления иммунной системы в результате старения или хронического заболевания, являются группой высокого риска развития осложнений, как и дети в возрасте до одного года и дети, которые ранее не подвергались многократному воздействию вирусов гриппа. Беременные женщины подвергаются повышенному риску, который увеличивается с каждым триместром. [1] и длится до двух недель после родов. [11] [39] Ожирение, в частности индекс массы тела более 35–40, связано с большей репликацией вируса, увеличением тяжести вторичной бактериальной инфекции и снижением эффективности вакцинации. В группу риска также входят люди с сопутствующими заболеваниями, в том числе те, у кого есть врожденные или хронические проблемы с сердцем или заболеваниями легких (например, астма), почек, печени, крови, неврологические или метаболические (например, диабет ) расстройства. [10] [1] [11] как и люди с ослабленным иммунитетом в результате химиотерапии, асплении , длительного лечения стероидами, дисфункции селезенки или ВИЧ- инфекции. [11] Употребление табака, в том числе в прошлом, подвергает человека риску. [39] Роль генетики при гриппе недостаточно изучена. [1] но это может быть фактором смертности от гриппа. [13]
Эпидемиология

Грипп обычно характеризуется сезонными эпидемиями и спорадическими пандемиями. Большая часть бремени гриппа является результатом сезонов гриппа, вызванных вирусом гриппа А и вирусом гриппа В. Среди подтипов вируса гриппа А H1N1 и H3N2 циркулируют у людей и вызывают сезонный грипп. Случаи непропорционально возникают у детей, но наиболее тяжелые причины наблюдаются у пожилых, очень маленьких, [1] и люди с ослабленным иммунитетом. [4] В обычный год вирусами гриппа заражаются 5–15% населения планеты. [3] [46] вызывая 3–5 миллионов случаев тяжелых заболеваний ежегодно [1] [2] и ежегодно на их долю приходится 290 000–650 000 смертей из-за респираторных заболеваний. [3] [4] [51] Ежегодно гриппом заболевают 5–10% взрослых и 20–30% детей. [21] Зарегистрированное количество случаев гриппа обычно намного ниже фактического числа. [1] [41]
По оценкам, во время сезонных эпидемий около 80% здоровых людей, страдающих кашлем или болью в горле, болеют гриппом. [1] Примерно у 30–40% людей, госпитализированных по поводу гриппа, развивается пневмония, и около 5% всех тяжелых случаев пневмонии в больницах вызваны гриппом, который также является наиболее распространенной причиной ОРДС у взрослых. У детей грипп и респираторно-синцитиальный вирус являются двумя наиболее распространенными причинами ОРДС. [17] Около 3–5% детей ежегодно заболевают средним отитом, вызванным гриппом. [10] Взрослые, у которых развивается органная недостаточность в результате гриппа, и дети с оценкой PIM и острой почечной недостаточностью имеют более высокий уровень смертности. [17] При сезонном гриппе смертность концентрируется среди очень молодых и пожилых людей, тогда как во время пандемий гриппа чаще всего заболевают молодые люди. [13]

В регионах с умеренным климатом число случаев гриппа варьируется от сезона к сезону. Снижение уровня витамина D , предположительно из-за меньшего количества солнечного света. [35] более низкая влажность, более низкая температура и незначительные изменения в белках вируса, вызванные антигенным дрейфом, способствуют ежегодным эпидемиям, пик которых приходится на зимний сезон. В северном полушарии это период с октября по май (точнее, с декабря по апрель). [13] ), а в южном полушарии это с мая по октябрь (точнее с июня по сентябрь). [13] ). Таким образом, в регионах с умеренным климатом каждый год наблюдается два различных сезона гриппа: один в северном полушарии и один в южном полушарии. [1] [11] [2] В тропических и субтропических регионах сезонность более сложна и, по-видимому, зависит от различных климатических факторов, таких как минимальная температура, количество солнечных часов, максимальное количество осадков и высокая влажность. [1] [52] Таким образом, грипп в этих регионах может возникать круглый год. [13] Эпидемии гриппа в наше время имеют тенденцию начинаться в восточном или южном полушарии. [52] при этом Азия является ключевым резервуаром. [13]
Вирус гриппа А и вирус гриппа В циркулируют совместно, поэтому имеют одинаковые пути передачи. [1] Однако сезонность вируса гриппа С плохо изучена. Инфекция вируса гриппа С чаще всего встречается у детей в возрасте до двух лет, а к взрослому возрасту большинство людей подвергаются воздействию вируса. Госпитализация, связанная с вирусом гриппа С, чаще всего происходит у детей в возрасте до трех лет и часто сопровождается коинфекцией другим вирусом или бактерией, что может усугубить тяжесть заболевания. При рассмотрении всех случаев госпитализации детей раннего возраста по поводу респираторных заболеваний вирус гриппа С, по-видимому, составляет лишь небольшой процент таких случаев. Могут возникать крупные вспышки инфекции вируса гриппа С, поэтому заболеваемость значительно варьируется. [12]
Вспышки гриппа, вызванные новыми вирусами гриппа, являются обычным явлением. [25] В зависимости от уровня ранее существовавшего иммунитета у населения новые вирусы гриппа могут быстро распространяться и вызывать пандемии с миллионами смертей. Эти пандемии, в отличие от сезонного гриппа, вызваны антигенными сдвигами с участием вирусов гриппа животных. На сегодняшний день все известные пандемии гриппа были вызваны вирусами гриппа А и следовали одной и той же схеме распространения от точки происхождения до остального мира в течение нескольких волн в течение года. [1] [11] [39] Пандемические штаммы, как правило, связаны с более высоким уровнем заболеваемости пневмонией у здоровых людей. [17] Обычно после каждой пандемии гриппа пандемический штамм продолжает циркулировать как причина сезонного гриппа, заменяя предыдущие штаммы. [1] С 1700 по 1889 год пандемии гриппа случались примерно раз в 50–60 лет. С тех пор пандемии возникали примерно раз в 10–50 лет, поэтому со временем они могут стать более частыми. [52]
История
Первая эпидемия гриппа могла произойти около 6000 г. до н. э. в Китае. [54] а возможные описания гриппа существуют в греческих писаниях V века до нашей эры. [52] [55] И в 1173–1174 гг., и в 1387 г. по всей Европе произошли эпидемии, получившие название «грипп». Неясно, были ли эти эпидемии или другие эпидемии вызваны гриппом, поскольку в то время не существовало единой схемы наименования эпидемических респираторных заболеваний, а «грипп» стал четко ассоциироваться с респираторными заболеваниями лишь столетия спустя. [56] Грипп, возможно, был завезен в Америку еще в 1493 году, когда эпидемическое заболевание, напоминающее грипп, убило большую часть населения Антильских островов . [57] [58]
Первое убедительное свидетельство о пандемии гриппа было сделано в 1510 году . Это началось в Восточной Азии, а затем распространилось на Северную Африку, а затем на Европу. [59] После пандемии возник сезонный грипп с последующими пандемиями в 1557 и 1580 годах. [56] Пандемия гриппа 1557 года потенциально была первым случаем, когда грипп был связан с выкидышами и смертью беременных женщин. [60] Пандемия гриппа 1580 года возникла летом в Азии, распространилась на Африку, затем на Европу и, наконец, на Америку. [52] К концу XVI века грипп стал восприниматься как специфическое, узнаваемое заболевание с эпидемическими и эндемическими формами. [56] В 1648 году было обнаружено, что лошади тоже болеют гриппом. [59]
Данные о гриппе после 1700 года более точны, поэтому после этого момента легче идентифицировать пандемии гриппа. [61] Первая пандемия гриппа XVIII века началась весной 1729 года в России и в течение трех лет распространялась по всему миру отчетливыми волнами, причем более поздние были более смертоносными. Другая пандемия гриппа произошла в 1781–1782 годах и началась осенью в Китае. [52] В результате этой пандемии грипп стал ассоциироваться с внезапными вспышками лихорадочных заболеваний. [61] Следующая пандемия гриппа произошла с 1830 по 1833 год и началась зимой в Китае. Эта пандемия имела высокий уровень заболеваемости, но уровень смертности был низким. [30] [52]
Незначительная пандемия гриппа произошла с 1847 по 1851 год одновременно с третьей пандемией холеры и была первой пандемией гриппа, произошедшей с регистрацией естественной статистики, поэтому смертность от гриппа была четко зафиксирована впервые. [61] Высокопатогенный птичий грипп был признан в 1878 г. [61] и вскоре был связан с передачей вируса людям. [59] Ко времени пандемии 1889 года , которая, возможно, была вызвана штаммом H2N2, [62] грипп стал легко узнаваемой болезнью. [59]
Микробный агент, ответственный за грипп, был ошибочно идентифицирован в 1892 году Р.Ф. Дж. Пфайффером как вид бактерий Haemophilus influenzae , в названии которого сохранилось слово «грипп». [59] [61] С 1901 по 1903 год итальянские и австрийские исследователи смогли доказать, что птичий грипп, названный тогда «птичьей чумой», [31] Был вызван микроскопическим агентом, меньшим, чем бактерии, в результате использования фильтров со слишком маленькими порами, чтобы бактерии могли пройти через них. Однако фундаментальные различия между вирусами и бактериями еще не были полностью поняты. [61]

С 1918 по 1920 год пандемия испанского гриппа стала самой разрушительной пандемией гриппа и одной из самых смертоносных пандемий в истории. Пандемия, вероятно, вызванная H1N1, вероятно, началась в Соединенных Штатах, а затем распространилась по всему миру через солдат во время и после Первой мировой войны . Первоначальная волна в первой половине 1918 года была относительно незначительной и напоминала прошлые пандемии гриппа, но вторая волна, случившаяся позднее в том же году, имела гораздо более высокий уровень смертности. [52] Третья волна с более низкой смертностью произошла во многих местах через несколько месяцев после второй. [30] По оценкам, к концу 1920 года около трети [13] до половины всех людей в мире были инфицированы, причем десятки миллионов человек умерли, причем непропорционально молодые люди. [52] Во время пандемии 1918 года был четко определен респираторный путь передачи инфекции. [30] и было показано, что грипп вызывается «проходцем через фильтр», а не бактерией, но еще десять лет не было единого мнения о причине гриппа, и исследования гриппа пошли на спад. [61] После пандемии H1N1 циркулировал среди людей в сезонной форме. [1] до следующей пандемии. [61]
В 1931 году Ричард Шоп опубликовал три статьи, в которых вирус был назван причиной свиного гриппа, недавно обнаруженной болезни среди свиней, которая характеризовалась во время второй волны пандемии 1918 года. [60] [61] Исследования Шопа активизировали исследования человеческого гриппа, и с тех пор в результате исследований гриппа возникли многие достижения в области вирусологии, серологии, иммунологии, экспериментальных моделей на животных, вакцинологии и иммунотерапии. [61] Всего через два года после открытия вирусов гриппа, в 1933 году, вирус гриппа А был идентифицирован как возбудитель человеческого гриппа. [60] [64] Подтипы вируса гриппа А были открыты в 1930-х годах. [61] а вирус гриппа B был открыт в 1940 году. [21]
Во время Второй мировой войны правительство США работало над разработкой инактивированных вакцин против гриппа, в результате чего в 1945 году в США была лицензирована первая вакцина против гриппа. [1] Вирус гриппа С был обнаружен два года спустя, в 1947 году. [21] В 1955 году было подтверждено, что птичий грипп вызывается вирусом гриппа А. [31] После Второй мировой войны произошло четыре пандемии гриппа. Первым из них был азиатский грипп с 1957 по 1958 год, вызванный штаммом H2N2. [1] [44] и начинается в китайской Юньнань провинции . Число смертей, вероятно, превысило один миллион, в основном среди очень молодых и очень старых людей. [52] Это была первая пандемия гриппа, произошедшая при наличии глобальной системы эпиднадзора и лабораторий, способных изучать новый вирус гриппа. [30] После пандемии H2N2 стал подтипом вируса гриппа А, ответственным за сезонный грипп. [1] Первый противовирусный препарат против гриппа, амантадин , был одобрен в 1966 году, а с 1990-х годов стали использоваться дополнительные противовирусные препараты. [4]
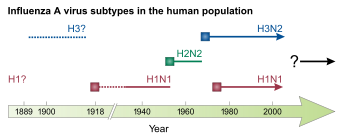
В 1968 году H3N2 был завезен людям в результате реаранжировки птичьего штамма H3N2 и штамма H2N2, циркулировавшего у людей. Новый штамм H3N2 появился в Гонконге и распространился по всему миру, вызвав пандемию гонконгского гриппа , которая привела к гибели 500 000–2 000 000 человек. Это была первая пандемия, которая значительно распространилась воздушным транспортом. [3] [30] H2N2 и H3N2 циркулировали совместно после пандемии до 1971 года, когда распространенность H2N2 снизилась и был полностью заменен H3N2. [3] В 1977 году H1N1 вновь появился у людей, возможно, после того, как он был выпущен из морозильной камеры в результате несчастного случая в лаборатории, и вызвал псевдопандемию . [30] [61] Этот штамм H1N1 был антигенно похож на штаммы H1N1, циркулировавшие до 1957 года. С 1977 года как H1N1, так и H3N2 циркулируют среди людей как часть сезонного гриппа. [1] В 1980 году была введена система классификации, используемая для подтипирования вирусов гриппа. [65]

В какой-то момент вирус гриппа B разделился на два штамма, названные B/Victoria-like и B/Yamagata-like, оба из которых циркулируют среди людей с 1983 года. [21] В 1996 году HPAI H5N1 был обнаружен в провинции Гуандун , Китай. [31] а год спустя появился в птицеводстве в Гонконге, постепенно распространившись оттуда по всему миру. Тогда произошла небольшая вспышка вируса H5N1 среди людей в Гонконге. [37] и спорадические случаи заболевания людей произошли с 1997 года с высоким уровнем смертности. [19] [46] Самой последней пандемией гриппа была пандемия свиного гриппа 2009 года , которая возникла в Мексике и привела к сотням тысяч смертей. [30] Заболевание было вызвано новым штаммом H1N1, который представлял собой реассортацию вирусов человеческого, свиного и птичьего гриппа. [20] [4] Пандемия 2009 года привела к замене ранее находившихся в обращении штаммов H1N1 новым штаммом, но не другими вирусами гриппа. Следовательно, вирусы H1N1, H3N2 и обе линии вируса гриппа B циркулируют в сезонной форме после пандемии 2009 года. [1] [30] [31]
В 2011 году вирус гриппа D был обнаружен у свиней в Оклахоме, США, а крупный рогатый скот позже был идентифицирован как основной резервуар вируса гриппа D. [12] [21] В том же году, [46] птичий H7N9 был обнаружен в Китае и начал вызывать инфекции среди людей в 2013 году, начиная с Шанхая и Аньхоя и оставаясь в основном в Китае. HPAI H7N9 появился где-то в 2016 году и иногда случайно заражал людей. С 1990-х годов люди реже заражались другими вирусами гриппа, включая H5N6 , H6N1 , H7N2-4, H7N7 и H10N7-8. [19] а подтипы HPAI H, такие как H5N1-3, H5N5-6 и H5N8 , начали распространяться по большей части мира с 2010-х годов. Будущие пандемии гриппа, которые могут быть вызваны вирусом гриппа птичьего происхождения, [31] рассматриваются как почти неизбежные, а растущая глобализация облегчила распространение новых вирусов. [30] поэтому предпринимаются постоянные усилия по подготовке к будущим пандемиям. [60] и улучшить профилактику и лечение гриппа. [1]
Этимология
Слово грипп происходит от итальянского слова influenza , от средневекового латинского influentia , первоначально означавшего «посещение» или «влияние». Такие термины, как influenza di freddo , что означает «влияние холода», и influenza di stelle , что означает «влияние звезд», засвидетельствованы с 14 века. Последнее указывало на причину болезни, которую в то время некоторые приписывали неблагоприятным астрологическим условиям. Еще в 1504 году грипп стал означать «посещение» или «вспышку» какого-либо заболевания, поражающего одновременно множество людей в одном месте. Во время вспышки гриппа в 1743 году, которая началась в Италии и распространилась по всей Европе, это слово достигло английского языка и было переведено на английский язык в произношении. С середины 1800-х годов слово «грипп» также использовалось для обозначения тяжелых простудных заболеваний. [66] [67] [68] Сокращенная форма слова «грипп» впервые засвидетельствована в 1839 году как грипп, а правописание гриппа подтверждено в 1893 году. [69] Другие названия, которые использовались для гриппа, включают эпидемический катар , la Grippe с французского , потливость и, особенно когда речь идет о пандемическом штамме 1918 года, испанскую лихорадку . [70]
Исследовать

Исследования гриппа включают попытки понять, как вирусы гриппа проникают в организм человека, взаимосвязь между вирусами гриппа и бактериями, как развиваются симптомы гриппа и почему некоторые вирусы гриппа более смертоносны, чем другие. [72] Периодически обнаруживаются неструктурные белки, кодируемые вирусами гриппа, и их функции постоянно исследуются. [27] Прошлые пандемии, и особенно пандемия 1918 года, являются предметом многочисленных исследований, направленных на понимание пандемий гриппа. [52] В рамках обеспечения готовности к пандемии Глобальная система эпиднадзора за гриппом и реагирования представляет собой глобальную сеть лабораторий, которая отслеживает передачу гриппа и эпидемиологию. [73] Дополнительные области исследований включают способы улучшения диагностики, лечения и профилактики гриппа.
Существующие методы диагностики имеют ряд ограничений наряду со своими преимуществами. Например, NAT обладают высокой чувствительностью и специфичностью, но непрактичны в регионах с ограниченными ресурсами из-за их высокой стоимости, сложности, необходимости обслуживания и обучения. Недорогие портативные RIDT позволяют быстро диагностировать грипп, но имеют сильно варьирующую чувствительность и не способны определить подтип вируса гриппа А. В результате этих и других ограничений исследования новых методов диагностики вращаются вокруг разработки новых методов, которые являются экономически эффективными, менее трудоемкими и менее сложными, чем существующие методы, а также позволяют дифференцировать виды гриппа и подтипы вируса гриппа А. Одним из подходов в разработке являются «лаборатории на чипах» , которые представляют собой диагностические устройства, в которых используются различные диагностические тесты, такие как RT-PCR и серологические анализы, в форме микрочипов. Эти чипы имеют множество потенциальных преимуществ, включая высокую эффективность реакции, низкое энергопотребление и низкое образование отходов. [46]
Новые противовирусные препараты также находятся в разработке из-за исключения адамантинов из числа жизнеспособных лекарств и опасений по поводу устойчивости к осельтамивиру. К ним относятся: ингибиторы NA, которые можно вводить внутривенно, например, занамивир для внутривенного введения; фавипиравир , который представляет собой ингибитор полимеразы, используемый против нескольких РНК-вирусов; пимодивир , который предотвращает кэп-связывание, необходимое во время вирусной транскрипции; и нитазоксанид , который ингибирует созревание ГК. [1] [13] Уменьшение избыточного воспаления в дыхательных путях также является предметом многочисленных исследований, поскольку это один из основных механизмов гриппозной патологии. [13] [17] Другие формы терапии, находящиеся в стадии разработки, включают моноклональные и поликлональные антитела, нацеленные на вирусные белки, плазму выздоравливающих, различные подходы к изменению противовирусного ответа хозяина, [39] [74] и терапия на основе стволовых клеток для восстановления повреждений легких. [13]
Многие исследования LAIV сосредоточены на выявлении последовательностей генома, которые можно удалить для создания безвредных вирусов гриппа в вакцинах, которые по-прежнему обеспечивают иммунитет. [27] Однако высокая изменчивость и быстрая эволюция антигенов вируса гриппа являются серьезным препятствием для разработки эффективных вакцин. Кроме того, трудно предсказать, какие штаммы будут циркулировать в следующем сезоне гриппа, а производство достаточного количества вакцин против гриппа для следующего сезона затруднено. [2] LAIV имеют ограниченную эффективность, а повторная ежегодная вакцинация потенциально снижает эффективность. [1] По этим причинам исследуются «широкореактивные» или «универсальные» вакцины против гриппа, которые могут обеспечить защиту от многих или всех вирусов гриппа. Подходы к разработке такой вакцины включают методы на основе стеблей НА, такие как химеры, которые имеют один и тот же стебель, но разные головки, методы на основе головок НА, такие как компьютерно оптимизированные широко нейтрализующие антигены, антиидиотипические антитела и вакцины, вызывающие иммунные реакции на высокоэффективные вакцины. консервативные вирусные белки. [2] [74] Вакцины мРНК , обеспечивающие защиту от гриппа, также находятся в стадии исследования. [75]
В последние годы возникли разногласия по поводу этического обоснования некоторых исследований гриппа по «приобретению функции» (GOF). [76]
У животных
Птицы
Водные птицы, такие как утки, гуси, кулики и чайки, являются основным резервуаром вирусов гриппа А (IAV). [19] [20]
Из-за воздействия птичьего гриппа на экономически важные птицефермы в 1981 году была разработана система классификации, которая разделяла штаммы птичьего вируса на высокопатогенные (и, следовательно, потенциально требующие решительных мер контроля) и низкопатогенные. Тест на это основан исключительно на воздействии на цыплят - штамм вируса является высокопатогенным птичьим гриппом (ВПГП), если 75% или более цыплят умирают после преднамеренного заражения им. Альтернативной классификацией является низкопатогенный птичий грипп (LPAI), который вызывает легкие симптомы или не вызывает их вообще. [77] С тех пор эта система классификации была модифицирована с учетом структуры белка гемагглютинина вируса. [78] На генетическом уровне AIV можно идентифицировать как вирус HPAI, если он имеет многоосновный сайт расщепления в белке НА, который содержит дополнительные остатки в гене НА. [20] [31] Другие виды птиц, особенно водоплавающие, могут заразиться вирусом ВПГП, не проявляя серьезных симптомов, и могут распространять инфекцию на большие расстояния; Точные симптомы зависят от вида птицы и штамма вируса. [77] Классификация штамма птичьего вируса как HPAI или LPAI не позволяет предсказать, насколько серьезным может быть заболевание, если оно заразит людей или других млекопитающих. [77] [79]
Симптомы инфекции HPAI у кур включают отсутствие энергии и аппетита, снижение яйценоскости, яйца с мягкой или деформированной скорлупой, отек головы, гребня, сережек и скакательных суставов, пурпурную окраску сережек, гребней и ножек, выделения из носа, кашель. чихание, нарушение координации и диарея; птицы, инфицированные вирусом HPAI, также могут внезапно умереть без каких-либо признаков инфекции. [45] Большинство AIV являются LPAI. [ нужна ссылка ] Известные вирусы HPAI включают HPAI A (H5N1) и HPAI A (H7N9). Вирусы HPAI стали основным бременем болезней в 21 веке, что привело к гибели большого количества птиц. В случае H7N9 некоторые циркулирующие штаммы изначально были LPAI, но стали HPAI в результате приобретения многоосновного сайта расщепления HA. Птичий H9N2 также вызывает беспокойство, поскольку, хотя это и LPAI, он является частым донором генов H5N1 и H7N9 во время рекомбинации. [1]
Перелетные птицы могут распространять грипп на большие расстояния. Примером этого может служить случай, когда штамм H5N1 в 2005 году заразил птиц на озере Цинхай в Китае, которое является местом остановки и размножения многих перелетных птиц, что впоследствии распространило вирус более чем на 20 стран Азии, Европы и Ближнего Востока. [19] [31] ВПЧ могут передаваться от диких птиц домашним уткам на свободном выгуле и, в свою очередь, домашней птице через загрязненную воду, аэрозоли и фомиты. [1] Таким образом, утки выступают в качестве ключевых промежуточных звеньев между дикими и домашними птицами. [31] Передача вируса домашней птице обычно происходит на приусадебных фермах и на рынках живых животных, где несколько видов взаимодействуют друг с другом. Оттуда вирус AIV может распространиться на птицефабрики при отсутствии адекватной биобезопасности. Среди домашней птицы передача ВПГП происходит через аэрозоли и зараженные фекалии. [1] клетки, корма и мертвые животные. [19] Произошла обратная передача вирусов HPAI от домашних птиц диким птицам, что привело к массовой гибели и межконтинентальному распространению. [20]
Иногда вирусы AIV заражали людей через аэрозоли, фомиты и загрязненную воду. [1] Направленная передача от диких птиц встречается редко. [31] Вместо этого большая часть передачи происходит через домашнюю птицу, в основном кур, уток и гусей, а также множество других птиц, таких как цесарки, куропатки, фазаны и перепела. [20] Основным фактором риска заражения AIV является контакт с птицами на фермах и рынках живой птицы. [19] Обычно инкубационный период заражения ВГП составляет 3–5 дней, но может достигать 9 дней. H5N1 и H7N9 вызывают тяжелое заболевание нижних дыхательных путей, тогда как другие ВГВ, такие как H9N2, вызывают более легкое заболевание верхних дыхательных путей, обычно с конъюнктивитом. [1] Имела место ограниченная передача птичьих подтипов H2, H5-7, H9 и H10 от одного человека к другому воздушно-капельным путем, аэрозолями и фомитами. [1] [2] но устойчивой передачи AIV от человека к человеку не произошло. До 2013 года H5N1 был наиболее распространенным вирусом гриппа, заражающим людей. С тех пор H7N9 является причиной большинства случаев заболевания людей. [19]
Свиньи

Грипп свиней — это респираторное заболевание, похожее на грипп у людей, которое встречается во всем мире. Часто встречаются бессимптомные инфекции. Симптомы обычно появляются через 1–3 дня после заражения и включают лихорадку, вялость, анорексию, потерю веса, затрудненное дыхание, кашель, чихание и выделения из носа. У свиноматок беременность может прерваться. Осложнения включают вторичные инфекции и потенциально смертельную бронхопневмонию . Свиньи становятся заразными в течение дня после заражения и обычно распространяют вирус в течение 7–10 дней, что может быстро распространяться внутри стада. Свиньи обычно выздоравливают в течение 3–7 дней после появления симптомов. Меры профилактики и контроля включают инактивированные вакцины и выбраковку инфицированных стад. Вирус гриппа А подтипов H1N1, H1N2 и H3N2 обычно вызывает свиной грипп. [80]
Некоторые вирусы гриппа А могут передаваться аэрозольным путем от свиней к человеку и наоборот. [1] Свиньи вместе с летучими мышами и перепелами, [21] признаны сосудом для смешивания вирусов гриппа, поскольку в их дыхательных путях имеются рецепторы сиаловых кислот α-2,3 и α-2,6. По этой причине свиней могут инфицировать вирусы гриппа как птиц, так и млекопитающих. При коинфекции возможна рекомбинация. [20] Ярким примером этого стала рекомбинация вирусов свиного, птичьего и человеческого гриппа, вызвавшая пандемию гриппа 2009 года. [20] [4] Передача инфекции от человека к свиньям встречается чаще, чем от свиней к человеку. [20]
Другие животные
Вирусы гриппа были обнаружены у многих других животных, включая крупный рогатый скот, лошадей, собак, кошек и морских млекопитающих. Почти все вирусы гриппа А, очевидно, произошли от предковых вирусов птиц. Исключением являются гриппоподобные вирусы летучих мышей, происхождение которых неясно. Эти вирусы летучих мышей имеют подтипы HA и NA H17, H18, N10 и N11. H17N10 и H18N11 не способны реассортироваться с другими вирусами гриппа А, но они все еще способны реплицироваться у других млекопитающих. [1] AIV иногда переходят в млекопитающих. Например, в конце 2016 — начале 2017 года было обнаружено, что птичий штамм H7N2 заражает кошек в Нью-Йорке. [1]
Вирусы лошадиного гриппа А включают H7N7 и две линии. [1] H3N8 . Однако H7N7 не выявлялся у лошадей с конца 1970-х годов. [25] так что, возможно, он вымер у лошадей. [20] H3N8 у лошадей распространяется аэрозольным путем и вызывает респираторные заболевания. [1] Лошадиный H3N8 преимущественно связывается с α-2,3-сиаловыми кислотами, поэтому лошадей обычно считают тупиковыми хозяевами, но произошла передача вируса собакам и верблюдам, что вызывает опасения, что лошади могут смешивать сосуды для рекомбинации. У собак единственными циркулирующими вирусами гриппа А являются лошадиный H3N8 и птичий H3N2. Реассоциации собачьего H3N8 с другими подтипами не наблюдалось. H3N2 имеет гораздо более широкий круг хозяев и может реассоциироваться с H1N1 и H5N1. Изолированный случай заражения H6N1, вероятно, от курицы, был обнаружен при заражении собаки, поэтому у собак могут возникнуть другие вирусы AIV. [20]
Другие млекопитающие, инфицированные вирусами гриппа А, включают H7N7 и H4N5 у тюленей, H1N3 у китов и H10N4 и H3N2 у норок. [25] Были идентифицированы различные мутации, связанные с адаптацией AIV к млекопитающим. Поскольку белки HA различаются в зависимости от того, с какими сиаловыми кислотами они связываются, мутации в сайте связывания рецептора HA могут позволить AIV инфицировать млекопитающих. Другие мутации включают мутации, влияющие на то, какие белки NA сиаловых кислот расщепляются, и мутацию в субъединице полимеразы PB2, которая улучшает переносимость более низких температур в дыхательных путях млекопитающих и усиливает сборку RNP за счет стабилизации связывания NP и PB2. [20]
Вирус гриппа В в основном встречается у людей, но также обнаруживается у свиней, собак, лошадей и тюленей. [21] Аналогичным образом, вирус гриппа С в первую очередь заражает людей, но наблюдался у свиней, собак, крупного рогатого скота и дромадеров. [12] [21] Вирус гриппа D вызывает гриппоподобное заболевание у свиней, но его воздействие на его естественный резервуар – крупный рогатый скот – относительно неизвестно. Он может сам по себе вызывать респираторное заболевание, напоминающее человеческий грипп, или может быть частью комплекса респираторных заболеваний крупного рогатого скота (BRD) с другими патогенами во время коинфекции. BRD вызывает беспокойство в отрасли крупного рогатого скота, поэтому возможное участие вируса гриппа D в BRD привело к исследованию вакцин для крупного рогатого скота, которые могут обеспечить защиту от вируса гриппа D. [21] [24] В обращении находятся две антигенные линии: D/swine/Oklahoma/1334/2011 (D/OK) и D/bovine/Oklahoma/660/2013 (D/660). [21]
Ссылки
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и аль являюсь а к ап ак с как в В из хорошо топор является тот нет бб до нашей эры др. быть парень бг чб с минет БК с бм млрд быть б.п. БК бр бс БТ этот бв б бх к бз что CB копия компакт-диск Этот см. cg ч Там СиДжей ск кл см CN со КП cq Краммер Ф., Смит Г.Дж., Фушье Р.А., Пейрис М., Кедзерска К., Доэрти ПК. и др. (июнь 2018 г.). «Грипп» . Обзоры природы. Праймеры по болезням . 4 (1): 3. doi : 10.1038/s41572-018-0002-y . ПМК 7097467 . ПМИД 29955068 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот Саутто Г.А., Кирхенбаум Г.А., Росс Т.М. (январь 2018 г.). «На пути к универсальной вакцине против гриппа: разные подходы к одной цели» . Вирусологический журнал . 15 (1): 17. дои : 10.1186/s12985-017-0918-y . ПМЦ 5785881 . ПМИД 29370862 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п Аллен Джей Ди, Росс ТМ (2018). «Вирусы гриппа H3N2 у человека: вирусные механизмы, эволюция и оценка» . Человеческие вакцины и иммунотерапия . 14 (8): 1840–1847. дои : 10.1080/21645515.2018.1462639 . ПМК 6149781 . ПМИД 29641358 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д Лампехо Т. (июль 2020 г.). «Грипп и противовирусная резистентность: обзор» . Европейский журнал клинической микробиологии и инфекционных заболеваний . 39 (7): 1201–1208. дои : 10.1007/s10096-020-03840-9 . ПМЦ 7223162 . ПМИД 32056049 .
- ^ «Симптомы и диагностика гриппа» . Центры США по контролю и профилактике заболеваний (CDC) . 10 июля 2019 года. Архивировано из оригинала 27 декабря 2019 года . Проверено 24 января 2020 г.
- ^ «Симптомы и осложнения гриппа» . Центры США по контролю и профилактике заболеваний (CDC). 26 февраля 2019 года. Архивировано из оригинала 1 августа 2020 года . Проверено 6 июля 2019 г.
- ^ Позвоните С.А., Волленвейдеру М.А., Хорнунгу К.А., Симелу Д.Л., МакКинни В.П. (февраль 2005 г.). «Болеет ли этот пациент гриппом?». ДЖАМА . 293 (8): 987–997. дои : 10.1001/jama.293.8.987 . ПМИД 15728170 .
- ^ Аллан ГМ, Эрролл Б (февраль 2014 г.). «Профилактика и лечение простуды: осмысление доказательств» . CMAJ . 186 (3): 190–9. дои : 10.1503/cmaj.121442 . ПМЦ 3928210 . ПМИД 24468694 .
- ^ «Простуда против гриппа» . 11 августа 2016 года. Архивировано из оригинала 6 января 2017 года . Проверено 5 января 2017 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В Дхармапалан Д. (октябрь 2020 г.). «Грипп» . Индийский журнал педиатрии . 87 (10): 828–832. дои : 10.1007/s12098-020-03214-1 . ПМК 7091034 . ПМИД 32048225 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление Гебрехевет С., Макферсон П., Хо А. (декабрь 2016 г.). «Грипп» . БМЖ . 355 : i6258. дои : 10.1136/bmj.i6258 . ПМК 5141587 . ПМИД 27927672 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж Седердал Б.К., СП Уильямс (январь 2020 г.). «Эпидемиология и клиническая характеристика вируса гриппа С» . Вирусы . 12 (1): 89. дои : 10.3390/v12010089 . ПМК 7019359 . ПМИД 31941041 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т Петерандерл С., Герольд С., Шмольдт С. (август 2016 г.). «Инфекция вирусом гриппа человека» . Семинары по респираторной медицине и медицине интенсивной терапии . 37 (4): 487–500. дои : 10.1055/s-0036-1584801 . ПМК 7174870 . ПМИД 27486731 .
- ^ Триггл Н (28 сентября 2021 г.). «Как показывают исследования, люди также страдают «затяжным гриппом» . Новости BBC онлайн . Архивировано из оригинала 25 марта 2022 года . Проверено 10 июня 2024 г.
- ^ Зауэрвейн К. (14 декабря 2023 г.). « Длительный грипп» возник как последствие, аналогичное длительному COVID» . Медицинский факультет Вашингтонского университета в Сент-Луисе (пресс-релиз). Архивировано из оригинала 10 июня 2024 года . Проверено 10 июня 2024 г.
- ^ Се Ю, Чой Т, Аль-Али З (март 2024 г.). «Долгосрочные результаты после госпитализации по поводу COVID-19 по сравнению с сезонным гриппом: когортное исследование». «Ланцет». Инфекционные болезни . 24 (3): 239–255. дои : 10.1016/S1473-3099(23)00684-9 . ПМИД 38104583 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л Калил А.С., Томас П.Г. (июль 2019 г.). «Критические заболевания, связанные с вирусом гриппа: патофизиология и эпидемиология» . Критическая помощь . 23 (1): 258. дои : 10.1186/s13054-019-2539-x . ПМК 6642581 . ПМИД 31324202 .
- ^ «Таксономия вирусов: выпуск 2019 г.» . Международный комитет по таксономии вирусов. Архивировано из оригинала 20 марта 2020 года . Проверено 9 марта 2021 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п Ли Ю.Т., Линстер М., Менденхолл И.Х., Су Ю.К., Смит Г.Дж. (декабрь 2019 г.). «Вирусы птичьего гриппа у людей: уроки прошлых вспышек» . Британский медицинский бюллетень . 132 (1): 81–95. дои : 10.1093/bmb/ldz036 . ПМК 6992886 . PMID 31848585 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н Джозеф У, Су Ю.К., Виджайкришна Д., Смит Г.Дж. (январь 2017 г.). «Экология и адаптивная эволюция межвидовой передачи гриппа А» . Грипп и другие респираторные вирусы . 11 (1): 74–84. дои : 10.1111/irv.12412 . ПМК 5155642 . ПМИД 27426214 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с Аша К., Кумар Б. (февраль 2019 г.). «Новая угроза вируса гриппа D: что мы знаем на данный момент!» . Журнал клинической медицины . 8 (2): 192. дои : 10.3390/jcm8020192 . ПМК 6406440 . ПМИД 30764577 .
- ^ «Пересмотр системы номенклатуры вирусов гриппа: меморандум ВОЗ» . Бюллетень Всемирной организации здравоохранения . 58 (4): 585–91. 1980. ПМК 2395936 . ПМИД 6969132 .
- ^ Техническое примечание: Номенклатура вирусов гриппа . Панамериканская организация здравоохранения (отчет). 22 ноября 2022 года. Архивировано из оригинала 10 августа 2023 года . Проверено 27 мая 2024 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к Су С, Фу X, Ли Г, Керлин Ф, Вейт М (ноябрь 2017 г.). «Новый вирус гриппа D: эпидемиология, патология, эволюция и биологические характеристики» . Вирулентность . 8 (8): 1580–1591. дои : 10.1080/21505594.2017.1365216 . ПМК 5810478 . ПМИД 28812422 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я МакКоли Дж.В., Хонго С., Каверин Н.В., Кохс Г., Ламб Р.А., Матросович М.Н. и др. (2011). «Ортомиксовирусиды» . Международный комитет по таксономии вирусов. Архивировано из оригинала 8 августа 2022 года . Проверено 9 марта 2021 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г Шим Дж.М., Ким Дж., Тенсон Т., Мин Дж.Ю., Кайнов Д.Е. (август 2017 г.). «Инфекция вирусом гриппа, реакция интерферона, противовирусная реакция и апоптоз» . Вирусы . 9 (8): 223. дои : 10.3390/v9080223 . ПМК 5580480 . ПМИД 28805681 .
- ^ Jump up to: Перейти обратно: а б с д и ж г Хао В., Ван Л., Ли С. (октябрь 2020 г.). «Роль неструктурных белков вируса гриппа А» . Патогены . 9 (10): 812. doi : 10.3390/pathogens9100812 . ПМЦ 7600879 . ПМИД 33023047 .
- ^ Дадонайте Б., Виджаякришнан С., Фодор Э., Бхелла Д., Хатчинсон Э.К. (август 2016 г.). «Нитчатые вирусы гриппа» . Журнал общей вирусологии . 97 (8): 1755–1764. дои : 10.1099/jgv.0.000535 . ПМЦ 5935222 . ПМИД 27365089 .
- ^ Jump up to: Перейти обратно: а б Ю Э (февраль 2014 г.). «Исследование конформации и сцепления специфических олигосахаридов, связанных с H1N1, H5N1 и человеческим гриппом, для разработки второго тамифлю» . Биомолекулы и терапия . 22 (2): 93–99. дои : 10.4062/biomolther.2014.005 . ПМЦ 3975476 . ПМИД 24753813 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж Сондерс-Гастингс PR, Кревски Д. (декабрь 2016 г.). «Обзор истории пандемического гриппа: понимание закономерностей возникновения и передачи» . Патогены . 5 (4): 66. doi : 10.3390/pathogens5040066 . ПМК 5198166 . ПМИД 27929449 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л Лисетт С.Дж., Дюшатель Ф., Дигард П. (июнь 2019 г.). «Краткая история птичьего гриппа» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 374 : 20180257.doi : (1775 ) 10.1098/rstb.2018.0257 . ПМК 6553608 . ПМИД 31056053 .
- ^ Jump up to: Перейти обратно: а б с д Каттер Дж.С., Спронкен М.И., Фраай П.Л., Фушье Р.А., Херфст С. (февраль 2018 г.). «Пути передачи респираторных вирусов среди человека» . Современное мнение в вирусологии . 28 : 142–151. дои : 10.1016/j.coviro.2018.01.001 . ПМК 7102683 . ПМИД 29452994 .
- ^ Jump up to: Перейти обратно: а б с Киллингли Б., Нгуен-Ван-Там Дж. (сентябрь 2013 г.). «Пути передачи гриппа» . Грипп и другие респираторные вирусы . 7 (Приложение 2): 42–51. дои : 10.1111/irv.12080 . ПМЦ 5909391 . ПМИД 24034483 .
- ^ Вебер Т.П., Стилианакис Н.И. (ноябрь 2008 г.). «Инактивация вирусов гриппа А в окружающей среде и пути передачи: критический обзор» . Журнал инфекции . 57 (5): 361–373. дои : 10.1016/j.jinf.2008.08.013 . ПМЦ 7112701 . ПМИД 18848358 .
- ^ Jump up to: Перейти обратно: а б Морияма М., Хугентоблер В.Дж., Ивасаки А. (сентябрь 2020 г.). «Сезонность респираторных вирусных инфекций» (PDF) . Ежегодный обзор вирусологии . 7 (1): 83–101. doi : 10.1146/annurev-virology-012420-022445 . ПМИД 32196426 . Архивировано (PDF) из оригинала 28 декабря 2023 года . Проверено 28 декабря 2023 г.
- ^ Шао В., Ли Х, Горая М.У., Ван С., Чен Дж.Л. (август 2017 г.). «Эволюция вируса гриппа А путем мутации и реассортации» . Международный журнал молекулярных наук . 18 (8): 1650. doi : 10.3390/ijms18081650 . ПМК 5578040 . ПМИД 28783091 .
- ^ Jump up to: Перейти обратно: а б Штайнхауэр Д.А. (май 1999 г.). «Роль расщепления гемагглютинина в патогенности вируса гриппа» . Вирусология . 258 (1): 1–20. дои : 10.1006/виро.1999.9716 . ПМИД 10329563 .
- ^ Эйнав Т., Джентлес Л.Е., Блум Дж.Д. (июль 2020 г.). «SnapShot: Грипп в цифрах» . Клетка . 182 (2): 532–532.e1. doi : 10.1016/j.cell.2020.05.004 . ПМИД 32707094 . S2CID 220715148 .
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н тот п Чоу Э.Дж., Дойл Дж.Д., Уеки Т.М. (июнь 2019 г.). «Критические заболевания, связанные с вирусом гриппа: профилактика, диагностика, лечение» . Критическая помощь . 23 (1): 214. doi : 10.1186/s13054-019-2491-9 . ПМК 6563376 . ПМИД 31189475 .
- ^ Трегонинг Дж.С., Рассел Р.Ф., Киннер Э. (март 2018 г.). «Адъювантные вакцины против гриппа» . Человеческие вакцины и иммунотерапия . 14 (3): 550–564. дои : 10.1080/21645515.2017.1415684 . ПМЦ 5861793 . ПМИД 29232151 .
- ^ Jump up to: Перейти обратно: а б Принципи Н., Эспозито С. (март 2018 г.). «Защита детей от гриппа: новые проблемы» . Человеческие вакцины и иммунотерапия . 14 (3): 750–757. дои : 10.1080/21645515.2017.1279772 . ПМК 5861800 . ПМИД 28129049 .
- ^ Барр И.Г., Донис Р.О., Кац Дж.М., МакКоли Дж.В., Одагири Т., Трусхайм Х. и др. (октябрь 2018 г.). «Гриппозные вакцины, полученные из клеточных культур, в тяжелый эпидемический сезон 2017-2018 гг.: шаг к повышению эффективности противогриппозной вакцины» . НПЖ Вакцины . 3 : 44. doi : 10.1038/s41541-018-0079-z . ПМК 6177469 . ПМИД 30323955 .
- ^ Jump up to: Перейти обратно: а б с Джефферсон Т., Дули Л., Феррони Э., Аль-Ансари Л.А., ван Дрил М.Л., Бавазир Г.А. и др. (январь 2023 г.). «Физические вмешательства для прекращения или уменьшения распространения респираторных вирусов» . Кокрановская база данных систематических обзоров . 1 (1): CD006207. дои : 10.1002/14651858.CD006207.pub6 . ПМЦ 9885521 . ПМИД 36715243 .
- ^ Jump up to: Перейти обратно: а б Сондерс-Гастингс П., Криспо Дж.А., Сикора Л., Кревски Д. (сентябрь 2017 г.). «Эффективность мер индивидуальной защиты в снижении передачи пандемического гриппа: систематический обзор и метаанализ» . Эпидемии . 20 : 1–20. дои : 10.1016/j.epidem.2017.04.003 . HDL : 10393/38995 . ПМИД 28487207 .
- ^ Jump up to: Перейти обратно: а б «Птичий грипп (AI)» . Служба инспекции здоровья животных и растений Министерства сельского хозяйства США. Архивировано из оригинала 23 марта 2021 года . Проверено 9 марта 2021 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л Вемула С.В., Чжао Дж., Лю Дж., Ван Х., Бисвас С., Хьюлетт И. (апрель 2016 г.). «Современные подходы к диагностике вирусных инфекций гриппа у человека» . Вирусы . 8 (4): 96. дои : 10.3390/v8040096 . ПМЦ 4848591 . ПМИД 27077877 .
- ^ Jump up to: Перейти обратно: а б «Грипп: Медицинская энциклопедия MedlinePlus» . Национальная медицинская библиотека США. Архивировано из оригинала 14 февраля 2010 года . Проверено 7 февраля 2010 г.
- ^ Бандай АЗ, Арул А., Винеш П., Сингх М.П., Гоял К., Сингх С. (июль 2021 г.). «Болезнь Кавасаки и грипп – новые уроки старых ассоциаций» . Клиническая ревматология . 40 (7): 2991–2999. дои : 10.1007/s10067-020-05534-1 . ПМЦ 7778392 . ПМИД 33387094 .
- ^ «Ланинамивир» . Национальный центр развития трансляционных наук. Архивировано из оригинала 28 августа 2021 года . Проверено 9 марта 2021 г.
- ^ «Оценочное количество заболеваний гриппом, посещений врача, госпитализаций и смертей в США – сезон гриппа 2018–2019 гг.» . Центры США по контролю и профилактике заболеваний (CDC) . 9 января 2020 года. Архивировано из оригинала 9 декабря 2020 года . Проверено 5 марта 2020 г.
- ^ «Ежегодно до 650 000 человек умирают от респираторных заболеваний, связанных с сезонным гриппом» . Женева: Всемирная организация здравоохранения. 13 декабря 2017 г. Архивировано из оригинала 3 мая 2021 г. Проверено 16 июня 2021 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к Поттер CW (октябрь 2001 г.). «История гриппа». Журнал прикладной микробиологии . 91 (4): 572–579. дои : 10.1046/j.1365-2672.2001.01492.x . ПМИД 11576290 . S2CID 26392163 .
- ^ Палезе П. (декабрь 2004 г.). «Грипп: старые и новые угрозы» . Природная медицина . 10 (12 доп.): S82–S87. дои : 10.1038/nm1141 . ПМИД 15577936 . S2CID 1668689 .
- ^ Мордини Э., Грин М., ред. (2013). Интернет-информация в чрезвычайных ситуациях в области общественного здравоохранения: раннее выявление и реагирование на кризисы, вызванные вспышками заболеваний . ИОС Пресс. п. 67. ИСБН 978-1614991755 .
- ^ Мартин П.М., Мартин-Гранель Э. (июнь 2006 г.). «2500-летняя эволюция термина эпидемия» . Новые инфекционные заболевания . 12 (6): 976–980. дои : 10.3201/eid1206.051263 . ПМК 3373038 . ПМИД 16707055 .
- ^ Jump up to: Перейти обратно: а б с Моренс Д.М., Норт М., Таубенбергер Дж.К. (декабрь 2010 г.). «Рассказы очевидцев о пандемии гриппа 1510 года в Европе» . Ланцет . 376 (9756): 1894–1895. дои : 10.1016/S0140-6736(10)62204-0 . ПМК 3180818 . ПМИД 21155080 .
- ^ Герра Ф (1988). «Самая ранняя американская эпидемия. Грипп 1493 года». История социальных наук . 12 (3): 305–325. дои : 10.2307/1171451 . JSTOR 1171451 . ПМИД 11618144 .
- ^ Герра Ф (1993). «Европейско-американский обмен». История и философия наук о жизни . 15 (3): 313–327. ПМИД 7529930 .
- ^ Jump up to: Перейти обратно: а б с д и Моренс Д.М., Таубенбергер Дж.К., Фолкерс Г.К., Фаучи А.С. (декабрь 2010 г.). «500-летие пандемического гриппа» . Клинические инфекционные болезни . 51 (12): 1442–1444. дои : 10.1086/657429 . ПМК 3106245 . ПМИД 21067353 .
- ^ Jump up to: Перейти обратно: а б с д Форум Института медицины (США) по микробным угрозам (2005 г.). «1: История гриппа» . В Кноблер С., Мак А., Махмуд А., Лемон С. (ред.). Угроза пандемического гриппа: готовы ли мы? Краткое содержание семинара (2005 г.) . Вашингтон, округ Колумбия: Издательство национальных академий. стр. 60–61. дои : 10.17226/11150 . ISBN 978-0-309-09504-4 . ПМИД 20669448 . Архивировано из оригинала 10 июня 2024 года . Проверено 10 марта 2021 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л Таубенбергер Дж.К., Халтин Й.В., Моренс Д.М. (2007). «Открытие и характеристика вируса пандемического гриппа 1918 года в историческом контексте» . Противовирусная терапия . 12 (4 части Б): 581–591. дои : 10.1177/135965350701200S02.1 . ПМК 2391305 . ПМИД 17944266 .
- ^ Вийген Л., Кейартс Э., Моэс Э., Толен И., Воллантс Э., Леми П. и др. (февраль 2005 г.). «Полная геномная последовательность человеческого коронавируса OC43: анализ молекулярных часов предполагает относительно недавнее событие передачи зоонозного коронавируса» . Журнал вирусологии . 79 (3): 1595–1604. doi : 10.1128/JVI.79.3.1595-1604.2005 . ПМК 544107 . ПМИД 15650185 .
- ^ Таубенбергер Дж. К., Моренс Д. М. (январь 2006 г.). «Грипп 1918 года: мать всех пандемий» . Новые инфекционные заболевания . 12 (1): 15–22. дои : 10.3201/eid1201.050979 . ПМЦ 3291398 . ПМИД 16494711 .
- ^ Смит В., Эндрюс Ч., Лэйдлоу П. П. (1933). «Вирус, полученный от больных гриппом» . Ланцет . 2 (5732): 66–68. дои : 10.1016/S0140-6736(00)78541-2 .
- ^ Хайнен П.П. (15 сентября 2003 г.). «Свиной грипп: зооноз» . Ветеринары завтра . ISSN 1569-0830 . Архивировано из оригинала 11 февраля 2007 года . Проверено 28 декабря 2016 г.
- ^ Васкес-Эспиноса Э, Лагана С, Васкес Ф (октябрь 2020 г.). «Испанка и художественная литература» . Revista Espanola de Quimioterapia . 33 (5): 296–312. дои : 10.37201/req/049.2020 . ПМЦ 7528412 . ПМИД 32633114 .
- ^ «грипп (сущ.)» . Интернет-словарь этимологии. Архивировано из оригинала 28 января 2021 года . Проверено 9 марта 2021 г.
- ^ «грипп» . Оксфордский словарь английского языка. Архивировано из оригинала 16 октября 2021 года . Проверено 9 марта 2021 г.
- ^ «грипп (сущ.)» . Интернет-словарь этимологии. Архивировано из оригинала 21 июля 2021 года . Проверено 20 июля 2021 г.
- ^ Калишер CH (август 2009 г.). «Свиной грипп» . Хорватский медицинский журнал . 50 (4): 412–415. дои : 10.3325/cmj.2009.50.412 . ПМЦ 2728380 . ПМИД 19673043 .
- ^ «Спросите ученого CDC: доктор Терренс Тампи и реконструкция пандемического вируса 1918 года | Пандемический грипп (грипп) | CDC» . Архив: Центры по контролю и профилактике заболеваний . 24 мая 2018 года . Проверено 2 июля 2024 г.
- ^ «Фундаментальные исследования гриппа» . Национальный институт аллергии и инфекционных заболеваний. 13 марта 2017 г. Архивировано из оригинала 10 июня 2024 г. . Проверено 24 марта 2021 г.
- ^ «Глобальная система эпиднадзора за гриппом и реагирования (ГСЭГО)» . Всемирная организация здравоохранения. Архивировано из оригинала 3 октября 2011 года . Проверено 24 марта 2021 г.
- ^ Jump up to: Перейти обратно: а б Нахбагауэр Р., Краммер Ф. (апрель 2017 г.). «Универсальные вакцины против вируса гриппа и терапевтические антитела» . Клиническая микробиология и инфекции . 23 (4): 222–228. дои : 10.1016/j.cmi.2017.02.009 . ПМК 5389886 . ПМИД 28216325 .
- ^ Роза С.С., Празерес Д.М., Азеведо А.М., Маркес MP (апрель 2021 г.). «Производство мРНК-вакцин: проблемы и узкие места» . Вакцина . 39 (16): 2190–2200. doi : 10.1016/j.vaccine.2021.03.038 . ПМЦ 7987532 . ПМИД 33771389 .
- ^ Эванс Н.Г., Пенс Ч. (май 2023 г.). «Исследование усиления функций и модельные организмы в биологии» . Журнал медицинской этики . 50 (3): jme–2022–108853. дои : 10.1136/jme-2022-108853 . ПМИД 37188506 . S2CID 258688081 .
- ^ Jump up to: Перейти обратно: а б с Александр DJ, Браун IH (2009). «История высокопатогенного птичьего гриппа». Преподобный учёный. Тех . 28 (1): 19–38. doi : 10.20506/rst.28.1.1856 . ПМИД 19618616 .
- ^ «Информационный бюллетень по A(H5N1)» . www.ecdc.europa.eu . 15 июня 2017 года. Архивировано из оригинала 21 мая 2024 года . Проверено 21 мая 2024 г.
- ^ CDC (5 апреля 2024 г.). «Текущая ситуация с птичьим гриппом в США у людей» . Центры США по контролю и профилактике заболеваний (CDC) . Архивировано из оригинала 22 мая 2024 года . Проверено 22 мая 2024 г.
- ^ «Свиной грипп» . Всемирная организация здоровья животных. Архивировано из оригинала 4 марта 2021 года . Проверено 9 марта 2021 г.
Дальнейшее чтение
| Внешние видео | |
|---|---|
- Браун Дж. (2018). Грипп: столетняя охота за лечением самой смертельной болезни в истории . Нью-Йорк: Атрия. ISBN 978-1501181245 .
- Муриц А.А. (1921). Грипп: краткая история гриппа в США, Америке, Европе, на Гавайях . Гонолулу, Гавайи, США Америка: Издательство Advertiser Publishing Co.