Тимоцит
Тимоцит до того , – это иммунная клетка , присутствующая в тимусе как она подвергнется трансформации в Т-клетку . [1] Тимоциты производятся в виде стволовых клеток в костном мозге и достигают тимуса через кровь .
Тимопоэз описывает процесс, который превращает тимоциты в зрелые Т-клетки в соответствии с отрицательным или положительным отбором. Этот процесс отбора жизненно важен для формирования популяции тимоцитов в периферический пул Т-клеток, которые способны реагировать на чужеродные патогены организма , но остаются толерантными к собственным антигенам . Положительный отбор отбирает клетки, которые способны связывать молекулы MHC класса I или II по крайней мере со слабым сродством. Это устраняет (путем процесса, называемого «смерть из-за пренебрежения») те Т-клетки, которые были бы нефункциональными из-за неспособности связывать MHC. Отрицательный отбор разрушает тимоциты с высоким сродством к собственным пептидам или MHC. Это устраняет клетки, которые направляют иммунные реакции на собственные белки на периферии. Негативный отбор не эффективен на 100%, и некоторые аутореактивные Т-клетки ускользают и попадают в кровоток. Существуют дополнительные механизмы периферической толерантности , заставляющие эти клетки замолчать, но если они не помогают, возникает аутоиммунитет. может возникнуть.
Этапы созревания
[ редактировать ]Тимоциты подразделяются на ряд различных стадий созревания на основе экспрессии маркеров клеточной поверхности. Самая ранняя стадия тимоцитов - это двойная негативная стадия (отрицательная как для CD4, так и для CD8), которую в последнее время лучше описывать как Lineage-отрицательную и которую можно разделить на четыре подстадии. Следующей основной стадией является двойная положительная стадия (положительная как для CD4, так и для CD8). Заключительная стадия созревания — это единственная положительная стадия (положительная по CD4 или CD8).
У мышей
[ редактировать ]| Этап | Определение маркеров поверхности | Расположение | Значимые события |
| Двойной отрицательный 1 или ETP (прародитель ранней линии T) | Lineage- CD44 + CD25 - CD117 + | кора головного мозга | Пролиферация, потеря B и миелоидных потенциалов |
| Двойной отрицательный 2 | Lineage-CD44+CD25+CD117+ | кора головного мозга | - |
| Двойной отрицательный 3 | Lineage-CD44-CD25+ | кора головного мозга | Перегруппировка TCR-бета, бета-селекция |
| Двойной отрицательный 4 | Lineage-CD44-CD25- | кора головного мозга | - |
| Двойной позитив | CD4 + CD8 + | кора головного мозга | Перегруппировка TCR-альфа, положительный отбор, отрицательный отбор |
| Одиночный позитив | CD4+CD8- или CD4-CD8+ | мозговое вещество | Отрицательный выбор |
У людей
[ редактировать ]У человека циркулирующие CD34+ гемопоэтические стволовые клетки находятся в костном мозге. Они продуцируют предшественников Т-лимфоцитов, которые засеивают тимус (становясь таким образом тимоцитами) и дифференцируются под влиянием белка Notch и его лигандов.
Ранние двойно-негативные тимоциты экспрессируют (и могут быть идентифицированы) CD2 , CD5 и CD7 . Тем не менее, во время двойной негативной стадии экспрессия CD34 прекращается и CD1 экспрессируется . Экспрессия CD4 и CD8 делает их дважды положительными и созревает в клетки CD4+ или CD8+. [2]
События во время созревания
[ редактировать ]| тип: | функционал (бета-выбор) | функциональный (положительный отбор) | автореактивный (отрицательный отбор) |
| расположение: | кора головного мозга | кора головного мозга | кора/мозговой слой |
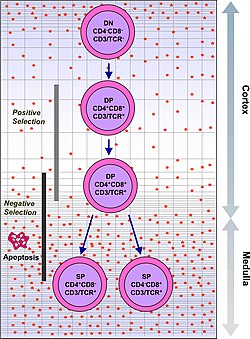 | Чтобы пройти контрольную точку β-отбора, β-цепь рецептора Т-клеток , реаранжированная тимоцитом, должна сохранять структурные свойства, позволяющие ей быть представленными на поверхности тимоцита с помощью pre-TCRα. Это устраняет тимоциты с грубыми дефектами, введенными в рецептор Т-клеток путем перестройки генов. | Чтобы пройти положительный отбор , тимоциты должны будут взаимодействовать с несколькими молекулами клеточной поверхности, MHC , чтобы обеспечить реактивность и специфичность. [3] Положительный отбор отбирает клетки с Т-клеточным рецептором, способным связывать молекулы MHC класса I или II с, по крайней мере, слабым сродством. Это устраняет (путем процесса, называемого «смерть из-за пренебрежения») те Т-клетки, которые были бы нефункциональными из-за неспособности связывать MHC. | Негативный отбор – это активная индукция апоптоза в тимоцитах с высоким сродством к собственным пептидам или MHC. Это устраняет клетки, которые направляют иммунные реакции на собственные белки на периферии. Негативный отбор не эффективен на 100%, некоторые аутореактивные Т-клетки избегают цензуры тимуса и попадают в кровоток. Для подавления этих клеток существуют дополнительные механизмы толерантности, активные на периферии, такие как анергия , делеция и регуляторные Т-клетки . Если эти механизмы периферической толерантности также терпят неудачу, аутоиммунитет может возникнуть . |
Тимус оседает
[ редактировать ]Тимоциты в конечном итоге происходят из кроветворных клеток-предшественников костного мозга [см. гемопоэтические стволовые клетки , кроветворение ], которые достигают тимуса через кровообращение. [4] Считается, что количество предшественников, ежедневно попадающих в тимус, чрезвычайно мало. Поэтому неизвестно, какие предшественники колонизируют тимус. В настоящее время предполагается, что Early Lymphoid Progenitors (ELP) заселяют тимус и, вероятно, являются предшественниками по крайней мере некоторых тимоцитов. ELPs представляют собой Lineage-CD44+CD25-CD117+ и, таким образом, очень напоминают ETPs, самые ранние предшественники в тимусе. Предшественники проникают в тимус через кортико-медуллярный переход. Молекулы, которые, как известно, важны для входа в тимус, включают P-селектин (CD62P) и хемокиновые рецепторы CCR7 и CCR9 . [5]
После входа в тимус предшественники пролиферируют, образуя популяцию ETP. За этим этапом следует генерация тимоцитов DN2, которые мигрируют от кортико-медуллярного соединения к капсуле тимуса. Тимоциты DN3 генерируются в субкапсулярной зоне.
Помимо пролиферации, в популяции DN-тимоцитов происходит дифференцировка и коммитация Т-линии. Приверженность или потеря альтернативных потенциалов клона (таких как потенциалы миелоидной, B и NK) зависит от передачи сигналов Notch и завершается к стадии DN3. После детерминации T-линии тимоциты DN3 подвергаются β-селекции. [6]
б-выбор
[ редактировать ]
Способность Т-клеток распознавать чужеродные антигены опосредована Т-клеточным рецептором (TCR), который представляет собой поверхностный белок, способный распознавать короткие белковые последовательности ( пептиды ), представленные на MHC . Целью развития тимоцитов является производство зрелых Т-клеток с разнообразным набором функциональных Т-клеточных рецепторов посредством процесса перестройки гена TCR.
В отличие от большинства генов, которые имеют стабильную последовательность в каждой экспрессирующей их клетке, рецептор Т-клеток состоит из ряда альтернативных генных фрагментов. Чтобы создать функциональный Т-клеточный рецептор, двойные негативные тимоциты используют ряд ферментов, взаимодействующих с ДНК, для клипирования ДНК и объединения отдельных фрагментов гена. Результатом этого процесса является то, что каждый рецептор Т-клеток имеет разную последовательность из-за различного выбора фрагментов гена и ошибок, возникающих во время процесса разрезания и соединения ( см. в разделе о рекомбинации V(D)J дополнительную информацию о реаранжировке TCR ). . Эволюционное преимущество наличия большого количества уникальных рецепторов Т-клеток заключается в том, что каждая Т-клетка способна распознавать разные пептиды, обеспечивая защиту от быстро развивающихся патогенов. [7]
Перегруппировка TCR происходит в два этапа. Сначала цепь TCRβ перестраивается на стадии DN3 развития Т-клеток. Цепь TCRβ соединяется с пре-Tα для образования пре-TCR. Клеточным недостатком процесса реаранжировки является то, что многие комбинации фрагментов гена рецептора Т-клеток нефункциональны. Чтобы устранить тимоциты, которые создали нефункциональный Т-клеточный рецептор , разрешается развиваться после стадии DN3 только клеткам, которые успешно перестроили бета-цепь для производства функционального пре-TCR. Клетки, которые не способны вырабатывать функциональный пре-TCR, уничтожаются путем апоптоза . Этот процесс называется контрольной точкой бета-отбора. Успешная бета-селекция требует, чтобы TCRβ продуцировался, TCRβ был способен соединяться с пре-Tα с образованием пре-TCR и чтобы пре-TCR мог взаимодействовать на поверхности клетки с сигнальными белками TCR.
На стадии β-селекции, как и зрелый TCR, пре-TCR также образует иммунологический синапс. [8] Хотя взаимодействие пре-TCR и связанного с пептидом MHC не является существенным для развития Т-клеток, [9] [10] он играет решающую роль в стимулировании преимущественной пролиферации клеток, пре-TCR которых может связывать собственный MHC. [11] [12]
После β-селекции тимоциты генерируют CD4+CD8+ двойные положительные клетки, которые затем подвергаются реаранжировке TCRα, что приводит к полностью собранному TCR.
Положительный отбор и приверженность родословной
[ редактировать ]
Тимоциты, прошедшие β-селекцию, экспрессируют Т-клеточный рецептор , способный собираться на поверхности. Однако многие из этих Т-клеточных рецепторов по-прежнему нефункциональны из-за неспособности связывать MHC . Следующим важным этапом развития тимоцитов является позитивный отбор, при котором сохраняются только те тимоциты, которые имеют Т-клеточный рецептор, способный связывать MHC. Рецептору Т-клеток требуется CD8 в качестве корецептора для связывания с MHC класса I и CD4 в качестве корецептора для связывания MHC класса II. На этом этапе тимоциты активируют как CD4 , так и CD8 , становясь двойными положительными клетками.
Двойные положительные тимоциты, имеющие рецептор Т-клеток, способный связывать MHC класса I или класса II (даже со слабым сродством), получают сигнал через рецептор Т-клеток. [3] Тимоциты, имеющие Т-клеточный рецептор, неспособный связывать MHC класса I или класса II, подвергаются апоптозу . Некоторые тимоциты способны спасти неудачный положительный отбор путем редактирования рецептора (перестройки другого аллеля рецептора Т-клеток для производства нового рецептора Т-клеток).
Двойные положительные тимоциты подвергаются коммитированию клона, созревая в CD8+ Т-клетку (распознающую MHC класс I) или CD4+ Т-клетку (распознающую MHC класс II). Коммитация клона происходит на поздней стадии положительного отбора и действует путем подавления как CD4, так и CD8 (снижения сигнала от рецептора Т-клеток), а затем усиления только CD4. Тимоциты, которые снова начинают получать сигнал, — это те, которые распознают MHC класса II, и становятся CD4+ Т-клетками. Тимоциты, которые не начинают снова получать сигнал, — это те, которые распознают MHC класса I, подавляют CD4 и повышают CD8, становясь CD8+ Т-клетками. Оба этих типа тимоцитов известны как одиночные положительные тимоциты.
Отрицательный выбор
[ редактировать ]Успех положительного отбора позволяет тимоциту претерпеть ряд изменений в процессе созревания во время перехода к одной положительной Т-клетке. Одиночные положительные Т-клетки усиливают активность хемокинового рецептора CCR7, вызывая миграцию из коры в мозговое вещество. На этом этапе ключевой процесс созревания включает негативный отбор, элиминацию аутореактивных тимоцитов.
Ключевым недостатком процесса генной реаранжировки рецепторов Т-клеток является то, что по случайности некоторые расположения фрагментов гена создают рецептор Т-клеток, способный связывать собственные пептиды, представленные в MHC класса I или MHC класса II. Если бы Т-клетки, несущие эти Т-клеточные рецепторы, попали на периферию, они были бы способны активировать иммунный ответ против себя, что привело бы к аутоиммунитету . Негативный отбор — это процесс, разработанный для снижения этого риска. Во время негативного отбора все тимоциты с высоким сродством к связыванию собственных пептидов, представленных в MHC класса I или класса II, индуцируются для повышения регуляции BCL2L11 , белка, который запускает апоптоз. Клетки, не обладающие высоким сродством к аутоантигенам, выживают при отрицательном отборе. На этом этапе некоторые клетки также отбираются для того, чтобы стать регуляторными Т-клетками , обычно это клетки, которые имеют промежуточное сродство к аутопептиду.
Негативный отбор может происходить на двойной позитивной стадии коры. Однако репертуар пептидов в коре головного мозга ограничен пептидами, экспрессируемыми эпителиальными клетками, а двойные положительные клетки плохо поддаются негативному отбору. Следовательно, наиболее важным местом негативного отбора является мозговое вещество, когда клетки находятся на единственной положительной стадии. Чтобы удалить тимоциты, реагирующие на периферические органы, факторы транскрипции Aire и Fezf2 управляют экспрессией множества периферических антигенов, таких как инсулин, что приводит к удалению клеток, специфичных для этих антигенов. [13] [14] Это позволяет одиночным положительным тимоцитам подвергаться воздействию более сложного набора аутоантигенов, чем тот, который присутствует в коре головного мозга, и, следовательно, более эффективно удаляет те Т-клетки, которые являются аутореактивными.
Одиночные положительные тимоциты остаются в мозговом веществе в течение 1–2 недель, исследуя аутоантигены для проверки аутореактивности. За это время они претерпевают окончательные изменения в процессе созревания, а затем выходят из тимуса с помощью S1P и CCR7. При попадании в периферический кровоток клетки считаются зрелыми Т-клетками, а не тимоцитами.
Негативный отбор не эффективен на 100%, некоторые аутореактивные Т-клетки избегают цензуры тимуса и попадают в кровоток. Для подавления этих клеток существуют дополнительные механизмы периферической толерантности, активные на периферии, такие как анергия , делеция и регуляторные Т-клетки . Если эти механизмы периферической толерантности также терпят неудачу, аутоиммунитет может возникнуть .
Трансплантация тимуса приводит к тому, что Т-клетки учат избегать реакции с донорскими антигенами, и они все еще могут реагировать со многими аутоантигенами в организме. Аутоиммунное заболевание является частым осложнением после трансплантации тимуса и обнаруживается у 42% субъектов в течение 1 года после трансплантации. [15] Однако частично это объясняется тем, что само показание, то есть полный синдром ДиДжорджа (отсутствие тимуса), увеличивает риск аутоиммунного заболевания. [16]
Рак
[ редактировать ]Тимоциты, которые приобретают онкогенные мутации, способствующие неконтролируемой пролиферации, могут стать лимфомами тимуса .
Альтернативные линии
[ редактировать ]Помимо классических αβ Т-клеток (их развитие описано выше), в тимусе развивается ряд других Т-линий, включая γδ Т-клетки и Т-клетки естественных киллеров (NKT). Кроме того, в тимусе могут развиваться другие гемопоэтические линии, отличные от Т, в том числе В-лимфоциты (В-клетки) и естественные киллерные лимфоциты (NK-клетки). [17] [18] ), миелоидные клетки и дендритные клетки. Однако тимус не является источником развития B, NKC или миелоида (это утверждение справедливо не для всех B-клеток или NKC). Развитие этих клеток в тимусе отражает мультипотентную природу гемопоэтических предшественников, которые засеивают тимус. В мозговом веществе также можно обнаружить зрелые B-клетки и другие АПК, которые способствуют процессам негативного отбора. [19]
Ссылки
[ редактировать ]- ^ «тимоцит» в Медицинском словаре Дорланда.
- ^ Рисунок 12-13 в: Митчелл, Ричард Шеппард; Кумар, Винай; Аббас, Абул К.; Фаусто, Нельсон (2007). Основная патология Роббинса . Филадельфия: Сондерс. ISBN 978-1-4160-2973-1 . 8-е издание.
- ^ Перейти обратно: а б Болдуин Т.А., Хогквист К.А., Джеймсон СК (2004). «Четвертый путь? Использование агрессивных тенденций в тимусе» . Дж Иммунол . 173 (11): 6515–20. дои : 10.4049/jimmunol.173.11.6515 . ПМИД 15557139 .
- ^ Шварц Б.А., Бхандула А. Транспортировка из костного мозга в тимус: необходимое условие тимопоэза . Иммунол Ред. 209:47, 2006. полный текст
- ^ Шварц Б.А., Самбандам А., Майяр I, Харман BC, Лав П.Е., Бхандула А. Селективное урегулирование тимуса, регулируемое цитокиновыми и хемокиновыми рецепторами. Дж Иммунол. 15 февраля 2007 г.; 178 (4): 2008–17. [1]
- ^ К. Клэр Блэкберн и Нэнси Р. Мэнли «Разработка новой парадигмы органогенеза тимуса» Nature Reviews Immunology, апрель 2004 г., стр. 278-289, дата обращения 04.10.12 [2]
- ^ Слекман Б.П., Сборка генов рецептора антигена лимфоцитов: несколько уровней регуляции. Immunol Res 32:153-8, 2005. полный текст. Архивировано 27 января 2008 г. в Wayback Machine.
- ^ Аллам, Амр Х.; Чарнли, Миррен; Фам, Ким; Рассел, Сара М. (01 марта 2021 г.). «Развивающиеся Т-клетки образуют иммунологический синапс для прохождения через контрольную точку β-селекции» . Журнал клеточной биологии . 220 (3): e201908108. дои : 10.1083/jcb.201908108 . ISSN 0021-9525 . ПМЦ 7814350 . ПМИД 33464309 .
- ^ Ирвинг, Брайан А.; Альт, Фредерик В.; Киллин, Найджел (8 мая 1998 г.). «Развитие тимоцитов в отсутствие внеклеточных доменов иммуноглобулина пре-Т-клеточных рецепторов» . Наука . 280 (5365): 905–908. Бибкод : 1998Sci...280..905I . дои : 10.1126/science.280.5365.905 . ISSN 0036-8075 . ПМИД 9572735 .
- ^ Коллер, Беверли Х.; Маррак, Филиппа; Капплер, Джон В.; Смитис, Оливер (01 мая 2010 г.). «Нормальное развитие мышей с дефицитом бета-2М, белков MHC класса I и CD8+ Т-клеток. 1990» . Журнал иммунологии . 184 (9): 4592–4595. ISSN 1550-6606 . ПМИД 20410496 .
- ^ Мижей, Река; Ли, Сяолун; Чен, Ван-На; Сабо, Моника; Ван, Цзя-хуай; Вагнер, Герхард; Рейнхерц, Эллис Л.; Маллис, Роберт Дж. (январь 2021 г.). «Общая стратегия химического сшивания для структурного анализа слабо взаимодействующих белков, применяемая к комплексам preTCR-pMHC» . Журнал биологической химии . 296 : 100255. дои : 10.1016/j.jbc.2021.100255 . ISSN 0021-9258 . ПМЦ 7948749 . ПМИД 33837736 .
- ^ Ли, Сяолун; Мижей, Река; Тан, Кемин; Маллис, Роберт Дж.; Дюк-Коэн, Джонатан С.; Акицу, Аой; Теттех, Пол В.; Дубей, Абхинав; Хван, Вонмук; Вагнер, Герхард; Лэнг, Мэтью Дж. (08 января 2021 г.). «Пре-Т-клеточные рецепторы топологически отбирают собственные лиганды во время β-селекции тимоцитов» . Наука . 371 (6525): 181–185. Бибкод : 2021Sci...371..181L . дои : 10.1126/science.abe0918 . ISSN 0036-8075 . ПМЦ 8011828 . ПМИД 33335016 .
- ^ Андерсон, MS и др. (2002)Проекция иммунологической тени внутри тимуса с помощью белка Aire. Наука 298 (5597), 1395-1401
- ^ Такаба, Х. и др. (2015) Fezf2 организует тимусные программы экспрессии собственного антигена для иммунной толерантности. Ячейка 163, 975–987
- ^ Трансплантация тимусаКнига «Патология вилочковой железы», страницы 255–267, Springer Milan, 2008 г. дои : 10.1007/978-88-470-0828-1 ISBN 978-88-470-0827-4 (печать) ISBN 978-88-470-0828-1 (онлайн) дои : 10.1007/978-88-470-0828-1_30
- ^ Маркерт М.Л., Девлин Б.Х., Алексиефф М.Дж. и др. (май 2007 г.). «Обзор 54 пациентов с полной аномалией ДиДжорджа, включенных в протоколы трансплантации тимуса: результат 44 последовательных трансплантаций» . Кровь . 109 (10): 4539–47. дои : 10.1182/blood-2006-10-048652 . ПМК 1885498 . ПМИД 17284531 .
- ^ ван ден Брандт Дж., Восс К., Шотт М., Хюниг Т., Вулф М.С., Райхардт Х.М. (май 2004 г.). «Ингибирование передачи сигналов Notch смещает развитие тимоцитов крысы в сторону линии NK-клеток» . Евро. Дж. Иммунол . 34 (5): 1405–13. дои : 10.1002/eji.200324735 . ПМИД 15114674 . S2CID 6270092 .
- ^ Санчес М.Дж., Спитс Х., Ланье Л.Л., Филлипс Дж.Х. (декабрь 1993 г.). «Тимоциты, коммитирующие естественные киллеры человека, и их связь с линией Т-клеток» . Дж. Эксп. Мед . 178 (6): 1857–66. дои : 10.1084/jem.178.6.1857 . ПМК 2191276 . ПМИД 7504051 .
- ^ Джеральдо А. Пассос Сезар А. Спек-Эрнандес Аманда Ф. Ассис Даниэлла А. Мендес-да-Крус. «Обновленная информация об Aire и отрицательном отборе тимуса».
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь )