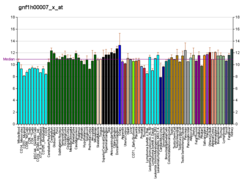
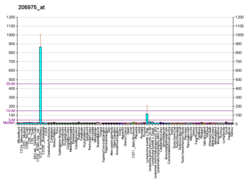
Лимфотоксин альфа
| ДСС | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | LTA , LT, TNFB, TNFSF1, лимфотоксин альфа, TNLG1E | |||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 153440 ; МГИ : 104797 ; Гомологен : 497 ; GeneCards : LTA ; ОМА : LTA – ортологи | |||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
Лимфотоксин-альфа ( LT-α ), ранее известный как фактор некроза опухоли-бета (TNF-β) [5] [6] — белок , который у человека кодируется LTA геном . [7] [8] Принадлежащий к линии гемопоэтических клеток, LT-α проявляет антипролиферативную активность и вызывает клеточную деструкцию линий опухолевых клеток. [7] Как цитотоксический белок LT-α выполняет множество важных ролей в иммунной регуляции в зависимости от формы, в которой он секретируется. В отличие от других членов суперсемейства TNF , LT-α обнаруживается только в виде растворимого гомотримера, а при обнаружении на поверхности клетки он обнаруживается только в виде гетеротримера с LTβ. [9]
LT-α оказывает значительное влияние на поддержание иммунной системы, включая развитие вторичных лимфоидных органов . [10] [11] Отсутствие LT-α приводит к нарушению развития желудочно-кишечного тракта, предотвращает развитие пейеровых пятен и приводит к дезорганизации селезенки. [12]
Как сигнальная молекула LT-α участвует в регуляции выживания, пролиферации , дифференцировки и апоптоза клеток . [13] LT-α играет важную роль в регуляции врожденного иммунитета , и было показано, что его присутствие предотвращает рост опухоли и уничтожает линии раковых клеток. [14] Напротив, нерегулируемая экспрессия LT-α может привести к постоянно активному сигнальному пути, что приводит к неконтролируемому клеточному росту и образованию опухолей . [13] Следовательно, в зависимости от контекста LT-α может предотвращать рост раковых клеток или способствовать развитию опухолей. Кроме того, эффекты LT-α зависят от типа органа, на который он действует, типа раковых клеток, клеточной среды, пола и времени воздействия во время иммунного ответа. [15] [14]
Ген
[ редактировать ]Человеческий ген, кодирующий LT-α, был клонирован в 1985 году. [7] [16] Ген LT-α расположен на хромосоме 6 и находится в непосредственной близости от гена, кодирующего главный комплекс гистосовместимости . [17]
Структура
[ редактировать ]LT-α транслируется как гликозилированный полипептид массой 25 кДа со 171 аминокислотным остатком. [8] Более того, человеческий LT-α на 72% идентичен мышиному LT-α по первичной последовательности белка. [18]
Экспрессия LTα в высокой степени индуцируема и при секреции образует растворимую гомотримерную молекулу. LT-α также может образовывать гетеротримеры с лимфотоксином-бета , который закрепляет лимфотоксин-альфа на поверхности клетки. Взаимодействие между LT-α и LT-β приводит к образованию мембраносвязанного комплекса (LT-α 1 -β 2 ). [11]
Функция
[ редактировать ]Лимфотоксин альфа, член суперсемейства факторов некроза опухоли , представляет собой цитокин, продуцируемый лимфоцитами . LT-α 1 -β 2 может взаимодействовать с рецепторами, такими как рецепторы LT-β . [13] Отсутствие LT-β на поверхности клеток уменьшит способность LT-α образовывать LT-α 1 -β 2 , тем самым уменьшая его эффективную способность в качестве цитокина . [10] [11] LT-α опосредует широкий спектр воспалительных , иммуностимулирующих и противовирусных реакций. LT-α также участвует в формировании вторичных лимфоидных органов во время развития и играет роль в апоптозе. [19]
У мышей с нокаутом LT -α пейеровы пятна и лимфатические узлы не развиваются, что иллюстрирует важную роль цитокина в иммунологическом развитии. [20]
Как цитотоксический белок LT-α вызывает разрушение линий раковых клеток, активирует сигнальные пути и эффективно убивает трансформированные опухолевые клетки. [10] [13] Однако мыши со сверхэкспрессией LT-α или LT-β показали повышенный рост опухоли и метастазирование в нескольких моделях рака. В других исследованиях у мышей с нокаутом гена LT-α наблюдался усиленный рост опухоли, что указывает на возможную защитную роль LT-α при раке. Однако в этих исследованиях использовались мыши с полным дефицитом LT-α, что не позволяло различить эффекты растворимого и мембраносвязанного LT. [21]
Сигнальный путь, опосредованный LT-α
[ редактировать ]Являясь членом семейства TNF , LT-α связывается с различными рецепторами и активирует путь NF-κB , тем самым способствуя иммунной регуляции посредством врожденного иммунного ответа. [13] Чтобы произошла активация, LT-α должен образовать комплекс с LT-β с образованием комплекса LT-α 1 -β 2 . Образование комплекса LT-α 1 -β 2 обеспечивает связывание с рецепторами LT-β и последующую активацию сигнальных путей. [22] Активация сигнальных путей, таких как NF-κB, в конечном итоге приводит к различным судьбам клеток, включая пролиферацию и гибель клеток. После активации рецептора LT-β образуются IKK-α, β и γ, что увеличивает деградацию I-κB , ингибитора NF-kB, и продуцирует NF-kB1 (p50) и ReIA (p60). [22] Продукция NF-kB1 и ReIA увеличивает скорость транскрипции генов цитокинов и молекул, индуцирующих воспаление. [22] [23]
Антиканцерогенные свойства
[ редактировать ]Активация LT-β-рецепторов способна индуцировать гибель раковых клеток и подавлять рост опухоли. [24] [25] Процесс гибели клеток опосредован присутствием IFN-γ и может включать апоптотические или некротические пути. [24] Видно, что LT-β-рецепторы способствуют активации молекул адгезии и рекрутированию лимфоцитов в опухолевые клетки для борьбы с ростом опухоли. [7] [13] Другими словами, взаимодействия LT-α с рецепторами LT-β могут усиливать противоопухолевые эффекты за счет прямого разрушения опухолевых клеток.
Проканцерогенные свойства
[ редактировать ]Однако недавние исследования показали вклад передачи сигналов, опосредованной LT-α, в развитие рака. [10] [13] [14] [15] Как упоминалось ранее, передача сигналов LT-α может способствовать воспалительным реакциям, но длительное воспаление может вызвать серьезное повреждение клеток и увеличить риск некоторых заболеваний, включая рак. [14] Таким образом, мутации регуляторных факторов в сигнальных путях LT-α могут способствовать нарушениям клеточной сигнализации и способствовать созданию линий раковых клеток. Одна из этих мутаций включает постоянное связывание комплекса LT-α 1 -β 2 с рецепторами LT-β, что приводит к постоянной активации альтернативного пути NF-κB. [13] [14] Наличие конститутивно активного пути NF-κB проявляется при множественной миеломе и других онкологических заболеваниях. [13] Было показано, что удаление LT-β-рецепторов ингибирует рост опухоли и снижает ангиогенез . [14] Таким образом, лимфотоксин и его последующая передача сигналов по пути NF-κB иллюстрируют влияние цитокина на развитие опухоли и метастазирование.
Было показано , что полностью гуманизированное антитело против LT-α ( Патеклизумаб или MLTA3698A) реагирует как с LT-α, так и с LT-β. [10] Клинические испытания этого антитела еще предстоит провести, но создание этого антитела предлагает альтернативные методы ингибирования пути NF-κB.
Влияние на желудочно-кишечную систему
[ редактировать ]Во время эмбрионального развития передача сигналов LT-α играет активную роль в формировании желудочно-кишечной иммунной системы. [12] В частности, передача сигналов, опосредованная LT-α, ответственна за развитие кишечных лимфоидных структур, таких как пейеровы бляшки . [26] [27] Этот кишечный лимфоидный фолликул играет важную роль в иммунной системе пищеварительного тракта.
Пейеровы бляшки – это узкоспециализированные лимфоидные узелки, расположенные в кишечнике. Они окружены фолликул-ассоциированным эпителием и способны взаимодействовать с другими иммунными клетками посредством трансцитоза чужеродных антигенов. [28] В дополнение к этой функции, пластыри Пейера способствуют выработке иммуноцитов, продуцирующих Ig-A , тем самым повышая эффективность адаптивной иммунной системы . [29]
Для развития пейеровых бляшек необходимо связывание и активация рецептора LT-β с комплексом LT-α 1 -β 2 . Эксперименты с участием трансгенных мышей показали, что отсутствие LT-α приводит к отсутствию пейеровых бляшек и других лимфатических узлов. [12] Также было показано, что отсутствие пейеровых пятен и других лимфатических узлов снижает уровень Ig-A. [12] Будучи наиболее продуцируемым иммуноглобулином, Ig-A защищает от патогенов слизистой оболочки , регулируя рост бактерий и ингибируя адгезию антигена в кишечнике в нормальных условиях. [30] Снижение уровня Ig-A значительно снижает иммунную регуляцию кишечника и ослабляет защиту от микробов, тем самым подчеркивая важность LT-опосредованного ответа для экспрессии Ig-A.
Номенклатура
[ редактировать ]Обнаруженный Грейнджером и его исследовательской группой в 1968 году, LT-альфа был известен как лимфотоксин. [31] С течением времени его название было изменено на фактор некроза опухоли-бета (ФНО-β). [32] Позднее открытие комплекса LT-β и LT-α 1 -β 2 привело к отказу от TNF-β и разделению LT на два класса: LT-α и LT-β. [33] [34]
Взаимодействия
[ редактировать ]Было показано, что лимфотоксин альфа взаимодействует с LTB . [35] [36] [37]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с ENSG00000223919, ENSG00000173503, ENSG00000226275, ENSG00000230279, ENSG00000238130, ENSG00000226979 GRCh38: Версия ансамбля 89: ENSG00000231408, 0000223919, ENSG00000173503, ENSG00000226275, ENSG00000230279, ENSG00000238130, ENSG00000226979 – ансамбль , май 2017 г.
- ^ Jump up to: а б с GRCm38: Ensembl, выпуск 89: ENSMUSG00000024402 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Лимфотоксин Альфа - обзор | Темы ScienceDirect» .
- ^ Кальмон-Хамати Ф., Комб Б., Хане М., Морель Дж. Еще раз о лимфотоксине α: общие особенности и последствия при ревматоидном артрите. Артрит Res Ther. 26 июля 2011 г.; 13 (4): 232. дои: 10.1186/ar3376. ПМИД 21861866; PMCID: PMC3239340.
- ^ Jump up to: а б с д Недвин Дж.Е., Нейлор С.Л., Сакагути А.Ю., Смит Д., Джарретт-Недвин Дж., Пенника Д., Гёддел Д.В., Грей П.В. (сентябрь 1985 г.). «Гены лимфотоксина человека и фактора некроза опухолей: структура, гомология и хромосомная локализация» . Исследования нуклеиновых кислот . 13 (17): 6361–73. дои : 10.1093/нар/13.17.6361 . ПМК 321958 . ПМИД 2995927 .
- ^ Jump up to: а б Аггарвал Б.Б., Эессалу Т.Э., Хасс П.Е. (февраль 1986 г.). «Характеристика рецепторов фактора некроза опухолей человека и их регуляция гамма-интерфероном». Природа . 318 (6047): 665–7. дои : 10.1038/318665a0 . ПМИД 3001529 . S2CID 4341571 .
- ^ Кальмон-Хамати, Флавия; Комб, Бернард; Хане, Майкл; Морель, Жак (2011). «Возвращение к лимфотоксину α: общие особенности и последствия при ревматоидном артрите» . Исследования и терапия артрита . 13 (4): 232. дои : 10.1186/ar3376 . ISSN 1478-6354 . ПМК 3239340 . ПМИД 21861866 .
- ^ Jump up to: а б с д и Раддл, Нью-Хэмпшир (апрель 2014 г.). «Лимфотоксин и ФНО: с чего все начиналось – дань памяти путешественникам» . Обзоры цитокинов и факторов роста . 25 (2): 83–9. doi : 10.1016/j.cytogfr.2014.02.001 . ПМК 4027955 . ПМИД 24636534 .
- ^ Jump up to: а б с Нго В.Н., Корнер Х., Ганн М.Д., Шмидт К.Н., Риминтон Д.С., Купер М.Д., Браунинг Дж.Л., Седжвик Дж.Д., Цистер Дж.Г. (январь 1999 г.). «Лимфотоксин альфа/бета и фактор некроза опухоли необходимы для экспрессии стромальных клеток самонаводящихся хемокинов в областях В- и Т-клеток селезенки» . Журнал экспериментальной медицины . 189 (2): 403–12. дои : 10.1084/jem.189.2.403 . ПМК 2192983 . ПМИД 9892622 .
- ^ Jump up to: а б с д Губернаторова Е.О., Туманов А.В. (ноябрь 2016 г.). «Фактор некроза опухоли и лимфотоксин в регуляции воспаления кишечника». Биохимия. Биохимия . 81 (11): 1309–1325. дои : 10.1134/S0006297916110092 . ПМИД 27914457 . S2CID 15764230 .
- ^ Jump up to: а б с д и ж г час я Бауэр Дж., Наминени С., Райзингер Ф., Золлер Дж., Юань Д., Хайкенвальдер М. (01.01.2012). «Лимфотоксин, NF-ĸB и рак: темная сторона цитокинов». Пищеварительные заболевания . 30 (5): 453–68. дои : 10.1159/000341690 . ПМИД 23108301 . S2CID 13165828 .
- ^ Jump up to: а б с д и ж Фернандес М.Т., Дежарден Э., душ Сантос Н.Р. (апрель 2016 г.). «Контекст-зависимая роль передачи сигналов рецептора лимфотоксина-β в развитии рака» . Biochimica et Biophysical Acta (BBA) - Обзоры о раке . 1865 (2): 204–19. дои : 10.1016/j.bbcan.2016.02.005 . hdl : 10400.1/9527 . ПМИД 26923876 .
- ^ Jump up to: а б Вонг Г.Х., Каспар Р.Л., Цвайгер Г., Карлсон С., Фонг С.Е., Эхсани Н., Вехар Г. (январь 1996 г.). «Стратегии управления апоптозом для терапии рака с помощью фактора некроза опухоли и лимфотоксина» . Журнал клеточной биохимии . 60 (1): 56–60. doi : 10.1002/(SICI)1097-4644(19960101)60:1<56::AID-JCB9>3.0.CO;2-2 . ПМИД 8825416 . S2CID 42014048 .
- ^ Похолок Д.К., Маруляков И.Г., Купраш Д.В., Алимжанов М.Б., Козлов С.В., Новобранцева Т.И., Турецкая Р.Л., Грин Ю.Е., Недоспасов С.А. (январь 1995 г.). «Клонирование и анализ экспрессии гена бета-лимфотоксина мыши» . Труды Национальной академии наук Соединенных Штатов Америки . 92 (3): 674–8. Бибкод : 1995PNAS...92..674P . дои : 10.1073/pnas.92.3.674 . ПМК 42682 . ПМИД 7846035 .
- ^ Недоспасов С.А., Хирт Б., Шахов А.Н., Добрынин В.Н., Кавашима Э., Акколла Р.С., Джонджинил К.В. (октябрь 1986 г.). «Гены фактора некроза опухоли (TNF-альфа) и лимфотоксина (TNF-бета) тандемно расположены на 17-й хромосоме мыши» . Исследования нуклеиновых кислот . 14 (19): 7713–25. дои : 10.1093/нар/14.19.7713 . ПМК 311791 . ПМИД 3490653 .
- ^ Пенника Д., Недвин Дж.Е., Хейфлик Дж.С., Сибург П.Х., Деринк Р., Палладино М.А., Кор В.Дж., Аггарвал Б.Б., Гёддел Д.В. (1984). «Фактор некроза опухоли человека: структура предшественника, экспрессия и гомология с лимфотоксином». Природа . 312 (5996): 724–9. Бибкод : 1984Natur.312..724P . дои : 10.1038/312724a0 . hdl : 21.11116/0000-0000-D4ED-6 . ПМИД 6392892 . S2CID 4245957 .
- ^ «Ген Энтреза: LTA-лимфотоксин альфа (суперсемейство TNF, член 1)» .
- ^ Акирав Э., Ляо С., Раддл Н. (2008). «Глава 2: Лимфоидные ткани и органы». В Поле В. (ред.). Фундаментальная иммунология (6-е изд.). Филадельфия: Липпинкотт Уильямс и Уилкинс. стр. 27–55 . ISBN 978-0-7817-6519-0 .
- ^ Корнеев К.В., Атретханы К.Н., Друцкая М.С., Гривенников С.И., Купраш Д.В., Недоспасов С.А. (январь 2017). «Передача сигналов TLR и провоспалительные цитокины как движущие силы онкогенеза». Цитокин . 89 : 127–135. дои : 10.1016/j.cyto.2016.01.021 . ПМИД 26854213 .
- ^ Jump up to: а б с Мюллер-младший, Siebenlist U (апрель 2003 г.). «Бета-рецептор лимфотоксина индуцирует последовательную активацию различных факторов NF-каппа B через отдельные сигнальные пути» . Журнал биологической химии . 278 (14): 12006–12. дои : 10.1074/jbc.M210768200 . ПМИД 12556537 .
- ^ Йилмаз З.Б., Вей Д.С., Сивакумар В., Вей Ф. (январь 2003 г.). «RelB необходим для развития пейеровой бляшки: дифференциальная регуляция p52-RelB лимфотоксином и TNF» . Журнал ЭМБО . 22 (1): 121–30. дои : 10.1093/emboj/cdg004 . ПМК 140043 . ПМИД 12505990 .
- ^ Jump up to: а б Браунинг Дж.Л., Миатковски К., Сайзинг I, Гриффитс Д., Зафари М., Бенджамин К.Д., Мейер В., Маккей Ф. (март 1996 г.). «Передача сигналов через бета-рецептор лимфотоксина вызывает гибель некоторых линий опухолей аденокарциномы» . Журнал экспериментальной медицины . 183 (3): 867–78. дои : 10.1084/jem.183.3.867 . ПМК 2192357 . ПМИД 8642291 .
- ^ Лукашев М., ЛеПейдж Д., Уилсон С., Байи В., Гарбер Е., Лукашин А. и др. (октябрь 2006 г.). «Нацеливание на рецептор бета-лимфотоксина с помощью антител-агонистов как потенциальная терапия рака» . Исследования рака . 66 (19): 9617–24. дои : 10.1158/0008-5472.CAN-06-0217 . ПМИД 17018619 .
- ^ Фу YX, Чаплин Д.Д. (1 января 1999 г.). «Развитие и созревание вторичных лимфоидных тканей». Ежегодный обзор иммунологии . 17 : 399–433. doi : 10.1146/annurev.immunol.17.1.399 . ПМИД 10358764 .
- ^ Рэндалл Т.Д., Каррагер Д.М., Рангел-Морено Дж. (1 января 2008 г.). «Развитие вторичных лимфоидных органов» . Ежегодный обзор иммунологии . 26 : 627–50. doi : 10.1146/annurev.immunol.26.021607.090257 . ПМК 2590644 . ПМИД 18370924 .
- ^ Корнес Дж.С. (июнь 1965 г.). «Количество, размер и распределение пейеровых бляшек в тонкой кишке человека: Часть I. Развитие пейеровых бляшек» . Гут . 6 (3): 225–9. дои : 10.1136/gut.6.3.225 . ПМЦ 1552287 . ПМИД 18668776 .
- ^ Крейг С.В., Себра Джей-Джей (июль 1971 г.). «Пластыри Пейера: обогащенный источник предшественников иммуноцитов, продуцирующих IgA, у кроликов» . Журнал экспериментальной медицины . 134 (1): 188–200. дои : 10.1084/jem.134.1.188 . ПМК 2139023 . ПМИД 4934147 .
- ^ Фэгэрашан С .; Хондзё Т. (январь 2003 г.). «Синтез кишечного IgA: регуляция передовых защитных сил организма». Обзоры природы. Иммунология . 3 (1): 63–72. дои : 10.1038/nri982 . ПМИД 12511876 . S2CID 2586305 .
- ^ Уильямс Т.В., Грейнджер Г.А. (сентябрь 1968 г.). «Цитотоксичность лимфоцитов in vitro: лимфотоксины нескольких видов млекопитающих» . Природа . 219 (5158): 1076–7. Бибкод : 1968Natur.219.1076W . дои : 10.1038/2191076a0 . ПМИД 5673378 . S2CID 4171855 .
- ^ Шалаби М.Р., Аггарвал Б.Б., Риндеркнехт Э., Сведерский Л.П., Финкл Б.С., Палладино М.А. (сентябрь 1985 г.). «Активация функций полиморфно-ядерных нейтрофилов человека гамма-интерфероном и факторами некроза опухоли» . Журнал иммунологии . 135 (3): 2069–73. doi : 10.4049/jimmunol.135.3.2069 . ПМИД 3926894 . S2CID 22218299 .
- ^ Браунинг Дж.Л., Нгам-ек А., Лоутон П., ДеМаринис Дж., Тизард Р., Чоу Э.П., Хессион С., О'Брин-Греко Б., Фоли С.Ф., Уэр К.Ф. (март 1993 г.). «Лимфотоксин бета, новый член семейства TNF, который образует гетеромерный комплекс с лимфотоксином на поверхности клетки». Клетка . 72 (6): 847–56. дои : 10.1016/0092-8674(93)90574-а . ПМИД 7916655 . S2CID 28961163 .
- ^ Кони П.А., Сакка Р., Лоутон П., Браунинг Дж.Л., Раддл Н.Х., Флавелл Р.А. (апрель 1997 г.). «Различная роль лимфотоксинов альфа и бета в лимфоидном органогенезе выявлена у мышей с дефицитом бета-лимфотоксина» . Иммунитет . 6 (4): 491–500. дои : 10.1016/s1074-7613(00)80292-7 . ПМИД 9133428 .
- ^ Уильямс-Эбботт Л., Уолтер Б.Н., Чунг Т.С., Гох С.Р., Портер А.Г., Ware CF (август 1997 г.). «Субъединица лимфотоксина-альфа (LTalpha) необходима для сборки, но не для специфичности рецептора, заякоренного в мембране гетеротримерного лиганда LTalpha1beta2» . Журнал биологической химии . 272 (31): 19451–6. дои : 10.1074/jbc.272.31.19451 . ПМИД 9235946 .
- ^ Браунинг Дж.Л., Сайзинг И.Д., Лоутон П., Бурдон П.Р., Реннерт П.Д., Мажо Г.Р., Амброуз К.М., Хессион С., Миатковски К., Гриффитс Д.А., Нгам-ек А., Мейер В., Бенджамин К.Д., Хохман П.С. (октябрь 1997 г.). «Характеристика комплексов лимфотоксин-альфа-бета на поверхности лимфоцитов мыши» . Журнал иммунологии . 159 (7): 3288–98. дои : 10.4049/jimmunol.159.7.3288 . ПМИД 9317127 . S2CID 25608697 .
- ^ Браунинг Дж.Л., Дугас И., Нгам-ек А., Бурдон П.Р., Эренфельс Б.Н., Миатковски К., Зафари М., Ямпалья А.М., Лоутон П., Мейер В. (январь 1995 г.). «Характеристика поверхностных форм лимфотоксина. Использование специфических моноклональных антител и растворимых рецепторов» . Журнал иммунологии . 154 (1): 33–46. дои : 10.4049/jimmunol.154.1.33 . ПМИД 7995952 . S2CID 22313274 .
Дальнейшее чтение
[ редактировать ]- Кернер Х., Седжвик Дж. Д. (октябрь 1996 г.). «Фактор некроза опухоли и лимфотоксин: молекулярные аспекты и роль в тканеспецифическом аутоиммунитете». Иммунология и клеточная биология . 74 (5): 465–72. дои : 10.1038/icb.1996.77 . ПМИД 8912010 . S2CID 22305752 .
- Ван Ц (май 2005 г.). «Молекулярная генетика ишемической болезни сердца» . Современное мнение в кардиологии . 20 (3): 182–8. дои : 10.1097/01.hco.0000160373.77190.f1 . ПМК 1579824 . ПМИД 15861005 .
- Коупленд К.Ф. (декабрь 2005 г.). «Модуляция транскрипции ВИЧ-1 цитокинами и хемокинами». Мини-обзоры по медицинской химии . 5 (12): 1093–101. дои : 10.2174/138955705774933383 . ПМИД 16375755 .
- Элеваут Д., Ware CF (апрель 2007 г.). «Нетрадиционная роль LT альфа-бета в дифференцировке Т-клеток». Тенденции в иммунологии . 28 (4): 169–75. дои : 10.1016/j.it.2007.02.005 . ПМИД 17336158 .