Стафилококк эпидермидис
| Стафилококк эпидермидис | |
|---|---|
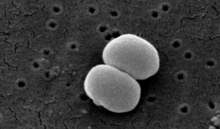 | |
| Сканирующее электронное изображение S. epidermidis . | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Бациллота |
| Сорт: | Бациллы |
| Заказ: | Бациллы |
| Семья: | Стафилококковые |
| Род: | стафилококк |
| Разновидность: | С. эпидермидис |
| Биномиальное имя | |
| Стафилококк эпидермидис (Уинслоу и Уинслоу, 1908 г.) Эванс 1916 год | |
| Синонимы | |
Стафилококк белый Розенбах 1884 г. | |
Staphylococcus epidermidis — грамположительная бактерия, одна из более чем 40 видов, принадлежащих к роду Staphylococcus . [1] Он является частью нормальной микробиоты человека , обычно микробиоты кожи и реже микробиоты слизистых оболочек, а также встречается в морских губках. [2] [3] Это факультативные анаэробные бактерии . Хотя S. epidermidis обычно не является патогенным , пациенты с ослабленной иммунной системой подвергаются риску развития инфекции. Эти инфекции обычно являются внутрибольничными . [4] S. epidermidis вызывает особую тревогу у людей с катетерами или другими хирургическими имплантатами, поскольку известно, что он образует биопленки , которые растут на этих устройствах. [5] Будучи частью нормальной микробиоты кожи, S. epidermidis часто контаминирует образцы, отправляемые в диагностическую лабораторию. [6]
Некоторые штаммы S. epidermidis обладают высокой солеустойчивостью и обычно встречаются в морской среде. [3] Если Пол и др. (2021) [3] выделили и идентифицировали солеустойчивые штаммы S. epidermidis (штаммы ISP111A , ISP111B и ISP111C ) из Cliona viridis губок в районе острова Сен-Мартен в Бенгальском заливе , Бангладеш .
Комменсальный S. epidermidis является важной частью здоровой микробиоты кожи . Он способствует поддержанию здорового кожного барьера, заживлению порезов кожи, защите микробиоты кожи от колонизации кожных патогенов и действует как модулятор иммунной системы. [7]

Этимология
[ редактировать ]«Стафилококк» — гроздь виноградоподобных ягод, «эпидермидис» — эпидермис. [8]
Открытие
[ редактировать ]Фридрих Юлиус Розенбах отличил S. epidermidis от S. aureus в 1884 году, первоначально назвав S. epidermidis S. albus . [9] Он выбрал aureus и albus , поскольку бактерии образовывали желтые и белые колонии соответственно.
Микробиология
[ редактировать ]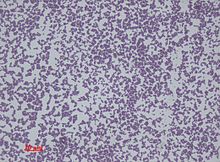
Staphylococcus epidermidis — очень выносливый микроорганизм, состоящий из неподвижных грамположительных кокков, собранных в гроздья, похожие на виноградные гроздья. После инкубации в течение ночи он образует белые, приподнятые, сплоченные колонии диаметром около 1–2 мм и не оказывает гемолитического действия на кровяном агаре. [5] Это каталаза -положительный, [10] коагулазонегативные , факультативные анаэробы , способные размножаться за счет аэробного дыхания или ферментации . Некоторые штаммы могут не ферментироваться. [3] [11]
Биохимические тесты показывают, что этот микроорганизм также дает слабоположительную реакцию на тест на нитратредуктазу . Он положителен для выработки уреазы , отрицателен по оксидазе и может использовать глюкозу, сахарозу и лактозу для образования кислых продуктов. В присутствии лактозы также будет выделяться газ. Непатогенный S. epidermidis, в отличие от патогенного S. aureus , не обладает ферментом желатиназой , поэтому не может гидролизовать желатин. [12] [13] Он чувствителен к новобиоцину , что позволяет отличить его от Staphylococcus saprophyticus , который также является коагулазонегативным, но устойчивым к новобиоцину. [4]
Как и у S. aureus , клеточные стенки S. epidermidis содержат белок, связывающий трансферрин, который помогает организму получать железо из трансферрина . Считается, что тетрамеры поверхностного белка, глицеральдегид-3-фосфатдегидрогеназы, связываются с трансферрином и удаляют из него железо. Последующие этапы включают перенос железа на поверхностные липопротеины, а затем на транспортные белки, которые переносят железо в клетку. [5]
Биохимические характеристики
[ редактировать ]Колония, морфологические, физиологические и биохимические характеристики морского S. epidermidis представлены в таблице ниже. [3]
| Тип теста | Тест | Характеристики |
| Персонажи колонии | Размер | С булавочной головкой/Очень маленький |
| Тип | Круглый | |
| Цвет | Непрозрачный | |
| Форма | Выпуклый | |
| Морфологические символы | Форма | Кокки |
| Физиологические признаки | Подвижность | – |
| Рост при 6,5% NaCl | + | |
| Биохимические признаки | Окраска по Граму | + |
| Оксидаза | – | |
| Каталаза | + | |
| Окислительно-ферментативный | Ферментативный | |
| Подвижность | – | |
| Метиловый красный | – | |
| Фогес-Проскауэр | + | |
| Индол | – | |
| H 2 Производство S | + | |
| Уреаза | + | |
| Нитратредуктаза | + | |
| β-галактозидаза | + | |
| Гидролиз | Желатин | – |
| Эскулин | + | |
| Казеин | + | |
| Твин 40 | + | |
| Твин 60 | + | |
| Твин 80 | + | |
| Производство кислоты из | Глицерин | – |
| Галактоза | В | |
| D-глюкоза | + | |
| D-фруктоза | + | |
| D-манноза | + | |
| Маннитол | – | |
| N-ацетилглюкозамин | + | |
| Амигдалин | + | |
| Мальтоза | + | |
| D-Мелибиоза | + | |
| D-трегалоза | + | |
| Гликоген | + | |
| D-Тураноза | + |
Примечание: + = положительный, – = отрицательный, W = слабо положительный.
Идентификация
[ редактировать ]Обычная практика обнаружения S. epidermidis заключается в использовании внешнего вида колоний на селективных средах, морфологии бактерий с помощью световой микроскопии, тестирования каталазы и слайд-коагулазы. Агар Зобелля полезен для выделения Staphylococcus epidermidis из морских организмов. [3] На агаре Бэрда-Паркера с яичного желтка добавкой такие методы, как количественная ПЦР все чаще используются колонии выглядят маленькими и черными. Для быстрого обнаружения и идентификации штаммов стафилококка . [14] [15] Обычно чувствительность к десферриоксамину также можно использовать, чтобы отличить его от большинства других стафилококков, за исключением случая Staphylococcus hominis , который также чувствителен. [16] продукцию кислоты из трегалозы S. hominis . В этом случае для различия этих двух видов можно использовать [ нужна ссылка ]
Микробная экология
[ редактировать ]Роль в запахе ног
[ редактировать ]Распространенное заблуждение о запахе ног и тела в целом заключается в том, что пот сам по себе пахнет и заставляет людей пахнуть. Однако сам пот практически не имеет запаха. Скорее, микробы , присутствующие на коже, метаболизируют определенные соединения с потом как источник питательных веществ, производя при этом соединения с неприятным запахом. [17] S. epidermidis процветает в теплой и влажной среде и является распространенной бактерией микробиома человека ; [18] таким образом, он в первую очередь ответственен за запах ног, поскольку на ногах больше потовых желез, чем на любой другой части тела, и поэтому они часто влажные, что создает идеальную среду для процветания S. epidermidis. Бактерии производят ферменты , которые расщепляют лейцин, присутствующий в поту, образуя летучие соединения с неприятным запахом, такие как изовалериановая кислота. Ноги с более сильным запахом имеют более высокую плотность микроорганизмов, чем ноги с более слабым запахом. [18]
Роль в болезни
[ редактировать ]Факторы вирулентности
[ редактировать ]
Образование биопленки
[ редактировать ]S. epidermidis вызывает рост биопленок на пластиковых устройствах, помещенных в тело. [19] Чаще всего это происходит на внутривенных катетерах и медицинских протезах . [20] Инфекция также может возникнуть у пациентов, находящихся на диализе, или у людей с имплантированными пластиковыми устройствами, которые могли быть загрязнены. Он также вызывает эндокардит , чаще всего у пациентов с дефектами сердечных клапанов. В некоторых других случаях сепсис может возникнуть и у стационарных пациентов. [ нужна ссылка ]
Способность образовывать биопленки на пластиковых изделиях является основным фактором вирулентности S. epidermidis . Одной из вероятных причин являются поверхностные белки, которые связывают белки крови и внеклеточного матрикса. Он производит внеклеточный материал, известный как полисахаридный межклеточный адгезин (PIA), который состоит из сульфатированных полисахаридов . Это позволяет другим бактериям связываться с уже существующей биопленкой, создавая многослойную биопленку. Такие биопленки снижают метаболическую активность находящихся в них бактерий. Это снижение метаболизма в сочетании с нарушением диффузии антибиотиков затрудняет эффективное лечение антибиотиками этого типа инфекции. [5]
Антибиотики в значительной степени неэффективны для очистки биопленок. Наиболее распространенным методом лечения этих инфекций является удаление или замена инфицированного имплантата, хотя во всех случаях профилактика идеальна. Препаратом выбора часто является ванкомицин , к которому рифампицин или аминогликозид . можно добавить [ нужна ссылка ] Доказано, что мытье рук снижает распространение инфекции.
Устойчивость к антибиотикам
[ редактировать ]Штаммы S. epidermidis часто устойчивы к антибиотикам , включая рифамицин , фторхинолоны , гентамицин , тетрациклин , клиндамицин и сульфаниламиды . [19] Резистентность к метициллину особенно широко распространена: 75–90% больничных изолятов устойчивы к метициллину. [19] Устойчивые организмы чаще всего обнаруживаются в кишечнике, но организмы, живущие на коже, также могут стать устойчивыми из-за регулярного воздействия антибиотиков, выделяемых с потом. [ нужна ссылка ]
Обыкновенные угри
[ редактировать ]Предварительные исследования также показывают, что S. epidermidis повсеместно встречается в пораженных порах обыкновенных угрей , где Cutibacterium Acnes обычно является единственным обитателем. [21]
Staphylococcus epidermidis в нормальной коже непатогенен. Но при аномальных поражениях он становится патогенным, например, при обыкновенных угрях . Staphylococcus epidermidis проникает в сальную железу (колонизированную Propionibacterium Acnes , основной бактерией, вызывающей обыкновенные угри) и повреждает волосяные фолликулы, вырабатывая липолитические ферменты, которые изменяют кожное сало из фракционной формы в плотную (густую), что приводит к воспалительному эффекту. [22]
Более того, образование биопленки S. epidermidis путем высвобождения экзополисахаридной межклеточной адгезии (PIA) обеспечивает восприимчивую анаэробную среду для колонизации P.acnes и защищает ее от молекул врожденного иммунитета человека. [23]
И P.acnes , и S.epidermidis могут взаимодействовать друг с другом, защищая здоровье кожи хозяина от колонизации патогенов. Но в случае конкуренции они используют один и тот же источник углерода (например, глицерин) для производства короткоцепочечных жирных кислот, которые действуют друг против друга как антибактериальное средство. Кроме того, S. epidermidis помогает поддерживать гомеостаз кожи и уменьшает патогенное воспаление, вызванное P.acnes, за счет уменьшения выработки белка TLR2 , который вызывает воспаление кожи. [24]
Роль в здоровье кожи
[ редактировать ]Укрепление кожного барьера
[ редактировать ]Также было показано, что комменсальный S. epidermidis способствует гомеостазу кожного барьера за счет выработки защитных церамидов, которые помогают поддерживать целостность кожного барьера. Модулируя влажную внутреннюю оболочку некоторых органов и полостей тела и их специфические механизмы иммунной защиты, кожные комменсалы взаимодействуют с инфекционными агентами, такими как патогены. Сфингомиелин-фосфодиэстераза является основным фактором выработки epidermidis S. церамидов — липидов, включающих сфингозин и сфингозин-1-фосфат . Этот липид одновременно получает питательные вещества, необходимые для бактерий, и помогает хозяину в производстве церамидов. Керамиды являются важными компонентами эпителиального барьера и играют ключевую роль в предотвращении потери кожей влаги; он действует как защитное средство и предотвращает обезвоживание и старение кожи. [25]
Метаболическое взаимодействие
[ редактировать ]S. epidermidis играет ключевую роль в метаболических процессах, влияющих на состояние кожи. Бактерия может влиять на биохимические пути внутри клеток кожи, что может влиять на здоровье кожи и болезненные состояния. В частности, это проявляется в модуляции арильного углеводородного рецептора . [7]
В неатопической коже S. epidermidis помогает активировать путь рецептора ариловых углеводородов, что одновременно усиливает барьерную функцию кожи и помогает уменьшить воспаление. Атопическая кожа обычно имеет обратный эффект, действуя как блокатор этого пути и, возможно, усугубляя проблемы с кожей. [7]
Иммунный ответ
[ редактировать ]Комменсальный S. epidermidis также влияет на иммунный ответ кожи. Благодаря взаимодействию с иммунными клетками хозяина усиливается иммунная защита слизистой оболочки кожи против различных патогенов. Комменсалы кожи будут непосредственно мешать вредным патогенам. [25]
В случае S. aureus S. epidermidis может усиливать врожденный иммунный ответ, вызывая реакцию кератиноцитов на этот патоген. [7]
S. epidermidis продуцирует такие молекулы, как липотейхоевая кислота (LTA), полисахариды клеточной стенки, пептидогликан и альдегиддипептиды, которые распознаются толл-подобными рецепторами (TLR) как молекулы, модулирующие иммунный ответ. Эти иммуномодулирующие молекулы создают связь между бактериями и кератиноцитами и оказывают значительное влияние на модуляцию врожденного иммунного ответа, главным образом, благодаря их взаимодействию с TLR. [7]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Шлейфер К.Х., Клоос В.Е. (январь 1975 г.). «Выделение и характеристика стафилококков из кожи человека I. Исправленные описания Staphylococcus epidermidis и Staphylococcus saprophyticus и описания трех новых видов: Staphylococcus cohnii, Staphylococcus haemolyticus и Staphylococcus xylosus» . Международный журнал систематической бактериологии . 25 (1): 50–61. дои : 10.1099/00207713-25-1-50 .
- ^ Фей П.Д., Олсон М.Э. (июнь 2010 г.). «Современные концепции формирования биопленок Staphylococcus epidermidis» . Будущая микробиология . 5 (6): 917–933. дои : 10.2217/fmb.10.56 . ПМК 2903046 . ПМИД 20521936 .
- ^ Перейти обратно: а б с д и ж Пол С.И., Рахман М.М., Салам М.А., Хан М.А., Ислам М.Т. (15 декабря 2021 г.). «Идентификация бактерий, связанных с морскими губками, на острове Сен-Мартен в Бенгальском заливе с акцентом на профилактику подвижной септицемии Aeromonas у Labeo rohita» . Аквакультура . 545 : 737156. doi : 10.1016/j.aquacultural.2021.737156 . ISSN 0044-8486 .
- ^ Перейти обратно: а б Левинсон В. (2010). Обзор медицинской микробиологии и иммунологии (11-е изд.). стр. 94–99.
- ^ Перейти обратно: а б с д Сальерс А.А., Уитт Д.Д. (2002). Бактериальный патогенез: молекулярный подход (2-е изд.). Вашингтон, округ Колумбия: ASM Press. ISBN 978-1-55581-171-6 .
- ^ Квик С.Ю., Отто М. (2008). «Staphylococcus epidermidis и другие коагулазонегативные стафилококки» . Стафилококк: молекулярная генетика . Кайстер Академик Пресс. ISBN 978-1-904455-29-5 .
- ^ Перейти обратно: а б с д и Ландемейн Л., Да Коста Г., Фиссье Э., Фрэнсис С., Моран С., Вербеке Дж. и др. (2023). « Изоляты Staphylococcus epidermidis из атопической или здоровой кожи оказывают противоположное воздействие на клетки кожи: потенциальное значение модуляции пути AHR» . Границы в иммунологии . 14 : 1098160. дои : 10.3389/fimmu.2023.1098160 . ПМЦ 10250813 . ПМИД 37304256 .
- ^ « Эпидермидный стафилококк » . ВетБакт .
- ^ Фридрих Юлиус Розенбах в книге «Кто это назвал?»
- ^ «Онлайн-учебник бактериологии Тодара: золотистый стафилококк и стафилококковая болезнь» . Кеннет Тодар, доктор философии . Проверено 7 декабря 2013 г.
- ^ «Геномы бактерий – Staphylococcus epidermidis» . Геномы Карин . ЭМБЛ-ЭБИ. Архивировано из оригинала 4 марта 2010 года . Проверено 23 декабря 2011 г.
- ^ Дела Круз Т.Э., Торрес Дж.М. (ноябрь 2012 г.). «Протокол испытаний на гидролиз желатина» . Американское общество микробиологии . Проверено 1 января 2021 г.
- ^ Чаби Р., Момтаз Х (05.12.2019). «Факторы вирулентности и свойства устойчивости к антибиотикам штаммов Staphylococcus epidermidis , выделенных от госпитальных инфекций в Ахвазе, Иран» . Тропическая медицина и здоровье . 47 (1): 56. дои : 10.1186/s41182-019-0180-7 . ПМК 6896349 . ПМИД 31844416 .
- ^ Франсуа П., Шренцель Дж. (2008). «Экспресс-диагностика и типирование золотистого стафилококка» . Стафилококк: молекулярная генетика . Кайстер Академик Пресс. ISBN 978-1-904455-29-5 .
- ^ Маккей ИМ, изд. (2007). ПЦР в реальном времени в микробиологии: от диагностики к характеристике . Кайстер Академик Пресс. ISBN 978-1-904455-18-9 .
- ^ Антунес А.Л., Секки С., Рейтер К.К., Перес Л.Р., де Фрейтас А.Л., Д'Азеведо П.А. (январь 2008 г.). «Возможная идентификация Staphylococcus epidermidis с использованием дисков десферриоксамина и фосфомицина». АПМИС . 116 (1): 16–20. дои : 10.1111/j.1600-0463.2008.00796.x . ПМИД 18254775 . S2CID 205804740 .
- ^ «Запах тела: причины, изменения, основные заболевания и лечение» . Кливлендская клиника . Проверено 11 мая 2023 г.
- ^ Перейти обратно: а б Ара К., Хама М., Акиба С., Койке К., Окисака К., Хагура Т. и др. (апрель 2006 г.). «Запах ног из-за микробного метаболизма и его контроля». Канадский журнал микробиологии . 52 (4): 357–364. дои : 10.1139/w05-130 . ПМИД 16699586 .
- ^ Перейти обратно: а б с Отто М (август 2009 г.). «Staphylococcus epidermidis — «случайный» патоген» . Обзоры природы. Микробиология . 7 (8): 555–567. дои : 10.1038/nrmicro2182 . ПМК 2807625 . ПМИД 19609257 .
- ^ Хедин Г (1993). «Staphylococcus epidermidis - больничная эпидемиология и выявление резистентности к метициллину». Скандинавский журнал инфекционных заболеваний. Дополнение . 90 : 1–59. ПМИД 8303217 .
- ^ Бек-Томсен М., Ломхольт Х.Б., Килиан М. (октябрь 2008 г.). «Угри не связаны с еще некультивированными бактериями» . Журнал клинической микробиологии . 46 (10): 3355–3360. дои : 10.1128/JCM.00799-08 . ПМК 2566126 . ПМИД 18716234 .
- ^ Мустаричи Р., Сулитянингсих С., Рунади Д. (29 января 2020 г.). «Испытание антибактериальной активности экстрактов и фракций листьев маниоки ( Manihot esculenta Crantz) против клинических изолятов Staphylococcus epidermidis и Propionibacteriumacnes, вызывающих прыщи» . Международный журнал микробиологии . 2020 : 1975904. дои : 10.1155/2020/1975904 . ПМК 7008253 . ПМИД 32089694 .
- ^ Кумар Б., Патхак Р., Мэри П.Б., Джа Д., Сардана К., Гаутам Х.К. (1 июня 2016 г.). «Новый взгляд на патогенез прыщей: изучение роли микробных популяций, связанных с прыщами» . Дерматологическая Синика . 34 (2): 67–73. дои : 10.1016/j.dsi.2015.12.004 .
- ^ Клодель Ж.П., Ауффрет Н., Лечча М.Т., Поли Ф., Корвек С., Дрено Б. (2019). «Staphylococcus epidermidis: потенциальный новый игрок в физиопатологии прыщей?» . Дерматология . 235 (4): 287–294. дои : 10.1159/000499858 . ПМИД 31112983 . S2CID 162170301 .
- ^ Перейти обратно: а б Чжэн Ю., Хант Р.Л., Вилларуз А.Е., Фишер Э.Л., Лю Р., Лю К. и др. (март 2022 г.). «Комменсальный Staphylococcus epidermidis способствует гомеостазу кожного барьера, вырабатывая защитные церамиды» . Клетка-хозяин и микроб . 30 (3): 301–313.е9. дои : 10.1016/j.chom.2022.01.004 . ПМЦ 8917079 . ПМИД 35123653 .
Дальнейшее чтение
[ редактировать ]- Баррос Дж., Гренхо Л., Мануэль С.М., Феррейра С., Мело Л., Нуньес О.К. и др. (май 2014 г.). «Влияние свойств поверхности наногидроксиапатита на образование биопленки Staphylococcus epidermidis». Журнал применения биоматериалов . 28 (9): 1325–1335. дои : 10.1177/0885328213507300 . hdl : 10216/103571 . ПМИД 24122400 . S2CID 37361193 .
- Донг Й., Глейзер К., Шлегель Н., Клаус Х., Шпеер К.П. (ноябрь 2019 г.). «Недооцененный патоген: Staphylococcus epidermidis вызывает провоспалительные реакции в альвеолярных эпителиальных клетках человека». Цитокин . 123 : 154761. doi : 10.1016/j.cyto.2019.154761 . ПМИД 31226437 . S2CID 195260717 .
- Фэн Дж., Ченг Ю., Воробо Р.В., Борка-Тащук Д.А., Морару К.И. (октябрь 2019 г.). «Нанопористый анодный оксид алюминия снижает образование биопленки стафилококка» . Письма по прикладной микробиологии . 69 (4): 246–251. дои : 10.1111/lam.13201 . ПМИД 31357240 .
- Гилл С.Р., Фаутс Д.Е., Арчер Г.Л., Монгодин Э.Ф., Дебой Р.Т., Равель Дж. и др. (апрель 2005 г.). «Понятия об эволюции вирулентности и устойчивости на основе полного анализа генома раннего метициллин-резистентного штамма Staphylococcus aureus и продуцирующего биопленку метициллин-резистентного штамма Staphylococcus epidermidis» . Журнал бактериологии . 187 (7): 2426–2438. дои : 10.1128/JB.187.7.2426-2438.2005 . ПМЦ 1065214 . ПМИД 15774886 .
- Гетц Ф. (март 2002 г.). «Стафилококк и биопленки». Молекулярная микробиология . 43 (6): 1367–1378. дои : 10.1046/j.1365-2958.2002.02827.x . ПМИД 11952892 . S2CID 10516046 .
- Хайдамак Дж., Давила Дос Сантос Дж., Лима Б.Дж., Соарес В.М., де Менезес Р.В., Биссон А.А. и др. (сентябрь 2019 г.). «Изменения микробиоты кожи головы у детей с педикулезом» . Инфекция, генетика и эволюция . 73 : 322–331. дои : 10.1016/j.meegid.2019.05.016 . ПМИД 31121305 .
- Изано Э.А., Амаранте М.А., Кхер В.Б., Каплан Дж.Б. (январь 2008 г.). «Дифференциальная роль поверхностного полисахарида поли-N-ацетилглюкозамина и внеклеточной ДНК в биопленках Staphylococcus aureus и Staphylococcus epidermidis» . Прикладная и экологическая микробиология . 74 (2): 470–476. Бибкод : 2008ApEnM..74..470I . дои : 10.1128/АЕМ.02073-07 . ПМЦ 2223269 . ПМИД 18039822 .
- Мерик Дж., Мирагайя М., де Бин М., Яхара К., Паско Б., Магейрос Л. и др. (апрель 2015 г.). «Экологическое перекрытие и горизонтальный перенос генов у Staphylococcus aureus и Staphylococcus epidermidis» . Геномная биология и эволюция . 7 (5): 1313–1328. дои : 10.1093/gbe/evv066 . ПМЦ 4453061 . ПМИД 25888688 .
- Накацудзи Т., Чен Т.Х., Батчер А.М., Трзосс Л.Л., Нам С.Дж., Сиракава К.Т. и др. (февраль 2018 г.). «Комменсальный штамм Staphylococcus epidermidis защищает от неоплазии кожи» . Достижения науки . 4 (2): eaao4502. Бибкод : 2018SciA....4.4502N . дои : 10.1126/sciadv.aao4502 . ПМК 5834004 . ПМИД 29507878 .
- Отто М (август 2009 г.). «Staphylococcus epidermidis — «случайный» патоген» . Обзоры природы. Микробиология . 7 (8): 555–567. дои : 10.1038/nrmicro2182 . ПМК 2807625 . ПМИД 19609257 .
- Цинь З, Оу Ю, Ян Л, Чжу Ю, Толкер-Нильсен Т, Молин С и др. (июль 2007 г.). «Роль опосредованного аутолизином высвобождения ДНК в формировании биопленок Staphylococcus epidermidis» . Микробиология . 153 (Часть 7): 2083–2092. дои : 10.1099/mic.0.2007/006031-0 . ПМИД 17600053 .
- Шеффер CR, Хоанг Т.Н., Судбек CM, Алави М., Толо И.Е., Робинсон Д.А. и др. (5 октября 2016 г.). «Универсальность молекул матрикса биопленки в клинических изолятах Staphylococcus epidermidis и важность экспрессии полисахаридного межклеточного адгезина во время высокого напряжения сдвига» . мСфера . 1 (5). дои : 10.1128/mSphere.00165-16 . ПМК 5064449 . ПМИД 27747298 .
- Шахруи М., Хира В., Ходапараст Л., Ходапараст Л., Стийлеманс Б., Кучарикова С. и др. (октябрь 2012 г.). «Вакцинация SesC снижает образование биопленки Staphylococcus epidermidis» . Инфекция и иммунитет . 80 (10): 3660–3668. дои : 10.1128/IAI.00104-12 . ПМЦ 3457580 . ПМИД 22802343 .