Стрептококк мутанс
| Стрептококк мутанс | |
|---|---|
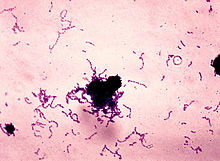 | |
| Окраска S. mutans в культуре тиогликолятного бульона . | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Бациллота |
| Сорт: | Бациллы |
| Заказ: | лактобактерии |
| Семья: | Стрептококковые |
| Род: | Стрептококк |
| Разновидность: | С. mutans |
| Биномиальное имя | |
| Стрептококк мутанс Кларк 1924 г. | |
Streptococcus mutans — факультативно анаэробный грамположительный ) , кокк (круглая бактерия обычно встречающийся в человека ротовой полости и вносящий значительный вклад в развитие кариеса . [1] [2] Это часть « стрептококков », неофициального общего названия всех видов рода Streptococcus . Микроб был впервые описан Джеймсом Килианом Кларком в 1924 году. [3]
Эта бактерия, наряду с близкородственным видом Streptococcus sobrinus , может сосуществовать во рту: обе способствуют заболеваниям полости рта, и затраты на их дифференциацию в лабораторных исследованиях часто не являются клинически необходимыми. Поэтому в клинических целях их часто рассматривают вместе как группу, называемую стрептококками mutans . [4] Эту группу сходных бактерий со схожим тропизмом можно также увидеть у стрептококков viridans , другой группы видов Streptococcus .
Экология
[ редактировать ]S. mutans естественным образом присутствует в микробиоте полости рта человека наряду с по меньшей мере 25 другими видами стрептококков полости рта. Таксономия . этих бактерий остается предварительной [5] Различные области ротовой полости представляют собой разные экологические ниши, и каждый вид обладает специфическими свойствами для колонизации различных участков полости рта. S. mutans наиболее распространен на ямках и трещинах , составляя 39% от общего количества стрептококков в полости рта. Меньше бактерий S. mutans обнаружено на буккальной поверхности (2–9%). [6]
Совместная бактериально-грибковая коагрегация может способствовать увеличению кариесогенного потенциала S. mutans . Симбиотические отношения с S. mutans и Candida albicans приводят к увеличению выработки глюканов и усилению образования биопленок. Таким образом, это усиливает кариесогенный эффект S. mutans . [7]
Стрептококки полости рта включают как безвредные, так и вредные бактерии. Однако в особых условиях комменсальные стрептококки могут стать условно-патогенными микроорганизмами, инициируя заболевание и повреждая хозяина. Дисбаланс микробной биоты может инициировать заболевания полости рта. [ нужна ссылка ]
C. albicans — условно-патогенные дрожжи, которые можно обнаружить в полости рта. [8] Его присутствие в биопленке способствует повышению уровня S. mutans при изучении раннего детского кариеса . [8] Стимулирует образование микроколоний S. mutans . [8] Это достигается за счет низких концентраций перекрестных метаболитов, таких как фарнезол , полученных из биопленки . [8] Было высказано предположение, что когда присутствуют оба микроба, образуется больше матрицы биопленки с большей плотностью. [8] Когда фарнезол находится в высокой концентрации, он подавляет рост как S. mutans , так и C. albicans . [8] Это уменьшает патогенез биопленки и, следовательно, ее кариеса . потенциал, способствующий развитию [8] Это дает возможность использовать противогрибковые средства для профилактики кариеса . [8]
Роль в болезни
[ редактировать ]Кариес
[ редактировать ]Ранними колонизаторами поверхности зубов являются в основном Neisseria spp. и стрептококки , включая S. mutans . Они должны выдерживать очищающие силы полости рта (например, слюну и движения языка) и в достаточной степени прилегать к твердым тканям зубов. Рост и метаболизм этих видов-пионеров меняют местные условия окружающей среды (например, Eh, pH, коагрегацию и доступность субстрата), тем самым позволяя более прихотливым организмам продолжать колонизировать их, образуя зубной налет . [9] Наряду с S. sobrinus , S. mutans играет важную роль в разрушении зубов, метаболизируя сахарозу до молочной кислоты . [2] [10] Кислая среда , создаваемая во рту в результате этого процесса, делает высокоминерализованную зубную эмаль уязвимой для разрушения. S. mutans — один из немногих специализированных организмов, оснащенных рецепторами, улучшающими адгезию к поверхности зубов. S. mutans использует фермент глюкансахаразу для превращения сахарозы в липкий внеклеточный декстрана на основе полисахарид , который позволяет им слипаться , образуя бляшки. S. mutans производит декстран с помощью фермента декстрансукразы ( гексозилтрансферазы ) с использованием сахарозы в качестве субстрата в следующей реакции:
- н сахароза → (глюкоза) н + н фруктоза
Сахароза — единственный сахар, который бактерии могут использовать для образования липкого полисахарида. [1]
Однако другие сахара — глюкоза , фруктоза , лактоза — также могут перевариваться S. mutans , но они производят молочную кислоту в качестве конечного продукта . Сочетание зубного налета и кислоты приводит к разрушению зубов. [11] Из-за роли S. mutans в развитии кариеса было предпринято множество попыток создать вакцину против этого организма. До сих пор такие вакцины не принесли успеха на людях. [12] Недавно было показано, что белки, участвующие в колонизации зубов S. mutans, продуцируют антитела, ингибирующие кариесогенный процесс. [13] Предполагается , что молекула Keep 32 , недавно синтезированная в Йельском университете и Университете Чили, способна убивать S. mutans . Другим кандидатом является пептид под названием C16G2, синтезированный в Калифорнийском университете в Лос-Анджелесе. [ нужна ссылка ]
Считается, что Streptococcus mutans приобрел ген, который позволяет ему производить биопленки посредством горизонтального переноса генов с другими видами молочнокислых бактерий, такими как Lactobacillus . [14]
Жизнь в полости рта
[ редактировать ]Выживая в полости рта, S. mutans является основным возбудителем и патогенным видом, ответственным за кариес зубов (кариес или кариес), особенно на стадиях зарождения и развития. [15] [16]
Зубной налет , который обычно является предшественником кариеса, содержит более 600 различных микроорганизмов, вносящих вклад в общую динамическую среду полости рта, которая часто претерпевает быстрые изменения pH, доступности питательных веществ и напряжения кислорода. Зубной налет прилипает к зубам и состоит из бактериальных клеток, а налет представляет собой биопленку на поверхности зубов. Зубной налет и S. mutans часто подвергаются воздействию «токсичных соединений» продуктов ухода за полостью рта, пищевых добавок и табака. [ нужна ссылка ]
Пока S. mutans растет в биопленке, клетки поддерживают баланс метаболизма, включающий выработку и детоксикацию. Биопленка – это совокупность микроорганизмов, клетки которой прилипают друг к другу или к поверхности. Бактерии в сообществе биопленок могут фактически генерировать различные токсичные соединения, которые мешают росту других конкурирующих бактерий. [ нужна ссылка ]
S. mutans со временем разработала стратегии успешной колонизации и поддержания доминирующего присутствия в полости рта. Биопленка полости рта постоянно подвергается воздействию изменений условий окружающей среды. В ответ на такие изменения бактериальное сообщество эволюционировало с отдельными членами и их специфическими функциями, необходимыми для выживания в полости рта. S. mutans смог эволюционировать от условий, ограничивающих питание, и защитить себя в экстремальных условиях. [17] Стрептококки составляют 20% бактерий полости рта и фактически определяют развитие биопленок. Хотя S. mutans могут противостоять колонизаторам-первопроходцам, как только они станут доминировать в биопленках полости рта, может развиться и процветать кариес зубов. [17]
Кариесогенный потенциал
[ редактировать ]Возбудитель кариеса зубов связан с его способностью метаболизировать различные сахара, образовывать прочную биопленку, производить обильное количество молочной кислоты и процветать в создаваемой им кислой среде. [18] Исследование pH зубного налета показало, что критический pH для повышенной деминерализации твердых тканей зубов (эмали и дентина) составляет 5,5. Кривая Стефана показывает, как быстро pH зубного налета может упасть ниже 5,5 после перекуса или еды. [19]
Кариес зубов — это заболевание полости рта, связанное с образованием зубной биопленки, связанное с повышенным потреблением диетического сахара и ферментируемых углеводов. Когда зубные биопленки остаются на поверхности зубов, а также при частом воздействии сахаров, ацидогенные бактерии (члены зубных биопленок) будут метаболизировать сахара до органических кислот. Невылеченный кариес зубов является наиболее распространенным заболеванием, поражающим людей во всем мире. [20] . Сохранение этой кислой среды способствует размножению ацидогенных и ацидурических бактерий вследствие их способности выживать в среде с низким pH. Среда с низким pH в матриксе биопленки разрушает поверхность зубов и начинает «начинать» кариес. [18] Streptococcus mutans — бактерия, широко распространенная в среде полости рта. [21] и считается жизненно важным микроорганизмом, который способствует этому инициированию. [22] S. mutans процветает в кислых условиях, становясь основной бактерией в культурах с постоянно пониженным pH. [23] . Если прилипание S. mutans к поверхности зубов или физиологическую способность (кислотность и кислотность) S. mutans в зубных биопленках можно уменьшить или устранить, потенциал подкисления зубных биопленок и последующих кариесных образований может быть снижен. [18]
В идеале мы можем остановить раннее развитие различных поражений после стадии белого пятна. Попав сюда, поверхность эмали необратимо повреждается и не подлежит биологическому восстановлению. [24] У маленьких детей боль от кариозного поражения может быть весьма мучительной, а восстановительное лечение может вызвать раннюю тревогу у стоматолога. [25] Стоматологическая тревога имеет побочные эффекты как для стоматологов, так и для пациентов. Планирование лечения и, следовательно, успех лечения могут быть поставлены под угрозу. Стоматологический персонал может испытывать стресс и разочарование, работая с тревожными детьми. Это может поставить под угрозу их отношения с ребенком и его родителями. [26] Исследования показали, что существует цикл, в результате которого пациенты, беспокоящиеся о зубах, избегают заботы о здоровье тканей полости рта. Иногда они могут избегать гигиены полости рта и стараются избегать обращения за стоматологической помощью до тех пор, пока боль не станет невыносимой. [27]
Восприимчивость к заболеванию варьируется у разных людей, и были предложены иммунологические механизмы, обеспечивающие защиту или восприимчивость к заболеванию. Эти механизмы еще полностью не выяснены, но кажется, что, хотя антигенпредставляющие клетки активируются S. mutans in vitro , они не реагируют in vivo . Иммунологическая толерантность к S. mutans на поверхности слизистой оболочки может сделать людей более склонными к колонизации S. mutans и, следовательно, повысить восприимчивость к кариесу зубов. [28]
У детей
[ редактировать ]S. mutans часто приобретается в полости рта после прорезывания зубов, но также обнаруживается в полости рта у предзубных детей. Обычно, но не исключительно, он передается вертикальным путем от лица, осуществляющего уход (обычно матери), к ребенку. Это также часто может произойти, когда родитель прикладывает губы к бутылочке ребенка, чтобы попробовать ее на вкус, или чтобы почистить соску ребенка, а затем кладет ее в рот ребенка. [29] [30]
Сердечно-сосудистые заболевания
[ редактировать ]S. mutans участвует в патогенезе некоторых сердечно-сосудистых заболеваний и является наиболее распространенным видом бактерий, обнаруживаемым в удаленных тканях сердечного клапана, а также в атероматозных бляшках, с частотой 68,6% и 74,1% соответственно. [31] Было показано, что Streptococcus sanguinis , тесно связанный с S. mutans и также обнаруживаемый в полости рта, вызывает инфекционный эндокардит. [32]
Streptococcus mutans ассоциирован с бактериемией и инфекционным эндокардитом (ИЭ). ИЭ разделяют на острую и подострую формы, причем бактерию выделяют в подострых случаях. Общие симптомы: лихорадка, озноб, потливость, анорексия, потеря веса и недомогание. [33]
S. mutans разделен на четыре серотипа; в, е, е и к. Классификация серотипов основана на химическом составе серотип-специфичных полимеров рамнозы-глюкозы. Например, серотип k, первоначально обнаруженный в изолятах крови, имеет значительное сокращение боковых цепей глюкозы, прикрепленных к рамнозному остову. S. mutans имеет следующие поверхностные белковые антигены: глюкозилтрансферазы, белковый антиген и глюкансвязывающие белки. Если эти поверхностные белковые антигены отсутствуют, то бактерия представляет собой мутант с дефектом белкового антигена и наименьшую восприимчивость к фагоцитозу, поэтому наносит наименьший вред клеткам. [ нужна ссылка ]
Кроме того, эксперименты на крысах показали, что заражение такими дефектными стрептококка мутантами (штаммы S. mutans без глюкозилтрансфераз, выделенные из разрушенного сердечного клапана больного инфекционным эндокардитом) приводило к более длительной бактериемии. Результаты показывают, что вирулентность инфекционного эндокардита, вызванного S. mutans, связана со специфическими компонентами клеточной поверхности.
Кроме того, ДНК S. mutans была обнаружена в образцах сердечно-сосудистой системы в более высоком соотношении, чем ДНК других пародонтальных бактерий. Это подчеркивает его возможное участие в различных типах сердечно-сосудистых заболеваний, не ограничивающихся только бактериемией и инфекционным эндокардитом. [34]
Профилактика и лечение
[ редактировать ]Практика хорошей гигиены полости рта, включая ежедневную чистку зубов щеткой, зубной нитью и использование подходящих ополаскивателей для рта, может значительно снизить количество бактерий полости рта, включая S. mutans , и подавить их размножение. S. mutans часто обитают в зубном налете , поэтому эффективным способом избавления от него является механическое удаление налета. [35] Лучшим методом чистки зубов, позволяющим уменьшить образование зубного налета и снизить риск кариеса, является модифицированная техника Басса . Чистка зубов два раза в день может помочь снизить риск кариеса. [36] Однако есть некоторые средства, используемые при лечении бактериальных инфекций полости рта в сочетании с механической чисткой. К ним относятся фторид , который оказывает прямое ингибирующее действие на фермент енолазу , а также хлоргексидин , который действует, предположительно, препятствуя бактериальной адгезии.
Кроме того, ионы фтора могут оказывать вредное воздействие на метаболизм бактериальных клеток. Фторид напрямую ингибирует гликолитические ферменты и H+АТФазы. Ионы фтора также снижают pH цитоплазмы. Это означает, что во время бактериального гликолиза будет вырабатываться меньше кислоты. [37] Таким образом, фторсодержащие жидкости для полоскания рта, зубные пасты, гели и лаки могут помочь снизить распространенность кариеса. [38] Однако результаты исследований влияния фторсодержащего лака на уровень Streptococcus mutans в среде полости рта у детей позволяют предположить, что уменьшение кариеса не может быть объяснено снижением уровня Streptococcus mutans в слюне или зубных отложениях. [39] Обработка фтористым лаком с предварительной гигиеной полости рта или без нее не оказывает существенного влияния на уровень зубного налета и слюны, вызванной S. mutans . [40]
S. mutans секретирует глюкозилтрансферазу на своей клеточной стенке, которая позволяет бактериям производить полисахариды из сахарозы. Эти липкие полисахариды отвечают за способность бактерий агрегировать друг с другом и прикрепляться к зубной эмали, то есть образовывать биопленки . Использование иммуноглобулина Y против клеточно-ассоциированной глюкозилтрансферазы (Anti-CA-gtf) нарушает способность S. mutans прикрепляться к эмали зубов, тем самым предотвращая ее размножение. Исследования показали, что Anti-CA-gtf IgY способен эффективно и специфично подавлять S. mutans в полости рта. [41]
Другие распространенные профилактические меры направлены на снижение потребления сахара. Один из способов сделать это — использовать заменители сахара, такие как ксилит или эритрит, которые не могут метаболизироваться в сахара, которые обычно усиливают рост S. mutans . Молекула ксилита, пятиуглеродного сахара, нарушает выработку энергии S.mutans , образуя токсичный промежуточный продукт во время гликолиза. [42] [43] Были предложены или изучены различные другие природные средства, в том числе деглицирризинированный экстракт корня солодки , [44] [45] масло чайного дерева , [46] мускатный орех (содержится в мускатном орехе ), [47] куркуминоиды (основные компоненты куркумы ), [48] и эвгенол (содержится в лавровом листе, листьях корицы и гвоздике). Кроме того, различные чаи были протестированы на активность против S. mutans и другие преимущества для зубов. [49] [50] [51] [52] [53] низкомолекулярные ингибиторы, избирательно ингибирующие или диспергирующие биопленки S. mutans . Недавно были идентифицированы и разработаны [54] [55] [56] [57] Кроме того, в ходе разработки лекарств на основе структуры были выявлены селективные ингибиторы, нацеленные на S. mutans . глюкозилтрансферазы [58] [59] Эти свинцовые соединения эффективны в доклинических моделях на животных. [60] Однако ни одно из этих средств не подвергалось клиническим испытаниям и не рекомендовано ведущими стоматологическими организациями для лечения S. mutans . [ нужна ссылка ]
Добавление биоактивных стеклянных шариков в стоматологические композиты снижает проникновение S. mutans в маргинальные промежутки между зубом и композитом. [61] Они обладают противомикробными свойствами, уменьшая проникновение бактерий. [61] Это снижает риск развития вторичного кариеса, частой причины неудачных реставраций зубов . [61] Это означает, что долговечность и эффективность композитных реставраций могут быть улучшены. [61]
бактериофаги (вирусы, поражающие бактерии), нацеленные на S. mutans Были исследованы . Фаги показали многообещающую эффективность в сокращении количества S. mutans в лабораторных условиях, потенциально предлагая целенаправленный подход к профилактике кариеса без ущерба для естественного микробиома полости рта. [62] [63] [64] [65] Было обнаружено несколько различных фагов, инфицирующих S. mutans , включая SMHBZ8 . [64] [65]
Выживание в стрессовых условиях
[ редактировать ]Условия в полости рта разнообразны и сложны, часто переходят от одной крайности к другой. Таким образом, чтобы выжить в полости рта, S. mutans должен переносить резкие колебания окружающей среды и воздействие различных противомикробных агентов. [17] Трансформация – это бактериальная адаптация, включающая перенос ДНК от одной бактерии к другой через окружающую среду. Трансформация — примитивная форма полового размножения . Чтобы бактерия могла связать, поглотить и рекомбинировать экзогенную ДНК в свою хромосому, она должна войти в особое физиологическое состояние, называемое «компетентностью» . У S. mutans пептидных феромонов сигнальная система кворума контролирует генетическую компетентность. [66] Эта система функционирует оптимально, когда клетки S. mutans находятся в скученных биопленках. [67] Клетки S. mutans, растущие в биопленке, трансформируются со скоростью в 10–600 раз большей, чем одиночные клетки, растущие в стесненных условиях (планктонные клетки). [66] Индукция компетентности, по-видимому, является адаптацией для восстановления повреждений ДНК, вызванных перенаселенными стрессовыми условиями. [68]
Знание о чувстве кворума приводит к потенциальной разработке лекарств и методов лечения. Пептидами, чувствительными к кворуму, можно манипулировать, чтобы вызвать самоубийство цели. Более того, подавление чувства кворума может привести к предотвращению устойчивости к антибиотикам. [69]
Эволюция
[ редактировать ]развились три ключевые черты У S. mutans , которые увеличили его вирулентность за счет повышения его способности адаптироваться к полости рта: повышенное производство органических кислот, способность образовывать биопленки на твердых поверхностях зубов и способность выживать и развиваться при низком pH. среда. [70]
В ходе своей эволюции S. mutans приобрела способность увеличивать количество углеводов, которые он мог метаболизировать, и, следовательно, в качестве побочного продукта производилось больше органической кислоты. [71] Это имеет значение в формировании кариеса зубов , поскольку повышенная кислотность в полости рта усиливает скорость деминерализации зуба, что приводит к кариозному поражению. [72] Считается, что этот признак развился у S. mutans посредством латерального переноса генов с другими видами бактерий, присутствующими в полости рта. Существует несколько генов, SMU.438 и SMU.1561, участвующих в углеводном обмене, активность которых повышена у S. mutans . Эти гены, возможно, произошли от Lactococcus Lactis и S. Gallolyticus соответственно. [71]
Другой случай латерального переноса генов ответственен за приобретение S. mutans гена глюкозилтрансферазы (GTF). Гены GTF, обнаруженные у S. mutans , скорее всего, произошли от других анаэробных бактерий, обитающих в полости рта, таких как Lactobacillus или Leuconostoc . Кроме того, гены GTF у S. mutans обнаруживают гомологию с аналогичными генами, обнаруженными у Lactobacillus и Leuconostoc . Считается, что общий предковый ген использовался для гидролиза и связывания углеводов. [14]
Третья черта, развившаяся у S. mutans, — это способность не только выживать, но и процветать в кислых условиях. Эта особенность дает S. mutans селективное преимущество перед другими представителями микробиоты полости рта. В результате S. mutans может вытеснить другие виды и занять дополнительные области рта, такие как развитые зубные бляшки , уровень кислотности которых может достигать уровня 4,0. [72] Естественный отбор , скорее всего, является основным эволюционным механизмом, ответственным за эту черту. [ нужна ссылка ]
При обсуждении эволюции S. mutans необходимо учитывать роль, которую сыграли люди, и коэволюцию, произошедшую между этими двумя видами. По мере того как люди развивались антропологически, бактерии развивались биологически. Широко признано, что появление сельского хозяйства у ранних человеческих популяций создало условия, необходимые S. mutans для превращения в вирулентную бактерию, которой она является сегодня. Сельское хозяйство ввело ферментированные продукты, а также продукты, богатые углеводами, в рацион исторических популяций человечества. Эти новые продукты привели к появлению новых бактерий в полости рта и создали новые условия окружающей среды. Например, Lactobacillus или Leuconostoc обычно содержатся в таких продуктах, как йогурт и вино. Кроме того, потребление большего количества углеводов увеличивало количество сахаров, доступных S. mutans для метаболизма, и снижало pH ротовой полости. Эта новая кислая среда обитания будет отбирать те бактерии, которые смогут выжить и размножаться при более низком pH. [71]
Еще одно существенное изменение в среде полости рта произошло во время промышленной революции . Более эффективная обработка и производство продуктов питания увеличили доступность и количество сахарозы , потребляемой людьми. Это обеспечило S. mutans большим количеством энергетических ресурсов и, таким образом, усугубило и без того растущий уровень кариеса. [14] Рафинированный сахар — это чистая сахароза, единственный сахар, который можно превратить в липкие глюканы, позволяющие бактериям образовывать толстые, прочно прилипающие бляшки. [73]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б Райан К.Дж., Рэй К.Г., ред. (2004). Медицинская микробиология Шерриса (4-е изд.). МакГроу Хилл. ISBN 978-0-8385-8529-0 . [ нужна страница ]
- ^ Jump up to: а б Леше В.Дж. (1996). «Глава 99: Микробиология кариеса зубов и заболеваний пародонта» . У барона С. (ред.). Медицинская микробиология барона (4-е изд.). Медицинский филиал Техасского университета. ISBN 978-0-9631172-1-2 . ПМИД 21413316 .
- ^ Томас В.Дж., Роуз Ф.Д. (1924). «Этнические различия в переживании боли» . Социальные науки и медицина . 32 (9): 1063–6. дои : 10.1016/0277-9536(91)90164-8 . ПМК 2047899 . ПМИД 2047899 .
- ^ Стоматологическая школа Университета Ньюкасла. « Streptococcus mutans и стрептококки mutans. В: Среда полости рта, онлайн-учебник» . Архивировано из оригинала 5 ноября 2013 г. Проверено 4 ноября 2013 г.
- ^ Николя Г.Г., Lavoie MC (январь 2011 г.). «[Streptococcus mutans и стрептококки полости рта в зубном налете]». Канадский журнал микробиологии . 57 (1): 1–20. дои : 10.1139/W10-095 . ПМИД 21217792 .
- ^ Икеда Т., Сандхэм HJ (октябрь 1971 г.). «Распространенность Streptococcus mutans на различных поверхностях зубов у негритянских детей». Архивы оральной биологии . 16 (10): 1237–40. дои : 10.1016/0003-9969(71)90053-7 . ПМИД 5289682 .
- ^ Метвалли К.Х., Хан С.А., Кром Б.П., Джабра-Ризк М.А. (17 октября 2013 г.). «Streptococcus mutans, Candida albicans и рот человека: неприятная ситуация» . ПЛОС Патогены . 9 (10): e1003616. дои : 10.1371/journal.ppat.1003616 . ПМЦ 3798555 . ПМИД 24146611 .
- ^ Jump up to: а б с д и ж г час «UTCAT3248, Обнаружено представление CAT, КРИТИЧЕСКИ ОЦЕНЕННЫЕ ТЕМЫ» . .cats.uthscsa.edu . Проверено 3 марта 2020 г.
- ^ Виноградов А.М., Уинстон М., Рупп С.Дж., Студли П. (2004). «Реология биопленок, образующихся из возбудителя зубного налета Streptococcus mutans » . Биопленки . 1 : 49–56. дои : 10.1017/S1479050503001078 .
- ^ «Исследователи-стоматологи: бактерии во рту: не слишком привязывайтесь» . 08.12.2010.
- ^ Мэдиган М., Мартинко Дж., ред. (2005). Брок Биология микроорганизмов (11-е изд.). Прентис Холл. ISBN 978-0-13-144329-7 . [ нужна страница ]
- ^ Кляйн Дж. П., Шоллер М. (декабрь 1988 г.). «Последние достижения в разработке вакцины против Streptococcus mutans». Европейский журнал эпидемиологии . 4 (4): 419–25. дои : 10.1007/BF00146392 . JSTOR 3521322 . ПМИД 3060368 . S2CID 33960606 .
- ^ Хаджишенгаллис Г., Рассел М.В. (2008). «Молекулярные подходы к вакцинации против инфекций полости рта» . Молекулярная оральная микробиология . Кайстер Академик Пресс. ISBN 978-1-904455-24-0 .
- ^ Jump up to: а б с Хосино Т., Фудзивара Т., Кавабата С. (2012). «Эволюция кариесогенного характера у Streptococcus mutans: горизонтальная передача генов семейства гликозилгидролаз 70» . Научные отчеты . 2 : 518. Бибкод : 2012NatSR...2E.518H . дои : 10.1038/srep00518 . ПМК 3399136 . ПМИД 22816041 .
- ^ Саймон Л. (1 декабря 2007 г.). «Роль Streptococcus mutans и экологии полости рта в формировании кариеса зубов» . Журнал юных исследователей . Архивировано из оригинала 21 декабря 2016 года . Проверено 21 декабря 2016 г.
- ^ Алалуусуа С, Ренконен О.В. (декабрь 1983 г.). «Выявление Streptococcus mutans и опыт кариеса зубов у детей от 2 до 4 лет». Скандинавский журнал стоматологических исследований . 91 (6): 453–457. дои : 10.1111/j.1600-0722.1983.tb00845.x . ПМИД 6581521 .
- ^ Jump up to: а б с Бисвас С, Бисвас I (апрель 2011 г.). «Роль VltAB, комплекса-транспортера ABC, в толерантности к виологену у Streptococcus mutans» . Антимикробные средства и химиотерапия . 55 (4): 1460–9. дои : 10.1128/AAC.01094-10 . ПМК 3067168 . ПМИД 21282456 .
- ^ Jump up to: а б с Аргимон С., Кофилд П.В. (март 2011 г.). «Распределение предполагаемых генов вирулентности в штаммах Streptococcus mutans не коррелирует с наличием кариеса» . Журнал клинической микробиологии . 49 (3): 984–92. дои : 10.1128/JCM.01993-10 . ПМК 3067729 . ПМИД 21209168 .
- ^ «Кривая Стефана | Процесс кариеса и стратегии профилактики: окружающая среда | Курс CE» . www.dentalcare.com . Проверено 23 ноября 2018 г.
- ^ Френкен Дж. Э., Шарма П., Стенхаус Л., Грин Д., Лаверти Д., Дитрих Т. (март 2017 г.). «Глобальная эпидемиология кариеса зубов и тяжелого пародонтита – комплексный обзор» . Журнал клинической пародонтологии . 44 (Приложение 18): S94–S105. дои : 10.1111/jcpe.12677 . ПМИД 28266116 .
- ^ «Роль Streptococcus mutans и экологии полости рта в формировании кариеса зубов» . Журнал юных исследователей . Проверено 02 марта 2020 г.
- ^ Гамбоа Ф., Пласас Л., Гарсиа Д.А., Аристисабаль Ф., Сарральде А.Л., Ламби К.П. и др. (декабрь 2018 г.). «Наличие и количество S. mutans у детей с кариесом зубов: до, во время и после обучения гигиене полости рта» (PDF) . Acta Odontologica Latinoamericana . 31 (3): 156–163. ПМИД 30829371 .
- ^ Мацуи Р., Цвиткович Д. (март 2010 г.). «Механизмы кислотоустойчивости, используемые Streptococcus mutans» . Будущая микробиология . 5 (3): 403–417. дои : 10.2217/fmb.09.129 . ПМЦ 2937171 . ПМИД 20210551 .
- ^ Гросс Э.Л., Билл СиДжей, Куч С.Р., Файерстоун Н.Д., Лейс Э.Дж., Гриффен А.Л. (16 октября 2012 г.). «Помимо Streptococcus mutans: начало кариеса зубов связано с несколькими видами согласно анализу сообщества 16S рРНК» . ПЛОС ОДИН . 7 (10): е47722. Бибкод : 2012PLoSO...747722G . дои : 10.1371/journal.pone.0047722 . ПМЦ 3472979 . ПМИД 23091642 .
- ^ Гао X, Хамза Ш., Ю К.К., МакГрат С., Кинг Н.М. (февраль 2013 г.). «Стоматологический страх и тревога у детей и подростков: качественное исследование с использованием YouTube» . Журнал медицинских интернет-исследований . 15 (2): е29. дои : 10.2196/jmir.2290 . ПМЦ 3636260 . ПМИД 23435094 .
- ^ Кальтабиано М.Л., Крокер Ф., Пейдж Л., Склавос А., Спитери Дж., Ханрахан Л. и др. (март 2018 г.). «Стоматологическая тревога у пациентов, посещающих студенческую стоматологическую поликлинику» . BMC Здоровье полости рта . 18 (1): 48. дои : 10.1186/s12903-018-0507-5 . ПМК 5859659 . ПМИД 29558935 .
- ^ Томсон В.М., Стюарт Дж.Ф., Картер К.Д., Спенсер А.Дж. (август 1996 г.). «Стоматологическая тревога среди австралийцев». Международный стоматологический журнал . 46 (4): 320–4. ПМИД 9147119 .
- ^ Батчер Дж. П., Малкольм Дж., Бенсон Р.А., Дэн Д.М., Брюэр Дж.М., Гарсайд П. и др. (октябрь 2011 г.). «Влияние Streptococcus mutans на активацию и функцию дендритных клеток». Журнал стоматологических исследований . 90 (10): 1221–7. дои : 10.1177/0022034511412970 . ПМИД 21690565 . S2CID 11422268 .
- ^ Берковиц Р.Дж. (2006). «Стрептококки Mutans: приобретение и передача». Детская стоматология . 28 (2): 106–9, обсуждение 192–8. ПМИД 16708784 .
- ^ де Абреу да Силва Бастос В., Фрейтас-Фернандес Л.Б., да Силва Фидальго Т.К., Мартинс С., Маттос К.Т., Рибейру де Соуза И.П. и др. (февраль 2015 г.). «Передача Streptococcus mutans от матери ребенку: систематический обзор и метаанализ». Журнал стоматологии . 43 (2): 181–91. дои : 10.1016/j.jdent.2014.12.001 . ПМИД 25486222 .
- ^ Накано К., Инаба Х., Номура Р., Немото Х., Такеда М., Ёсиока Х. и др. (сентябрь 2006 г.). «Обнаружение кариесогенного Streptococcus mutans в экстирпированных сердечных клапанах и образцах атероматозных бляшек» . Журнал клинической микробиологии . 44 (9): 3313–7. дои : 10.1128/JCM.00377-06 . ПМК 1594668 . ПМИД 16954266 .
- ^ Рао М., Джон Г., Ганеш А., Хосе Дж., Лалита М.К., Джон Л. (ноябрь 1990 г.). «Инфекционный эндокардит, вызванный Streptococcus sanguis I, возникающий на нормальном митральном клапане». Журнал Ассоциации врачей Индии . 38 (11): 866–8. ПМИД 2079476 .
- ^ Болезни сердца: учебник сердечно-сосудистой медицины . Филадельфия: У. Б. Сондерс. 1996. С. 1723 –50.
- ^ Накано К., Номура Р., Оошима Т. (2008). «Streptococcus mutans и сердечно-сосудистые заболевания» . Обзор японской стоматологической науки . 44 : 29–37. дои : 10.1016/j.jdsr.2007.09.001 .
- ^ Финкельштейн П., Йост К.Г., Гроссман Э. (1990). «Механические устройства в сравнении с противомикробными полосканиями в уменьшении зубного налета и гингивита». Клиническая профилактическая стоматология . 12 (3): 8–11. ПМИД 2083478 .
- ^ Патил С.П., Патил П.Б., Кашетти М.В. (май 2014 г.). «Эффективность различных приемов чистки зубов при удалении зубного налета у детей 6-8 лет Гульбарги» . Журнал Международного общества профилактической и общественной стоматологии . 4 (2): 113–6. дои : 10.4103/2231-0762.138305 . ПМЦ 4170543 . ПМИД 25254196 .
- ^ Бузалаф М.А., Пессан Дж.П., Онорио Х.М., Тен Кейт Дж.М. (2011). «Механизмы действия фторида в борьбе с кариесом». Монографии по устному делу . 22 : 97–114. дои : 10.1159/000325151 . ISBN 978-3-8055-9659-6 . ПМИД 21701194 .
- ^ Грейг В., Конвей Д.И. (2012). «Фторсодержащий лак оказался эффективным средством снижения кариеса у школьников с высоким риском кариеса в сельских районах Бразилии» . Доказательная стоматология . 13 (3): 78–79. дои : 10.1038/sj.ebd.6400874 . ПМИД 23059920 .
- ^ Центральный Кокрейновский регистр контролируемых исследований (CENTRAL), Влияние фторсодержащего лака на Streptococcus mutans в зубном налете и слюне, Скандинавский журнал стоматологических исследований, 1982, 90 (6), 2003, выпуск 3 - Зиккерт I, Эмильсон К.Г.
- ^ Журнал Индийского общества детской стоматологии и профилактической стоматологии, Влияние трех различных композиций фторсодержащих лаков для местного применения с предварительной пероральной профилактикой и без нее на количество Streptococcus mutans в образцах биопленок детей в возрасте 2–8 лет: рандомизированное контролируемое исследование, 2019, Страница: 286-291 - Сушма Ядав, Винод Сачдев, Манви Малик, Радхика Чопра
- ^ Нгуен С.В., Икатло ФК, Накано Т., Исогай Э., Хиросе К., Мизугай Х. и др. (август 2011 г.). «Антиклеточно-ассоциированная глюкозилтрансфераза иммуноглобулина Y, подавляющая стрептококки слюнных мутантов у здоровых молодых людей». Журнал Американской стоматологической ассоциации . 142 (8): 943–949. дои : 10.14219/jada.archive.2011.0301 . ПМИД 21804061 .
- ^ Ли К.А., Милгром П., Ротен М. (2006). «Ксилит, подсластители и кариес». Детская стоматология . 28 (2): 154–63, обсуждение 192–8. ПМИД 16708791 .
- ^ Хейнсон Т. (2013). «Какое влияние оказывают жевательные резинки, содержащие ксилит, на флору полости рта? Разработка количественного теста для выявления Streptococcus mutans на основе количественной полимеразной цепной реакции «в реальном времени»» [Жевательная резинка, содержащая ксилит, и бактериальная флора полости рта. Разработка количественного теста на Streptococcus mutans на основе количественной полимеразной цепной реакции в реальном времени] (PDF) . Young Science (Молодой исследователь) (на немецком языке). 97 :18-30. Архивировано из оригинала (PDF) 23 января 2015 года . Проверено 23 января 2015 г.
- ^ Ан С.Дж., Чо Э.Дж., Ким Х.Дж., Пак С.Н., Лим Ю.К., Кук Дж.К. (декабрь 2012 г.). «Противомикробное действие деглицирризинированного экстракта корня солодки на Streptococcus mutans UA159 как в планктонных, так и в биопленочных культурах». Анаэроб . 18 (6): 590–596. дои : 10.1016/j.anaerobe.2012.10.005 . ПМИД 23123832 .
- ^ Ху Ч., Хе Дж., Экерт Р., Ву XY, Ли Л.Н., Тянь Ю. и др. (январь 2011 г.). «Разработка и оценка безопасного и эффективного травяного леденца без сахара, который убивает бактерии, вызывающие кариес» . Международный журнал устных наук . 3 (1): 13–20. дои : 10.4248/IJOS11005 . ПМЦ 3469870 . ПМИД 21449211 .
- ^ Карсон К.Ф., Хаммер К.А., Райли ТВ (январь 2006 г.). «Масло Melaleuca alternifolia (чайного дерева): обзор противомикробных и других лечебных свойств» . Обзоры клинической микробиологии . 19 (1): 50–62. дои : 10.1128/CMR.19.1.50-62.2006 . ПМК 1360273 . ПМИД 16418522 .
- ^ Рукаяди Й., Ким К.Х., Хван Дж.К. (март 2008 г.). «Антибиопленочная активность мацелигнана, выделенного из Myristica fragrans Houtt., против первичных бактерий-колонизаторов полости рта». Фитотерапевтические исследования . 22 (3): 308–312. дои : 10.1002/ptr.2312 . ПМИД 17926328 . S2CID 11784891 .
- ^ Пандит С., Ким Х.Дж., Ким Дж.Э., Чон Дж.Г. (июнь 2011 г.). «Выделение эффективной фракции куркумы против биопленок Streptococcus mutans путем сравнения содержания куркуминоидов и антиацидогенной активности». Пищевая химия . 126 (4): 1565–1570. doi : 10.1016/j.foodchem.2010.12.005 . ПМИД 25213928 .
- ^ Субраманиам П., Эсвара У., Махешвар Редди К.Р. (январь – февраль 2012 г.). «Влияние различных видов чая на Streptococcus mutans: исследование in vitro» . Индийский журнал стоматологических исследований . 23 (1): 43–48. дои : 10.4103/0970-9290.99037 . ПМИД 22842248 .
- ^ Шуми В., Хоссейн М.А., Парк DJ, Парк С. (сентябрь 2014 г.). «Ингибирующее действие полифенола эпигаллокатехин галлата зеленого чая (EGCG) на выработку экзополисахаридов Streptococcus mutans в микрофлюидных условиях». Журнал БиоЧип . 8 (3): 179–86. дои : 10.1007/s13206-014-8304-y . S2CID 84209221 .
- ^ Маникья С., Ванишри М., Сурекха Р., Хунасги С., Анила К., Манвикар В. (январь – март 2014 г.). «Влияние зеленого чая на pH слюны и количество Streptococcus Mutans у здоровых людей» . Международный журнал патологии полости рта и челюстно-лицевой области . 5 (1): 13–16. ISSN 2231-2250 .
- ^ Авадалла Х.И., Рагаб М.Х., Бассуони М.В., Файед М.Т., Аббас М.О. (май 2011 г.). «Пилотное исследование влияния употребления зеленого чая на здоровье полости рта». Международный журнал стоматологической гигиены . 9 (2): 110–116. дои : 10.1111/j.1601-5037.2009.00440.x . ПМИД 21356006 .
- ^ Штаудер М., Папетти А., Далья М., Веццулли Л., Газзани Г., Варальдо П.Е. и др. (ноябрь 2010 г.). «Ингибирующая активность компонентов ячменного кофе в отношении биопленки Streptococcus mutans». Современная микробиология . 61 (5): 417–421. дои : 10.1007/s00284-010-9630-5 . ПМИД 20361189 . S2CID 19861203 .
- ^ Лю С., Уортингтон Р.Дж., Меландер С., Ву Х (июнь 2011 г.). «Новая небольшая молекула специфически подавляет кариесогенную бактерию Streptococcus mutans в многовидовых биопленках» . Антимикробные средства и химиотерапия . 55 (6): 2679–2687. дои : 10.1128/AAC.01496-10 . ПМК 3101470 . ПМИД 21402858 .
- ^ Чжан Ц, Ма Ц, Ван Ю, У Х, Цзоу Дж (сентябрь 2021 г.). «Молекулярные механизмы ингибирования глюкозилтрансфераз при образовании биопленок у Streptococcus mutans» . Международный журнал устных наук . 13 (1): 30. дои : 10.1038/s41368-021-00137-1 . ПМЦ 8481554 . ПМИД 34588414 .
- ^ Лю С., Чжан Х., Пэн Х., Блэкледж М.С., Фурлани Р.Э., Ли Х. и др. (июнь 2023 г.). «Маленькие молекулы ослабляют вирулентность бактерий, нацеливаясь на регулятор консервативного ответа» . мБио . 14 (3): e0013723. дои : 10.1128/mbio.00137-23 . ПМЦ 10294662 . ПМИД 37074183 .
- ^ Гарсия С.С., Блэкледж М.С., Михалек С., Су Л., Птачек Т., Эйперс П. и др. (июль 2017 г.). «Нацеливание на биопленки Streptococcus mutans с помощью новой малой молекулы предотвращает кариес зубов и сохраняет микробиом полости рта» . Журнал стоматологических исследований . 96 (7): 807–814. дои : 10.1177/0022034517698096 . ПМК 5480807 . ПМИД 28571487 .
- ^ Чжан К., Ниджампатнам Б., Хуа З., Нгуен Т., Цзоу Дж., Цай Икс и др. (июль 2017 г.). «Структурное открытие низкомолекулярных ингибиторов кариесогенной вирулентности» . Научные отчеты . 7 (1): 5974. Бибкод : 2017NatSR...7.5974Z . дои : 10.1038/s41598-017-06168-1 . ПМК 5519559 . ПМИД 28729722 .
- ^ Ниджампатнам Б., Чжан Х., Цай Х, Михалек С.М., Ву Х, Велу С.Э. (июль 2018 г.). «Ингибирование биопленок Streptococcus mutans природным стильбеном пикеатанолом посредством ингибирования глюкозилтрансфераз» . АСУ Омега . 3 (7): 8378–8385. дои : 10.1021/acsomega.8b00367 . ПМК 6072251 . ПМИД 30087944 .
- ^ Ахирвар П., Козловская В., Ниджампатнам Б., Рохас Э.М., Пукканасут П., Инман Д. и др. (июнь 2023 г.). «Ингибиторы биопленок, инкапсулированные в гидрогель, устраняют кариесогенную активность Streptococcus mutans » . Журнал медицинской химии . 66 (12): 7909–7925. doi : 10.1021/acs.jmedchem.3c00272 . ПМЦ 11188996 . ПМИД 37285134 . S2CID 259098374 .
- ^ Jump up to: а б с д «UTCAT3251, Обнаружено представление CAT, КРИТИЧЕСКИ ОЦЕНЕННЫЕ ТЕМЫ» . .cats.uthscsa.edu . Проверено 3 марта 2020 г.
- ^ Фан Ц, Инь Х, Хэ Ю, Фэн Ю, Чжан Л, Луо Х и др. (май 2024 г.). «Безопасность и эффективность применения фагов при бактериальной деколонизации: систематический обзор» . «Ланцет». Микроб . 5 (5): е489–е499. дои : 10.1016/S2666-5247(24)00002-8 . ПМИД 38452780 .
- ^ Линь Ю, Чжоу Х, Ли Ю (февраль 2022 г.). «Стратегии распространения биопленки Streptococcus mutans путем разрушения внеклеточных полимерных веществ». Молекулярная оральная микробиология . 37 (1): 1–8. дои : 10.1111/omi.12355 . ПМИД 34727414 .
- ^ Jump up to: а б Бен-Закен Х., Крайтман Р., Коппенгаген-Глейзер С., Халифа Л., Алкалай-Орен С., Гельман Д. и др. (май 2021 г.). «Выделение и характеристика фага Streptococcus mutans как возможного средства лечения кариеса» . Вирусы . 13 (5): 825. дои : 10.3390/v13050825 . ПМЦ 8147482 . ПМИД 34063251 .
- ^ Jump up to: а б Вольфовиз-Зильберман А., Крайтман Р., Хазан Р., Фридман М., Хури-Хаддад Ю., Бейт Н. (август 2021 г.). «Нацеливание на бактерии Streptococcus mutans in vitro и in vivo как метод профилактики кариеса» . Антибиотики . 10 (8): 1015. doi : 10.3390/antibiotics10081015 . ПМЦ 8389033 . ПМИД 34439064 .
- ^ Jump up to: а б Ли Ю.Х., Лау ПК, Ли Дж.Х., Эллен Р.П., Цвиткович Д.Г. (февраль 2001 г.). «Естественная генетическая трансформация Streptococcus mutans, растущих в биопленках» . Журнал бактериологии . 183 (3): 897–908. дои : 10.1128/JB.183.3.897-908.2001 . ПМК 94956 . ПМИД 11208787 .
- ^ Аспирас М.Б., Эллен Р.П., Цвиткович Д.Г. (сентябрь 2004 г.). «ComX-активность Streptococcus mutans, растущих в биопленках». Письма FEMS по микробиологии . 238 (1): 167–74. дои : 10.1016/j.femsle.2004.07.032 . ПМИД 15336418 .
- ^ Мишод Р.Э., Бернштейн Х., Недельку А.М. (май 2008 г.). «Адаптационное значение пола у микробных патогенов». Инфекция, генетика и эволюция . 8 (3): 267–85. дои : 10.1016/j.meegid.2008.01.002 . ПМИД 18295550 . как PDF
- ^ Люн В., Дюфур Д., Левеск К.М. (23 октября 2015 г.). «Смерть и выживание Streptococcus mutans: разные результаты воздействия сигнального пептида, чувствительного к кворуму» . Границы микробиологии . 6 : 1176. дои : 10.3389/fmicb.2015.01176 . ПМЦ 4615949 . ПМИД 26557114 .
- ^ Банас Дж.А., Миллер Дж.Д., Фускино М.Е., Хэзлетт К.Р., Тойофуку В., Портер К.А. и др. (январь 2007 г.). «Доказательства того, что накопление мутантов в биопленке отражает естественный отбор, а не вызванную стрессом адаптивную мутацию» . Прикладная и экологическая микробиология . 73 (1): 357–61. Бибкод : 2007ApEnM..73..357B . дои : 10.1128/aem.02014-06 . ПМК 1797100 . ПМИД 17085702 .
- ^ Jump up to: а б с Корнехо О.Э., Лефебюр Т., Битар П.Д., Ланг П., Ричардс В.П., Эйлертсон К. и др. (апрель 2013 г.). «Эволюционная и популяционная геномика полостных бактерий Streptococcus mutans» . Молекулярная биология и эволюция . 30 (4): 881–93. дои : 10.1093/molbev/mss278 . ПМК 3603310 . ПМИД 23228887 .
- ^ Jump up to: а б Такахаши Н., Нивад Б. (март 2011 г.). «Роль бактерий в процессе кариеса: экологические перспективы». Журнал стоматологических исследований . 90 (3): 294–303. дои : 10.1177/0022034510379602 . ПМИД 20924061 . S2CID 25740861 .
- ^ Дарлингтон В. (август 1979 г.). Метаболизм сахарозы Stepococcus sanguis 804 (NCTC 10904) и его влияние на среду полости рта (докторская диссертация). Университет Глазго.