Стрептококковая инфекция группы В
| Стрептококковая инфекция группы В | |
|---|---|
| Другие имена | Стрептококковая инфекция группы В |
 | |
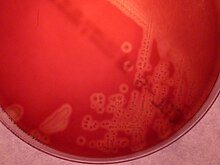
| Streptococcus agalactiae - окраска по Граму | |
| Специальность | Педиатрия |
Стрептококковая инфекция группы B , также известная как стрептококковая инфекция группы B или просто стрептококковая инфекция группы B, представляет собой инфекционное заболевание, вызываемое бактерией Streptococcus agalactiae . Streptococcus agalactiae — наиболее распространенный человеческий возбудитель, относящийся к группе B классификации Лансфилда по стрептококков , отсюда и название стретококков группы B (GBS). Заражение GBS может вызвать серьезное заболевание, а иногда и смерть, особенно у новорожденных, пожилых людей и людей с ослабленной иммунной системой . Наиболее тяжелой формой стрептококковой инфекции группы В является неонатальный менингит у младенцев, который часто приводит к летальному исходу и может вызвать стойкие нейрокогнитивные нарушения .
S. agalactiae была признана возбудителем крупного рогатого скота Эдмоном Нокаром и Моллеро в конце 1880-х годов. Это может вызвать мастит ( воспаление вымени ) у молочных коров. На это намекает видовое название «agalactiae», что означает «нет молока». Его значение как патогена для человека было впервые описано в 1938 году. [ 1 ] а в начале 1960-х годов СГБ был признан основной причиной инфекций у новорожденных. [ 2 ] У большинства людей Streptococcus agalactiae представляет собой безвредную комменсальную бактерию , которая является частью нормальной микробиоты человека , колонизирующей желудочно-кишечный и мочеполовой тракты. До 30% здоровых взрослых людей являются бессимптомными носителями СГБ. [ 3 ] [ 4 ]
Лабораторная идентификация стрептококка группы В
[ редактировать ]Как уже упоминалось, S. agalactiae представляет собой грамположительный кокк со склонностью к образованию цепочек, бета-гемолитический, каталазоотрицательный и факультативный анаэроб ( анаэробный организм ). СГБ легко растет на чашках с кровяным агаром в виде микробных колоний, окруженных узкой зоной β- гемолиза .
СГБ характеризуется наличием в клеточной стенке группы антигена В классификации Лансфилда ( группировка Лансфилда ), который можно обнаружить непосредственно у интактных бактерий с помощью реакции латекс-агглютинации . [ 5 ] [ 6 ] [ 7 ] [ 8 ] Тест CAMP также является еще одним важным тестом для выявления СГБ. Фактор CAMP действует синергически со стафилококковым β-гемолизином, вызывая усиленный гемолиз эритроцитов овцы или крупного рогатого скота . [ 5 ] СГБ также способен гидролизовать гиппурат , и этот тест также можно использовать для идентификации СГБ. [ 6 ] Гемолитические штаммы GBS при культивировании на среде гранада через 24-48 часов при температуре 35-37°С продуцируют ( гранадаен ) и развиваются в виде оранжево-кирпичных или красных колоний, что позволяет их прямую и однозначную идентификацию. [ 9 ] Идентификацию GBS также можно легко провести с помощью с матричной лазерной десорбцией и ионизацией и временем пролета ( MALDI-TOF ) масс-спектрометрии . [ 10 ] [ 11 ] и тесты на нуклеиновые кислоты (МАНК). [ 6 ] Кроме того, колонии GBS можно предварительно идентифицировать после их появления в хромогенной агаровой среде. [ 6 ] [ 12 ] [ 13 ] Тем не менее, GBS-подобные колонии, развивающиеся в хромогенной среде, следует подтверждать как GBS с помощью дополнительных надежных тестов (эглатекс-агглютинация или CAMP-тест), чтобы избежать возможной ошибочной идентификации. [ 6 ] [ 8 ] Краткое описание лабораторных методов идентификации GBS представлено в ссылке. [ 6 ]


Колонизация GBS против инфекции GBS
[ редактировать ]СГБ обнаруживается в желудочно-кишечном, мочеполовом тракте и ротоглотке человека. СГБ также является нормальным компонентом микробиоты кишечника и влагалища у некоторых женщин. [ 3 ] [ 14 ] [ 15 ] В различных исследованиях уровень вагинальной колонизации GBS колеблется от 4 до 36%, при этом в большинстве исследований сообщается о показателе более 20%, при этом оценка материнской колонизации GBS во всем мире составляет 18% с большими различиями между странами (11–35%). [ 16 ] Колонизация вагинального или ректального GBS может быть периодической, временной или постоянной. [ 14 ] Эти различия в зарегистрированной распространенности бессимптомной (без симптомов заболевания) колонизации могут быть связаны с различными используемыми методами обнаружения и различиями в изучаемых популяциях. [ 12 ] [ 17 ] [ 18 ] Хотя СГБ является бессимптомным и безвредным колонизатором желудочно-кишечного тракта человека почти у 30% здоровых взрослых, включая беременных женщин. [ 4 ] [ 17 ] Эта условно-патогенная безвредная бактерия в некоторых случаях может вызывать тяжелые инвазивные инфекции ( оппортунистические инфекции ). [ 3 ]
СГБ и беременность
[ редактировать ]Хотя колонизация GBS протекает бессимптомно и, как правило, не вызывает проблем, иногда она может вызвать серьезные заболевания у матери и ребенка во время беременности и после родов. Инфекции GBS у матери могут вызывать хориоамнионит (внутриамниотическую инфекцию или тяжелую инфекцию плацентарной ткани), нечасто, послеродовые инфекции (после рождения), и это было связано с недоношенностью и гибелью плода. [ 19 ] , вызванные СГБ Инфекции мочевыводящих путей , концентрация которых превышает 100 000 КОЕ ( колониеобразующие единицы )/мл, может вызывать роды у беременных женщин и вызывать преждевременные роды ( преждевременные роды ) и выкидыш , что требует лечения антибиотиками. Присутствие GBS в моче при любом количестве колоний является маркером тяжелой колонизации GBS и показанием для интранатальной антибиотикопрофилактики. [ 4 ] [ 14 ] [ 20 ]
СГБ и новорожденные
[ редактировать ]В западном мире СГБ (при отсутствии эффективных мер профилактики) является основной причиной бактериальных инфекций у новорожденных, таких как сепсис , пневмония и менингит , которые могут привести к смерти или отдаленным последствиям . [ 4 ] [ 21 ] [ 22 ] [ 23 ] Инфекции GBS у новорожденных подразделяются на два клинических типа: заболевание с ранним началом (GBS-EOD) и заболевание с поздним началом (GBS-LOD). СГБ-ЭОД проявляется у новорожденного в возрасте от 0 до 7 дней жизни, при этом в большинстве случаев ЭОД проявляется в течение 24 часов после рождения. GBS-LOD начинается между 7 и 90 днями после рождения. [ 4 ] [ 12 ] [ 14 ] [ 22 ] Примерно 50% новорожденных от матерей, колонизированных GBS, также колонизированы GBS, и (без мер профилактики) у 1-2% этих новорожденных разовьется GBS-EOD. [ 14 ] [ 24 ] Наиболее распространенными клиническими синдромами GBS-EOD являются сепсис, пневмония и (реже) менингит. Пневмония и сепсис часто наблюдаются вместе или последовательно. Новорожденные с менингитом часто проявляют себя так же, как и дети с другими синдромами, прежде чем у них появятся симптомы менингита. ребенка . исследование спинномозговой жидкости Для исключения менингита часто необходимо [ 4 ] [ 22 ] [ 25 ] [ 26 ] У меньшинства детей с сепсисом, вызванным S. agalactiae, имеется коинфекция , при этом один или несколько других видов бактерий также способствуют развитию септического заболевания. Наиболее распространенным из этих микроорганизмов является Staphylococcus aureus . [ 23 ] Колонизация GBS во время родов является основным фактором риска развития GBS-EOD. GBS-EOD передается вертикально ( вертикальная передача ), в результате воздействия GBS на плод или ребенка из влагалища инфицированной женщины либо внутриутробно (из-за восходящей инфекции), либо во время рождения, после разрыва плодных оболочек. Младенцы также могут заразиться при прохождении через родовые пути; однако новорожденные, заразившиеся GBS этим путем, могут стать только колонизированными, и у этих колонизированных младенцев обычно не развивается GBS-EOD. [ 14 ] [ 27 ]
Хотя колонизация GBS у матери является ключевым фактором, определяющим GBS-EOD, другие факторы также увеличивают риск. Этими факторами являются: [ 4 ] [ 12 ] [ 14 ]
- Начало родов до 37 недель беременности ( преждевременные роды )
- Длительный разрыв плодных оболочек (более продолжительный разрыв плодных оболочек) (≥18 часов до родов)
- СГБ Бактериурия во время беременности
- Интранатальная (во время родов) лихорадка (>38 °C, >100,4 °F)
- Амниотические инфекции (хориоамнионит)
- Молодой возраст матери
- ВИЧ-инфекция у матери [ 28 ]
Тем не менее, большинство детей, у которых развивается СГБ-ЭОД, рождаются у колонизированных матерей без каких-либо из этих факторов риска. [ 12 ] Тяжелая вагинальная колонизация GBS может быть связана с более высоким риском GBS-EOD. Женщины, у которых был один из этих факторов риска, но которые не были колонизированы GBS во время родов, имеют низкий риск развития GBS-EOD по сравнению с женщинами, которые были колонизированы внутриутробно, но не имели ни одного из вышеупомянутых факторов риска. [ 24 ] Наличие низкого уровня антикапсулярных антител против СГБ у матери также имеет большое значение для развития СГБ-ЭОД. [ 29 ] [ 30 ] По этой причине предыдущий брат или сестра с GBS-EOD также является важным фактором риска развития инфекции при последующих родах, что, вероятно, отражает отсутствие защитных антител у матери. [ 12 ] [ 22 ] В целом, уровень смертности от GBS-EOD снизился с 50%, наблюдавшихся в исследованиях 1970-х годов, до 2–10% в последние годы, главным образом, вследствие усовершенствований в терапии и ведении пациентов. Смертельные неонатальные инфекции, вызванные СГБ, чаще встречаются среди недоношенных детей. [ 4 ] [ 12 ] [ 31 ] Сегодня смертность, связанная с ЭОД СГБ, в США составляет 2,1% среди доношенных новорожденных и 19,2% среди недоношенных новорожденных. [ 22 ] [ 32 ]
GBS-LOD поражает детей с 7 дней. до 3-месячного возраста и имеет более низкий уровень смертности (1–6%), чем GBS-EOD. Клиническими синдромами СГБ-ЛОД являются бактериемия без очага (65%), менингит (25%), целлюлит , остеоартрит и пневмония. Сообщается, что недоношенность является основным фактором риска. Каждая неделя сокращения срока беременности увеличивает риск развития GBS-LOD в 1,34 раза. [ 33 ]
Повышенный риск GBS-LOD также связан с недоношенностью, низким весом при рождении, материнской колонизацией и многоплодной беременностью. [ 34 ] GBS-LOD можно получить не только посредством вертикальной передачи во время доставки; он также может быть получен позже от матери через грудное молоко, горло или из экологических, внутрибольничных и общественных источников. GBS-LOD обычно проявляется неспецифическими признаками, и диагноз следует ставить путем получения посева крови у лихорадящих новорожденных. Неонатальный менингит, вызванный S.agalactiae, не проявляется характерным признаком менингита взрослых - ригидностью шеи. Вместо этого он проявляется неспецифическими симптомами, такими как лихорадка, рвота и раздражительность, что, следовательно, может привести к поздней диагностике. Потеря слуха и умственные нарушения могут быть долгосрочными последствиями менингита GBS. [ 4 ] [ 21 ]
Профилактика неонатальной инфекции GBS – антибиотикопрофилактика во время родов (IAP)
[ редактировать ]В настоящее время единственным надежным способом предотвращения GBS-EOD является внутривенное (в/в) введение антибиотиков перед родами. То есть интранатальная антибиотикопрофилактика (ИАП). IAP прерывает вертикальную передачу GBS от матери к новорожденному и снижает частоту возникновения GBS-EOD. [ 35 ] Введение внутривенных антибиотиков во время родов. Было доказано, что внутривенное введение пенициллина или ампициллина женщинам, инфицированным GBS, в начале родов, а затем снова каждые четыре часа до родов очень эффективно предотвращает вертикальную передачу GBS от матери к ребенку и GBS-EOD. Пенициллин G, начальная доза 5 миллионов единиц внутривенно, затем по 3 миллиона единиц каждые 4 часа до родов или ампициллин, начальная доза 2 г внутривенно, затем по 1 г внутривенно каждые 4 часа до родов. [ 4 ] [ 12 ] [ 14 ] Соответствующее IAP у женщин с колонизацией GBS следует начинать как можно скорее после начала родов или отхождения вод. Если первая доза вводится как минимум за 4 часа до родов, риск неонатальной инфекции очень мал; более того, при приеме за 2–4 часа до родов риск снижается лишь частично. [ 36 ] [ 37 ] [ 38 ]
пенициллин Женщины с аллергией на в анамнезе без анафилаксии ( ангионевротический отек , респираторный дистресс или крапивница ) после введения пенициллина или цефалоспорина (низкий риск анафилаксии) могут получать цефазолин (начальная доза 2 г внутривенно, затем по 1 г внутривенно каждые 8 часов до доставки) вместо пенициллина или ампициллина. [ 12 ] [ 14 ] Если у женщины тяжелая аллергия на бета-лактамы и изолированный СГБ чувствителен к клиндамицину, то клиндамицин является рекомендуемой альтернативой. [ 14 ] Для женщин с аллергией на пенициллин высокого риска, у которых изолят GBS не чувствителен к клиндамицину, единственным допустимым вариантом является внутривенное введение ванкомицина (20 мг/кг внутривенно каждые 8 часов, максимум 2 г на разовую дозу). [ 14 ] [ 39 ] У женщин с высоким риском анафилаксии на пенициллин применение Эритромицина сегодня не рекомендуется из-за высокой доли резистентности СГБ к эритромицину (до 44,8%). [ 12 ] [ 14 ] Тестирование на аллергию на пенициллин может быть полезным для всех беременных женщин с СГБ и позволит отменить частое использование других антибиотиков при ВБП. [ 14 ] Тестирование чувствительности изолятов GBS к антибиотикам имеет решающее значение для правильного выбора антибиотиков для IAP у женщин с аллергией на пенициллин, поскольку среди изолятов GBS растет устойчивость к клиндамицину, наиболее часто используемому агенту (у женщин с аллергией на пенициллин). Соответствующие методологии (включая индуцируемую устойчивость к клиндамицину) для тестирования чувствительности к антибиотикам важны, поскольку устойчивость к клиндамицину ( резистентность к противомикробным препаратам ) может возникать у некоторых штаммов GBS, которые кажутся чувствительными ( чувствительность к антибиотикам ) к клиндамицину в определенных тестах на чувствительность. [ 8 ] [ 12 ] Для женщин, находящихся в группе риска по развитию аллергии на пенициллин, в лабораторных заявках должно быть четко указано это обстоятельство, чтобы гарантировать, что лаборатория осведомлена о необходимости тестирования изолятов СГБ на чувствительность к клиндамицину. Истинная аллергия на пенициллин встречается редко: оценочная частота анафилаксии составляет от одного до пяти эпизодов на 10 000 случаев терапии пенициллином. [ 40 ] [ 41 ] Пенициллин, назначаемый женщине, у которой в анамнезе не было аллергии на β-лактамы, имеет риск анафилаксии от 0,04 до 4 на 100 000. У матери возникает анафилаксия, связанная с ВБП СГБ, но любая заболеваемость, связанная с анафилаксией, в значительной степени компенсируется снижением частоты случаев СГБ-ЭОД. [ 12 ]
Считалось, что IAP связан с появлением резистентных бактериальных штаммов и увеличением частоты инфекций с ранним началом, вызванных другими возбудителями, главным образом грамотрицательными бактериями, такими как Escherichia coli . Тем не менее, большинство исследований не выявили увеличения частоты сепсиса с ранним началом, не связанного с СГБ, связанного с широким использованием ИАП. [ 12 ] [ 42 ] [ 43 ] [ 44 ] Ни пероральные, ни внутримышечные антибиотики не эффективны для снижения риска GBS-EOD. [ 14 ]
Были изучены другие стратегии предотвращения GBS-EOD, и было предложено интранатальное очищение влагалища хлоргексидином для предотвращения GBS-EOD, тем не менее, не было представлено никаких доказательств эффективности этого подхода. [ 12 ] [ 14 ] [ 45 ] [ 46 ] Тем не менее, в настоящее время не существует подходящего подхода для профилактики неонатального заболевания СГБ с поздним началом.
Определение кандидатов на получение IAP
[ редактировать ]Для отбора женщин-кандидатов в IAP используются два способа: подход скрининга на основе культуры и подход, основанный на риске. [ 47 ] Подход скрининга на основе культуры выявляет кандидатов с использованием нижних вагинальных и ректальных культур, полученных между 35 и 37 неделями беременности (или 36–37). [ 14 ] и IAP вводят всем женщинам, инфицированным GBS. Стратегия, основанная на оценке риска, выявляет кандидатов на получение IAP по вышеупомянутым факторам риска, которые, как известно, увеличивают вероятность GBS-EOD, без учета того, является ли мать носителем GBS. [ 4 ] [ 12 ] [ 48 ] IAP также рекомендуется женщинам с факторами риска во время родов, если их статус носительства GBS неизвестен на момент родов, женщинам с бактериурией GBS (при любом количестве колоний) во время беременности и женщинам, у которых родился ребенок с GBS-EOD. ранее. Подход, основанный на оценке риска, в целом менее эффективен, чем подход, основанный на культуре. [ 49 ] поскольку в большинстве случаев СГБ-ЭОД развивается среди новорожденных, рожденных от матерей без факторов риска. [ 12 ] [ 24 ] [ 50 ]
ВАК не требуется женщинам, перенесшим плановое кесарево сечение при отсутствии родов и с интактными плодными оболочками, независимо от известного носительства СГБ. В рекомендациях ACOG говорится: [ 14 ] «Женщинам с положительным результатом пренатальной культуры GBS, перенесшим кесарево сечение до начала родов и с неповрежденными плодными оболочками, не требуется IAP». Эта рекомендация основана на том факте, что дети, родившиеся с помощью кесарева сечения перед родами, меньше подвергаются воздействию GBS во влагалище и имеют более низкие показатели заражения GBS. Следовательно, несмотря на рекомендуемый универсальный ректовагинальный скрининг всех беременных женщин в сроке от 36 0/7 до 37 6/7 недель, женщинам, перенесшим предродовое кесарево сечение, не требуется IAP, независимо от результатов скринингового теста. [ 12 ] [ 14 ] [ 51 ]
Рутинный скрининг беременных женщин проводится в большинстве развитых стран, таких как США, Франция, Испания, Бельгия и Канада, и данные показывают снижение заболеваемости GBS-EOD после введения мер, основанных на скрининге, для предотвращения GBS-EOD. [ 18 ] [ 52 ] [ 53 ]
Стратегию, основанную на риске, пропагандируют, среди других стран, в Великобритании и Нидерландах. [ 18 ]
Вопрос экономической эффективности обеих стратегий выявления кандидатов на IAP менее однозначен, и некоторые исследования показали, что тестирование женщин с низким риском плюс IAP, назначенный женщинам из группы высокого риска, а также женщинам, у которых обнаружено наличие СГБ, обходится дороже. -эффективнее, чем текущая практика Великобритании (подход, основанный на риске). [ 54 ] Другие оценки также показали, что подход, основанный на культуре, является более экономически эффективным, чем подход, основанный на оценке риска, для профилактики GBS-EOD. [ 55 ] [ 56 ]
Сообщалось, что IAP не предотвращает все случаи GBS-EOD; его эффективность оценивается в 80%. Стратегия профилактики, основанная на оценке риска, не предотвращает около 33% случаев без факторов риска. [ 57 ] До 90% случаев GBS-EOD можно было бы предотвратить, если бы IAP предлагалась всем носителям GBS, выявленным в результате универсального скрининга на поздних сроках беременности, а также матерям, находящимся в ситуациях повышенного риска. [ 58 ] Если до родов внутривенно вводится недостаточное количество антибиотиков, ребенку можно дать антибиотики сразу после рождения, хотя данные о том, эффективна ли эта практика или нет, неубедительны. [ 12 ] [ 59 ] [ 60 ] [ 61 ]

Скрининг на колонизацию GBS у беременных
[ редактировать ]Примерно 10–30% женщин колонизируются СГБ во время беременности. Тем не менее, во время беременности колонизация может быть временной, периодической или постоянной. [ 12 ] Из-за этого статус колонизации GBS у женщин может меняться во время беременности, только посевы, проведенные за 5 недель до родов, позволяют довольно точно предсказать статус носительства GBS при родах. [ 62 ]
Напротив, если пренатальный посев проводится более чем за 5 недель до родов, он не позволяет точно предсказать статус носительства СГБ при родах. По этой причине сегодня ACOG рекомендует тестирование на колонизацию GBS у беременных на сроке 36–37 недель беременности. [ 12 ] [ 63 ] Важно отметить, что ACOG теперь рекомендует проводить универсальный скрининг GBS между 36 и 37 неделями беременности, а не в 35–37 недель, как ранее рекомендовал CDC. Эта новая рекомендация обеспечивает 5-недельный период для получения достоверных результатов посева, включая роды, произошедшие до гестационного возраста не менее 41 недели. [ 14 ]
Клинические образцы, рекомендуемые для посева на СГБ, представляют собой мазки, собранные из нижней части влагалища и прямой кишки через наружный анальный сфинктер . Образцы из влагалища и прямой кишки следует собирать предпочтительно с помощью тампонов. По сравнению с тампонами из волокна эти тампоны удаляют образцы и микроорганизмы более эффективно, чем обычные тампоны из волокна. [ 7 ] Образец следует собирать, протирая нижнюю часть влагалища (входящее влагалище), а затем прямую кишку (т. е. вводя тампон через анальный сфинктер) одним и тем же тампоном или двумя разными тампонами. Образцы из шейки матки, перианальной, периректальной или промежностной области не принимаются, и зеркало . для сбора проб не следует использовать [ 12 ] Образцы (мазки) могут быть взяты медицинскими работниками или взяты матерью самостоятельно после соответствующих инструкций. [ 64 ] [ 65 ] [ 66 ] [ 67 ]

Эти тампоны следует поместить в непитательную транспортную среду. [ 7 ] [ 12 ] Если это возможно, образцы следует хранить в холодильнике и как можно скорее отправлять в лабораторию. [ 7 ] [ 12 ] Соответствующие транспортные системы коммерчески доступны, и в этих транспортных средах GBS может сохранять жизнеспособность в течение нескольких дней при комнатной температуре. Однако восстановление GBS снижается в течение одного-четырех дней, особенно при повышенных температурах, что может привести к ложноотрицательным результатам. [ 7 ] [ 12 ] [ 68 ]
Культуральные методы выявления колонизации GBS у беременных
[ редактировать ]Образцы (вагинальные, ректальные или вагиноректальные мазки) следует инокулировать в селективный обогащенный бульон ( бульон Тодда Хьюитта с селективными антибиотиками), накопительную культуру. Это предполагает выращивание образцов в селективной обогащенной бульонной среде для повышения жизнеспособности GBS и одновременного снижения роста других встречающихся в природе бактерий. Подходящие обогащенные бульоны, имеющиеся в продаже, представляют собой бульоны Тодда-Хьюитта с гентамицином и налидиксовой кислотой (бульон Бейкера) или с колистином и налидиксовой кислотой (бульон Лима). [ 6 ] [ 7 ] После инкубации (18–24 часа, 35–37 °С) обогащенный бульон субкультивируют в течение ночи в чашках с кровяным агаром и GBS-подобными колониями (большие колонии диаметром 3–4 мм, окруженные узкой зоной гемолиза). [ 6 ] [ 7 ] идентифицируются с помощью теста CAMP или с помощью латекс-агглютинации с антисывороткой к GBS или MALDI-TOF. [ 6 ] [ 7 ] [ 12 ] [ 14 ]
В Великобритании этот метод описан в Стандартах микробиологических исследований Министерства здравоохранения Англии. [ 69 ]
После инкубации обогащенный бульон также можно пересеять на агар -среду Гранада , где GBS растет в виде розовато-красных колоний, и дальнейшие идентификационные тесты не требуются. [ 6 ] [ 9 ] [ 70 ] [ 71 ] После инкубации обогащенный бульон можно также пересеять на хромогенный агар, где СГБ растет в виде окрашенных колоний. [ 12 ] Тем не менее, GBS-подобные колонии, развивающиеся в хромогенной среде, должны быть подтверждены как GBS с использованием дополнительных надежных тестов во избежание ошибочной идентификации. [ 6 ]
Возможна непосредственная инокуляция вагинальных и ректальных мазков или вагиноректальных мазков в чашку с соответствующей культуральной средой (кровяной агар, среда Гранада или хромогенная среда). Однако этот метод (минуя этап селективного обогащенного бульона) может привести к некоторым ложноотрицательным результатам, и этот подход следует применять только в дополнение, а не вместо инокуляции в селективный бульон. [ 12 ]
Обнаружение колонизации GBS в Великобритании
[ редактировать ]Сегодня в Великобритании большинство лабораторий, обслуживающих Национальную службу здравоохранения, не предлагают обнаружение колонизации GBS с использованием метода обогащенного бульона. Однако реализация этого теста кажется жизнеспособным вариантом. В настоящее время посев на СГБ (с использованием обогащенной питательной среды) на сроке 35–37 недель для определения группы женщин из группы риска представляется наиболее экономически эффективной стратегией. [ 55 ] [ 56 ] Благотворительная организация Group B Strep Support опубликовала список больниц Великобритании, предлагающих выявление СГБ методом обогащения бульонной культуры (enrichment Culture Medium, ECM). [ 72 ] Этот тест также доступен в частном порядке по цене около 35 фунтов стерлингов за пакет для домашнего тестирования, и его предлагают частные клиники. [ 72 ] Тест также доступен в частном порядке для почтовой службы Великобритании. [ 73 ] [ 74 ]
Тестирование на месте оказания медицинской помощи, POCT
[ редактировать ]Ни один современный культуральный тест не является достаточно точным и быстрым, чтобы его можно было рекомендовать для выявления СГБ после начала родов. Покрытие образцов мазков требует времени для роста бактерий, а это означает, что его нельзя использовать в качестве теста во время родов (POCT или прикроватного тестирования). [ 14 ]
Быстро были разработаны альтернативные методы обнаружения GBS в клинических образцах (например, вагиноректальные мазки), такие как методы, основанные на тестах амплификации нуклеиновых кислот (NAAT), такие как тесты полимеразной цепной реакции (ПЦР) и зонды гибридизации ДНК . Эти тесты также можно использовать для обнаружения GBS непосредственно в бульонной среде после этапа обогащения, избегая пересева инкубированного накопительного бульона на соответствующую чашку с агаром. [ 6 ] [ 12 ] [ 75 ]
Тестирование женщин на колонизацию СГБ с использованием вагинальных или ректальных мазков и их культивирование в обогащенной среде не так быстро, как ПЦР-тест, который позволяет проверить, является ли беременная женщина носителем СГБ при родах. МААТ-тесты позволят начать ИАП при поступлении в родильное отделение у тех женщин, о которых неизвестно, являются ли они носителями СГБ. [ 12 ] NAAT для обнаружения носительства GBS, возможно, в будущем может быть достаточно точным, чтобы направлять IAP. Тем не менее, эта технология обнаружения СГБ должна быть улучшена и упрощена, чтобы сделать метод экономически эффективным и полностью полезным в качестве теста на месте оказания медицинской помощи .
По этой причине эти тесты до сих пор не могут заменить дородовой посев для точного выявления СГБ. [ 12 ] [ 14 ] [ 76 ] [ 77 ] POCT для выявления носителей GBS дополнительно требует, чтобы родильные отделения имели круглосуточное лабораторное оборудование, необходимое для проведения экспресс-тестирования. Тем не менее, тестирование на месте оказания медицинской помощи может использоваться для женщин, которые рожают с неизвестным статусом СГБ и без факторов риска, для подтверждения использования IAP. [ 14 ]
СГБ-бактериурия при беременности
[ редактировать ]Специальная группа профилактических служб США и ACOG рекомендуют проводить регулярный скрининг мочи всем беременным женщинам на ранних сроках беременности, даже при отсутствии симптомов мочеиспускания, для выявления бессимптомной бактериурии. Как и в случае с ИМП, любые случаи бессимптомной бактериурии (не только СГБ) с высокими значениями КОЕ/мл также вызывают пиелонефрит, низкую массу тела при рождении и преждевременные роды. [ 78 ] Следовательно, лечение этих бессимптомных случаев бактериурии антибиотиками на момент постановки диагноза так же важно, как и лечение симптоматических ИМП во время беременности, чтобы снизить эти риски. Помимо случаев GBS ИМВП и бессимптомной GBS-бактериурии с высоким содержанием КОЕ/мл, беременные женщины с бессимптомной GBS-бактериурией, даже с низким количеством КОЕ/мл, в любой момент беременности должны получать IAP для защиты новорожденного; независимо от результатов ректовагинального скрининга на более поздних сроках беременности. Это связано с тем, что бактериурия GBS, даже бессимптомная, при любом КОЕ/мл является признаком тяжелой аногенитальной колонизации. [ 14 ] [ 79 ]
Упущенные возможности профилактики неонатальных инфекций СГБ
[ редактировать ]Важными факторами успешной профилактики GBS-EOD с использованием IAP и универсального подхода скрининга являются: [ 80 ]
- Правильный сбор образцов
- Использование соответствующей процедуры для обнаружения GBS
- Администрирование правильного IAP для операторов GBS
- Охватить большинство беременных женщин дородовым скринингом
Большинство случаев GBS-EOD встречается у доношенных детей, рожденных от матерей с отрицательным результатом скрининга на колонизацию GBS, и у недоношенных детей, рожденных от матерей, которые не прошли скрининг, хотя некоторые ложноотрицательные результаты, наблюдаемые при скрининговых тестах на GBS, могут быть связаны с ограничениями теста. и к приобретению GBS между моментом скрининга и доставкой. Это показывает, что в некоторых условиях по-прежнему необходимы улучшения в методах сбора и обработки образцов для выявления СГБ. Ложноотрицательный скрининговый тест, а также неспособность получить IAP у женщин, родивших преждевременно с неизвестным статусом колонизации GBS, и назначение неподходящих агентов IAP женщинам с аллергией на пенициллин составляют большинство упущенных возможностей для предотвращения случаев GBS-EOD. [ 80 ] Инфекции GBS-EOD, возникающие у младенцев, чьи матери прошли скрининг на наличие отрицательной культуры GBS, вызывают особую тревогу и могут быть вызваны неправильным сбором образцов, задержкой в обработке образцов, неправильными лабораторными методами, недавним применением антибиотиков или колонизацией GBS после скрининга. было проведено. [ 50 ] [ 80 ] [ 81 ] [ 82 ] [ 83 ]
Домашние роды и роды в воде
[ редактировать ]Домашние роды становятся все более популярными в Великобритании и других странах. [ 84 ] [ 85 ] Рекомендации по профилактике инфекций СГБ у новорожденных такие же, как для домашних, так и для родов в больнице. Около 25% женщин, рожающих дома, вероятно, несут GBS во влагалище во время родов, не зная об этом, и может быть трудно правильно следовать рекомендациям IAP и бороться с риском тяжелой аллергической реакции на антибиотики за пределами больничных условий. . [ 86 ] Рекомендации RCOG и ACOG предполагают, что роды в бассейне не противопоказаны для носителей СГБ, которым была предложена соответствующая IAP, если нет других противопоказаний к погружению в воду. [ 14 ] [ 87 ]
Эпидемиология неонатальной инфекции GBS
[ редактировать ]Подсчитано, что в 2020 году во всем мире 19,7 миллиона беременных женщин имели ректовагинальную колонизацию GBS. А у 400 000 детей было выявлено неонатальное заболевание GBS, вызывающее 232 000 GBS-EOD, 162 000 GBS-LOD, а у 37 100 детей развились нарушения нервного развития. По оценкам, произойдет 90 000 смертей новорожденных, большинство из них в странах к югу от Сахары. [ 88 ] [ 89 ]
В 2000–2001 гг. зарегистрированная общая заболеваемость GBS-инфекцией у новорожденных в Великобритании составляла 0,72 на 1000 живорождений, 0,47 на 1000 для GBS-EOD и 0,25 на 1000 для GBS-LOD. Наблюдались очень заметные различия: заболеваемость в Шотландии составляла 0,42 на 1000, а в Северной Ирландии - 0,9 на 1000 живорождений. [ 90 ] [ 91 ] Тем не менее, это может быть серьезной недооценкой реальной заболеваемости СГБ-инфекцией у новорожденных. Правдоподобным объяснением этого является то, что у значительного числа младенцев с вероятным GBS-EOD были отрицательные результаты культурального исследования в результате предшествующего лечения матери антибиотиками, которые подавляют рост GBS в крови и культурах спинномозговой жидкости, но не маскируют клинические симптомы. [ 92 ] [ 93 ] Данные собирались проспективно для новорожденных, которым требовался септический скрининг в первые 72 часа. жизней в Великобритании в 2003 году, показало, что совокупный уровень определенной и вероятной инфекции GBS-EOD составил 3,6 на 1000 живорождений. [ 94 ] Другое исследование эпидемиологии инвазивных инфекций GBS в Англии и Уэльсе сообщило о росте заболеваемости GBS-EOD в период с 2000 по 2010 год с 0,28 до 0,41 на 1000 живорождений. Показатели GBS-LOD также увеличились в период с 1991 по 2010 год с 0,11 до 0,29 на 1000 живорождений в Англии и Уэльсе. [ 95 ]
В прошлом заболеваемость GBS-EOD колебалась от 0,7 до 3,7 на тысячу живорождений в США. [ 4 ] и от 0,2 до 3,25 на тысячу в Европе. [ 18 ] В 2008 году, после широкого использования дородового скрининга и интранатальной антибиотикопрофилактики, Центры по контролю и профилактике заболеваний в США сообщили о заболеваемости 0,28 случаев GBS-EOD на тысячу живорождений в США. С 2006 по 2015 год заболеваемость СГБ ЭОД снизилась с 0,37 до 0,23 на тысячу живорождений в США. [ 32 ] [ 96 ] В отличие от GBS-EOD, заболеваемость GBS-LOD оставалась стабильной в США и составляла 0,31 на 1000 живорождений с 2006 по 2015 год. [ 32 ] В 2021 году в США CDC сообщил о заболеваемости 0,21. на 1000 живорождений GBS-EOD и 0,23 на тысячу живорождений GBS-LOD. По оценкам, в 2021 году в США в общей сложности 1970 случаев смерти (0,59 на 100 000 населения) были вызваны неонатальными инфекциями, вызванными СГБ. [ 97 ] По оценкам, в 2021 году в США у 226 младенцев (49 на 100 000) была клинически значимая инфекция СГБ, и примерно 11 (2,4%) из этих случаев закончились смертью. [ 97 ]
В Испании заболеваемость вертикальным сепсисом СГБ снизилась на 73,6%, с 1,25/1000 живорождений в 1996 г. до 0,33/1000 в 2008 г. [ 98 ] В Испании в районе Барселоны в период с 2004 по 2010 год заболеваемость GBS-EOD составляла 0,29 на тысячу живых новорожденных без существенных различий по годам. Смертность составила 8,16%. [ 50 ] [ 99 ] Grupo de Hospitales Fundación Castrillo также сообщила в 2018 году в Испании, что частота GBS-EOD составила 0,17/1000 живорождений и 0,05/1000 GBS LOD. [ 100 ]

Во Франции с 2001 года также сообщалось о быстром снижении заболеваемости неонатальными инфекциями GBS после широкого использования IAP с 0,7 до 0,2 на 1000 родившихся в период с 1997 по 2006 год. Сообщается, что в 2011 году заболеваемость инфекциями GBS-EOD составила 0,2 на 1000 живорождений. [ 101 ] [ 102 ]
С 2012 года частота неонатальной инфекции GBS оценивается как 0,53 на 1000 рождений в европейском регионе, 0,67 в Америке и 0,15 в Австралазии. В странах, сообщивших об отсутствии использования IAP, частота случаев GBS-EOD была в 2,2 раза выше, чем в странах, сообщивших об использовании IAP. [ 31 ] [ 91 ]
Оценки заболеваемости GBS-EOD на 1000 рождений различаются в разных странах: Япония 0,09, Панама 0,58, Гонконг 0,76 и 2,35 в Доминиканской Республике. В целом, показатели самые высокие в Африке и самые низкие в Азии. По оценкам, глобальная заболеваемость LOD СГБ составляет 0,26 случаев на 1000 живорождений. [ 103 ]
Было подсчитано, что инфекции GBS ежегодно вызывают по меньшей мере 409 000 случаев заболевания матерей/плодов/младенцев и 147 000 мертворождений и младенческих смертей во всем мире. [ 104 ]
Ниже приведены оценки вероятности заражения ребенка неонатальной инфекцией GBS, если не будут приняты профилактические меры и отсутствуют другие факторы риска: [ 105 ]
- Один из 1000, когда женщина не является известным носителем СГБ.
- Один из 400, у которого женщина является носителем СГБ во время беременности.
- Одна из 300, у которой женщина носит СГБ при родах
- Один из 100, у которого предыдущий ребенок был инфицирован СГБ
Если женщине-носителю СГБ вводить IAP во время родов, риск для ребенка значительно снижается:
- Один из 8000, у которого мать является носителем СГБ во время беременности;
- Один из 6000, у которого мать носит СГБ при родах; и
- Один из 2200, у матери которого ранее был ребенок, инфицированный СГБ.
Рекомендации по профилактике неонатальных инфекций, вызванных СГБ
[ редактировать ]Великобритания
[ редактировать ]Королевский колледж акушеров и гинекологов (RCOG)
[ редактировать ]Королевский колледж акушеров и гинекологов (RCOG) впервые опубликовал свое Зеленое руководство № 36 «Профилактика раннего неонатального стрептококкового заболевания группы B» в 2003 году. В этом руководстве четко сказано: «Регулярное бактериологическое обследование всех беременных женщин на предмет дородового носительства СГБ не рекомендуется, а вагинальные мазки не следует брать во время беременности, если для этого нет клинических показаний». Но «если во время текущей беременности в вагинальном мазке обнаружен СГБ, следует предложить интранатальную антибиотикопрофилактику». [ нужна ссылка ] Руководство RCOG 2003 г. было пересмотрено в сентябре 2017 г. без существенных изменений. [ 39 ] В Великобритании RCOG по-прежнему не рекомендует бактериологический скрининг всех беременных женщин на предмет дородового носительства GBS в своих рекомендациях 2017 года, хотя и заявляет, что женщинам, у которых во время предыдущей беременности был положительный результат теста и ребенок был здоров, следует предложить возможность пройти тестирование. и им предлагается антимикробная профилактика во время родов или проведение IAP без тестирования. [ 87 ] Тем не менее, утверждается, что если носительство СГБ обнаружено случайно или при преднамеренном тестировании, женщинам следует предложить ИАП. И что всем беременным женщинам должна быть предоставлена соответствующая информационная брошюра о СГБ и беременности (опубликована в декабре 2017 г.). [ 106 ] Вместо этого к женщинам относятся в соответствии с риском родов. IAP предлагается роженицам, у которых в моче или вагинальных/ректальных мазках, взятых во время беременности, был обнаружен СГБ, а также женщинам, у которых ранее был ребенок с заболеванием СГБ. Немедленную индукцию родов и ВБД следует предложить всем женщинам с предродовым разрывом плодных оболочек на сроке 37 недель беременности и более, женщинам, у которых разрыв околоплодных вод произошел более чем через 18 часов, а также тем, у кого наблюдается лихорадка во время родов. [ нужна ссылка ] Женщинам с лихорадкой во время родов следует предложить антибиотики широкого спектра действия, включая антибиотик, подходящий для профилактики EOD-GBS. [ 87 ] Также было предложено тестирование беременных женщин для выявления носителей GBS и назначение IAP тем, кто носит GBS, и женщинам из группы высокого риска, и этот подход значительно более экономически эффективен, чем использование подхода с учетом факторов риска. В одной исследовательской работе подсчитана ожидаемая чистая выгода для правительства Великобритании от такого подхода в размере около 37 миллионов фунтов стерлингов в год по сравнению с нынешним подходом RCOG . [ 54 ] [ 55 ]
Рекомендации NICE
[ редактировать ]Великобритании Национальный институт здравоохранения и передового опыта (NICE) не рекомендует рутинное тестирование на СГБ, заявляя: «Беременным женщинам не следует предлагать рутинный дородовой скрининг на стрептококк группы B, поскольку доказательства его клинической и экономической эффективности остаются неопределенными». [ 107 ]
Это руководство было обновлено в 2021 году, однако скрининг и тестирование на СГБ вышли за рамки этого нового руководства. Однако в рекомендациях говорится, что «на первом дородовом приеме (и позже, если это необходимо) обсудите и предоставьте информацию об… инфекциях, которые могут повлиять на ребенка во время беременности или во время родов (например, стрептококк группы B, простой герпес и цитомегаловирус)» [ 108 ] Тем не менее, в рекомендациях NICE по неонатальным инфекциям говорится: «Предлагайте антибиотики во время родов женщинам, которые:
- у вас преждевременные роды или
- у вас есть колонизация стрептококков группы B, бактериурия или инфекция во время текущей беременности или
- у вас была колонизация стрептококков группы B, бактериурия или инфекция во время предыдущей беременности, и у вас не было отрицательного результата теста на стрептококк группы B с помощью накопительной культуры или ПЦР на образце ректовагинального мазка, взятого между 35 и 37 неделями беременности или 3-5 неделями до предполагаемой даты родов при текущей беременности или
- у предыдущего ребенка была инвазивная стрептококковая инфекция группы В или
- имеют клинический диагноз хориоамнионит. [2021] ». [ 109 ]
Национальный отборочный комитет
[ редактировать ]Текущая политическая позиция Национального скринингового комитета Великобритании в отношении СГБ такова: «скрининг не следует предлагать всем беременным женщинам. [ 110 ] Это решение подверглось резкой критике со стороны благотворительной организации Group B Strep Support как игнорирование как пожеланий общественности, так и роста заболеваемости GBS-инфекцией в Великобритании. [ 111 ]
Соединенные Штаты
[ редактировать ]Рекомендации по IAP для предотвращения перинатального СГБ были выпущены CDC в 1996 году. В этих рекомендациях было рекомендовано использование одного из двух методов профилактики: либо подхода, основанного на оценке риска, либо подхода, основанного на культуральном скрининге. [ 47 ] CDC выпустил обновленные рекомендации в 2002 году; в этих рекомендациях рекомендуется проводить универсальный культуральный скрининг всех беременных женщин на сроке беременности 35–37 недель для оптимизации выявления женщин, которые должны получать IAP. CDC также рекомендовал женщинам с неизвестным статусом колонизации GBS на момент родов лечиться в соответствии с наличием интранатальных факторов риска. Благодаря этой стратегии в США наблюдалось значительное снижение заболеваемости GBS-EOD. [ 112 ]
CDC снова выпустил обновленные рекомендации в 2010 году, однако основы профилактики в рекомендациях CDC 2010 года остались неизменными. [ 12 ] Ниже приведены основные дополнения к руководящим принципам 2010 года:
- Расширенные возможности лабораторного обнаружения СГБ включают использование пигментированных сред и ПЦР-анализов.
- Для лабораторий был установлен пересмотренный порог подсчета колоний для регистрации GBS в моче беременных женщин.
- Пересмотренные алгоритмы скрининга СГБ и использования ВБД у женщин с угрозой преждевременных родов включают один алгоритм для преждевременных родов и один для преждевременного преждевременного излития околоплодных вод.
- Рекомендации по препаратам IAP представлены в виде алгоритма с целью содействия использованию наиболее подходящего антибиотика у женщин с аллергией на пенициллин.
- В дозировку пенициллина были внесены незначительные изменения, чтобы облегчить внедрение в учреждениях с различными упакованными пенициллиновыми продуктами.
- Область применения алгоритма неонатального ведения была расширена и теперь применима ко всем новорожденным.
- Рекомендации по ведению зависят от клинического состояния новорожденного и других факторов риска, таких как хориоамнионит у матери, адекватность ВБД, если она показана матери, гестационный возраст и продолжительность разрыва мембраны.
- В алгоритм были внесены изменения, чтобы уменьшить количество ненужных обследований у новорожденных с хорошим внешним видом и относительно низким риском GBS-EOD.
В 2018 году задача по пересмотру и обновлению рекомендаций по профилактике СГБ была передана от CDC ACOG , Американской академии педиатрии , AAP и Американскому обществу микробиологии , ASM. [ 14 ] [ 113 ] В 2019 году комитет ACOG выпустил обновленный документ «Профилактика раннего заболевания, вызванного стрептококком группы B, у новорожденных». [ 14 ] Руководство ACOG заменило рекомендации 2010 года, опубликованные CDC. [ 12 ] Этот документ не вносит важных изменений в рекомендации CDC. Ключевыми мерами, необходимыми для предотвращения раннего развития неонатального СГБ, по-прежнему остаются универсальный пренатальный скрининг с использованием культуры СГБ из мазков, собранных из нижних отделов влагалища и прямой кишки, правильный сбор и микробиологическая обработка образцов, а также правильное проведение интранатальной антибиотикопрофилактики. Также важно отметить, что ACOG рекомендовала проводить универсальный скрининг на СГБ между 36 и 37 неделями беременности. Эта новая рекомендация предусматривает 5-недельное окно. [ 62 ] для действительных результатов посева, включая роды, произошедшие до гестационного возраста не менее 41 недели. В 2019 году Американская академия педиатрии (AAP) опубликовала новый клинический отчет «Ведение младенцев из группы риска неонатального заболевания СГБ». [ 22 ] Клинический отчет AAP заменяет рекомендации 2010 года, опубликованные CDC. [ 12 ] Американское общество микробиологии (ASM) опубликовало в 2021 году обновленные рекомендации по лабораторным процедурам обнаружения и идентификации ГБ. В этих новых руководящих принципах ASM культура по-прежнему остается основным моментом обнаружения СГБ. Учитывая, что надежный скрининговый тест важнее быстрого и менее точного результата. ASM также заявляет, что допустимо использовать идентификацию GBS на основе NAAT из обогащенного бульона (после 18-24-часовой инкубации) с высокой чувствительностью и что для проведения теста доступны коммерческие анализы, одобренные FDA. [ 8 ]
Однако проведение МАНК непосредственно из образца не рекомендуется из-за низкой чувствительности и высокой частоты ложноотрицательных результатов. [ 8 ] ACOG положительно относится к использованию МАНК и заявляет, что МАНК, полученные при тестировании на обогащенном бульоне, является разумным, имеет более высокую чувствительность для выявления СГБ, чем культуральное исследование, и, следовательно, возможно, является лучшим тестом. [ 14 ] Эта рекомендация основана на данных, доказывающих ценную полезность теста. [ 114 ] ACOG также позволяет использовать МАНК без обогащенного бульона. [ 14 ] несмотря на высокий уровень ложноотрицательных результатов, в качестве экспресс-теста POCT (по месту оказания медицинской помощи) для женщин, у которых роды неизвестны с неизвестным статусом GBS. Однако и ASM, и ACOG признают, что тестирование на основе NAAT не позволяет определить чувствительность к антибиотикам, необходимую для определения режима IAP, необходимого для женщин с аллергией на пенициллин. [ 8 ] [ 14 ]
Другие рекомендации
[ редактировать ]Национальные руководства большинства стран пропагандируют использование универсального скрининга беременных женщин на поздних сроках беременности для выявления носительства СГБ и использования ВБП у всех колонизированных матерей. например, Канада, [ 115 ] Испания, [ 116 ] Швейцария, [ 117 ] Германия, [ 118 ] Польша, [ 119 ] Чешская Республика, [ 120 ] Франция, [ 121 ] Бельгия, [ 122 ] Аргентина [ 123 ] и Колумбия [ 124 ]
Напротив, были выпущены руководящие принципы, основанные на факторах риска (в дополнение к рекомендациям Великобритании). [ 87 ] ) в Нидерландах, [ 125 ] Королевский колледж акушеров и гинекологов Австралии и Новой Зеландии рекомендует, чтобы все родильные отделения имели установленный план профилактики неонатального СГБ. Тем не менее, не рекомендуется однозначно использовать одну стратегию профилактики. [ 126 ]
Инфекция GBS у взрослых
[ редактировать ]СГБ также является важным инфекционным агентом, способным вызывать инвазивные инфекции у взрослых. Серьезные, опасные для жизни инвазивные инфекции GBS все чаще выявляются у пожилых людей и у людей, страдающих от основных заболеваний, таких как диабет, цирроз печени и рак. [ 103 ] [ 127 ] Инфекции GBS у взрослых включают инфекции мочевыводящих путей, инфекции кожи и мягких тканей ( инфекции кожи и структур кожи ), бактериемию без очага, остеомиелит, менингит и эндокардит . [ 3 ] Инфекция GBS у взрослых может быть серьезной, а смертность среди взрослых выше, чем среди новорожденных. [ 103 ]
В целом пенициллин является антибиотиком выбора для лечения инфекций, вызванных СГБ. Эритромицин или клиндамицин не следует использовать для лечения пациентов с аллергией на пенициллин, если не подтверждена чувствительность инфекционного изолята GBS к этим агентам. Гентамицин плюс пенициллин (для синергизма антибиотиков ) можно использовать у пациентов с опасными для жизни инфекциями GBS. [ 127 ] [ 128 ] [ 129 ]
Инвазивные инфекции, вызванные СГБ, у небеременных взрослых вызывают рост трудностей в большинстве развитых стран. Вакцинация для предотвращения заражения GBS может стать решающим подходом к предотвращению заболевания GBS у взрослых. [ 130 ] [ 131 ]
Синдром токсического шока (СТШ) — острое мультисистемное опасное для жизни заболевание, приводящее к полиорганной недостаточности. Тяжесть этого заболевания часто требует немедленного медицинского лечения. СТШ вызывают в первую очередь некоторые штаммы Staphylococcus aureus и Streptococcus pyogenes , которые продуцируют экзотоксины. Тем не менее, инвазивная инфекция СГБ может, хотя и довольно редко, осложняться стрептококковым токсическим шокоподобным синдромом (СТЛС). [ 132 ]
Вакцины для предотвращения инфекций GBS
[ редактировать ]Хотя введение национальных руководств по скринингу беременных женщин на носительство GBS и использование IAP значительно снизило бремя заболевания GBS-EOD, оно не оказало никакого влияния на предотвращение ни GBS-LOD у младенцев, ни инфекций GBS у взрослых. [ 133 ] По этой причине, если бы была доступна эффективная вакцина против СГБ, она стала бы эффективным средством борьбы не только с заболеванием СГБ у младенцев, но и с инфекциями у взрослых. [ 131 ]
Существует ряд проблем с назначением антибиотиков роженицам. Такие риски воздействия антибиотиков включали тяжелые аллергические реакции и трудности скрининга беременных женщин на СГБ. Если бы беременным женщинам можно было сделать вакцину против СГБ, это потенциально могло бы предотвратить большинство случаев СГБ без необходимости использования антибиотиков или скрининга. Вакцинация считается идеальным решением для предотвращения не только раннего и позднего начала заболевания, но и инфекций СГБ у взрослых, находящихся в группе риска. [ 134 ]
Разработка вакцины против СГБ для иммунизации матерей была определена Всемирной организацией здравоохранения в качестве приоритета из-за высоких неудовлетворенных потребностей. [ 135 ] [ 136 ] Эффективная по СГБ материнская вакцина может оказать большое влияние на заболеваемость и смертность новорожденных. Было подсчитано, что эта вакцина может предотвратить около 127 000 случаев GBS-EOD, 87 000 GBS-LOD, 31 000 случаев смерти и 18 000 случаев нарушений нервного развития. [ 137 ] Еще в 1976 году [ 29 ] Было показано, что низкие уровни материнских антител против капсульного полисахарида GBS коррелируют с чувствительностью к GBS-EOD и GBS-LOD. Материнские антитела, переданные от матери новорожденному, смогли обеспечить защиту младенцев от инфекции GBS. [ 138 ] Капсульный GBS полисахарид , который является важным фактором вирулентности, также является отличным кандидатом для разработки эффективной вакцины. [ 18 ] [ 138 ] [ 139 ] [ 140 ]
Вакцины на основе белка GBS также находятся в разработке и являются весьма многообещающими, поскольку они смогут защитить от инфекции GBS любого серотипа. [ 131 ] [ 141 ] [ 142 ] [ 143 ] [ 144 ] [ 145 ]
В настоящее время лицензирование вакцин против СГБ затруднено из-за сложности проведения клинических испытаний на людях из-за низкой заболеваемости неонатальных заболеваний СГБ. [ 18 ] [ 140 ] [ 146 ] Тем не менее, хотя исследования и клинические испытания по разработке эффективной вакцины для предотвращения инфекций GBS продолжаются, по состоянию на 2023 год вакцины не будет. [ 141 ] [ 144 ] [ 147 ] [ 148 ] [ 149 ] [ 150 ]
По состоянию на зиму 2023 года существуют две вакцины на стадии клинической разработки для профилактики инвазивного заболевания СГБ. Шестивалентная вакцина GBS от Pfizer [PF-06760805], GBS6 представляет собой конъюгированный полисахарид CRM197, содержащий 6 наиболее известных серотипов GBS во всем мире. [ 151 ] Вакцина, которая в настоящее время находится на этапе планирования фазы 3, может обеспечить значительную защиту от инвазивных заболеваний у новорожденных и детей раннего возраста на основании результатов ее иммуногенности в исследовании фазы 2 [NCT03765073], которые были опубликованы в Медицинском журнале Новой Англии. [ 148 ] Датская компания MinervaX ApS также разрабатывает белковую вакцину против GBS (GBS-NN/NN2), разработанную с использованием слияния высокоиммуногенных и защитных белковых доменов из выбранных поверхностных белков GBS (семейства альфа-подобных белков). [ 152 ] Вакцина, безопасность и иммуногенность которой доказана у материнского населения, также находится на стадии подготовки к планированию третьей фазы. MinervaX также завершила набор в исследование фазы 1 для взрослых [NCT05782179]; первые иммунологические результаты ожидаются в четвертом квартале 2023 года. Недавний анализ глобального спроса на вакцины против СГБ показал, что потенциальный рынок иммунизации матерей и взрослых против СГБ оценивается в 798 миллионов долларов в год. и 2023 миллиона долларов в год. в 2034 году соответственно. [ 153 ] Другие программы доклинической вакцинации против СГБ реализуют американские биотехнологические компании Omniose и Inventprise. [ нужна ссылка ]
Общество и культура
[ редактировать ]Июль был признан Международным месяцем осведомленности о стрептококке группы B. [ 154 ] время, когда распространяется информация о стрептококкене группы B, предназначенная для семей и медицинских работников, преимущественно в Великобритании и США. В Великобритании эту работу возглавляет Служба поддержки стрептококков группы B. [ 155 ]
Нечеловеческие инфекции GBS
[ редактировать ]СГБ был обнаружен у многих млекопитающих и других животных, таких как верблюды, собаки, кошки, тюлени, дельфины и крокодилы. [ 156 ]
Крупный рогатый скот
[ редактировать ]У крупного рогатого скота СГБ вызывает мастит – инфекцию вымени. Это может вызвать острое лихорадочное заболевание или подострое, более хроническое заболевание. Оба приводят к уменьшению выработки молока (отсюда и название: agalactiae, что означает «нет молока»). [ 157 ] СГБ может выживать и персистировать в молочных железах коров, образуя биопленки. [ 158 ] Мастит, связанный с СГБ, может оказывать важное влияние на количество и качество производимого молока, а также связан с повышенным количеством соматических клеток и общего количества бактерий в молоке. [ 159 ] Вспышки в стадах являются обычным явлением, и это имеет большое значение для молочной промышленности. [ 160 ] Программы по снижению воздействия СГБ применяются во многих странах. [ 157 ] Такие программы привели к почти полной ликвидации мастита у крупного рогатого скота, вызванного СГБ, в Великобритании, Северной Европе и Канаде. Тем не менее, в последние годы повторное появление мастита крупного рогатого скота, вызванного СГБ, наблюдалось в Северной Европе, что позволяет предположить внедрение человеческих линий в популяцию крупного рогатого скота вследствие обратной зоонозной передачи. [ 161 ]
Рыба
[ редактировать ]GBS также является важным патогеном для различных видов рыб, что приводит к серьезным экономическим потерям для многих видов рыб во всем мире. СГБ вызывает серьезные эпидемии среди выращиваемой рыбы, вызывая сепсис, а также внешние и внутренние кровотечения. Заражение GBS было зарегистрировано от диких и содержащихся в неволе рыб, и оно стало причиной эпизоотий во многих странах. [ 162 ] [ 163 ] [ 164 ] Вспышки СГБ в аквакультуре тилапии могут привести к серьезным заболеваниям со смертностью до 80%. [ 163 ] Сообщалось также о вспышке инвазивного заболевания человека пищевого происхождения, вызванного употреблением в пищу тилапии, инфицированной GBS. [ 163 ] Вакцины для защиты рыб от инфекций, вызванных СГБ, находятся в стадии разработки. [ 165 ] [ 166 ] [ 167 ]
Ссылки
[ редактировать ]- ^ Фрай Р.М. (1938). «Смертельные инфекции, вызванные гемолитическим стрептококком группы Б». Ланцет . 231 (5969): 199–201. дои : 10.1016/S0140-6736(00)93202-1 .
- ^ Эйкхофф Т.К., Кляйн Д.О., Дейли А.К., Ингалл Д., Финляндия М. (декабрь 1964 г.). «Неонатальный сепсис и другие инфекции, вызванные бета-гемолитическими стрептококками группы B». Медицинский журнал Новой Англии . 271 (24): 1221–1228. дои : 10.1056/NEJM196412102712401 . ПМИД 14234266 .
- ^ Перейти обратно: а б с д Эдвардс М.С., Бейкер С.Дж. (2010). Streptococcus agalactiae (стрептококк группы В). Манделл Г.Л., Беннетт Дж.Э., Долин Р. (ред.) Принципы и практика лечения инфекционных заболеваний. Том 2 (7-е изд.). Эльзевир. стр. Глава 202. ISBN 978-0-443-06839-3 .
- ^ Перейти обратно: а б с д и ж г час я дж к л Эдвардс М.С., Низет В. (2011). Стрептококковые инфекции группы В. Инфекционные болезни плода и новорожденного (7-е изд.). Эльзевир. стр. 419–469. ISBN 978-0-443-06839-3 .
- ^ Перейти обратно: а б Тилле П (2014). Диагностическая микробиология Бейли и Скотта (13-е изд.). Эльзевир. ISBN 978-0-323-08330-0 .
- ^ Перейти обратно: а б с д и ж г час я дж к л Роза-Фрайле М., Спеллерберг Б. (сентябрь 2017 г.). «Надежное выявление стрептококка группы В в клинической лаборатории» . Журнал клинической микробиологии . 55 (9): 2590–2598. дои : 10.1128/JCM.00582-17 . ПМЦ 5648696 . ПМИД 28659318 .
- ^ Перейти обратно: а б с д и ж г час Филкинс Л., Хаузер Дж.Р., Робинсон-Данн Б., Тиббетс Р., Боянтон Б.Л., Ревелл П. (декабрь 2020 г.). «Американское общество микробиологии предоставляет рекомендации на 2020 год по обнаружению и идентификации стрептококка группы B» . Журнал клинической микробиологии . 59 (1). дои : 10.1128/JCM.01230-20 . ПМЦ 7771461 . ПМИД 33115849 .
- ^ Перейти обратно: а б с д и ж «Руководство по обнаружению и идентификации стрептококка группы В» . АСМ.орг . Проверено 3 мая 2023 г.
- ^ Перейти обратно: а б Роза-Фрайле М., Родригес-Грейнджер Дж., Куэто-Лопес М., Сампедро А., Гэй Э.Б., Аро Х.М., Андреу А. (август 1999 г.). «Использование среды Гранады для выявления колонизации стрептококками группы В у беременных» . Журнал клинической микробиологии . 37 (8): 2674–2677. doi : 10.1128/JCM.37.8.2674-2677.1999 . ПМЦ 85311 . ПМИД 10405420 .
- ^ Бинхуай Л., Яньли С., Шучен З., Фэнся З., Донг Л., Яньчао С. (октябрь 2014 г.). «Использование масс-спектрометрии MALDI-TOF для быстрой идентификации стрептококка группы B на агаре chromID Strepto B» . Международный журнал инфекционных заболеваний . 27 : 44–48. дои : 10.1016/j.ijid.2014.06.023 . ПМИД 25220051 .
- ^ К.Н., Корнуэллу Э., Дэниелу Р., Гунесекере С., Яунейкайте Э., Чалкеру В., Ле Доаре К. (февраль 2019 г.). «Оценка времяпролетной масс-спектрометрии с матричной лазерной десорбцией и ионизацией (MALDI-TOF MS) для идентификации стрептококка группы B» . Исследовательские заметки BMC . 12 (1): 85. дои : 10.1186/s13104-019-4119-1 . ПМЦ 6376729 . ПМИД 30764872 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в Верани-младший, МакГи Л., Шраг С.Дж. (2010). «Профилактика перинатальной стрептококковой инфекции группы B: пересмотренные рекомендации CDC» (PDF) . Рекомендация MMWR. Представитель . 59 ((РР-10)): 1–32.
- ^ Эль Айла Н.А., Тенси И., Клейс Г., Саеренс Б., Кулс П., Верстрален Х. и др. (сентябрь 2010 г.). «Сравнение различных методов отбора проб и различных культуральных методов выявления носительства стрептококка группы В у беременных» . БМК Инфекционные болезни . 10 :285. дои : 10.1186/1471-2334-10-285 . ПМЦ 2956727 . ПМИД 20920213 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление «Профилактика раннего стрептококкового заболевания группы B у новорожденных: мнение комитета ACOG, номер 797» . Акушерство и гинекология . 135 (2): e51–e72. Февраль 2020 г. doi : 10.1097/AOG.0000000000003668 . ПМИД 31977795 . S2CID 210891255 .
- ^ Ролофф К., Степанян Г., Валенсуэла Г. (2018). «Распространенность колонизации ротоглотки стрептококком группы B у матерей, членов семьи и медицинских работников» . ПЛОС ОДИН . 13 (9): e0204617. Бибкод : 2018PLoSO..1304617R . дои : 10.1371/journal.pone.0204617 . ПМК 6161895 . ПМИД 30265687 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Рассел Нью-Джерси, Сил А.С., О'Дрисколл М., О'Салливан С., Бьянки-Джассир Ф., Гонсалес-Гуарин Дж. и др. (ноябрь 2017 г.). «Материнская колонизация стрептококками группы B и распространение серотипов во всем мире: систематический обзор и метаанализ» . Клинические инфекционные болезни . 65 (дополнение_2): S100–S111. дои : 10.1093/cid/cix658 . ПМЦ 5848259 . ПМИД 29117327 .
- ^ Перейти обратно: а б Баркайте Е, Бартусявичюс А, Тамелиен Р, Ключинскас М, Малецкене Л, Надисаускене Р (2008). «Распространенность материнской стрептококковой колонизации группы B в европейских странах» . Acta Obstetricia et Gynecologica Scandinavica . 87 (3): 260–271. дои : 10.1080/00016340801908759 . ПМИД 18307064 . S2CID 25897076 .
- ^ Перейти обратно: а б с д и ж Родригес-Грейнджер Дж., Альваргонсалес Х.К., Берарди А., Бернер Р., Кунце М., Хуфнагель М. и др. (сентябрь 2012 г.). «Возврат к профилактике стрептококковых заболеваний новорожденных, вызванных стрептококком группы B. Европейский проект DEVANI». Европейский журнал клинической микробиологии и инфекционных заболеваний . 31 (9): 2097–2104. дои : 10.1007/s10096-012-1559-0 . ПМИД 22314410 . S2CID 15588906 .
- ^ Мюллер А.Э., Оствогель П.М., Стигерс Э.А., Дорр П.Дж. (2016). «Заболеваемость, связанная с материнскими стрептококковыми инфекциями группы В» . Acta Obstetricia et Gynecologica Scandinavica . 85 (9): 1027–1037. дои : 10.1080/00016340600780508 . ПМИД 16929406 . S2CID 11745321 .
- ^ Каннингем Ф.Г., Левено К., Блум С., Спонг С., Дэш Дж., Хоффман Б., Кейси Б., Шеффилд Дж. (2014). Акушерство Виллиана (24-е изд.). МакГроу Хилл. ISBN 978-0-07-179894-5 .
- ^ Перейти обратно: а б Либстер Р., Эдвардс К.М., Левент Ф., Эдвардс М.С., Ренч М.А., Кастанини Л.А. и др. (июль 2012 г.). «Отдаленные исходы стрептококкового менингита группы В». Педиатрия . 130 (1): е8-15. дои : 10.1542/пед.2011-3453 . ПМИД 22689869 . S2CID 1013682 .
- ^ Перейти обратно: а б с д и ж Пуополо К.М., Линфилд Р., Каммингс Дж.Дж. (август 2019 г.). «Ведение младенцев из группы риска стрептококковой инфекции группы B» . Педиатрия . 144 (2): e20191881. дои : 10.1542/пед.2019-1881 . ПМИД 31285392 . S2CID 195843897 .
- ^ Перейти обратно: а б Раабе, Ванесса Н.; Шейн, Энди Л. (март 2019 г.). «Стрептококк группы В (Streptococcus agalactiae)» . Микробиологический спектр . 7 (2): 10.1128/microbiolspec.GPP3–0007–2018. doi : 10.1128/microbiolspec.GPP3-0007-2018 . ISSN 2165-0497 . ПМК 6432937 . ПМИД 30900541 .
- ^ Перейти обратно: а б с Бойер К.М., Готофф С.П. (1985). «Стратегии химиопрофилактики инфекций с ранним началом GBS1». Стратегии химиопрофилактики инфекций с ранним началом GBS . Антибиотики и химиотерапия. Том. 35. С. 267–280. дои : 10.1159/000410380 . ISBN 978-3-8055-3953-1 . ПМИД 3931544 .
- ^ Полин РА (май 2012 г.). «Ведение новорожденных с подозрением или доказанным бактериальным сепсисом с ранним началом» . Педиатрия . 129 (5): 1006–1015. дои : 10.1542/пед.2012-0541 . ПМИД 22547779 . S2CID 230591 .
- ^ Мартинес Э., Минтеги С., Вилар Б., Мартинес М.Дж., Лопес А., Катедиано Э., Гомес Б. (май 2015 г.). «Распространенность и предикторы бактериального менингита у детей раннего возраста с лихорадкой без источника». Журнал детских инфекционных заболеваний . 34 (5): 494–498. doi : 10.1097/inf.0000000000000629 . ПМИД 25461476 . S2CID 43717212 .
- ^ Рассел Нью-Джерси, Сил А.С., О'Салливан С., Ле Доар К., Хит П.Т., Лоун Дж.Э. и др. (ноябрь 2017 г.). «Риск раннего неонатального стрептококкового заболевания группы B с материнской колонизацией во всем мире: систематический обзор и метаанализ» . Клинические инфекционные болезни . 65 (дополнение_2): S152–S159. дои : 10.1093/cid/cix655 . ПМК 5850448 . ПМИД 29117325 .
- ^ Доби Н., Чамех М., Мелин П., Слогроув А.Л., Гётгебуер Т. (2016). «Повышенный риск инвазивной инфекции, вызванной стрептококком группы B , у ВИЧ-инфицированных, но неинфицированных младенцев: обзор данных и возможных механизмов» . Границы в иммунологии . 7 : 505. дои : 10.3389/fimmu.2016.00505 . ПМК 5110531 . ПМИД 27899925 .
- ^ Перейти обратно: а б Бейкер С.Дж., Каспер Д.Л. (апрель 1976 г.). «Корреляция дефицита материнских антител с восприимчивостью к неонатальной стрептококковой инфекции группы B». Медицинский журнал Новой Англии . 294 (14): 753–756. дои : 10.1056/nejm197604012941404 . ПМИД 768760 .
- ^ Бейкер С.Дж., Эдвардс М.С., Каспер Д.Л. (октябрь 1981 г.). «Роль антител к нативному полисахариду типа III стрептококка группы B в детской инфекции». Педиатрия . 68 (4): 544–549. дои : 10.1542/педс.68.4.544 . ПМИД 7033911 . S2CID 38905874 .
- ^ Перейти обратно: а б Эдмонд К.М., Корцалиудаки С., Скотт С., Шраг С.Дж., Заиди А.К., Казенс С., Хит П.Т. (февраль 2012 г.). «Стрептококковая инфекция группы B у детей младше 3 месяцев: систематический обзор и метаанализ» . Ланцет . 379 (9815): 547–556. дои : 10.1016/s0140-6736(11)61651-6 . ПМИД 22226047 . S2CID 15438484 .
- ^ Перейти обратно: а б с Нандури С.А., Пети С., Смелзер С., Апостол М., Олден Н.Б., Харрисон Л.Х. и др. (март 2019 г.). «Эпидемиология инвазивных стрептококковых заболеваний группы B с ранним и поздним началом в США, 2006–2015 гг.: Лабораторный и популяционный надзор в нескольких штатах» . JAMA Педиатрия . 173 (3): 224–233. doi : 10.1001/jamapediatrics.2018.4826 . ПМК 6439883 . ПМИД 30640366 .
- ^ Лин Ф.Ю., Вейсман Л.Е., Троендл Дж., Адамс К. (июль 2003 г.). «Недоношенность является основным фактором риска позднего начала заболевания, вызванного стрептококком группы В» . Журнал инфекционных болезней . 188 (2): 267–271. дои : 10.1086/376457 . ПМИД 12854082 .
- ^ Карампатсас К., Дэвис Х., Минарек М., Эндрюс Н., Хит П.Т., Ле Доар К. (2022). «Клинические факторы риска, связанные с поздним инвазивным стрептококковым заболеванием группы B: систематический обзор и метаанализ» . Клин Инфекционный Дис . 75 (7): 1255–1264. дои : 10.1093/cid/ciac206 . ПМЦ 9525091 . ПМИД 35275986 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Бойер К.М., Гадзала К.А., Келли П.Д., Готофф С.П. (ноябрь 1983 г.). «Селективная интранатальная химиопрофилактика неонатального стрептококкового заболевания группы В с ранним началом. III. Прерывание передачи инфекции от матери ребенку». Журнал инфекционных болезней . 148 (5): 810–816. дои : 10.1093/infdis/148.5.810 . ПМИД 6355318 .
- ^ Лин Ф.Ю., Бреннер Р.А., Джонсон Ю.Р., Азими П.Х., Филипс Дж.Б., Риган Дж.А. и др. (май 2001 г.). «Эффективность интранатальной химиопрофилактики, основанной на оценке риска, для профилактики стрептококковой инфекции группы В у новорожденных с ранним началом». Американский журнал акушерства и гинекологии . 184 (6): 1204–1210. дои : 10.1067/моб.2001.113875 . ПМИД 11349189 .
- ^ де Куэто М., Санчес М.Дж., Сампедро А., Миранда Х.А., Эррусо А.Дж., Роза-Фрайар М. (январь 1998 г.). «Время введения ампициллина во время родов и профилактика вертикальной передачи стрептококка группы B». Акушерство и гинекология 91 (1): 112–114. дои : 10.1016/s0029-7844(97) 00587-5 ПМИД 9464732 . S2CID 43765652 .
- ^ Берарди А, Росси С, Биазини А, Миннити С, Вентурелли С, Феррари Ф, Факкинетти Ф (апрель 2011 г.). «Эффективность интранатальной химиопрофилактики продолжительностью менее 4 часов». Журнал медицины матери, плода и новорожденных . 24 (4): 619–625. дои : 10.3109/14767058.2010.511347 . ПМИД 20828241 . S2CID 6697604 .
- ^ Перейти обратно: а б «Профилактика раннего неонатального стрептококкового заболевания группы B: Зеленое руководство № 36» . БЖОГ . 124 (12): е280–е305. Ноябрь 2017 г. doi : 10.1111/1471-0528.14821 . ПМИД 28901693 . S2CID 32700635 .
- ^ Десаи С.Х., Каплан М.С., Чен К., Мэйси Э.М. (2017). «Заболеваемость беременных женщин, связанная с неподтвержденной аллергией на пенициллин, применением антибиотиков и инфекциями, вызванными стрептококком группы B» . Журнал «Перманенте» . 21 :16–080. дои : 10.7812/TPP/16-080 . ПМЦ 5363897 . ПМИД 28333608 .
- ^ Бхаттачарья С. (январь 2010 г.). «Факты об аллергии на пенициллин: обзор» . Журнал передовых фармацевтических технологий и исследований . 1 (1): 11–17. дои : 10.4103/2231-4040.70513 . ПМЦ 3255391 . ПМИД 22247826 .
- ^ Балтимор Р.С., Хьюи С.М., Мик Дж.И., Шучат А., О'Брайен К.Л. (ноябрь 2001 г.). «Ранний неонатальный сепсис в эпоху профилактики стрептококка группы B». Педиатрия . 108 (5): 1094–1098. дои : 10.1542/педс.108.5.1094 . ПМИД 11694686 .
- ^ Саткин Г., Крон М.А., Гейне Р.П., Свит Р.Л. (март 2005 г.). «Антибиотикопрофилактика и неонатальный сепсис, вызванный стрептококком не группы B». Акушерство и гинекология . 105 (3): 581–586. дои : 10.1097/01.aog.0000153492.30757.2f . ПМИД 15738028 . S2CID 22019440 .
- ^ Шраг С.Дж., Хадлер Дж.Л., Арнольд К.Е., Мартелл-Клири П., Рейнгольд А., Шучат А. (август 2006 г.). «Факторы риска инвазивных инфекций, вызванных Escherichia coli, с ранним началом в эпоху широкого применения антибиотиков во время родов». Педиатрия . 118 (2): 570–576. дои : 10.1542/пед.2005-3083 . ПМИД 16882809 . S2CID 34908773 .
- ^ Катленд К.Л., Мадхи С.А., Зелл Э.Р., Куванда Л., Лак М., Грум М. и др. (декабрь 2009 г.). «Хлоргексидиновые салфетки для влагалища матери и тела новорожденного при сепсисе и вертикальной передаче патогенных бактерий в Южной Африке: рандомизированное контролируемое исследование». Ланцет . 374 (9705): 1909–1916. дои : 10.1016/S0140-6736(09)61339-8 . ПМИД 19846212 . S2CID 23418670 .
- ^ Олссон А., Шах против, Стаде BC (декабрь 2014 г.). «Вагинальный хлоргексидин во время родов для предотвращения ранней неонатальной стрептококковой инфекции группы В» . Кокрановская база данных систематических обзоров . 12 (12): CD003520. дои : 10.1002/14651858.CD003520.pub3 . ПМЦ 11262555 . ПМИД 25504106 .
- ^ Перейти обратно: а б Центр по контролю и профилактике заболеваний (1996). «Профилактика перинатальной стрептококковой инфекции группы B: взгляд на общественное здравоохранение» . ММВР . 45-РР7: 1–24.
- ^ Клиффорд В., Гарланд С.М., Гримвуд К. (сентябрь 2012 г.). «Профилактика неонатальной стрептококковой инфекции группы В в 21 веке». Журнал педиатрии и здоровья детей . 48 (9): 808–815. дои : 10.1111/j.1440-1754.2011.02203.x . ПМИД 22151082 . S2CID 36906520 .
- ^ Шраг С.Дж., Зелл Э.Р., Линфилд Р., Рум А., Арнольд К.Е., Крейг А.С. и др. (июль 2002 г.). «Популяционное сравнение стратегий профилактики стрептококковой инфекции группы B с ранним началом у новорожденных» . Медицинский журнал Новой Англии . 347 (4): 233–239. дои : 10.1056/nejmoa020205 . ПМИД 12140298 .
- ^ Перейти обратно: а б с Хименес М., Санфелиу I, Сьерра М. и др. (2015). «[Стрептококковый неонатальный сепсис группы B с ранним началом в районе Барселоны (2004-2010 гг.). Анализ упущенных возможностей профилактики]». Инфекционные болезни и клиническая микробиология . 33 (7): 446–450. дои : 10.1016/j.eimc.2014.10.015 . ПМИД 25541009 . S2CID 196362631 .
- ^ Хоканссон С., Аксемо П., Бремме К. и др. (январь 2008 г.). «Носительство стрептококка группы B в Швеции: национальное исследование факторов риска колонизации матери и ребенка» . Acta Obstetricia et Gynecologica Scandinavica . 87 (1): 50–58. дои : 10.1080/00016340701802888 . ПМИД 18158627 . S2CID 38090766 .
- ^ Фарес К.Р., Линфилд Р., Фарли М.М., Моле-Боэтани Дж., Харрисон Л.Х., Пети С. и др. (май 2008 г.). «Эпидемиология инвазивного стрептококка группы B в США, 1999-2005 гг.» . ДЖАМА . 299 (17): 2056–2065. дои : 10.1001/jama.299.17.2056 . ПМИД 18460666 .
- ^ Ле Доар К., О'Дрисколл М., Тернер К., Сидат Ф. (2017). «Стратегия интранатальной химиопрофилактики антибиотиками для профилактики стрептококковой инфекции группы B во всем мире: систематический обзор» . Клин Инфекционный Дис . 65 (Приложение 2): с143-151. дои : 10.1093/cid/cix654 . ПМЦ 5850619 . ПМИД 29117324 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б Колборн Т., Ассебург С., Бойке Л., Филипс З., Клакстон К., Адес А.Е., Гилберт Р.Э. (август 2007 г.). «Стратегии пренатального скрининга и лечения для предотвращения стрептококковых инфекций группы B и других бактериальных инфекций в раннем детстве: экономическая эффективность и ожидаемая ценность информационного анализа» . Оценка технологий здравоохранения . 11 (29): 1–226, iii. дои : 10.3310/hta11290 . ПМИД 17651659 .
- ^ Перейти обратно: а б с Колборн Т.Э., Ассебург С., Бойке Л., Филипс З., Велтон Н.Дж., Клакстон К. и др. (сентябрь 2007 г.). «Стратегии профилактики стрептококковых инфекций группы B и других бактериальных инфекций в раннем детстве: экономическая эффективность и ценность информационного анализа» (PDF) . БМЖ . 335 (7621): 655. doi : 10.1136/bmj.39325.681806.AD . ЧВК 1995477 . ПМИД 17848402 .
- ^ Перейти обратно: а б Каамбва Б., Брайан С., Грей Дж., Милнер П., Дэниелс Дж., Хан К.С., Робертс Т.Е. (декабрь 2010 г.). «Экономическая эффективность быстрых тестов и других существующих стратегий скрининга и лечения стрептококка группы B с ранним началом во время родов» . БЖОГ . 117 (13): 1616–1627. дои : 10.1111/j.1471-0528.2010.02752.x . ПМИД 21078057 . S2CID 25561127 .
- ^ Верьяно С., Эмблтон Н., Коллинсон А., Менсон Э., Рассел А.Б., Хит П. (январь 2010 г.). «Упущенные возможности предотвращения заражения стрептококком группы В». Архив болезней в детстве. Издание для плода и новорожденного . 95 (1): Ф72–Ф73. дои : 10.1136/adc.2009.160333 . ПМИД 19439431 . S2CID 38297857 .
- ^ Стир Пи Джей, Пламб Джей (октябрь 2011 г.). «Миф: Стрептококковая инфекция группы В во время беременности: постигнута и побеждена». Семинары по фетальной и неонатальной медицине . 16 (5): 254–258. дои : 10.1016/j.siny.2011.03.005 . ПМИД 21493170 .
- ^ Сигел Дж. Д., Cushion NB (май 1996 г.). «Профилактика стрептококковой инфекции группы B с ранним началом: еще один взгляд на однократное введение пенициллина при рождении». Акушерство и гинекология . 87 (5, часть 1): 692–698. дои : 10.1016/0029-7844(96)00004-x . ПМИД 8677068 . S2CID 40716699 .
- ^ Велафи С., Сигел Дж.Д., Вендел Г.Д., Кушон Н., Ид В.М., Санчес П.Дж. (март 2003 г.). «Раннее начало стрептококковой инфекции группы B после комбинированной стратегии химиопрофилактики стрептококка группы B у матери и новорожденного». Педиатрия . 111 (3): 541–547. дои : 10.1542/педс.111.3.541 . ПМИД 12612234 .
- ^ Вудгейт П., Фленади В., Стир П. (2004). «Внутримышечное введение пенициллина для профилактики раннего развития стрептококковой инфекции группы В у новорожденных» . Кокрановская база данных систематических обзоров . 2004 (3): CD003667. дои : 10.1002/14651858.CD003667.pub2 . ПМК 9029842 . ПМИД 15266494 .
- ^ Перейти обратно: а б Янси М.К., Шучат А., Браун Л.К., Вентура В.Л., Маркенсон Г.Р. (ноябрь 1996 г.). «Точность поздних антенатальных скрининговых культур в прогнозировании колонизации генитальных стрептококков группы B при родах». Акушерство и гинекология . 88 (5): 811–815. дои : 10.1016/0029-7844(96)00320-1 . ПМИД 8885919 .
- ^ Валкенбург-ван ден Берг А.В., Хаутман-Рулофсен Р.Л., Оствогель П.М., Деккер Ф.В., Дорр П.Дж., Сприй А.Дж. (2010). «Время проведения скрининга на стрептококк группы B во время беременности: систематический обзор». Гинекологическое и акушерское обследование . 69 (3): 174–183. дои : 10.1159/000265942 . ПМИД 20016190 . S2CID 26709882 .
- ^ Прайс Д., Шоу Э., Ховард М., Зазулак Дж., Уотерс Х., Качоровски Дж. (декабрь 2006 г.). «Самостоятельный отбор проб на стрептококк группы B у женщин на сроке от 35 до 37 недель беременности является точным и приемлемым: рандомизированное перекрестное исследование». Журнал акушерства и гинекологии Канады . 28 (12): 1083–1088. дои : 10.1016/s1701-2163(16)32337-4 . ПМИД 17169231 .
- ^ Хикс П., Диас-Перес М.Дж. (2009). «Самостоятельный сбор пациенткой образцов стрептококка группы B во время беременности» (PDF) . Журнал Американского совета семейной медицины . 22 (2): 136–140. дои : 10.3122/jabfm.2009.02.080011 . ПМИД 19264936 . S2CID 2208746 .
- ^ Арья А., Крайан Б., О'Салливан К., Грин Р.А., Хиггинс-младший (июль 2008 г.). «Мазки из половых органов, собранные самостоятельно и медицинским работником, для выявления распространенности стрептококка группы B: сравнение предпочтений и эффективности пациентов». Европейский журнал акушерства, гинекологии и репродуктивной биологии . 139 (1): 43–45. дои : 10.1016/j.ejogrb.2007.12.005 . ПМИД 18255214 .
- ^ Одубамово К., Гарсия М., Муриити Ф., Оголла Р., Дэниелс Дж. П., Уокер К. Ф. (2023). «Мазк, собранный самостоятельно, в сравнении с мазком, взятым медицинским работником для выявления вагинально-ректальной колонизации стрептококком группы B на поздних сроках беременности: систематический обзор» . Eur J Obstet Gynecol Reprod Biol . 286 : 95–101. дои : 10.1016/j.ejogrb.2023.05.027 . ПМИД 37229964 . S2CID 258860996 . Проверено 27 ноября 2023 г.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Роза-Фрайле М., Камачо-Муньос Э., Родригес-Грейнджер Х., Лиебана-Мартос К. (февраль 2005 г.). «Хранение образцов в транспортной среде и обнаружение стрептококков группы В культуральным путем» . Журнал клинической микробиологии . 43 (2): 928–930. doi : 10.1128/jcm.43.2.928-930.2005 . ПМК 548104 . ПМИД 15695709 .
- ^ Правительство Великобритании (26 июня 2018 г.). «СМИ Б 58: выявление носительства стрептококков группы В. Обновлено 2018 г.» . Проверено 28 февраля 2021 г.
- ^ Хиль Э.Г., Родригес М.К., Бартоломе Р., Берхано Б., Каберо Л., Андреу А. (август 1999 г.). «Оценка агаровой пластинки Гранады на выявление вагинальных и ректальных стрептококков группы В у беременных» . Журнал клинической микробиологии . 37 (8): 2648–2651. doi : 10.1128/JCM.37.8.2648-2651.1999 . ПМЦ 85303 . ПМИД 10405415 .
- ^ Клейс Г., Вершреген Г., Теммерман М. (январь 2001 г.). «Модифицированная агаровая среда Гранада для выявления носительства стрептококка группы В у беременных» . Клиническая микробиология и инфекции . 7 (1): 22–24. дои : 10.1046/j.1469-0691.2001.00156.x . ПМИД 11284939 .
- ^ Перейти обратно: а б Где я могу пройти тест ECM? «Тестирование ЕСМ» . Поддержка стрептококка группы B. Проверено 22 ноября 2023 г.
- ^ «Скрининговый тест на стрептококк группы В» . Медисэйв ЮК Лтд . Проверено 20 ноября 2023 г.
- ^ «Тестирование на стрептококк группы В» . Лаборатория врачей . Архивировано из оригинала 4 марта 2016 года . Проверено 20 ноября 2021 г.
- ^ Бьюкен Б.В., Фарон М.Л., Фуллер Д., Дэвис Т.Э., Мейн Д., Ледебур Н.А. (февраль 2015 г.). «Многоцентровая клиническая оценка анализа Xpert GBS LB для обнаружения стрептококка группы B в образцах пренатального скрининга» . Журнал клинической микробиологии . 53 (2): 443–448. дои : 10.1128/jcm.02598-14 . ПМЦ 4298547 . ПМИД 25411176 .
- ^ Коливер-Брандл Х., Нил А., Бирри Дж., Сакс М., Циммерманн Р., Збинден Р., Балсайт Д. (2023). «Оценка двух быстрых коммерческих тестов для обнаружения Streptococcus agalactiae из вагинальных образцов» . Acta Obstet Gynecol Scand . 102 (4): 450–456. дои : 10.1111/aogs.14519 . ПМЦ 10008276 . ПМИД 36772902 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Дэниелс Дж., Грей Дж., Паттисон Х., Робертс Т., Эдвардс Э., Милнер П. и др. (сентябрь 2009 г.). «Быстрое тестирование на стрептококк группы В во время родов: исследование точности теста с оценкой приемлемости и экономической эффективности» . Оценка технологий здравоохранения . 13 (42): 1–154, iii–iv. дои : 10.3310/hta13420 . ПМИД 19778493 .
- ^ Оуэнс Д.К., Дэвидсон К.В., Крист А.Х., Барри М.Дж., Кабана М., Коги А.Б. и др. (сентябрь 2019 г.). «Скрининг бессимптомной бактериурии у взрослых: Рекомендательное заявление Целевой группы профилактических служб США» . ДЖАМА . 322 (12): 1188–1194. дои : 10.1001/jama.2019.13069 . ПМИД 31550038 . S2CID 202746652 .
- ^ Смайлл, Фиона М.; Васкес, Хуан К. (25 ноября 2019 г.). «Антибиотики при бессимптомной бактериурии у беременных» . Кокрановская база данных систематических обзоров . 2019 (11): CD000490. дои : 10.1002/14651858.CD000490.pub4 . ПМЦ 6953361 . ПМИД 31765489 .
- ^ Перейти обратно: а б с Пулвер Л.С., Хопфенбек М.М., Янг П.С., Стоддард Г.Дж., Коргенски К., Дейли Дж., Байингтон К.Л. (январь 2009 г.). «Продолжение стрептококковых инфекций группы B с ранним началом в эпоху интранатальной профилактики» . Журнал перинатологии . 29 (1): 20–25. дои : 10.1038/jp.2008.115 . ПМИД 18704032 .
- ^ Мелин П. (сентябрь 2011 г.). «Неонатальная стрептококковая инфекция группы В: от патогенеза к профилактической стратегии» . Клиническая микробиология и инфекции . 17 (9): 1294–1303. дои : 10.1111/j.1469-0691.2011.03576.x . ПМИД 21672083 .
- ^ Берарди А., Лугли Л., Барончиани Д., Росси С., Чичча М., Крети Р. и др. (февраль 2010 г.). «Раннее начало заболевания, вызванного стрептококком группы B, в Эмилии-Романье: обзор после внедрения подхода, основанного на скрининге». Журнал детских инфекционных заболеваний . 29 (2): 115–121. дои : 10.1097/inf.0b013e3181b83cd9 . ПМИД 19915512 . S2CID 31548613 .
- ^ Шраг С.Дж., Верани-младший (август 2013 г.). «Интранатальная антибиотикопрофилактика для профилактики перинатальной стрептококковой инфекции группы B: опыт США и значение для потенциальной стрептококковой вакцины группы B» . Вакцина . 31 (Приложение 4): D20–D26. doi : 10.1016/j.vaccine.2012.11.056 . ПМИД 23219695 .
- ^ Гиллен П., Бамидел О., Хили М. (2023). «Систематический обзор опыта женщин по планированию домашних родов в консультации с поставщиками услуг по охране материнства в странах со средним и высоким уровнем дохода» . Акушерство . 124 . дои : 10.1016/j.midw.2023.103733 . ПМИД 37307778 . Проверено 3 июля 2024 г.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Уиттингтон-младший, Гаремани Т., Уитэм М., Филлипс А.М., Спрэчер Б.Н., Маганн Э.Ф. (2023). «Альтернативные стратегии рождения» . Int J Женское здоровье . 15 : 1151–1159. дои : 10.2147/IJWH.S405533 . ПМЦ 10368118 . ПМИД 37496517 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ ПОДДЕРЖКА СТРЕП ГРУППЫ Б. «Часто задаваемые вопросы35. Вынашивание СГБ и домашние роды?» . Проверено 4 марта 2021 г.
- ^ Перейти обратно: а б с д «Профилактика раннего неонатального стрептококкового заболевания группы B: Зеленое руководство № 36» . БЖОГ . 124 (12): е280–е305. Ноябрь 2017 г. doi : 10.1111/1471-0528.14821 . ПМИД 28901693 . S2CID 32700635 .
- ^ Гонсалвес Б.П., Проктер С.Р., Пол П., Чандна Дж., Левин А. (2022). «Инфекция стрептококком группы B во время беременности и младенчества: оценки регионального и глобального бремени» . Ланцет Глоб Здоровье . 10 (6): е807–е819. дои : 10.1016/S2214-109X(22)00093-6 . ПМК 9090904 . ПМИД 35490693 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Прома П., Гонсалвес Б.П., Ле Доар К., Лоун Э. (2023). «20 миллионов беременных женщин с носительством стрептококка группы В: последствия, проблемы и возможности профилактики» . Курр Опин Педиатр . 35 (2): 223–230. дои : 10.1097/MOP.0000000000001223 . ПМЦ 9994794 . ПМИД 36749143 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Хит П.Т., Бальфур Г., Вейснер А.М., Эфстратиу А., Ламаньи Т.Л., Тайг Х. и др. (январь 2004 г.). «Стрептококковая инфекция группы B у младенцев в возрасте до 90 дней в Великобритании и Ирландии». Ланцет . 363 (9405): 292–294. дои : 10.1016/s0140-6736(03)15389-5 . ПМИД 14751704 . S2CID 22371160 .
- ^ Перейти обратно: а б Ле Доар К., Хит PT (август 2013 г.). «Обзор глобальной эпидемиологии СГБ». Вакцина . 31 (Приложение 4): D7-12. doi : 10.1016/j.vaccine.2013.01.009 . ПМИД 23973349 .
- ^ Бригцен А.К., Якобсен А.Ф., Деди Л., Мелби К.К., Фугельсет Д., Уайтлоу А. (2015). «Материнская колонизация стрептококком группы B связана с увеличением количества младенцев, переводимых в отделение интенсивной терапии новорожденных». Неонатология . 108 (3): 157–163. дои : 10.1159/000434716 . ПМИД 26182960 . S2CID 24711146 .
- ^ Карбонелл-Эстрани X, Фигерас-Алой Дж, Сальседо-Абизанда С, де ла Роза-Фрайле М (март 2008 г.). «Вероятный стрептококковый неонатальный сепсис группы B с ранним началом: серьезное клиническое состояние, связанное с внутриутробной инфекцией». Архив болезней в детстве. Издание для плода и новорожденного . 93 (2): Ф85–Ф89. дои : 10.1136/adc.2007.119958 . ПМИД 17704105 . S2CID 10300571 .
- ^ Лак С., Торни М., д'Агапеев К., Питт А., Хит П., Брейнак А., Рассел А.Б. (июнь 2003 г.). «Предполагаемое стрептококковое заболевание новорожденных группы B с ранним началом». Ланцет . 361 (9373): 1953–1954. дои : 10.1016/S0140-6736(03)13553-2 . ПМИД 12801740 . S2CID 33025300 .
- ^ Ламаньи Т.Л., Кешишян С., Эфстратиу А., Гай Р., Хендерсон К.Л., Бротон К., Шеридан Э. (сентябрь 2013 г.). «Новые тенденции в эпидемиологии инвазивной стрептококковой инфекции группы B в Англии и Уэльсе, 1991-2010 гг.» . Клинические инфекционные болезни . 57 (5): 682–688. дои : 10.1093/cid/cit337 . ПМИД 23845950 .
- ^ Бейкер CJ (август 2013 г.). «Спектр перинатальной стрептококковой инфекции группы В». Вакцина . 31 (Приложение 4): D3–D6. doi : 10.1016/j.vaccine.2013.02.030 . ПМИД 23973344 .
- ^ Перейти обратно: а б Центры по контролю и профилактике заболеваний. «Отчет о базовом наблюдении за активными бактериями, Сеть программ по новым инфекциям, стрептококк группы B, 2021 г.» (PDF) . Центры по контролю и профилактике заболеваний. 2021 . Проверено 17 ноября 2023 г.
- ^ Лопес Састре Дж., Фернандес Коломер Б., Кото Коталло Хиль Д. и др. (Группа больниц Кастрилло) (2009 г.). «Неонатальный сепсис вертикальной передачи. Эпидемиологическое исследование Grupo de Hospitales Castrillo» . Раннее развитие человека . 85 (10): С100. дои : 10.1016/j.earlhumdev.2009.08.049 .
- ^ Андреу А., Санфелиу И., Виньяс Л., Барранко М., Бош Дж., Допико Е. и др. (апрель 2003 г.). «[Снижение заболеваемости перинатальной стрептококковой инфекцией группы B (Барселона, 1994–2002 гг.). Связь с политикой больничной профилактики]». Инфекционные болезни и клиническая микробиология . 21 (4): 174–179. дои : 10.1016/s0213-005x(03)72913-9 . ПМИД 12681128 .
- ^ Роза-Фрайле М, Алос Дж.И. (2022). «Неонатальные инфекции, вызванные стрептококком группы B, текущая история». Энферм Инфекк Микробиол Клин . 40 (7): 349–352. doi : 10.1016/j.eimce.2022.01.002 . ПМИД 35906029 .
- ^ Альбуи-Ллати М., Надо С., Декомб Э., Пьер Ф., Мижо В. (август 2012 г.). «Улучшение перинатального скрининга на стрептококк группы B с помощью показателей процесса». Журнал оценки в клинической практике . 18 (4): 727–733. дои : 10.1111/j.1365-2753.2011.01658.x . ПМИД 21414110 .
- ^ Сикиас П., Биран В., Фуа-Л'Элиас Л., Пленверт С., Буало П., Бонакорси С.; Исследовательская группа ЭОС. (2022). «Ранний неонатальный сепсис в районе Парижа: популяционное эпиднадзорное исследование с 2019 по 2021 год» . Arch Dis Детский Фетальный Неонатальный . 108 (2): 114–120. doi : 10.1136/archdischild-2022-324080 . ПМЦ 9985718 . ПМИД 35902218 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б с Раабе В.Н., Шейн А.Л. (март 2019 г.). группы В « Стрептококк ( Streptococcus agalactiae )» . Микробиологический спектр . 7 (2). doi : 10.1128/microbiolspec.GPP3-0007-2018 . ПМК 6432937 . ПМИД 30900541 .
- ^ Сил А.С., Бьянки-Джассир Ф., Рассел Н.Дж., Кохли-Линч М., Танн С.Дж., Холл Дж. и др. (ноябрь 2017 г.). «Оценки бремени стрептококковой инфекции группы B во всем мире для беременных женщин, мертворожденных и детей» . Клинические инфекционные болезни . 65 (дополнение_2): С200–С219. дои : 10.1093/cid/cix664 . ПМК 5849940 . ПМИД 29117332 .
- ^ Бенитц В.Е., Гулд Дж.Б., Друзин М.Л. (июнь 1999 г.). «Факторы риска стрептококкового сепсиса группы B с ранним началом: оценка отношения шансов на основе критического обзора литературы» . Педиатрия . 103 (6): е77. дои : 10.1542/peds.103.6.e77 . ПМИД 10353974 .
- ^ РКОГ-ГБСС. «Информация для вас. Стрептококк группы В (СГБ) у беременных и новорожденных» (PDF) . Проверено 2 декабря 2023 г.
- ^ Скрининг на инфекции.1.8.9 Стрептококк группы В (26 марта 2008 г.). «Дородовой уход при неосложненной беременности. Рекомендации NICE [CG62]: март 2008 г.» . NICE Национальный институт передового опыта в области здравоохранения и ухода . Проверено 27 ноября 2019 г. .
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ «Рекомендации | Дородовая помощь | Руководство | NICE» . www.nice.org.uk. 19 августа 2021 г. Проверено 21 мая 2022 г.
- ^ «Рекомендации | Неонатальные инфекции: антибиотики для профилактики и лечения | Руководство | NICE» . www.nice.org.uk. 20 апреля 2021 г. Проверено 21 мая 2022 г.
- ^ Национальный отборочный комитет Великобритании. «Текущий СНБ Великобритании от Национального отборочного комитета Великобритании (НКНС Великобритании)» . Проверено 4 марта 2021 г.
- ^ «Ведущий детский благотворительный фонд опустошен решением не вводить спасательный скрининг беременных женщин. 2012» . кампания-archive2.com . Проверено 4 марта 2021 г.
- ^ Центры по контролю и профилактике заболеваний – CDC, MMWR (2002). «Пересмотренные рекомендации CDC по профилактике перинатальной стрептококковой инфекции группы B. 2002» . Еженедельный отчет о заболеваемости и смертности . 51-РР11: 1–22 . Проверено 4 марта 2021 г.
- ^ CDC. «Руководство по профилактике. Обновление рекомендаций 2019 года» . Проверено 4 марта 2021 г.
- ^ Кутюрье Б.А., Вес Т, Элмер Х., Шлаберг Р. (сентябрь 2014 г.). Кэрролл К.С. (ред.). «Дородовой скрининг на стрептококк группы B с помощью трех молекулярных тестов, одобренных FDA, и влияние сокращенной накопительной культуры на уровень молекулярного обнаружения» . Журнал клинической микробиологии . 52 (9): 3429–3432. дои : 10.1128/JCM.01081-14 . ПМЦ 4313176 . ПМИД 25009049 .
- ^ Деньги Д., Аллен В.М. (август 2018 г.). "Н тот стрептококковой инфекции гинекологии Канады – и акушерства . Журнал группы Профилактика ранней неонатальной » 298 B S2CID 51980587 .
- ^ Алос Кортес Х.И., Андреу Доминго А., Аррибас Мир Л., Каберо Роура Л., Куэто Лопес М., Лопес Састре Дж. и др. (март 2012 г.). «[Профилактика перинатальной стрептококковой инфекции группы B. Обновленные испанские рекомендации, 2012 г.]» (PDF) . Испанский журнал химиотерапии . 25 (1): 79–88. ПМИД 22488547 . Проверено 25 ноября 2019 г.
- ^ Комиссия по обеспечению качества Швейцарского общества гинекологии и акушерства (2007). «[Профилактика неонатальной инфекции стрептококком группы Б. Экспертная переписка № 19 от 29 декабря 2006 г.]». Гинеколого-акушерский осмотр . 47 (2): 103–104. дои : 10.1159/000100342 . ПМИД 17440274 . S2CID 77887846 .
- ^ «Профилактика неонатального сепсиса - ранней формы, вызванного стрептококками группы B» (PDF) . Проверено 25 ноября 2023 г.
- ^ Котарски Ю., Хечко П.Б., Лаутербах Р., Немец Т., Лещиньска-Горзелак Б. (2008). «Рекомендации Польского гинекологического общества по выявлению носителей СГБ у беременных и профилактике инфекций у новорожденных .] (PDF) . Гинеколь Пол (на польском языке). 79 : 221–223.
- ^ Мечурова А, Влк Р, Унзейтиг В, Швиховец П, Машата Дж (2013). «Диагностика и лечение стрептококков группы В во время беременности и родов – рекомендуемая процедура» [Диагностика и лечение стрептококков группы В во время беременности и родов – рекомендуемая процедура.] (PDF) . Чешский гинеколог. (на чешском языке). 78 : 11–14.
- ^ профилактика риска ранней неонатальной бактериальной инфекции» « Антенатальная (PDF) . и оценки здоровья ( Национальное агентство аккредитации на французском языке). 2001 . Проверено 2 марта 2021 г.
- ^ Бельгийский совет здравоохранения. «Профилактика перинатальных стрептококковых инфекций группы В. Рекомендации. 2003 г.» (PDF) . Архивировано из оригинала (PDF) 4 марта 2016 года . Проверено 25 ноября 2023 г.
- ^ «Работа теста на выявление стрептококка Agalactiae группы B у всех беременных женщин со сроком беременности от 35 до 37 недель» (на испанском языке). 2008 год . Проверено 27 ноября 2023 г.
- ^ «Резолюция 3280» (PDF) (на испанском языке). 2018 . Проверено 27 ноября 2023 г.
- ^ «Профилактика неонатального стрептококкового заболевания группы B (GBS-болезнь), версия 2.0» [Профилактика неонатального стрептококкового заболевания группы B (GBS-болезнь), версия 2.0] (PDF) . Голландская ассоциация акушерства и гинекологии на ( голландском языке). Мед-Инфо. 2008 год . Проверено 25 ноября 2019 г.
- ^ Королевский колледж акушеров и гинекологов Австралии и Новой Зеландии. РАНЦКОГ. «Стрептококк (GBS) при беременности: скрининг и лечение. Июль 2019 г.» (PDF) . Проверено 25 ноября 2023 г.
- ^ Перейти обратно: а б Скофф Т.Х., Фарли М.М., Пети С., Крейг А.С., Шаффнер В., Гершман К. и др. (июль 2009 г.). «Увеличение бремени инвазивного стрептококкового заболевания группы B у небеременных взрослых, 1990-2007 гг.» . Клинические инфекционные болезни . 49 (1): 85–92. дои : 10.1086/599369 . ПМИД 19480572 .
- ^ Фарли М.М. (август 2001 г.). «Стрептококковая инфекция группы B у небеременных взрослых» . Клинические инфекционные болезни . 33 (4): 556–561. дои : 10.1086/322696 . ПМИД 11462195 .
- ^ Эдвардс М.С., Бейкер С.Дж. (сентябрь 2005 г.). «Стрептококковые инфекции группы В у пожилых людей» . Клинические инфекционные болезни . 41 (6): 839–847. дои : 10.1086/432804 . ПМИД 16107984 .
- ^ Коллин С.М., Шетти Н., Ламаньи Т. (2020). «Инвазивные стрептококковые инфекции группы B у взрослых, Англия, 2015–2016 гг.» . Экстренное заражение Dis . 26 (6): 1174–1181. дои : 10.3201/eid2606.191141 . ПМЦ 7258460 . ПМИД 32441619 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б с Граукс Э., Хайтс М., Мартини Д., Майяр Э., Дельфорж М., Мелин П., Доби Н. (март 2021 г.). «Инвазивный стрептококк группы B среди небеременных взрослых в Брюссельском столичном регионе, 2005–2019 гг.» . Европейский журнал клинической микробиологии и инфекционных заболеваний . 40 (3): 515–523. дои : 10.1007/s10096-020-04041-0 . ПМК 7498195 . ПМИД 32944894 .
- ^ Аль Ахрасс Ф., Абдалла Л., Бергер С., Ханна Р., Рейнольдс Н., Томпсон С. и др. (январь 2013 г.). «Синдром токсического шока Streptococcus agalactiae: два описания случаев и обзор литературы» . Лекарство . 92 (1): 10–14. дои : 10.1097/MD.0b013e31827dea11 . ПМК 5370747 . ПМИД 23263717 .
- ^ Джордан Х.Т., Фарли М.М., Крейг А., Моле-Боэтани Дж., Харрисон Л.Х., Пети С. и др. (декабрь 2008 г.). «Возврат к необходимости вакцинопрофилактики стрептококковой инфекции группы B у новорожденных с поздним началом: популяционный анализ в нескольких штатах» . Журнал детских инфекционных заболеваний . 27 (12): 1057–1064. дои : 10.1097/inf.0b013e318180b3b9 . ПМИД 18989238 . S2CID 1533957 .
- ^ Эдвардс М.С., Ренч М.А., Ринаудо К.Д., Фаббрини М., Тускано Г., Баффи Г. и др. (ноябрь 2016 г.). «Иммунные ответы на инвазивную стрептококковую болезнь группы B у взрослых» . Новые инфекционные заболевания . 22 (11): 1877–1883. дои : 10.3201/eid2211.160914 . ПМК 5088039 . ПМИД 27767008 .
- ^ Всемирная организация здравоохранения. «Вакцина против стрептококка группы B: полная оценка вакцины» (PDF) . Проверено 6 июля 2024 г.
- ^ Всемирная организация здравоохранения. «Техническая дорожная карта исследований и разработок вакцины GBS и характеристики предпочтительного продукта ВОЗ» . Архивировано из оригинала 22 апреля 2017 года . Проверено 26 ноября 2023 г.
- ^ Проктер С.Р., Гонсалвес Б.П., Пол П., Чандна Дж., Сидат Ф., Кукунари А., Хутубесси Р., Троттер С., Лоун Дж.Э., Джит М. (2023). «Материнская иммунизация против стрептококка группы B: глобальный анализ воздействия на здоровье и экономической эффективности» . ПЛОС Мед . 20 (3): e1004068. дои : 10.1371/journal.pmed.1004068 . ПМЦ 10013922 . ПМИД 36917564 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б Бейкер С.Дж., Кэри В.Дж., Ренч М.А., Эдвардс М.С., Хиллер С.Л., Каспер Д.Л., Платт Р. (март 2014 г.). «Материнские антитела при родах защищают новорожденных от раннего начала стрептококковой инфекции группы B» . Журнал инфекционных болезней . 209 (5): 781–788. дои : 10.1093/infdis/jit549 . ПМЦ 3923540 . ПМИД 24133184 .
- ^ Мадхи С.А., Катленд С.Л., Хосе Л., Коэн А., Говендер Н., Виттке Ф. и др. (август 2016 г.). «Безопасность и иммуногенность исследуемой материнской трехвалентной вакцины против стрептококка группы B у здоровых женщин и их детей: рандомизированное исследование фазы 1b/2». «Ланцет». Инфекционные болезни . 16 (8): 923–934. дои : 10.1016/S1473-3099(16)00152-3 . ПМИД 27139805 .
- ^ Перейти обратно: а б Эдвардс М.С., Гоник Б. (август 2013 г.). «Профилактика широкого спектра перинатальной заболеваемости и смертности посредством вакцинации против стрептококка группы В». Вакцина . 31 (Приложение 4): D66–D71. doi : 10.1016/j.vaccine.2012.11.046 . ПМИД 23200934 .
- ^ Перейти обратно: а б Хит PT (июнь 2016 г.). «Состояние исследований вакцин и разработки вакцин против СГБ» . Вакцина . 34 (26): 2876–2879. doi : 10.1016/j.vaccine.2015.12.072 . ПМИД 26988258 .
- ^ Сон JY, Лим JH, Лим С, Ён Z, Со HS (2018). «Прогресс в создании вакцины против стрептококка группы B» . Человеческие вакцины и иммунотерапия . 14 (11): 2669–2681. дои : 10.1080/21645515.2018.1493326 . ПМК 6314413 . ПМИД 29995578 .
- ^ Гупалова Т, Леонтьева Г, Крамская Т, Грабовская К, Бормотова Е, Коржевский Д, Суворов А (2018). «Разработка экспериментальной вакцины GBS для иммунизации слизистых оболочек» . ПЛОС ОДИН . 13 (5): e0196564. Бибкод : 2018PLoSO..1396564G . дои : 10.1371/journal.pone.0196564 . ПМЦ 5935385 . ПМИД 29727446 .
- ^ Перейти обратно: а б Каррерас-Абад К., Рамхелавон Л., Хит П.Т., Ле Доар К. (2020). «Вакцина против стрептококка группы B : последние достижения» . Инфекции и устойчивость к лекарствам . 13 : 1263–1272. дои : 10.2147/IDR.S203454 . ПМЦ 7196769 . ПМИД 32425562 . Проверено 26 ноября 2023 г.
- ^ Домингес К., Рэндис ТМ. (2022). «На пути к разработке белковой вакцины против стрептококка группы В» . Cell Rep Med . 3 (2): 10.1016/j.xcrm.2022.100536. дои : 10.1016/j.xcrm.2022.100536 . ПМК 8861943 . ПМИД 35243427 .
- ^ Нуччителли А, Ринаудо КД, Майоне Д (май 2015 г.). «Вакцина против стрептококка группы В: современное состояние» . Терапевтические достижения в области вакцин . 3 (3): 76–90. дои : 10.1177/2051013615579869 . ПМК 4530403 . ПМИД 26288735 .
- ^ Дэвис Х.Г., Каррерас-Абад К., Ле Доар К., Хит П.Т. (июнь 2019 г.). «Стрептококк группы B: испытания и невзгоды» . Журнал детских инфекционных заболеваний . 38 (6S, Приложение 1): S72–S76. дои : 10.1097/INF.0000000000002328 . ПМИД 31205250 . S2CID 189943251 . Проверено 26 ноября 2023 г.
- ^ Перейти обратно: а б Мадхи С.А. (июнь 2023 г.). «Возможность введения матери вакцин против стрептококка группы B у младенцев» . Медицинский журнал Новой Англии . 389 (3): 215–227. дои : 10.1056/NEJMoa2116045 . ПМИД 37467497 . S2CID 259995252 .
- ^ Абсалон Дж., Саймон Р., Рэдли Д., Джардина П.С., Кури К., Янсен К.У., Андерсон А.С. (2022). «Достижения в области лицензирования материнской вакцины для профилактики инвазивного заболевания, вызванного стрептококком группы B, у младенцев: обсуждение различных подходов» . Хум Вакцина Иммунотер . 18 (1): 2037350. дои : 10.1080/21645515.2022.2037350 . ПМК 9009955 . ПМИД 35240933 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Троттер К.Л., Олдерсон М., Дангор З., Ип М., Ле Доар К., Накабембе Э., Проктер С.Р., Секикубо М., Ламбах П. (2023). «Профиль ценности вакцины для стрептококка группы B» . Вакцина . 41 : Приложение 2: S41-S52. doi : 10.1016/j.vaccine.2023.04.024 . ПМИД 37951694 . Проверено 7 июля 2024 г.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Буурман ET (июнь 2019 г.). «Новая шестивалентная капсульная полисахаридная конъюгированная вакцина (GBS6) для профилактики неонатальных стрептококковых инфекций группы B путем иммунизации матери» . J Заразить Дис . 220 (1): 105–115. дои : 10.1093/infdis/jiz062 . ПМК 6548902 . ПМИД 30778554 .
- ^ Корпоративный веб-сайт MinervaX https://www.MinervaX.com/MinervaX-provides-clinical-update-on-its-maternal-gbs-vaccine/
- ^ «MarketVIEW: Вакцины против стрептококка группы B» . Вакцинная аналитика . Проверено 26 ноября 2023 г.
- ^ Поддержка стрептококков группы B (GBSS) (24 июня 2019 г.). «Главная»Принимайте участие»Кампания»Месяц осведомленности о стрептококке группы B» . Проверено 23 ноября 2023 г.
- ^ «Главная страница» . Поддержка стрептококка группы B.
- ^ Деланной С.М., Крамлиш М., Фонтейн М.С., Поллок Дж., Фостер Г., Даглиш М.П. и др. (февраль 2013 г.). «Человеческие штаммы Streptococcus agalactiae у водных млекопитающих и рыб» . БМК Микробиология . 13:41 . дои : 10.1186/1471-2180-13-41 . ПМЦ 3585737 . ПМИД 23419028 .
- ^ Перейти обратно: а б Киф GP (июль 1997 г.). «Мастит, вызванный Streptococcus agalactiae: обзор» . Канадский ветеринарный журнал . 38 (7): 429–437. ПМЦ 1576741 . ПМИД 9220132 .
- ^ Ченг В.Н., Хан С.Г. (2020). «Мастит крупного рогатого скота: факторы риска, терапевтические стратегии и альтернативные методы лечения – обзор» . Азиатско-Австралазийский журнал зоотехники . 33 (11): 1699–1713. дои : 10.5713/ajas.20.0156 . ПМК 7649072 . ПМИД 32777908 .
- ^ Рюгг PL (декабрь 2017 г.). «100-летний обзор: выявление, лечение и профилактика мастита» . Журнал молочной науки . 100 (12): 10381–10397. дои : 10.3168/jds.2017-13023 . ПМИД 29153171 . S2CID 6122209 . Проверено 26 ноября 2023 г.
- ^ Моралес-Убальдо А.Л., Риверо-Перес Н., Валладарес-Карранса Б., Веласкес-Ордоньес В., Дельгадильо-Руис Л., Сарагоса-Бастида А. (2023). «Мастит крупного рогатого скота, всемирное заболевание: распространенность, устойчивость к противомикробным препаратам и жизнеспособные альтернативные подходы» . Ветеринарная анимация . 21 : 100306. doi : 10.1016/j.vas.2023.100306 . ПМЦ 10400929 . ПМИД 37547227 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Крестани С., Форд Т.Л., Лисетт С.Дж., Холмс М.А., Фаст С., Перссон-Уоллер К., Задокс Р.Н. (2021). «Падение и рост стрептококка группы B среди молочного скота: реинтродукция из-за скачка хозяина от человека к крупному рогатому скоту?» . Микробная геномика . 7 (9): 000648. doi : 10.1099/mgen.0.000648 . ПМЦ 8715428 . ПМИД 34486971 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Эванс Дж.Дж., Клезиус П.Х., Пасник Дж.Дж., Бонсак Дж.Ф. (май 2009 г.). «Человеческий изолят Streptococcus agalactiae из нильской тилапии (Oreochromis niloticus)» . Новые инфекционные заболевания . 15 (5): 774–776. дои : 10.3201/eid1505.080222 . ПМК 2687030 . ПМИД 19402966 .
- ^ Перейти обратно: а б с Продовольственная и сельскохозяйственная организация Объединенных Наций. «ПРОФИЛЬ РИСКА Streptococcus группы B (GBS) Streptococcus agalactiae последовательности типа (ST) 283 у пресноводных рыб» (PDF) . Проверено 26 ноября 2023 г.
- ^ Лю Г, Чжан В, Лу С (ноябрь 2013 г.). «Сравнительный геномный анализ Streptococcus agalactiae показывает, что изоляты из культивируемой тилапии в Китае тесно связаны с человеческим штаммом A909» . БМК Геномика . 14 :775. дои : 10.1186/1471-2164-14-775 . ПМЦ 3831827 . ПМИД 24215651 .
- ^ Ли Л.П., Ван Р., Лян В.В., Хуан Т., Хуан Ю., Луо Ф.Г. и др. (август 2015 г.). «Разработка живой аттенуированной вакцины Streptococcus agalactiae для тилапии путем непрерывного пассажа in vitro». Иммунология рыб и моллюсков . 45 (2): 955–963. Бибкод : 2015FSI....45..955L . дои : 10.1016/j.fsi.2015.06.014 . ПМИД 26087276 .
- ^ Чжан Д., Гао Ю, Ли Ц, Кэ Х, Лю Цз, Лу М, Ши С (март 2020 г.). «Эффективная живая аттенуированная вакцина против инфекции Streptococcus agalactiae у выращиваемой нильской тилапии (Oreochromis niloticus)». Иммунология рыб и моллюсков . 98 : 853–859. Бибкод : 2020FSI....98..853Z . дои : 10.1016/j.fsi.2019.11.044 . ПМИД 31751658 . S2CID 208226408 .
- ^ Томпсон К.Д., Родхум С., Банной А., Тангсунан П., Китиёдом С., Шугар Йоставорнкул Дж., Ята Т., Пирарат Н. (2023). «Решение стратегии нановакцины для тилапии » Вакцина . 11 8):1356.doi : ( 10.3390/vaccines11081356 . ПМК 10459980 . ПМИД 37631924 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )