Пептидная вакцина
Синтетические вакцины на основе пептидов ( эпитопные вакцины ) представляют собой субъединичные вакцины, изготовленные из пептидов . Пептиды имитируют эпитопы антигена , вызывающего прямой или мощный иммунный ответ. [1] Пептидные вакцины могут не только обеспечивать защиту от инфекционных патогенов и неинфекционных заболеваний, но также использоваться в качестве терапевтических противораковых вакцин , где пептиды из опухолеассоциированных антигенов используются для индукции эффективного противоопухолевого Т-клеточного ответа . [2]
История [ править ]
Традиционные вакцины представляют собой цельные живые или фиксированные возбудители. Вакцины второго поколения представляют собой преимущественно белок, очищенный от возбудителя. Третье поколение вакцин представляет собой ДНК или плазмиду, способную экспрессировать белки возбудителя. Пептидные вакцины являются последним шагом в эволюции вакцин. [3]
Преимущества и недостатки [ править ]
По сравнению с традиционными вакцинами, такими как цельные фиксированные патогены или белковые молекулы, пептидные вакцины имеют ряд преимуществ и недостатков. [4]
Преимущества:
- Вакцины полностью синтезируются методом химического синтеза и могут рассматриваться как химические соединения .
- Благодаря более совершенному твердофазному синтезу пептидов (SPPS) с использованием автоматических и микроволновых методов производство пептидов становится более эффективным.
- Вакцины не имеют биологического загрязнения, поскольку они синтезированы химическим путем.
- Вакцины водорастворимы и могут сохранять стабильность в простых условиях.
- Пептиды могут быть специально разработаны для обеспечения специфичности. Одна пептидная вакцина может быть разработана так, чтобы иметь несколько эпитопов для генерации иммунных ответов на несколько заболеваний.
- Вакцины содержат только короткую пептидную цепь, поэтому они менее склонны вызывать аллергические или аутоиммунные реакции.
Недостатки:
- Плохая иммуногенность.
- Нестабилен в клетках.
- Отсутствие нативной конформации .
- Эффективен только для ограниченной группы населения.
дизайн Эпитопный
Цельная пептидная вакцина должна имитировать эпитоп антигена, поэтому дизайн эпитопа является наиболее важным этапом разработки вакцины и требует точного понимания аминокислотной последовательности интересующего иммуногенного белка. Ожидается, что разработанный эпитоп вызовет сильный и долговременный иммуноответ против патогена. При разработке эпитопа следует учитывать следующие моменты:
- Недоминантный эпитоп может вызывать более сильный иммунный ответ, чем доминантный эпитоп. Бывший. Антитела людей, инфицированных нематодой, могут распознавать доминантный эпитоп антигена, называемый белком Necator americanus APR-1, но антитела не могут индуцировать защиту от анкилостомоза . Однако другие недоминантные эпитопы белка APR-1 демонстрируют способность индуцировать выработку нейтрализующих антител против анкилостомоза. Следовательно, недоминантные эпитопы являются лучшими кандидатами для пептидных вакцин против инфекции анкилостомоза. [5]
- Учитывайте гиперчувствительность . Бывший. Некоторые IgE -индуцирующие эпитопы вызывают гиперчувствительности реакции после вакцинации у людей из-за перекрытия с эпитопами IgG в белке Na-ASP-2, который является антигеном анкилостомоза. [6]
- Некоторые короткие пептидные эпитопы нуждаются в удлинении для сохранения нативной конформации. Удлиненные последовательности могут включать правильную вторичную структуру . Кроме того, некоторые короткие пептиды можно стабилизировать или циклизировать вместе для поддержания правильной конформации. Бывший. Эпитопы В-клеток могли содержать только 5 аминокислот. Чтобы вызвать иммунный ответ, используется последовательность дрожжевого белка GCN4 для улучшения конформации пептидных вакцин путем формирования альфа-спирали . [7]
- Используйте адъюванты, связанные с эпитопом, для индукции иммунного ответа. [8]
Приложения [ править ]
Рак [ править ]
- Вакцина с пептидом Gp100 изучается для лечения меланомы . Для создания более сильного ответа CTL in vitro пептид gp100:209-217(210M) модифицируется и связывается с HLA-A2*0201. После вакцинации большее количество циркулирующих Т-клеток может распознавать и уничтожать раковые клетки меланомы in vitro . [10]
- Риндопепимут — это пептидная вакцина, полученная из рецептора эпидермального фактора роста (EGFR), для лечения мультиформной глиобластомы (GBM). 14-мерный пептид связан с гемоцианином улитки улитки (KLH), который может снизить риск развития рака. [11]
- E75, GP2 и AE37 — это три разные HER2/ neu, монопептидные вакцины, полученные из для лечения рака молочной железы. HER2/neu обычно имеет низкую экспрессию в здоровых тканях. Е75, состоящий из 9 аминокислот, является иммунодоминантным эпитопом белка HER2. Субдоминантным эпитопом является GP2, состоящий из 9 аминокислот. И E75, и GP2 стимулируют CD8+ лимфоциты , но GP2 имеет более низкое сродство, чем E75. AE37 стимулирует CD4+ лимфоциты . [12]
Другие распространенные заболевания
- EpiVacCorona — вакцина против COVID-19 на основе пептидов .
- IC41 является кандидатом на пептидную вакцину против С. вируса гепатита Он состоит из пяти синтетических пептидов и синтетического адъюванта, называемого поли-L-аргинином. [13]
- Мультимерик-001 является наиболее эффективной кандидатной пептидной вакциной против гриппа . Он содержит эпитопы В- и Т-клеток гемагглютинина . Матрица I и нуклеопротеин объединены в один рекомбинантно экспрессируемый полипептид. [14] [15]
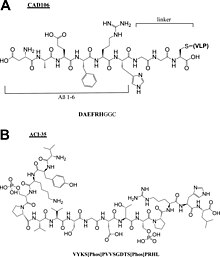
- Пептидные вакцины против болезни Альцгеймера : CAD106, [16] УБ311, [17] Лу, AF20513, [18] АБвак40, [19] АКИ-35, [20] ААДвак-1. [21]
Ссылки [ править ]
- ^ Скварчинский М, Тот I (февраль 2016 г.). «Синтетические вакцины на основе пептидов» . Химическая наука . 7 (2): 842–854. дои : 10.1039/C5SC03892H . ПМЦ 5529997 . ПМИД 28791117 .
- ^ Мелиф С.Дж., ван дер Бург С.Х. (май 2008 г.). «Иммунотерапия установленных (пред) злокачественных заболеваний с помощью синтетических длинных пептидных вакцин». Обзоры природы. Рак . 8 (5): 351–360. дои : 10.1038/nrc2373 . ПМИД 18418403 . S2CID 205468352 .
- ^ Шнебле Э., Клифтон Г.Т., Хейл Д.Ф., Peoples GE (2016). «Стратегия вакцинации против рака на основе пептидов и клинические результаты». В Томасе С. (ред.). Дизайн вакцины . Методы молекулярной биологии. Том. 1403. Нью-Йорк, штат Нью-Йорк: Спрингер. стр. 797–817. дои : 10.1007/978-1-4939-3387-7_46 . ISBN 978-1-4939-3387-7 . ПМИД 27076168 .
- ^ Скварчинский М, Тот I (февраль 2016 г.). «Синтетические вакцины на основе пептидов» . Химическая наука . 7 (2): 842–854. дои : 10.1039/C5SC03892H . ПМЦ 5529997 . ПМИД 28791117 .
- ^ Пирсон М.С., Пикеринг Д.А., Триболет Л., Купер Л., Малвенна Дж., Оливейра Л.М. и др. (май 2010 г.). «Нейтрализующие антитела к гемоглобиназе анкилостомы Na-APR-1: значение для мультивалентной вакцины против анкилостомоза и шистосомоза» . Журнал инфекционных болезней . 201 (10): 1561–1569. дои : 10.1086/651953 . ПМИД 20367477 .
- ^ Димерт Д.Д., Пинто А.Г., Фрейре Дж., Джаривала А., Сантьяго Х., Гамильтон Р.Г. и др. (июль 2012 г.). «Генерализованная крапивница, индуцированная вакциной Na-ASP-2: значение для разработки вакцин против гельминтов» . Журнал аллергии и клинической иммунологии . 130 (1): 169–76.e6. дои : 10.1016/j.jaci.2012.04.027 . ПМИД 22633322 .
- ^ Купер Дж.А., Хейман В., Рид С., Кагава Х., Гуд М.Ф., Сол А. (апрель 1997 г.). «Картирование конформационных эпитопов В-клеток в альфа-спиральных белках со спиральной спиралью». Молекулярная иммунология . 34 (6): 433–440. дои : 10.1016/S0161-5890(97)00056-4 . ПМИД 9307059 .
- ^ Азми Ф., Ахмад Фуаад А.А., Скварчински М., Тот И. (март 2014 г.). «Недавний прогресс в открытии адъювантов для субъединичных вакцин на основе пептидов» . Человеческие вакцины и иммунотерапия . 10 (3): 778–796. дои : 10.4161/hv.27332 . ПМК 4130256 . ПМИД 24300669 .
- ^ Малонис Р.Дж., Лай Дж.Р., Верньолл О. (март 2020 г.). «Вакцины на основе пептидов: текущий прогресс и будущие проблемы» . Химические обзоры . 120 (6): 3210–3229. doi : 10.1021/acs.chemrev.9b00472 . ПМЦ 7094793 . ПМИД 31804810 .
- ^ Маринкола Ф.М., Ривольтини Л., Салгаллер М.Л., Игрок М., Розенберг С.А. (июль 1996 г.). «Дифференциальная активность CTL анти-MART-1/MelanA в периферической крови пациентов с меланомой HLA-A2 по сравнению со здоровыми донорами: свидетельства праймирования опухолевыми клетками in vivo». Журнал иммунотерапии с акцентом на иммунологии опухолей . 19 (4): 266–277. дои : 10.1097/00002371-199607000-00003 . ПМИД 8877721 .
- ^ Нил Д.Э., Шарплс Л., Смит К., Феннелли Дж., Холл Р.Р., Харрис А.Л. (апрель 1990 г.). «Рецептор эпидермального фактора роста и прогноз рака мочевого пузыря» . Рак . 65 (7): 1619–1625. doi : 10.1002/1097-0142(19900401)65:7<1619::aid-cncr2820650728>3.0.co;2-q . ПМИД 2311071 . S2CID 12449093 .
- ^ Палатник-де-Соуза CB, Соарес И.С., Роза Д.С. (18 апреля 2018 г.). «Редакционная статья: Открытие эпитопов и разработка синтетической вакцины» . Границы в иммунологии . 9 : 826. дои : 10.3389/fimmu.2018.00826 . ПМЦ 5915546 . ПМИД 29720983 .
- ^ Фирбас С., Джилма Б., Таубер Е., Бюргер В., Еловчан С., Линнау К. и др. (май 2006 г.). «Иммуногенность и безопасность новой терапевтической пептидной вакцины против вируса гепатита С (ВГС): рандомизированное плацебо-контролируемое исследование по оптимизации дозы у 128 здоровых субъектов». Вакцина . 24 (20): 4343–4353. doi : 10.1016/j.vaccine.2006.03.009 . ПМИД 16581161 .
- ^ Ацмон Дж., Карако Ю., Зив-Сефер С., Шайкевич Д., Абрамов Е., Волохов И. и др. (октябрь 2014 г.). «Применение новой универсальной вакцины против гриппа (Multimeric-001) - путь к улучшению иммунного ответа у пожилых людей». Вакцина . 32 (44): 5816–5823. doi : 10.1016/j.vaccine.2014.08.031 . ПМИД 25173483 .
- ^ ван Дорн Э., Лю Х., Бен-Йедидиа Т., Хассин С., Визонтай И., Норли С. и др. (март 2017 г.). «Оценка иммуногенности и безопасности разработанной BiondVax универсальной вакцины против гриппа (Multimeric-001) либо в качестве отдельной вакцины, либо в качестве праймера к вакцине против гриппа H5N1: протокол исследования фазы IIb» . Лекарство . 96 (11): e6339. дои : 10.1097/md.0000000000006339 . ПМК 5369918 . ПМИД 28296763 .
- ^ Висснер С., Видерхольд К.Х., Тиссо А.С., Фрей П., Даннер С., Джейкобсон Л.Х. и др. (июнь 2011 г.). «Активная иммунотерапия Aβ второго поколения CAD106 снижает накопление амилоида у трансгенных мышей APP, одновременно сводя к минимуму потенциальные побочные эффекты» . Журнал неврологии . 31 (25): 9323–9331. doi : 10.1523/jneurosci.0293-11.2011 . ПМК 6623465 . ПМИД 21697382 .
- ^ Ван С.И., Финстад С.Л., Уолфилд А.М., Сиа С., Соколл К.К., Чанг Т.Ю. и др. (апрель 2007 г.). «Сайт-специфическая вакцина UBITh-бета-амилоид для иммунотерапии болезни Альцгеймера». Вакцина . 25 (16): 3041–3052. doi : 10.1016/j.vaccine.2007.01.031 . ПМИД 17287052 .
- ^ Давтян Х, Гочикян А, Петрушина И, Овакимян А, Давтян А, Погосян А и др. (март 2013 г.). «Иммуногенность, эффективность, безопасность и механизм действия эпитопной вакцины (Lu AF20513) против болезни Альцгеймера: прелюдия к клиническим испытаниям» . Журнал неврологии . 33 (11): 4923–4934. doi : 10.1523/jneurosci.4672-12.2013 . ПМЦ 3634356 . ПМИД 23486963 .
- ^ Лакоста А.М., Паскуаль-Лукас М., Пезини П., Касабона Д., Перес-Грихальба В., Маркос-Кампос И. и др. (январь 2018 г.). «Безопасность, переносимость и иммуногенность активной вакцины против Aβ 40 (ABvac40) у пациентов с болезнью Альцгеймера: рандомизированное двойное слепое плацебо-контролируемое исследование фазы I» . Исследования и терапия болезни Альцгеймера . 10 (1): 12. дои : 10.1002/alz.045720 . ПМЦ 5789644 . ПМИД 29378651 .
- ^ Хикман Д.Т., Лопес-Дебер М.П., Ндао Д.М., Сильва А.Б., Нанд Д., Пильгрен М. и др. (апрель 2011 г.). «Независимый от последовательности контроль конформации пептидов в липосомальных вакцинах для борьбы с болезнями, вызванными неправильным сворачиванием белков» . Журнал биологической химии . 286 (16): 13966–13976. дои : 10.1074/jbc.m110.186338 . ПМК 3077597 . ПМИД 21343310 .
- ^ Концекова Е, Зилка Н, Ковачеч Б, Новак П, Новак М (2014). «Первая в мире тау-вакцина, нацеленная на структурные детерминанты, необходимые для патологического взаимодействия тау-тау, снижает олигомеризацию тау и нейрофибриллярную дегенерацию в модели болезни Альцгеймера» . Исследования и терапия болезни Альцгеймера . 6 (4): 44. дои : 10.1186/alzrt278 . ПМЦ 4255368 . ПМИД 25478017 .