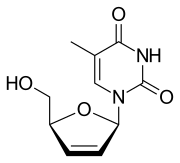
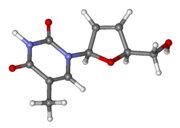
Ставудин
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | звук |
| Другие имена | 2',3'-дидегидро-2',3'-дидезокситимидин |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а694033 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | >80% |
| Связывание с белками | Незначительный |
| Метаболизм | Удаление почек (~ 40%) |
| Период полувыведения | 0,8–1,5 часа (у взрослых) |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| НИАИД Химическая база данных | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.169.180 |
| Химические и физические данные | |
| Формула | С 10 Н 12 Н 2 О 4 |
| Молярная масса | 224.216 g·mol −1 |
| 3D model ( JSmol ) | |
| (проверять) | |
Ставудин ( d4T под торговой маркой Зерит ), продаваемый, среди прочего, , представляет собой антиретровирусный препарат, используемый для профилактики и лечения ВИЧ/СПИДа . [ 4 ] Обычно его рекомендуется использовать с другими антиретровирусными препаратами. [ 4 ] Его можно использовать для профилактики после травмы от укола иглой или другого потенциального воздействия. [ 4 ] Однако это не лечение первой линии. [ 4 ] Его дают через рот. [ 4 ]
Общие побочные эффекты включают головную боль , диарею, рвоту, сыпь и с периферическими нервами . проблемы [ 4 ] Серьезные побочные эффекты включают высокий уровень лактата в крови , панкреатит и увеличение печени . [ 4 ] Обычно это не рекомендуется во время беременности . [ 4 ] Ставудин относится к классу нуклеозидных аналогов ингибиторов обратной транскриптазы (НИОТ). [ 4 ]
Ставудин был впервые описан в 1966 году и одобрен к использованию в США в 1994 году. [ 5 ] Он доступен в виде непатентованного лекарства . [ 4 ]
Медицинское использование
[ редактировать ]Ставудин используется для лечения инфекции ВИЧ-1 , но не является лекарством. Обычно его не рекомендуют в качестве первоначального лечения. [ 6 ] Ставудин также может снизить риск развития инфекции ВИЧ-1 после контакта с вирусом на работе (например, укол иглой) или в результате контакта с инфицированной кровью или другими жидкостями организма. [ 7 ] Он всегда используется в сочетании с другими препаратами против ВИЧ для лучшего контроля инфекции и снижения осложнений ВИЧ. [ 8 ]
Всемирная организация здравоохранения (ВОЗ) рекомендует прекратить прием ставудина из-за его высокого уровня токсичности. Если препарат необходимо применять, рекомендуется использовать низкие дозировки, чтобы уменьшить возникновение побочных эффектов; однако Кокрейновский обзор 2015 года не обнаружил явного преимущества между режимами высокой и низкой дозировки. [ 9 ]
Беременность и кормление грудью
[ редактировать ]В исследованиях на животных было продемонстрировано влияние Ставудина на плод, однако данные исследований на людях отсутствуют. [ 2 ] Поэтому беременным женщинам следует назначать ставудин только в том случае, если потенциальная польза превышает потенциальный вред для плода. Кроме того, сообщалось о случаях фатального лактоацидоза у беременных женщин, получавших комбинированную терапию ставудином и диданозином с другими противовирусными препаратами. [ 2 ]
Центры по контролю и профилактике заболеваний рекомендуют ВИЧ-инфицированным матерям не кормить детей грудью, чтобы избежать риска передачи ВИЧ через грудное молоко. [ 10 ] Имеются также данные о том, что ставудин попадает в грудное молоко животных, хотя данные о грудном молоке человека отсутствуют. [ 2 ]
Дети
[ редактировать ]Ставудин безопасен для применения у детей, инфицированных ВИЧ, от рождения до подросткового возраста. Побочные эффекты и профиль безопасности такие же, как у взрослых. [ 2 ]
Пожилые
[ редактировать ]Данных о применении ставудина у ВИЧ-инфицированных взрослых в возрасте 65 лет и старше нет. Однако среди 12 000 человек старше 65 лет у 30% развилась периферическая нейропатия . [ 2 ] Кроме того, поскольку у пожилых людей чаще наблюдается снижение функции почек, у них чаще развиваются токсические побочные эффекты. [ 11 ]
Побочные эффекты
[ редактировать ]Общие побочные эффекты [ 2 ]
- Тошнота
- Рвота
- Диарея
- Головная боль
- Расстройство желудка
Тяжелые побочные эффекты [ 2 ]
- Периферическая нейропатия
- Лактацидоз
- Панкреатит
- Гепатотоксичность
- Гепатомегалия со стеатозом
- Липоатрофия / липодистрофия (перераспределение/накопление жира)
За людьми ведется наблюдение на предмет развития этих серьезных побочных эффектов. Показано, что развитие периферической нейропатии зависит от дозы и может исчезнуть при отмене препарата. Этот побочный эффект развивается чаще у лиц с запущенной стадией ВИЧ-1, периферической невропатией в анамнезе или у лиц, принимающих другие препараты, связанные с невропатией. [ 2 ]
Лабораторные испытания показали, что ставудин генотоксичен , но при применении в клинических дозах его канцерогенные эффекты отсутствуют. гиперлактатемия, потеря минеральной плотности костной ткани (МПК), уменьшение жира на конечностях и увеличение уровня триглицеридов При применении высоких доз были обнаружены . Это также один из наиболее вероятных противовирусных препаратов, вызывающих липодистрофию , и по этой причине он больше не считается подходящим лечением для большинства пациентов в развитых странах.
Согласно исследованию, проведенному в Таиланде, HLA-B*4001 может использоваться в качестве генетического маркера для прогнозирования того, у каких пациентов разовьется липодистрофия, связанная со ставудином, чтобы избежать или сократить продолжительность приема ставудина. [ 12 ]
Он по-прежнему используется в качестве терапии первого выбора в условиях бедных ресурсов, например, в Индии. Только в случае развития периферической нейропатии или беременности его меняют на препарат следующего выбора — зидовудин . О безопасности и эффективности титрования дозы у пациентов, ранее не получавших лечение, не сообщалось. Об этом сообщалось только у пациентов с устойчивой вирусологической супрессией. Эти результаты не распространяются на применение ставудина у пациентов, ранее не получавших АРТ, с высокой вирусной нагрузкой.
В ноябре 2009 года Всемирная организация здравоохранения (ВОЗ) заявила, что «[ВОЗ] рекомендует странам поэтапно отказываться от использования ставудина, или d4T, из-за его долгосрочных, необратимых побочных эффектов. Ставудин по-прежнему широко используется в первую очередь. В развивающихся странах из-за своей низкой стоимости и широкой доступности зидовудин (АЗТ) или тенофовир (ТДФ) рекомендуются как менее токсичные и столь же эффективные альтернативы». [ 13 ]
Механизм действия
[ редактировать ]нуклеозидный аналог тимидина . Ставудин — Он фосфорилируется клеточными киназами в активный трифосфат. Ставудинтрифосфат ингибирует обратную транскриптазу ВИЧ , конкурируя с природным субстратом тимидинтрифосфатом . Обратная транскриптаза — это фермент, который вирус использует для создания ДНК-копии своей РНК, чтобы вставить свой генетический материал в ДНК хозяина. Ставудинтрифосфат при включении в цепь ДНК вызывает прекращение репликации ДНК .
Фармакокинетика
[ редактировать ]Всасывание. Ставудин обладает быстрой абсорбцией и хорошей биодоступностью при пероральном приеме (F = 0,86). [ 8 ]
Распределение. Ставудин не связывается с белками крови. [ 8 ]
Метаболизм. На клиренс ставудина печеночный метаболизм влияет минимально. Окисление и глюкуронидация приводят к образованию второстепенных метаболитов. [ 8 ]
Выведение: Ставудин выводится большей частью с мочой и преимущественно в неизмененной форме. [ 8 ]
Взаимодействие с лекарственными средствами
[ редактировать ]Одновременное применение зидовудина не рекомендуется, так как он может ингибировать внутриклеточное фосфорилирование ставудина. Другие препараты против ВИЧ этим свойством не обладают.
Ставудин не связывается с белками и не ингибирует основные изоформы цитохрома P450. Таким образом, значительные лекарственные взаимодействия с лекарствами, метаболизирующимися этими путями, или препаратами, связанными с белками, маловероятны. [ 8 ]
История
[ редактировать ]Ставудин был впервые создан Джеромом Хорвицем в 1960-х годах и первоначально назывался D4T. [ 14 ] Когда в 1980-х годах произошла эпидемия СПИДа, Уильям Прусофф и другие сотрудники Йельского университета обнаружили анти-ВИЧ свойства ставудина. [ 15 ]
В 1990 году Йельский университет запатентовал использование препарата ставудин (d4T) для лечения ВИЧ и предоставил компании Bristol-Myers Squibb эксклюзивную лицензию на производство препарата под торговой маркой Зерит. [ 15 ] С тех пор ставудин стал ключевым препаратом для лечения ВИЧ. Однако из-за высокой цены (более 1600 долларов в год) Зерит был недоступен для инфицированных людей в развивающихся странах. Организация «Врачи без границ» (MSF) нашла индийского производителя, который был готов продавать ставудин в Южной Африке по цене 40 долларов в год на пациента. Однако эта сделка сорвалась, поскольку Йельский университет запатентовал ставудин в Южной Африке и не пожелал выдавать лицензию индийскому производителю дженериков. Студенты встали на сторону организации «Врачи без границ» и обратились в Йельский университет с идеей оказать давление на Bristol-Myers Squibb , чтобы она снизила цены на Ставудин в Южной Африке и/или выдала патентные лицензии производителям дженериков. После того, как проблема была обнародована, Bristol-Myers Squibb объявила, что не будет обеспечивать соблюдение патента на ставудин в Южной Африке и будет продавать Зерит в странах Африки к югу от Сахары за 55 долларов в год. [ 16 ]
США (FDA) предоставило статус параллельного отслеживания Ставудин был первым препаратом, которому в 1992 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов , что позволило агентству сделать Ставудин доступным для пациентов до того, как он будет одобрен. Ставудин был представлен в рамках ускоренного процесса одобрения FDA. Благодаря этому процессу эффективность Ставудина измерялась по его влиянию на суррогатный маркер CD4 , а не по клиническим конечным точкам. FDA пришло к выводу, что увеличение количества клеток CD4 является показателем того, насколько эффективен препарат против СПИДа и ВИЧ-инфекции. Ставудин был четвертым препаратом, одобренным FDA для лечения СПИДа и ВИЧ-инфекции 27 июня 1994 года. Даже после одобрения исследования продолжались для оценки клинической пользы препарата. Если нет никаких признаков клинической пользы, ускоренное одобрение может быть отозвано. [ 17 ]
В 2018 году Mylan Pharmaceuticals прекратила производство ставудина в капсулах по 20, 30 и 40 мг. [ 18 ]
Ссылки
[ редактировать ]- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ Jump up to: а б с д и ж г час я «Ставудин капсула» . ДейлиМед . 21 сентября 2019 года . Проверено 13 октября 2020 г.
- ^ «Зерит ЭПАР» . Европейское агентство лекарственных средств (EMA) . 17 сентября 2018 года . Проверено 13 октября 2020 г.
- ^ Jump up to: а б с д и ж г час я дж «Монография Ставудина для профессионалов — Drugs.com» . www.drugs.com . Архивировано из оригинала 10 ноября 2016 года . Проверено 9 ноября 2016 г.
- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 505. ИСБН 9783527607495 . Архивировано из оригинала 8 сентября 2017 года.
- ^ «Обновленные рекомендации по постконтактной антиретровирусной профилактике после сексуального, инъекционного употребления наркотиков или другого непрофессионального контакта с ВИЧ — США, 2016 г.» (PDF) . Центр по контролю и профилактике заболеваний . Анналы неотложной медицины. Архивировано (PDF) из оригинала 20 ноября 2016 года . Проверено 11 августа 2016 г.
- ^ «Руководство по использованию антиретровирусных препаратов у ВИЧ-1-инфицированных взрослых и подростков» (PDF) . Группа экспертов по антиретровирусным рекомендациям для взрослых и подростков . Министерство здравоохранения и социальных служб США (HHS). 14 июля 2016 г. Архивировано из оригинала (PDF) 1 ноября 2016 г. . Проверено 11 августа 2016 г.
- ^ Jump up to: а б с д и ж «Информация о назначении препарата Зерит (ставудин) в капсулах и порошке для приготовления раствора для перорального применения» (PDF) . Принстон, Нью-Джерси: Бристол-Майерс Сквибб. Декабрь 2012 г. Архивировано (PDF) из оригинала 31 января 2017 г.
- ^ Магула Н., Дедикоат М. (январь 2015 г.). «Низкая доза ставудина по сравнению с высокой дозой для лечения людей с ВИЧ-инфекцией» . Кокрановская база данных систематических обзоров . 1 (1): CD007497. дои : 10.1002/14651858.CD007497.pub2 . ПМЦ 10862382 . ПМИД 25627012 .
- ^ «Беременные женщины, младенцы и дети | Пол | ВИЧ по группам | ВИЧ / СПИД | CDC» . www.CDC.gov . Архивировано из оригинала 15 ноября 2016 года . Проверено 15 ноября 2016 г.
- ^ «Руководство FDA для промышленности: гериатрическое население» (PDF) . Управление по контролю за продуктами и лекарствами США. Август 1994 г. Архивировано (PDF) из оригинала 14 сентября 2016 г.
- ^ Вангсомбунсири В., Махасиримонгкол С., Чантарансу С., Киртибуранакул С., Чароеньингваттана А., Коминдр С. и др. (февраль 2010 г.). «Связь между HLA-B*4001 и липодистрофией среди ВИЧ-инфицированных пациентов из Таиланда, получавших антиретровирусную схему, содержащую ставудин» . Клинические инфекционные болезни . 50 (4): 597–604. дои : 10.1086/650003 . ПМИД 20073992 .
- ^ «Новые рекомендации по ВИЧ для улучшения здоровья, снижения инфекций и спасения жизней» . Всемирная организация здравоохранения . 30 ноября 2009 г. Архивировано из оригинала 18 января 2010 г.
- ^ «Некролог Джерома Хорвица» . Телеграф.co.uk . Архивировано из оригинала 7 ноября 2016 года . Проверено 6 ноября 2016 г.
- ^ Jump up to: а б Прусов В. (19 марта 2001 г.). «Рассказ учёного» . Нью-Йорк Таймс . ISSN 0362-4331 . Архивировано из оригинала 7 ноября 2016 года . Проверено 6 ноября 2016 г.
- ^ Уэллетт LL (сентябрь 2010 г.). «Сколько патентов нужно, чтобы создать лекарство? Последующие фармацевтические патенты и университетское лицензирование» . Обзор законодательства штата Мичиган в области телекоммуникаций и технологий . 17 (1): 299–336.
- ^ «Одобрение FDA Ставудина (d4T) | Новости | СПИДинфо» . СПИДинфо . Архивировано из оригинала 7 ноября 2016 года . Проверено 6 ноября 2016 г.
- ^ «Ставудин» . О прекращении производства сообщили в FDA . США Управление по контролю за продуктами и лекарствами (FDA). 30 апреля 2018 г.