Открытие и разработка ингибиторов ВИЧ-протеазы
Многие основные физиологические процессы зависят от регуляции активности протеолитических ферментов может иметь серьезные последствия равновесия между ферментом и его субстратами , и нарушение . В этой перспективе открытие низкомолекулярных лигандов , таких как ингибиторы протеаз , которые могут модулировать каталитическую активность, имеет огромный терапевтический эффект. [ 1 ] Следовательно, ингибирование протеазы ВИЧ является одним из наиболее важных подходов к терапевтическому вмешательству при ВИЧ- инфекции. [ 2 ] и их разработка рассматривается как крупный успех в разработке лекарств на основе структуры . [ 3 ] Они очень эффективны против ВИЧ. [ 4 ] и с 1990-х годов являются ключевым компонентом антиретровирусной терапии ВИЧ/ СПИДа . [ 5 ]
История
[ редактировать ]Вирус иммунодефицита человека (ВИЧ) — это лентивирус , имеющий два основных вида: ВИЧ-1 , который вызывает большую часть эпидемии , и ВИЧ-2 , его близкий родственник, распространение которого сосредоточено в Западной Африке. [ 6 ] ВИЧ- инфекция была впервые описана в 1981 году в Сан-Франциско и Нью-Йорке. [ 7 ] В 1985 году ВИЧ был идентифицирован как возбудитель синдрома приобретенного иммунодефицита (СПИД), и его полный геном сразу же стал доступен . Эти знания проложили путь к разработке селективных ингибиторов . [ 6 ]
ВИЧ-2 несет несколько меньший риск передачи, чем ВИЧ-1, и инфекция имеет тенденцию медленнее прогрессировать до СПИДа. [ 7 ] В обычном использовании ВИЧ обычно подразумевает ВИЧ-1. [ 8 ]
Протеаза ВИЧ-1 — одна из наиболее известных аспарагиновых протеаз и привлекательная мишень для лечения СПИДа. [ 9 ]
После открытия протеазы ВИЧ потребовалось всего 10 лет, чтобы ее первый ингибитор появился на рынке. [ 10 ] Первые сообщения о высокоселективных антагонистах протеазы ВИЧ были опубликованы в 1987 году. Фаза I испытаний саквинавира началась в 1989 году, и это был первый ингибитор протеазы ВИЧ, одобренный для использования по рецепту в 1995 году. Четыре месяца спустя появились два других ингибитора протеазы. ритонавир и индинавир были одобрены. [ 6 ] В 2009 году на рынок поступило десять ингибиторов протеазы для лечения ВИЧ, но один ингибитор протеазы, ампренавир , был снят с рынка в 2004 году. [ 6 ] [ 11 ]
Жизненный цикл ВИЧ
[ редактировать ]
ВИЧ принадлежит к классу вирусов, называемых ретровирусами , которые несут генетическую информацию в форме РНК . ВИЧ инфицирует Т-клетки , несущие CD4 на своей поверхности антиген . Когда ВИЧ заражает клетку-мишень, необходимо слияние вирусной и клеточной мембран. [ 12 ] Первым шагом является взаимодействие между белками оболочки вируса (gp120, gp41) и специфическими поверхностными рецепторами клетки-хозяина (например, рецептором CD4) на клетке-мишени. Затем вирус связывается с хемокиновыми корецепторами CXCR4 или CCR5 , что приводит к конформационным изменениям белков оболочки. В результате этого слияния создается пора, через которую вирусный капсид проникает в клетку. [ 13 ] После проникновения в клетку РНК вируса обратно транскрибируется в ДНК с помощью первого кодируемого вирусом фермента — обратной транскриптазы . Вирусная ДНК попадает в ядро , где она интегрируется в генетический материал клетки с помощью интегразы , второго фермента, кодируемого вирусом. Активация клетки-хозяина приводит к транскрипции вирусной ДНК в мРНК . Затем мРНК транслируется в вирусные белки, и третий кодируемый вирусом фермент, а именно протеаза ВИЧ, необходим для расщепления предшественника вирусного полипротеина на отдельные зрелые белки. Вирусная РНК и вирусные белки собираются на поверхности клетки в новые вирионы . Вирионы отпочковываются от клетки и высвобождаются для заражения других клеток. Все инфицированные клетки в конечном итоге погибают из-за этого обширного повреждения клеток, от разрушения генетической системы хозяина до почкования и высвобождения вирионов. [ 12 ]
Механизм действия
[ редактировать ]Есть несколько этапов жизненного цикла ВИЧ, в которые можно вмешаться, тем самым остановив репликацию вируса. Очень важным этапом является протеолитическое расщепление предшественников полипептидов на зрелые ферменты и структурные белки, катализируемое протеазой ВИЧ. [ 12 ] Ингибиторы протеазы ВИЧ представляют собой пептидоподобные химические вещества, которые конкурентно ингибируют действие аспартилпротеазы вируса. Эти препараты предотвращают протеолитическое расщепление полипротеинов ВИЧ Gag и Pol, которые включают важные структурные и ферментативные компоненты вируса. Это предотвращает превращение частиц ВИЧ в их зрелую инфекционную форму. [ 6 ]
Ингибиторы протеазы могут изменять адипоцитов метаболизм , вызывая липодистрофию — распространенный побочный эффект , связанный с использованием большинства ингибиторов протеазы ВИЧ. Было предложено множество механизмов, например ингибирование дифференцировки адипоцитов , накопление триглицеридов и усиление липолиза . Теории, рассматривающие влияние ингибиторов протеазы на стимулируемое инсулином поглощение глюкозы, также связаны с липодистрофическим синдромом. Вполне возможно, что ингибиторы протеазы могут вызывать снижение инсулином стимулируемого тирозина фосфорилирования IRS-1, что представляет собой ингибирование ранних этапов передачи сигналов инсулина. Снижение секреции адипонектина и индуцированная экспрессия интерлейкина-6, связанная с ингибиторами протеазы ВИЧ, также могут способствовать ингибированию стимулируемого инсулином поглощения глюкозы. [ 14 ]
Дизайн
[ редактировать ]Ингибиторы протеазы были разработаны для имитации переходного состояния протеазы реальных субстратов . Пептидная связь, состоящая из –NH-CO-, заменена гидроксиэтиленовой группой (-CH 2 -CH(OH)-), которую протеаза не способна расщепить. Ингибиторы ВИЧ-протеазы соответствуют активному центру аспартил-протеазы аспарагиновой протеазы ВИЧ и были рационально разработаны с использованием знаний о механизме действия . Наиболее многообещающим аналогом переходного состояния был гидроксиэтиламин, который привел к открытию первого ингибитора протеазы, саквинавира . После этого открытия другие ингибиторы протеазы ВИЧ были разработаны с использованием того же принципа. [ 15 ]
Связывающий сайт
[ редактировать ]
Протеаза ВИЧ представляет собой C2-симметричный гомодимерный фермент, состоящий из двух по 99 аминокислот мономеров . Каждый мономер содержит остаток аспарагиновой кислоты , который необходим для катализа. [ 6 ] Асп-25 и Асп-25´. Протеаза ВИЧ имеет последовательность Asp- Thr - Gly , которая консервативна среди других ферментов аспарагиновой протеазы млекопитающих. Расширенная область бета-листа на мономерах, известная как лоскут, частично представляет собой сайт связывания субстрата с двумя аспартильными остатками, лежащими на дне гидрофобной полости. [ 12 ] [ 16 ] [ 17 ] Каждый гибкий лоскут содержит три характерных участка: боковые цепи, идущие наружу ( Met 46, Phe 53), гидрофобные цепи, идущие внутрь ( Ile 47, Ile54), и богатый глицином участок (Gly48, 49, 51, 52). Ile50 остается на кончике витка, и когда фермент не связан, молекула воды образует водородные связи с основной цепью Ile50 на каждом мономере. [ 17 ]
ВИЧ-протеазы катализируют гидролиз пептидных связей с высокой селективностью последовательности и каталитической эффективностью. Механизм действия протеазы ВИЧ имеет много общих черт с механизмом действия остальных представителей семейства аспарагиновых протеаз, хотя полный подробный механизм действия этого фермента до конца не изучен. [ 12 ] Молекула воды, по-видимому, играет роль в открытии и закрытии створок, а также в увеличении сродства между ферментом и субстратом. Аспартильные остатки участвуют в гидролизе пептидных связей. [ 17 ] Предпочтительным сайтом расщепления для этого фермента является N-концевая сторона остатков пролина, особенно между фенилаланином и пролином или тирозином и пролином . [ 6 ] [ 16 ]
Разработка
[ редактировать ]Первый ингибитор протеазы ВИЧ, саквинавир, представляет собой пептидомиметик гидроксиэтиламин. [ 6 ] и поступил в продажу в 1995 году. [ 18 ] Это аналог переходного состояния нативного субстрата протеазы. [ 6 ] Основным критерием дизайна было наблюдение, что протеаза ВИЧ-1 расщепляет последовательности, содержащие дипептиды Tyr-Pro или Phe-Pro. [ 19 ] Добавление группы декагидроизохинолина (DIQ) было одной из наиболее значительных модификаций, которые привели к открытию саквинавира. Этот заместитель улучшает растворимость в воде и эффективность за счет ограничения конформационной свободы ингибитора. [ 20 ] Саквинавир эффективен как против ВИЧ-1, так и против ВИЧ-2. [ 5 ] и обычно хорошо переносится, но высокая концентрация в сыворотке не достигается. [ 11 ]
Ритонавир , пептидомиметический ингибитор ВИЧ-протеазы, поступил в продажу в 1996 году. [ 18 ] Он был разработан с учетом C2-симметрии сайта связывания протеазы. [ 6 ] Разработчики ритонавира, компания Abbott Laboratories , начали с соединений, которые были активны против вируса, но имели плохую биодоступность . Были внесены некоторые улучшения, например, были удалены концевые фенильные остатки и вместо них добавлены пиридильные группы для повышения растворимости в воде. Конечным продуктом этих улучшений стал ритонавир. [ 19 ] Значительные побочные эффекты со стороны желудочно-кишечного тракта и большое количество таблеток являются основными недостатками ритонавира и поэтому не используются в качестве монотерапии. [ 11 ] Однако он является сильным ингибитором метаболизма, опосредованного ферментом цитохрома P450. [ 19 ] и он используется только в комбинированной терапии с другими ингибиторами протеазы для усиления фармакокинетики. [ 11 ]
Индинавир , который представляет собой пептидомиметический ингибитор гидроксиэтилен-протеазы ВИЧ, появился на рынке в 1996 году. [ 6 ] [ 18 ] При разработке индинавира руководствовались молекулярным моделированием и рентгеновской кристаллической структурой ингибированного ферментного комплекса. Концевые фенильные компоненты способствуют гидрофобному связыванию, повышая эффективность . [ 19 ] Это аналог фенилаланин-пролинового сайта расщепления Gag-полипротеина ВИЧ. [ 6 ]
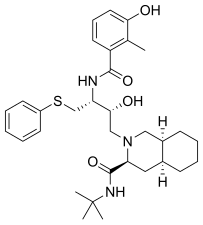
Нелфинавир был первым ингибитором протеазы, не обладающим пептидомиметическим действием. В процессе разработки нелфинавира, перорально биодоступного и непептидного ингибитора, использовался итеративный анализ сокристаллической структуры белков пептидных ингибиторов, при этом части ингибиторов были заменены непептидными заместителями. [ 19 ] Нельфинавир содержит новую 2-метил-3-гидроксибензамидную группу, тогда как его карбоксильный конец содержит ту же группу DIQ, что и саквинавир. [ 19 ] Нелфинавир поступил в продажу в 1997 году. [ 18 ] и был первым ингибитором протеазы, показанным для лечения СПИДа у детей . [ 19 ]
Ампренавир появился на рынке в 1999 году. [ 18 ] Это N , N -замещенный аминосульфонамидный непептидный ингибитор ВИЧ-протеазы. [ 6 ] и имеет некоторые общие черты с предыдущими ингибиторами протеазы. Его ядро похоже на ядро саквинавира, но с разными функциональными группами на обоих концах. На одном конце он имеет карбаматную группу тетрагидрофурана , а на другом конце представляет собой изобутилфенилсульфонамид с добавленным амидом. Такая структура приводит к меньшему количеству хиральных центров, что облегчает синтез и повышает растворимость в воде. Это, в свою очередь, обеспечивает лучшую биодоступность при пероральном приеме. [ 19 ] Однако ампренавир был снят с рынка в 2004 году, поскольку его пролекарство фосампренавир оказалось превосходящим его по многим аспектам. [ 6 ]
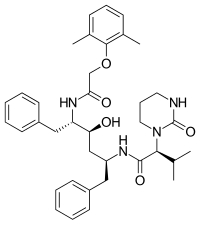
Лопинавир поступил в продажу в 2000 году. [ 18 ] и первоначально был разработан для уменьшения взаимодействия ингибитора с Val 82 протеазы ВИЧ-1, остатком, который часто мутирует в устойчивых к лекарствам штаммах вируса. [ 19 ] Это пептидомиметический ингибитор протеазы ВИЧ. [ 6 ] и его ядро идентично ритонавиру. Вместо 5- тиазолильной концевой группы в ритонавире лопинавир имеет феноксиацетильную группу, а 2-изопропилтиазолильная группа в ритонавире заменена модифицированным валином, в котором к аминоконцу присоединена шестичленная циклическая мочевина . [ 19 ]
Фосампренавир поступил в продажу в 2003 году. [ 18 ] и представляет собой пролекарство фосфоэфира, которое быстро и интенсивно метаболизируется до ампренавира. [ 21 ] Растворимость и биодоступность лучше, чем у ампренавира. [ 6 ] что приводит к снижению ежедневной нагрузки на таблетки. [ 22 ]
Атазанавир поступил в продажу в 2003 году. [ 18 ] и является ингибитором азапептидной протеазы [ 18 ] разработан с учетом C2-симметрии сайта связывания фермента. [ 11 ] Атазанавир показал лучшие профили резистентности, чем предыдущие ингибиторы протеазы ВИЧ. [ 4 ] Он уникален среди других ингибиторов протеаз, поскольку может всасываться только в кислой среде. [ 11 ]
Типранавир — непептидный ингибитор протеазы ВИЧ-1. [ 11 ] и вышел на рынок в 2005 году. [ 18 ] В отличие от других ингибиторов протеазы ВИЧ, представленных на рынке, типранавир был разработан на основе непептидной матрицы кумарина , и его антипротеазная активность была обнаружена с помощью высокопроизводительного скрининга . [ 23 ] Этот сульфонамид, содержащий 5,6-дигидро-4-гидрокси-2-пирон, появился в результате скрининга 3-замещенных кумаринов и дигидропиронов. [ 24 ] Он обладает широкой противовирусной активностью в отношении ВИЧ-1, устойчивого к множественным ингибиторам протеаз. [ 25 ]
Дарунавир вышел на рынок в 2006 году. [ 18 ] и является непептидным аналогом ампренавира с критическим изменением концевой тетрагидрофурановой (ТГФ) группы. Вместо одной группы ТГФ дарунавир содержит две группы ТГФ, слитые в соединении с образованием фрагмента бис-ТГФ , что делает его более эффективным, чем ампренавир. Благодаря этому структурному изменению стереохимия вокруг фрагмента бис-ТГФ приводит к ориентационным изменениям, что позволяет продолжать связывание с протеазой, у которой развилась устойчивость к ампренавиру. [ 26 ]
Все ингибиторы протеазы, одобренные FDA, перечислены ниже.

|
|

|
|
| Саквинавир | Нелфинавир | Ритонавир | Лопинавир |

|

|

|
|
| Ампренавир | Фосампренавир | Дарунавир | |

|

|

|
|
| Индинавир | Атазанавир | Типранавир |
Отношения структура-деятельность
[ редактировать ]
Все имеющиеся на рынке ингибиторы протеазы ВИЧ содержат центральный мотив, состоящий из гидроксиэтиленового каркаса, за исключением центрального ядра типранавира, основанного на кумариновом каркасе. [ 15 ] Очень важной группой ингибиторов протеазы ВИЧ является гидроксильная группа основного мотива, которая образует водородную связь с карбоновой кислотой на остатках Asp-25 и Asp-25´ в сайте связывания. [ 16 ] [ 27 ] Водородные связи между молекулой воды, которая связана с Ile50 и Ile50', и карбонильными группами пептидомиметических ингибиторов, по-видимому, соединяют их с областями лоскута. [ 19 ] С другой стороны, у непептидных ингибиторов имеется акцептор протона, который заменяет тетракоординированную молекулу воды и напрямую взаимодействует с двумя остатками Ile50 на лоскуте фермента. [ 28 ] Специфические карманы в сайте связывания протеазы ВИЧ, часто называемые S1, S1', S2 и S2', распознают гидрофобные аминокислоты на природных субстратах. Таким образом, эффективность ингибиторов, несущих гидрофобные группы, дополняющие эти области, увеличивается. [ 29 ] Некоторые остатки в сайте связывания фермента способны образовывать водородные связи с гидрофильными группами ингибитора, например с фрагментами ТГФ ампренавира и дарунавира. Поскольку дарунавир имеет фрагмент бис-ТГФ, а не один фрагмент ТГФ, как в ампренавире, он может образовывать больше водородных связей и увеличивать энергию связывания . [ 26 ]
Сопротивление
[ редактировать ]Мутации, кодирующие изменения конформационной формы, способствуют устойчивости ВИЧ к ингибиторам протеазы. [ 26 ] Эти мутации локализуются преимущественно в активном сайте фермента протеазы ВИЧ, а также за его пределами, в том числе в сайтах протеазного расщепления в предшественниках полипротеина Gag-Pol. Сайты расщепления имеют очень разнообразные последовательности, поэтому протеаза распознает свои субстраты не на основе последовательности, а скорее на основе консервативной трехмерной формы, которую разделяют субстраты при связывании в активном сайте. Эта консервативная форма была названа оболочкой подложки . [ 30 ] Было показано, что мутации активного центра напрямую изменяют взаимодействие ингибиторов и в основном происходят в положениях, где ингибиторы контактируют с остатками протеазы за пределами оболочки субстрата. [ 31 ] Считается, что мутации неактивного сайта влияют на другие механизмы, например, на стабильность димеров и конформационную гибкость. [ 32 ] [ 33 ]
более 100 точечных мутаций Описано одного гена, из которых по меньшей мере 26 специфичны для ингибиторов протеаз. Из них существует около 15 первичных или основных мутаций, которые достаточно значительны, чтобы изменить активность лекарства. [ 26 ] В протеазе ВИЧ-1 было обнаружено множество мутированных остатков, которые вызывают устойчивость к лекарственным средствам, например, замена Leu33 на Ile, Val или Phe; Val82 — Ala , Phe, Leu или Thr; Иль84 к Валу; и 90 леев в Мет. [ 34 ] Различные мутации влияют на разные ингибиторы протеазы. Например, мутации Leu90, очевидно, влияют на саквинавир и нелфинавир, в то время как на активность индинавира влияют мутации Met46, Val82 и Ile84, а на фосампренавир влияют изменения Ile50 на Val и Ile84. Сочетание мутаций может привести к развитию лекарственной устойчивости высокого уровня, но единичные мутации обычно не приравниваются к лекарственной устойчивости к ингибиторам протеазы. [ 26 ] Мутации можно разделить на первичные и вторичные мутации. Первичные мутации часто оказывают лишь незначительное влияние на устойчивость. Химические структуры большинства ингибиторов протеаз весьма схожи, поэтому неудивительно, что некоторые первичные мутации приводят одновременно к устойчивости к множеству ингибиторов протеаз. Перекрестная резистентность является одной из основных проблем лечения ингибиторами протеаз. [ 35 ] Дополнительные мутации, возникающие в протеазе во время непрерывной терапии ингибиторами протеаз, обычно называют вторичными мутациями. Это может привести к высокому уровню устойчивости к ингибиторам протеаз. [ 35 ]
Стэнфордская база данных последовательностей ОТ и протеаз ВИЧ (также называемая «База данных по лекарственной устойчивости ВИЧ») была сформирована в 1998 году на основе последовательностей обратной транскриптазы и протеазы ВИЧ от людей с хорошо охарактеризованной историей антиретровирусного лечения и общедоступна для поиска мутаций устойчивости и генотипа. - лечение, корреляции генотип-фенотип и генотип-результат. [ нужна ссылка ]
Хотя оболочка субстрата обеспечивает общую стратегию разработки ингибиторов, которые имитируют субстрат и остаются внутри оболочки, чтобы избежать устойчивости, вызываемой большинством мутаций активного сайта, [ 36 ] [ 37 ] не существует общей стратегии решения проблемы лекарственной устойчивости, особенно среди тех, кто находится за пределами активного места. Исследования, направленные на разработку новых методов лечения СПИДа, направлены на предотвращение перекрестной резистентности к лекарствам, которые уже имеются на рынке. [ 12 ]
Текущий статус
[ редактировать ]В январе 2018 года дарунавир по-прежнему оставался последним ингибитором протеазы ВИЧ, поступившим на рынок. [ 38 ]
В 2006 году GlaxoSmithKline прекратила II фазу клинической разработки бреканавира , исследуемого ингибитора протеазы для лечения ВИЧ, из-за непреодолимых проблем, связанных с его рецептурой. [ 39 ]
Летом 2009 года GlaxoSmithKline и Concert Pharmaceuticals объявили о сотрудничестве по разработке и коммерциализации дейтерийсодержащих лекарств. Одним из них является CTP-518, ингибитор протеазы для лечения ВИЧ, клинические испытания которого, как ожидается, вступят в фазу I во второй половине 2009 года. CTP-518 — это новый ингибитор протеазы ВИЧ, разработанный путем замены некоторых ключевых атомов водорода атазанавира на дейтерий. Доклинические исследования показали, что эта модификация полностью сохраняет противовирусную эффективность, но, очевидно, может замедлять метаболизм в печени и тем самым увеличивать период полувыведения и минимальные уровни в плазме . Таким образом, CTP-518 потенциально может стать первым ингибитором протеазы ВИЧ, который устранит необходимость совместного дозирования с бустерным агентом, таким как ритонавир. [ 40 ]
См. также
[ редактировать ]- Антиретровирусный препарат
- Ингибитор обратной транскриптазы
- Ингибитор интегразы
- Ингибитор входа
- Открытие и разработка ненуклеозидных ингибиторов обратной транскриптазы.
- Открытие и разработка ингибиторов NS5A
Ссылки
[ редактировать ]- ^ Куччиолони, М; Мозикафреддо, М; Бонфили, Л; Чекарини, В; Элеутери, AM; Анджелетти, М (2009). «Природные полифенолы как шаблон для разработки лекарств. Фокус на сериновых протеазах» . Химическая биология и дизайн лекарств . 74 (1): 1–15. дои : 10.1111/j.1747-0285.2009.00836.x . ПМИД 19519739 .
- ^ Чен, X; Кемпф, диджей; Ли, Л; Шам, HL; Васаванонда, С; Видебург, штат Небраска; Салдивар, А; Марш, Канзас; Макдональд, Э; Норбек, Д.В. (2003). «Синтез и исследования SAR мощных ингибиторов протеазы ВИЧ, содержащих новые диметилфеноксилацетаты в качестве лигандов P2». Письма по биоорганической и медицинской химии . 13 (21): 3657–60. дои : 10.1016/j.bmcl.2003.08.043 . ПМИД 14552751 .
- ^ Адачи, М; Охара, Т; Курихара, К; Тамада, Т; Хондзё, Э; Окадзаки, Н; Арай, С; Сёяма, Ю; Кимура, К; Мацумура, Х; Сугияма, С; Адачи, Х; Такано, К; Мори, Ю; Хидака, К; Кимура, Т; Хаяши, Ю; Кисо, Ю; Куроки, Р. (2009). «Структура протеазы ВИЧ-1 в комплексе с мощным ингибитором КНИ-272, определенная методами рентгеновской и нейтронной кристаллографии высокого разрешения» . Труды Национальной академии наук . 106 (12): 4641–6. Бибкод : 2009PNAS..106.4641A . дои : 10.1073/pnas.0809400106 . ПМК 2660780 . ПМИД 19273847 .
- ^ Jump up to: а б Янчунас-младший, Дж; Лэнгли, ДР; Тао, Л; Роуз, RE; Фрибур, Дж; Колонно, Р.Дж.; Дойл, ML (2005). «Молекулярная основа повышенной чувствительности изолятов с заменой I50L, придающей устойчивость к атазанавиру, к другим ингибиторам протеазы» . Антимикробные средства и химиотерапия . 49 (9): 3825–32. doi : 10.1128/AAC.49.9.3825-3832.2005 . ПМЦ 1195399 . ПМИД 16127059 .
- ^ Jump up to: а б Брауэр, ET; Бача, UM; Кавасаки, Ю; Фрейре, Э (2008). «Ингибирование протеазы ВИЧ-2 ингибиторами протеазы ВИЧ-1 при клиническом использовании». Химическая биология и дизайн лекарств . 71 (4): 298–305. дои : 10.1111/j.1747-0285.2008.00647.x . ПМИД 18312292 . S2CID 8461472 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п Брантон, Луизиана; Лазо, Дж.С.; Паркер, КЛ (2006). «Фармакологические основы терапии» Гудмана и Гилманса (11-е изд.). МакГроу-Хилл. [ нужна страница ]
- ^ Jump up to: а б ВИЧ-инфекция в электронной медицине
- ^ Куруп, Алка; Мекапати, Суреш; Гарг, Раджни; Ханш, Корвин (2003). «Ингибиторы протеазы ВИЧ-1: сравнительный анализ QSAR». Современная медицинская химия . 10 (17): 1679–88. дои : 10.2174/0929867033457070 . ПМИД 12871116 .
- ^ Ши, Хайбин; Лю, Кай; Леонг, Венди, Вайоминг; Яо, Шао Ц. (2009). «Целесообразное твердофазный синтез как симметричных, так и асимметричных библиотек диолов, нацеленных на аспарагиновые протеазы». Письма по биоорганической и медицинской химии . 19 (14): 3945–8. дои : 10.1016/j.bmcl.2009.03.041 . ПМИД 19328682 .
- ^ Турок, Борис (2006). «Нацеливание на протеазы: успехи, неудачи и перспективы на будущее». Nature Reviews Открытие лекарств . 5 (9): 785–99. дои : 10.1038/nrd2092 . ПМИД 16955069 . S2CID 4156908 .
- ^ Jump up to: а б с д и ж г Грациани, Эми Л. (17 июня 2014 г.). «Ингибиторы протеазы ВИЧ» . До настоящего времени.
- ^ Jump up to: а б с д и ж Брик А. и Вонг CH (2003)Протеаза ВИЧ-1: механизм и открытие лекарств. Органическая и биомолекулярная химия . 1(1); 5–14.
- ^ Варнке Д., Баррето Дж. и Темесген З. (2007) Антиретровирусные препараты. Журнал клинической фармакологии . 47(12); 1570–1579.
- ^ Ким, Р.Дж., Уилсон, К.Г., Вабич, М., Лазар, М.А. и Степпан, СМ (2006)Специфические для ингибитора протеазы ВИЧ изменения в дифференцировке и метаболизме адипоцитов человека. Ожирение . 14; 994–1002.
- ^ Jump up to: а б Де Клерк, Э. (2009) История антиретровирусных препаратов: ключевые открытия за последние 25 лет. Обзоры по медицинской вирусологии . 19; 287–299.
- ^ Jump up to: а б с Мимото Т., Хаттори Н., Такаку Х. и др. (2000)Взаимосвязь между структурой и активностью пероральных мощных ингибиторов протеазы ВИЧ на основе трипептидов, содержащих гидроксиметилкарбонилизостер. Химический и фармацевтический вестник . 48(9); 1310–1326 гг.
- ^ Jump up to: а б с Перес, МАС, Фернандес, П.А. и Рамос, М.Дж. (2007)Разработка лекарств: новые ингибиторы протеазы ВИЧ-1 на основе нельфинавира в качестве свинца. Журнал молекулярной графики и моделирования . 26; 634–642.
- ^ Jump up to: а б с д и ж г час я дж к Флекснер, К. (2007) Разработка лекарств от ВИЧ: следующие 25 лет. Nature Reviews Открытие лекарств . 6; 959–966.
- ^ Jump up to: а б с д и ж г час я дж к Влодавер, А. (2002) Рациональный подход к разработке лекарств от СПИДа с помощью структурной биологии. Ежегодный обзор медицины . 53; 595–614.
- ^ Смит, Х.Дж. и Саймонс, К. (2005) Ферменты и их ингибирование: разработка лекарств (6-е издание). Соединенные Штаты Америки: CRC Press
- ^ Чепмен, Т.М., Плоскер, Г.Л. и Перри, К.М. (2004) Фосампренавир – обзор его использования при лечении пациентов с ВИЧ-инфекцией, ранее не получавших антиретровирусную терапию. Наркотики . 64; 2101–2124 гг.
- ^ Jump up to: а б с д и Маккой, К. (2007) Дарунавир: непептидный антиретровирусный ингибитор протеазы. Клиническая терапия . 29(8); 1559–1576.
- ^ Лю Ф., Ковалевский А.Ю., Тай Ю., Гош А.К., Харрисон Р.В. и Вебер И.Т. (2008) Влияние лоскутных мутаций на структуру ВИЧ-протеазы и ингибирование саквинавиром и дарунавиром. Журнал молекулярной биологии . 381(1); 102–115
- ^ Лебон Ф. и Ледек М. (2000) Подходы к разработке эффективных ингибиторов протеазы ВИЧ-1. Современная медицинская химия . 7; 455–477.
- ^ Блюм, А. и др. (2008)Ахиральные олигоамины как универсальный инструмент для разработки ингибиторов аспарагиновой протеазы. Биоорганическая и медицинская химия . 16; 8574–8586.
- ^ Прабу-Джеябалан, Наливайка Э, Шиффер, Калифорния. (2002)Форма субстрата определяет специфичность распознавания протеазы ВИЧ-1: анализ кристаллических структур шести субстратных комплексов. «Структура» 10(3):369-81.
- ^ Кинг Н.М., Прабу-Джеябалан М., Наливайка Э.А., Шиффер Калифорния (2004)Борьба с восприимчивостью к лекарственной устойчивости: уроки протеазы ВИЧ-1. Chem Biol. 11(10) октября:1333-8.
- ^ Бихани, С.К., Дас, А., Прашар, В., Феррер, Ж.-Л. и Хосур; MV (2009)Механизм устойчивости, выявленный с помощью кристаллических структур мутантов неактивного сайта протеазы ВИЧ-1, устойчивых к нелфинавиру, N88D и N88S. Связь с биохимическими и биофизическими исследованиями . 389; 295–300.
- ^ де Вера IM, Смит AN, Дэнсел MC, Хуан X, Данн BM, Fanucci GE. (2013) Биохимия. Выяснение связи между конформационной выборкой и лекарственной устойчивостью протеазы ВИЧ-1. 14;52(19):3278-88. дои: 10.1021/bi400109d. Epub 2013, 1 мая.
- ^ Лемке, Т.Л., Уильямс, Д.А., Рош, В.Ф. и Зито, С.В. (2008) Принципы медицинской химии Фоя (6-е издание). Соединенные Штаты Америки: Lippincott Williams & Wilkins, предприятие Wolters Kluwer.
- ^ Jump up to: а б Маарсевин, Н.В. и Баучер, К. (2008) Антиретровирусная резистентность в клинической практике . Лондон: Mediscript Ltd.
- ^ Кайрис В., Гилсон М.К., Латер В., Шиффер Калифорния, Фернандес MX. (2009)На пути к разработке устойчивых к мутациям ингибиторов ферментов: дальнейшая оценка гипотезы оболочки субстрата. Chem Biol Drug Des. Сентябрь; 74 (3): 234-45. doi: 10.1111/j.1747-0285.2009.00851.x
- ^ Налам М.Н., Али А., Альтман М.Д., Редди Г.С., Челлаппан С., Кайрис В., Озен А., Цао Х., Гилсон М.К., Тидор Б., Рана Т.М., Шиффер Калифорния. (2010)Оценка гипотезы субстрата-оболочки: структурный анализ новых ингибиторов протеазы ВИЧ-1, разработанных для обеспечения устойчивости к лекарственной устойчивости. Дж Вирол. Май 2010 г.;84(10):5368-78. doi: 10.1128/JVI.02531-09. Электронная публикация 2010 г., 17 марта.
- ^ Де Клерк, Э. (2009) Препараты против ВИЧ: 25 соединений, одобренных в течение 25 лет после открытия ВИЧ. Международный журнал противомикробных средств . 33; 307–320.
- ^ «GlaxoSmithKline прекращает клинические разработки исследуемого ингибитора протеазы бреканавира (640385)» . Архивировано из оригинала 3 декабря 2008 г. Проверено 11 июня 2008 г. Компания GlaxoSmithKline прекращает клинические разработки исследуемого ингибитора протеазы бреканавира (640385) . Получено 4 ноября. 2009.
- ^ «GSK и Concert Pharmaceuticals создают альянс для разработки новых препаратов, модифицированных дейтерием» . Архивировано из оригинала 31 августа 2009 г. Проверено 5 ноября 2009 г. GSK и Concert Pharmaceuticals создают альянс для разработки новых препаратов, модифицированных дейтерием . Получено 4 ноября. 2009.