Открытие и разработка ингибиторов желудочно-кишечной липазы.
| Ингибитор липазы | |
|---|---|
| Класс препарата | |
 | |
| Идентификаторы классов | |
| код АТС | А08АБ |
| Способ действия | Ингибирует желудочную липазу и липазу поджелудочной железы. |
| Юридический статус | |
| В Викиданных | |
Ингибиторы липазы относятся к классу препаратов, которые используются в качестве средств против ожирения . Их механизм действия заключается в ингибировании желудка и поджелудочной железы липаз , ферментов , которые играют важную роль в переваривании пищевых жиров . [ 2 ] Ингибиторы липазы классифицируются в системе классификации ATC как A08AB (средства против ожирения периферического действия). [ 3 ] Многие соединения были либо выделены из природы, либо полусинтезированы , либо полностью синтезированы , а затем проверены на их ингибирующую активность в отношении липазы. [ 4 ] но единственным ингибитором липазы на рынке (октябрь 2016 г.) является орлистат (Ксеникал, Алли). [ 5 ] Ингибиторы липазы также продемонстрировали противораковую активность, ингибируя синтазу жирных кислот . [ 6 ]
Открытие ингибиторов липазы и их разработка
[ редактировать ]Ингибитор панкреатической липазы был первоначально обнаружен и выделен из ферментированного бульона бактерии Streptomyces toxytricini в 1981 году и назван липстатином . [ 7 ] Это селективный и мощный необратимый ингибитор липаз желудка и поджелудочной железы человека. Тетрагидролипстатин , более известный как орлистат, представляет собой насыщенное производное, получаемое путем гидрирования . Он был разработан в 1983 году компанией Hoffmann-La Roche и представляет собой более простое и стабильное соединение, чем липстатин. [ 5 ] [ 8 ] [ 9 ] По этой причине орлистат был выбран вместо липстатина при разработке препарата против ожирения. [ 1 ] [ 10 ] Это единственный доступный пероральный ингибитор липазы, одобренный FDA , известный на рынке как Xenical и Alli. [ 5 ] Первоначально орлистат разрабатывался как средство для лечения дислипидемии , а не как средство против ожирения. Когда исследователи обнаружили, что он способствует меньшему потреблению энергии, внимание было переключено на ожирение. [ 11 ]
Орлистат имеет несколько побочных эффектов . Большинство зарегистрированных побочных эффектов связаны с желудочно-кишечным трактом; включая жидкий стул , стеаторею и боли в животе . Более тяжелым и серьезным является взаимодействие орлистата и антикоагулянтов при их совместном применении. Это может увеличить МНО , что может привести к недостаточному лечению антикоагулянтами и кровотечению. [ 12 ] Эти побочные эффекты орлистата чаще наблюдаются на ранних этапах терапии, но обычно уменьшаются со временем. Панкреатические липазы влияют не только на гидролиз триглицеридов, но также необходимы для гидролиза жирорастворимых витаминов . За счет этого может снизиться всасывание жирорастворимых витаминов. Поэтому во время терапии орлистатом рекомендуется принимать поливитаминные добавки. [ 9 ] [ 12 ]
Цетилистат , новый ингибитор липазы, является экспериментальным препаратом для лечения ожирения. В октябре 2016 года препарат все еще находился на стадии клинических испытаний . [ 13 ] Цетилистат был разработан для преодоления неблагоприятного воздействия орлистата на желудочно-кишечный тракт. Он имеет другую структуру, но аналогичен ингибирующей активности желудочно-кишечной липазы. Однако цетилистат по-другому взаимодействует с жировыми мицеллами переваренной пищи, поэтому имеет меньше побочных эффектов и лучшую переносимость . [ 14 ]
Механизм действия
[ редактировать ]
Ингибиторы липазы липстатин и орлистат действуют локально в кишечном тракте. Они минимально всасываются в кровоток из-за своей липофильности . [ 7 ] Следовательно, они не влияют на системные липазы. [ 11 ]
Механизм действия ингибиторов липазы в переваривании жиров показан на рисунке 1. Эти ингибиторы ковалентно связываются в виде сложного эфира с гидроксильной группой серина в активном центре липаз поджелудочной железы и желудка и образуют стабильный комплекс. [ 7 ] [ 15 ] Это приводит к конформационным изменениям фермента, которые вызывают обнажение каталитического активного центра. Когда активный центр обнажен, гидроксильная группа остатка серина ацилируется . Это приводит к необратимой инактивации фермента. Неактивная липаза не способна гидролизовать жиры до всасываемых жирных кислот и моноглицеридов, поэтому триглицериды выводятся с калом в непереваренном виде. [ нужна ссылка ] При таком способе действия потребление калорий из жиров в пище ограничивается, следовательно, снижается масса тела. [ 16 ] [ 17 ] Таким образом, основная роль ингибиторов липазы заключается в ингибировании липаз в желудочно-кишечном тракте, но они не обладают значительной активностью против протеаз , амилаз или других пищеварительных ферментов . [ 11 ]
Цетилистат имеет бициклическую структуру, но не имеет β-лактонового кольца. Он действует аналогично типичному ингибитору липазы, имеющему структуру β-лактона. [ 4 ] [ 16 ]
Цель по наркотикам
[ редактировать ]Липазы в желудочно-кишечном тракте играют решающую роль в переваривании жиров. Более 95% жиров в пище состоит из триглицеридов , которые классифицируются в зависимости от длины жирных кислот, связанных с глицеридным остовом. [ 18 ] Длина длинноцепочечных триглицеридов препятствует их всасыванию через слизистую оболочку кишечника . [ 19 ] По этой причине липазы в желудочно-кишечном тракте должны гидролизовать его до более мелких молекул, свободных жирных кислот и моноглицеридов . [ 20 ] до того, как произойдет абсорбция. [ 21 ]
Желудочная липаза
[ редактировать ]Желудочная и лингвальная липазы представляют собой два кислых липолитических фермента, происходящих в предуоденальной зоне, но у людей желудочная липаза находится в гораздо более высоких уровнях. Желудочная липаза синтезируется и секретируется из главных клеток желудка и стабильна при pH 1,5-8. [ 21 ] но имеет максимальную активность при pH 3-6. [ 20 ] Переваривание жиров начинается, когда желудочная липаза гидролизует пищевые триглицериды, отщепляя только одну длинную, среднюю или короткую ацильную цепь от глицеридного остова и высвобождая свободные жирные кислоты и диацилглицерины. Фермент гидролизует сложные эфиры в положении sn-3 , ацильной цепи внизу, быстрее, чем сложные эфиры в положении sn-1, ацильной цепи вверху глицеридной основной цепи. Однако активность желудочной липазы в отношении фосфолипидов и эфиров холестерина низкая.
Желудочная липаза состоит из 379 аминокислот . Полностью гликозилированный белок имеет массу 50 кДа, а негликозилированный фермент — 43 кДа. Однако дегликозилирование фермента не влияет на активность фермента. [ 21 ] Гидрофобная каталитической область вокруг Ser152, имеющая гексапептидную последовательность Val-Gly-His-Ser-Gln-Gly, важна для активности желудочной липазы. На N-конце Lys4 необходим ферменту для связывания на границе раздела липид-вода. [ 21 ]

Панкреатическая липаза
[ редактировать ]Панкреатическая липаза – важнейший липолитический фермент желудочно-кишечного тракта. [ 21 ] и необходим для переваривания жиров. [ 23 ] Панкреатическая липаза секретируется ацинарными клетками поджелудочной железы. [ 24 ] и его секреция вместе с соком поджелудочной железы в тонкую кишку стимулируется гормонами . Эти гормоны индуцируются в желудке гидролизованными продуктами желудочного пищеварения. [ 25 ] [ 26 ] Панкреатическая липаза секретируется в тонкую кишку, где она наиболее активна при рН 7-7,5. [ 20 ] Панкреатическая липаза гидролизует триглицериды и диглицериды, расщепляя ацильные цепи в положениях sn-1 и sn-3. [ 21 ] и высвобождает свободные жирные кислоты и 2-моноглицериды. [ 23 ]
Панкреатическая липаза состоит из 465 аминокислот. Схематическое изображение липазы поджелудочной железы показано на рисунке 2. Липазы поджелудочной железы и желудка имеют небольшую гомологию, но имеют одинаковую гидрофобную область в активном центре , что важно для липолитической активности. Гидрофобная область имеет гексапептидную последовательность Val-Gly-His-Ser-Gln-Gly и находится на уровне Ser153 в липазах поджелудочной железы и Ser152 в липазах желудка. [ 21 ]
Химия ингибиторов липазы
[ редактировать ]класс β-лактонов
[ редактировать ]Химическая структура соединений играет важную роль в связывании с мишенью. Наиболее важной и необходимой химической группой для связывания и активности этих соединений является β-лактонное (бета-лактонное) кольцо, которое является центральным фармакофором . Фрагмент β-лактона показан красным в структурах в таблице ниже. Исследования показали, что расщепление β-лактонового кольца приводит к потере ингибирующей активности ингибиторов, что делает структуру β-лактона важной частью биологической активности . [ 5 ] [ 8 ] Лактоновая кольцевая структура необратимо связывается с активным центром липазы и образует ковалентную связь, что приводит к ингибированию. [ 27 ]
К препаратам этого класса относятся:
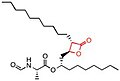
- Липстатин – первый известный ингибитор липазы. [ 4 ] происходит из природного источника. Он имеет β-пропиолактоновое кольцо, которое имеет 2,3-транс-дизамещенные линейные алкильные цепи, расположенные в α-(C6) и β-сайте (C13) соединения. Он содержит аминокислоту N-формил-L-лейцин, соединенную с β-алкильной цепью сложноэфирной связью . [ 5 ] Структура Липстатина представлена в таблице ниже. [ 28 ]
- Орлистат – полусинтетическое соединение, имеющее структуру, аналогичную липстатину. Они отличаются только насыщенностью β-алкильной цепи, где орлистат насыщен, а липстатин имеет две двойные связи в боковой цепи. [ 29 ] Структура орлистата показана в таблице из последнего раздела. [ 30 ]
Отношения структура-деятельность (SAR)
[ редактировать ]Большинство природных ингибиторов липазы различаются только строением боковых цепей и природой связанных аминокислот, но имеют одинаковое β-лактоновое кольцо. [ 5 ] в (S)-конфигурации как первичная структура. [ 1 ] Помимо роли β-лактонового кольца во взаимосвязи структура-активность , также имеет значение природа функциональных групп (например, сложноэфирных или простых эфиров и длина цепи в β-сайте). [ 4 ] Однако транс -положение боковых цепей β-лактонового кольца имеет решающее значение для его активности. [ 31 ]
| Липстатин | Орлистат | Эстераза | Валилактон | Панклицин Д | Эбелактон | Вибралактон | |
|---|---|---|---|---|---|---|---|
| Структура |  |
 |
 |
 |
 |
 | |
| IC 50 Значение | 6.9 × 10 −2 мкг/мл [ 1 ] | 1.2 × 10 −1 мкг/мл [ 1 ] | 2.0 × 10 −1 мкг/мл [ 1 ] | 1.4 × 10 −4 мкг/мл [ 1 ] | 3.9 × 10 −1 мкг/мл [ 1 ] | 1.0 × 10 −3 мкг/мл [ 1 ] | 4.0 × 10 −1 мкг/мл [ 1 ] |
Синтетический ингибитор липазы: цетистат.
[ редактировать ]| Цетилистат | |
|---|---|
| Структура | |
| ИЮПАК | 2-гексадетокси-6-метил-3,1-бензоксазин-4-он [ 32 ] |
| Химическая формула | С 25 Ч 39 НЕТ 3 [ 32 ] |
| Молярная масса (g/mol) | 401.6 [ 32 ] |
| ICIC50 | 5,95 нмоль/л = 2,39 × 10 −3 мкг/мл (липаза поджелудочной железы человека) [ 33 ] |
Цетилистат – синтетический ингибитор липазы. Вместо структуры β-лактона, как у большинства ингибиторов липазы, [ 16 ] он имеет бициклическое бензоксазиноновое кольцо. Это также липофильное соединение, но оно отличается гидро- и липофильной боковой цепью. [ 14 ] Структура и дополнительная информация о Цетилистате представлены в таблице справа. [ 32 ]
Другие ингибиторы липазы
[ редактировать ]Известны и другие ингибиторы липазы, например, из различных растительных продуктов. К ним относятся алкалоиды , каротиноиды , гликозиды , полифенолы , полисахариды , сапонины и терпеноиды . Однако ни один из них не использовался клинически в качестве ингибиторов липазы. Более активными ингибиторами липазы являются липофильные соединения микробного происхождения. [ 4 ]
Ингибиторы липазы микробного происхождения можно разделить на два класса в зависимости от их структуры. Те, у кого есть β-лактоновое кольцо, — это липстатин, валиктон, перцихинин, панклицин АЕ, эбелактон А и В, вибралактон и эстерастин. Те, у кого нет β-лактонового кольца, — это (E)-4-аминостирилацетат , ε– полилизин и каулерпенин. [ 8 ]
Ингибиторы липазы также были получены синтетически, например цетилистат, на основе структуры триглицеридов и других природных субстратов липазы. [ 8 ] Однако синтетические ингибиторы липазы различаются по структуре, и у некоторых из них отсутствует β-лактоновое кольцо. [ 4 ]
Дополнительные мероприятия
[ редактировать ]Потенциал лечения рака
[ редактировать ]Как обсуждалось далее, орлистат является ингибитором липазы поджелудочной железы и желудка. Орлистат также является мощным ингибитором тиоэстеразы и, следовательно, ингибирует синтазу жирных кислот (ФАС). Поскольку ФАС необходим для опухолевых клеток , для их роста и выживания, а также активируется и сверхэкспрессируется в различных опухолях, [ 34 ] ученые возлагают большие надежды на ФАС как на мишень для лечения онкологических заболеваний . [ 35 ] Орлистат ингибирует ФАС по тому же механизму, что и липазу поджелудочной железы, то есть путем ковалентного связывания с активным сериновым участком. [ 35 ] Этот эффект орлистата как ингибитора ФАС был впервые выявлен в ходе высокопроизводительного скрининга ферментов, ингибирующих активность рака простаты. Однако ФАС устойчив ко многим противораковым препаратам. Орлистат повышает чувствительность этих противораковых препаратов, устойчивых к ФАС, ингибируя ФАС. [ 36 ] В нормальных тканях экспрессия ФАС низкая, поэтому активность орлистата на нормальных клетках ограничена. Из-за разницы в экспрессии FAS между нормальными и раковыми клетками орлистат избирательно воздействует на опухолевые клетки. В связи с этим ФАС является потенциальной мишенью для лечения рака. [ 34 ] [ 37 ]
Орлистат действует локально в кишечнике как ингибитор липазы и поэтому имеет ряд ограничений при разработке в качестве системного препарата. Его плохая биодоступность и растворимость являются основными причинами разработки нового противоракового аналога для преодоления этих ограничений. [ 6 ] [ 34 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж Шефер Б. (2015). Натуральные продукты в химической промышленности . Берлин Гейдельберг: Springer.
- ^ Герчолини Р. (июнь 1997 г.). «Способ действия орлистата». Международный журнал ожирения и связанных с ним метаболических нарушений . 21 (Приложение 3): С12–23. ПМИД 9225172 .
- ^ «Все централизованные лекарственные средства для человека по коду АТС» . Общественное здравоохранение . Европейская комиссия . Проверено 1 октября 2016 г.
- ^ Jump up to: а б с д и ж Лунагария Н.А., Патель Н.К., Джагтап С.К., Бутани К.К. (2014). «Ингибиторы панкреатической липазы: современное состояние и клинические перспективы» . Журнал EXCLI . 13 : 897–921. ПМЦ 4464291 . ПМИД 26417311 .
- ^ Jump up to: а б с д и ж Бай Т, Чжан Д, Линь С, Лонг Ц, Ван Ю, Оу Х, Кан Ц, Дэн З, Лю В, Тао М (декабрь 2014 г.). «Оперон для биосинтеза липстатина, бета-лактонового ингибитора липазы поджелудочной железы человека» . Прикладная и экологическая микробиология . 80 (24): 7473–83. Бибкод : 2014ApEnM..80.7473B . дои : 10.1128/АЕМ.01765-14 . ПМК 4249243 . ПМИД 25239907 .
- ^ Jump up to: а б Пурохит В.К., Ричардсон Р.Д., Смит Дж.В., Ромо Д. (июнь 2006 г.). «Практический каталитический асимметричный синтез бета-лактонов посредством последовательного процесса димеризации/гидрирования кетенов: ингибиторы тиоэстеразного домена синтазы жирных кислот». Журнал органической химии . 71 (12): 4549–58. дои : 10.1021/jo060392d . ПМИД 16749788 .
- ^ Jump up to: а б с Медейрос-Нето Г.А., Халперн А., Бушар С. (2003). «Глава 9: Орлистат в лечении ожирения». В Халперне А. (ред.). Прогресс в исследованиях ожирения . Пресса о еде и питании.
- ^ Jump up to: а б с д Бирари Р.Б., Бутани К.К. (октябрь 2007 г.). «Ингибиторы панкреатической липазы из природных источников: неизведанный потенциал». Открытие наркотиков сегодня . 12 (19–20): 879–89. дои : 10.1016/j.drudis.2007.07.024 . ПМИД 17933690 .
- ^ Jump up to: а б Хек А.М., Яновский Дж.А., Чалис К.А. (март 2000 г.). «Орлистат, новый ингибитор липазы для лечения ожирения» . Фармакотерапия . 20 (3): 270–9. дои : 10.1592/phco.20.4.270.34882 . ПМК 6145169 . ПМИД 10730683 .
- ^ Помье А., Понс Дж. М., Коценски П. Дж. (ноябрь 1995 г.). «Первый полный синтез (-)-липстатина». Журнал органической химии . 60 (22): 7334–9. дои : 10.1021/jo00127a045 .
- ^ Jump up to: а б с Уайлдинг Дж. П. (2008). «Ингибиторы кишечной липазы». В Wilding JP (ред.). Фармакотерапия ожирения . Базель: Биркхойзер.
- ^ Jump up to: а б с «Краткое описание характеристик продукта» (PDF) . Ксеникал . Европейское агентство лекарственных средств. 19 декабря 2013 года . Проверено 1 октября 2016 г.
- ^ «Вопросы и ответы об инициативе FDA против загрязненных продуктов для похудания» . Управление по контролю за продуктами и лекарствами США . Министерство здравоохранения и социальных служб США . Проверено 1 октября 2016 г.
- ^ Jump up to: а б Брайсон А., де ла Мотт С., Дунк С. (март 2009 г.). «Снижение всасывания пищевых жиров с помощью нового ингибитора желудочно-кишечной липазы цетилистата у здоровых добровольцев» . Британский журнал клинической фармакологии . 67 (3): 309–15. дои : 10.1111/j.1365-2125.2008.03311.x . ПМК 2675041 . ПМИД 19220279 .
- ^ Брей Г.А., Райан Д. (2007). «Эктопический жир и метаболический синдром». В Толедо Ф.Г., Келли Д.Е. (ред.). Избыточный вес и метаболический синдром: от скамьи до постели . США: Спрингер.
- ^ Jump up to: а б с Падвал Р. (апрель 2008 г.). «Цетилистат, новый ингибитор липазы для лечения ожирения». Текущее мнение об исследуемых препаратах . 9 (4): 414–21. ПМИД 18393108 .
- ^ Гра Ж (декабрь 2013 г.). «Цетилистат для лечения ожирения». Наркотики сегодня . 49 (12): 755–9. дои : 10.1358/точка.2013.49.12.2099318 . ПМИД 24524093 .
- ^ Вацлавик В., Кристиан Э.В. (2007). Основы пищевой науки . Нью-Йорк: Спрингер.
- ^ Чоу Б.П., Шаффер Э.А., Парсонс Х.Г. (апрель 1990 г.). «Абсорбция триглицеридов в отсутствие липазы». Канадский журнал физиологии и фармакологии . 68 (4): 519–23. дои : 10.1139/y90-074 . ПМИД 2328454 .
- ^ Jump up to: а б с Мюллер Г., Петри С. (2006). «Физиология желудочно-кишечного липолиза и терапевтическое использование липаз и ингибиторов пищеварительных липаз». Липазы и фосфолипазы в разработке лекарств: от биохимии к молекулярной фармакологии . Уайли.
- ^ Jump up to: а б с д и ж г Дуань Р.Д. (2000). «Ферментативные аспекты переваривания жиров в желудочно-кишечном тракте». В Кристофе AB, Де Вризе С. (ред.). Переваривание и всасывание жиров . Шампейн, Иллинойс: AOCS. стр. 25–46. ISBN 978-1-893997-12-7 .
- ^ Чен Б., Цай З., Ву В., Хуан Ю., Плейс Дж., Линь З. (декабрь 2009 г.). «Морфинговая активность между структурно сходными ферментами: от безгемовой бромпероксидазы до липазы». Биохимия . 48 (48): 11496–504. дои : 10.1021/bi9014727 . ПМИД 19883129 .
- ^ Jump up to: а б Джонсон Л.Р. (2013). Желудочно-кишечная физиология. Переваривание и всасывание питательных веществ . Эльзевир Мосби.
- ^ Мансбах II CM, Цо П, Куксис А (июнь 2011 г.). Лоу М.Э. (ред.). Кишечный липидный обмен . Springer Science & Business Media.
- ^ Шахиди Ф (2006). «Влияние структуры на абсорбцию и метаболизм нутрицевтиков и специальных липидов». Нутрицевтики и специальные липиды и их сопутствующие продукты . ЦРК Пресс.
- ^ Хой CE, Му Х (2000). «Влияние структуры триацилглицерина на всасывание жира». В Кристофе AB, Де Вризе С. (ред.). Переваривание и всасывание жиров . Шампейн, Иллинойс: AOCS. стр. 218–34. ISBN 978-1-893997-12-7 .
- ^ Ядав Дж.С., Рао К.В., Редди М.С., Прасад А.Р. (июнь 2006 г.). «Стереоселективный синтез (-)-тетрагидролипстатина с помощью стратегии, основанной на радикальной циклизации». Буквы тетраэдра . 47 (26): 4393–5. дои : 10.1016/j.tetlet.2006.04.101 .
- ^ «(-)-Липстатин» . База данных соединений PubChem . Национальный центр биотехнологической информации . Проверено 1 октября 2016 г.
- ^ Голай А (2000). «Роль пищевых жиров при ожирении и терапии орлистатом». В Кристофе AB, Де Вризе С. (ред.). Переваривание и всасывание жиров . Шампейн, Иллинойс: AOCS. стр. 420–32. ISBN 978-1-893997-12-7 .
- ^ «Орлистат» . База данных соединений PubChem . Национальный центр биотехнологической информации . Проверено 1 октября 2016 г.
- ^ Бодкин Дж. А., Хамфрис Э. Дж., Маклеод, доктор медицинских наук (2003). «Полный синтез (–)-тетрагидролипстатина». Австралийский химический журнал . 56 (8): 795–803. дои : 10.1071/CH03121 .
- ^ Jump up to: а б с д «Цетилистат» . База данных соединений PubChem . Национальный центр биотехнологической информации . Проверено 1 октября 2016 г.
- ^ Ямада, Ю; Като, Т; Огино, Х; Ашина, С; Като, К. (август 2008 г.). «Цетилистат (ATL-962), новый ингибитор липазы поджелудочной железы, способствует увеличению массы тела и улучшает липидный профиль у крыс». Гормональные и метаболические исследования = Hormon- und Stoffwechselforschung = Hormones et Métabolisme . 40 (8): 539–43. дои : 10.1055/s-2008-1076699 . ПМИД 18500680 .
- ^ Jump up to: а б с Флавин Р., Пелусо С., Нгуен П.Л., Лода М. (апрель 2010 г.). «Синтаза жирных кислот как потенциальная терапевтическая мишень при раке» . Будущая онкология . 6 (4): 551–62. дои : 10.2217/фон.10.11 . ПМК 3197858 . ПМИД 20373869 .
- ^ Jump up to: а б Ричардсон Р.Д., Ма Г., Ойола Ю., Занканелла М., Ноулз Л.М., Чеплак П., Ромо Д., Смит Дж.В. (сентябрь 2008 г.). «Синтез новых бета-лактоновых ингибиторов синтазы жирных кислот» . Журнал медицинской химии . 51 (17): 5285–96. дои : 10.1021/jm800321h . ПМК 3172131 . ПМИД 18710210 .
- ^ Фако В.Е., Чжан Дж.Т., Лю Цзюй (октябрь 2014 г.). «Механизм гидролиза орлистата тиоэстеразой синтазы жирных кислот человека» . АКС-катализ . 4 (10): 3444–3453. дои : 10.1021/cs500956m . ПМЦ 4188697 . ПМИД 25309810 .
- ^ Пандей П.Р., Лю В., Син Ф., Фукуда К., Ватабе К. (май 2012 г.). «Противораковые препараты, нацеленные на синтазу жирных кислот (ФАС)». Недавние патенты на открытие противораковых препаратов . 7 (2): 185–97. дои : 10.2174/157489212799972891 . ПМИД 22338595 .
