Открытие и разработка ингибиторов фосфодиэстеразы 5.
Эту статью необходимо обновить . ( март 2017 г. ) |
Фосфодиэстеразы ФДЭ) представляют собой суперсемейство ферментов ( . Это суперсемейство далее классифицируется на 11 семейств, PDE1-PDE11, на основании регуляторных свойств, аминокислотных последовательностей, специфичности субстрата, фармакологических свойств и распределения в тканях. Их функция заключается в разложении внутриклеточных вторичных мессенджеров, таких как циклический аденинмонофосфат ( цАМФ ) и циклический гуанозинмонофосфат ( цГМФ ), что приводит к нескольким биологическим процессам, таким как влияние на внутриклеточный уровень кальция со стороны Ca. 2+ путь. [ 1 ]
Фосфодиэстераза 5 ( ФДЭ5 ) широко экспрессируется в нескольких тканях организма, например, в головном мозге, легких, почках, мочевом пузыре, гладких мышцах и тромбоцитах. [ 1 ] Предотвратить гидролиз цГМФ можно путем ингибирования ФДЭ5 и, следовательно, лечить заболевания, связанные с низким уровнем цГМФ, поскольку ФДЭ5 является идеальной мишенью для разработки ингибиторов. [ 2 ] Терапевтический эффект ингибирования ФДЭ5 был продемонстрирован при ряде сердечно-сосудистых заболеваний, хронической болезни почек и сахарном диабете . [ 3 ]
Основными ингибиторами ФДЭ5 (подгруппа ингибиторов фосфодиэстеразы ) являются силденафил , тадалафил , варденафил и аванафил , и хотя все они имеют одинаковый механизм действия, каждый из них обладает уникальными фармакокинетическими и фармакодинамическими свойствами, которые определяют их пригодность в различных условиях и профиль побочных эффектов. . [ 3 ]
Общий
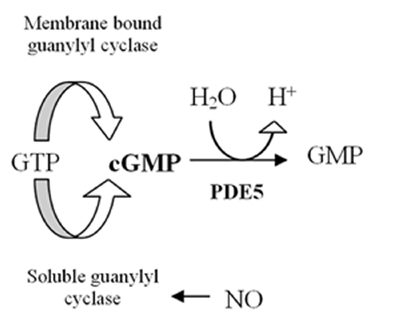
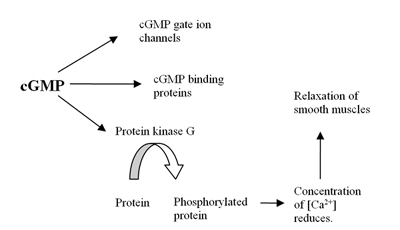
[ редактировать ]Геном человека содержит по меньшей мере 21 ген, участвующий в определении внутриклеточных уровней цАМФ и цГМФ путем экспрессии фосфодиэстеразы белков или ФДЭ. Эти PDE сгруппированы как минимум в 11 функциональных подсемейств, названных PDE1-PDE11. [ 4 ] ФДЭ — это ферменты, которые гидролизуют циклический аденозин-3,5-монофосфат (цАМФ) и циклический гуанозин-3,5-монофосфат (цГМФ), которые являются внутриклеточными вторичными мессенджерами , до АМФ и ГМФ. Эти вторичные мессенджеры контролируют многие физиологические процессы. [ 5 ] цАМФ АТФ образуется из цГМФ ферментом , аденилатциклазой , а образуется из ГТФ ферментом гуанилилциклазой , которые либо мембраносвязаны либо растворимы в цитозоле . В растворимом состоянии он действует как рецептор оксида азота (NO) (см. рисунок 1). [ 6 ] Образование цГМФ инициирует несколько реакций в организме, включая влияние на ионные каналы цГМФ , цГМФ связывающие белки, , и протеинкиназу G (PKG). Воздействие на ПКГ снижает уровень кальция , что приводит к расслаблению гладких мышц (см. рисунок 2). [ 7 ] Фермент PDE5 специфичен для цГМФ , что означает, что он гидролизует только цГМФ , но не цАМФ. [ 8 ] Селективность опосредована сложной сетью водородных связей , которая благоприятна для цГМФ, но неблагоприятна для цАМФ в ФДЭ5. [ 9 ] При ингибировании фермента ФДЭ5 концентрация цГМФ повышается и, следовательно, может увеличить расслабление гладких мышц. [ 7 ] ФДЭ5 имеет только один подтип, ФДЭ5А, из которых у человека существует 4 изоформы, называемые ФДЭ5А1-4. [ 8 ] Разница между изоформами PDE5A1-3 заключается только в 5'-конце мРНК и соответствующем N-конце белка. [ 10 ]
Распределение ФДЭ5 в организме
[ редактировать ]У человека распределение изоформ PDE5A1 и PDE5A2 одинаковое и их можно обнаружить в мозге , легочной ткани, сердце , печени , почках , мочевом пузыре , предстательной железе , уретре , половом члене , матке и скелетных мышцах . PDE5A2 встречается чаще, чем PDE5A1. PDE5A3 не так широко распространен, как две другие изоформы, и обнаруживается только в гладкомышечных тканях, он обнаруживается в сердце , мочевом пузыре , простате , уретре , половом члене и матке . [ 10 ] [ 11 ] Точное распределение изоформ PDE5A4 в литературе не обнаружено. Фермент ФДЭ5 у людей также обнаружен в тромбоцитах , клетках желудочно-кишечного тракта эпителиальных клетках Пуркинье мозжечка , , [ 12 ] тело пещеристое [ 5 ] поджелудочная железа , [ 13 ] плацента и толстая кишка, [ 4 ] кавернозное тело клитора, а также гладкие мышцы и эпителий влагалища. [ 11 ]
Структура PDE и SAR
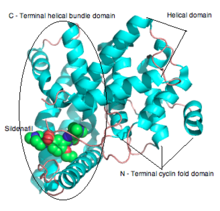
[ редактировать ]Ферменты PDE состоят из 3 функциональных доменов: N-концевого циклинового складчатого домена, линкерного спирального домена и С-концевого домена спирального пучка (см. рисунок 3). [ 9 ] Активный сайт представляет собой глубокий карман на стыке трех субдоменов и выстлан высококонсервативными остатками между изотипами ФДЭ. [ 14 ] Глубина кармана составляет примерно 15 Å, а размер отверстия — примерно 20 на 10 Å. По расчетам, объем активного сайта составляет от 875 до 927 Å. 3 . [ 14 ] Активный центр ФДЭ5 был описан как разделенный на 3 основных участка в зависимости от его кристаллической структуры в комплексе с силденафилом : [ 7 ]
- Сайт M: содержит ионы цинка и магния . Роль ионов заключается в стабилизации структуры и активации гидроксида для обеспечения реакции. Современные ингибиторы ФДЭ5 не взаимодействуют с ионами металлов, в отличие от цГМФ . Прямое или непрямое взаимодействие может улучшить эффективность будущих ингибиторов. [ 9 ]
- Карман Q: считается, что гуанидиновая группа цГМФ связывается в этой области, поскольку карман Q вмещает пиразолопиримидиноновую группу (см. рисунок 4) силденафила . Пиразолпиримидинон силденафила имитирует гуанин в цГМФ и имеет те же донорные и акцепторные свойства Н-связи, образуя бидендратную Н-связь с Q817. Кард и др. опишите карман Q как разделенный на 3 части: [ 14 ]
- Седло, образованное консервативным глутамином (Q817 в PDE5A, Q443 в PDE4B и Q369 в PDE4D) и P-зажимом (гидрофобный зажим на узкой стороне кармана активных центров, образованный инвариантным пуринселективным глютамином и парой консервативных остатки). [ 14 ]
- 2 узких гидрофобных кармана, Q1 и Q2, состоящие в основном из гидрофобных остатков, окружающих седло. [ 14 ]
- L-область: метилпиперазиновая группа (см. рисунок 4) силденафила окружена остатками Tyr 664, Met 816, Ala 823 и Gly 819, а остатки 662-664 образуют крышку над карманом, сужая вход в активный центр ФДЭ5. .
Чон и др. [ 9 ] также опишите четвертый карман, называемый H-карманом, который является гидрофобным и вмещает этоксифенильную группу силденафила. Три ингибитора ФДЭ5, уже имеющиеся на рынке, силденафил , тадалафил и варденафил , занимают часть активного сайта, в основном вокруг кармана Q, а иногда и кармана М, и все три взаимодействуют с активным сайтом тремя важными способами:
- взаимодействие между ионами металлов, опосредованное водой
- водородная связь с седлом Q-кармана
- гидрофобное взаимодействие с гидрофобными остатками, выстилающими полость активного центра. [ 14 ]
Также было описано, что гидрофобное взаимодействие с карманами Q1 и Q2 важно для эффективности ингибитора, а различия между изотипами ФДЭ в кармане Q2 можно использовать для селективности между изотипами. [ 14 ]

Роль в заболеваниях
[ редактировать ]Эректильная дисфункция
[ редактировать ]Препараты, ингибирующие ФДЭ5, силденафил , тадалафил и варденафил , используются для лечения эректильной дисфункции . [ 16 ] Эти ингибиторы повышают уровень цГМФ, расслабляют гладкие мышцы и, следовательно, вызывают эрекцию полового члена. [ 9 ] во время сексуальной стимуляции. [ 17 ]
Легочная артериальная гипертензия
[ редактировать ]Повышение регуляции экспрессии гена PDE5 наблюдалось на животных моделях легочной гипертензии и, как полагают, способствует вазоконстрикции в легких. [ 3 ] Несколько рандомизированных контролируемых исследований по изучению использования ингибиторов ФДЭ5 при легочной артериальной гипертензии, подтипе легочной гипертензии, продемонстрировали их мощный эффект в снижении легочной гипертензии и ремоделировании сосудов, а также в улучшении симптомов и смертности у пациентов с этим заболеванием. [ 3 ] [ 7 ] [ 18 ] Было показано, что длительное лечение ингибитором ФДЭ5 усиливает путь натрийуретический пептид-цГМФ, снижает регуляцию кальция. 2+ сигнальный путь и изменяют тонус сосудов в легочных артериях на крысиных моделях. [ 9 ]
Доброкачественная гиперплазия предстательной железы
[ редактировать ]С 2011 года препарат длительного действия тадалафил лицензирован для лечения симптомов мочеиспускания, возникающих в результате доброкачественной гиперплазии предстательной железы. [ 3 ]
Будущие показания к использованию ингибиторов ФДЭ5
[ редактировать ]Сердечно-сосудистые заболевания
[ редактировать ]Ингибиторы ФДЭ5 оказывают широкомасштабное воздействие на сердечно-сосудистую систему, выходя за рамки острого гемодинамического влияния. Например, было показано, что ингибиторы PDE5 улучшают некоторые параметры функции эндотелия. [ 3 ] их использование в лечении системной гипертензии (включая резистентную к лечению гипертензию), кардиопротекции , сердечной недостаточности и заболеваниях периферических артерий . Все чаще оценивается [ 3 ]
Сердечная недостаточность
[ редактировать ]Ингибиторы ФДЭ5 показали многообещающую эффективность в лечении сердечной недостаточности со сниженной фракцией выброса благодаря ряду положительных эффектов на сосуды легких , ремоделирование сердца и диастолическую функцию . [ 3 ] Исследование показало, что эффективное лечение легочной артериальной гипертензии силденафилом улучшает функциональные возможности и снижает массу правого желудочка у пациентов. Влияние на ремоделирование правого желудочка было значительно выше по сравнению с неселективным антагонистом эндотелиальных рецепторов бозентаном . [ 7 ] Однако ингибиторы ФДЭ5 могут быть вредными для пациентов с сердечной недостаточностью с сохраненной фракцией выброса из-за потенциальных отрицательных инотропных эффектов. [ 3 ]
Хроническая болезнь почек
[ редактировать ]Экспериментальные исследования на животных показали, что ингибиторы ФДЭ5 могут обратить вспять повреждение почек независимо от их влияния на артериальное давление посредством внутрипочечных механизмов. [ 3 ] Также было показано, что у людей ингибиторы ФДЭ5 снижают протеинурию , маркер повреждения почек. [ 3 ] Однако успешное внедрение ингибиторов SGLT2 и антагонистов рецепторов эндотелина в область почечной терапии делает разработку ингибиторов PDE5 для этой цели маловероятной. [ 3 ]
Сахарный диабет
[ редактировать ]Было показано, что ингибиторы ФДЭ5 обладают различными макрососудистыми , микрососудистыми и метаболическими преимуществами при сахарном диабете . [ 3 ] а в крупном исследовании мужчин с сахарным диабетом 2 типа было обнаружено, что эти препараты значительно снижают риск смерти пациентов от любой причины. [ 19 ] Неясно, в какой степени это наблюдение отражает защитное действие ингибиторов ФДЭ5 против сердечно-сосудистых и почечных заболеваний. [ 3 ]
Феномен Рейно
[ редактировать ]силденафил Было показано, что по меньшей мере так же эффективен, как и блокаторы кальциевых каналов , при лечении тяжелого синдрома Рейно (РП), связанного с системной склеродермией и изъязвлениями пальцев. [ 3 ] При приеме силденафила в течение 4 недель у субъектов наблюдалось снижение средней частоты и продолжительности приступов Рейно, а также значительное снижение средней оценки состояния Рейно. Скорость капиллярного кровотока также увеличилась у каждого отдельного пациента, а средняя скорость капиллярного кровотока у всех пациентов значительно увеличилась. Эти результаты были получены без значительного снижения системного артериального давления . [ 7 ] Однако терапевтические эффекты ингибиторов ФДЭ5 при первичном (идиопатическом) РП менее четко определены. [ 3 ]
Гладить
[ редактировать ]силденафил Было показано, что значительно улучшает нейрососудистую связь, не влияя на общий мозговой кровоток, за счет повышения уровня цГМФ в мозге, вызывая нейрогенез и уменьшая неврологический дефицит у крыс через 2 или 24 часа после инсульта. Эти экспериментальные данные позволяют предположить, что ингибиторы ФДЭ5 могут способствовать восстановлению после инсульта . [ 7 ] [ 9 ] [ 11 ] Однако исследования на людях остаются безрезультатными. [ 3 ]
Преждевременная эякуляция
[ редактировать ]добавление ингибиторов ФДЭ5 к препаратам СИОЗС (например, пароксетину) для лечения преждевременной эякуляции может привести к лучшему контролю эякуляции. Согласно недавним исследованиям, [ 11 ] Возможный механизм основан на системе трансдукции оксида азота (NO)/цГМФ как центрального и периферического медиатора ингибирующей неадренергической, нехолинергической нитрергической нейротрансмиссии в мочеполовой системе. [ 16 ]
Расстройство сексуального возбуждения у женщин
[ редактировать ]ФДЭ5 экспрессируется в пещеристых телах клитора, а также в гладких мышцах и эпителии влагалища. Таким образом, вполне возможно, что ингибиторы ФДЭ5 могут влиять на расстройство сексуального возбуждения у женщин, но необходимы дальнейшие исследования. Было показано, что повышенные уровни цГМФ наблюдаются в культивируемых у человека гладкомышечных клетках влагалища, обработанных ингибитором ФДЭ5, что позволяет предположить участие оси NO/цГМФ в женской сексуальной реакции. [ 11 ]
Расстройство сексуального истощения
[ редактировать ]Сходство многих ингибиторов ФДЭ5 со структурой многих аналогов кофеина , которые также являются антагонистами аденозина, позволяет предположить, что в будущем возможно будет создать ингибитор ФДЭ5, который, как и кофеин, также является антагонистом аденозина.
Открытие
[ редактировать ]ФДЭ5 — это фермент, который был впервые выделен в 1980 году из легких крыс. [ 20 ] ФДЭ5 преобразует внутриклеточный цГМФ в нуклеотид ГМФ. [ 21 ] ФДЭ5 содержится во многих тканях, таких как легкие, почки, мозг, тромбоциты, печень, простата, уретра, мочевой пузырь и гладкие мышцы. Из-за локализации ФДЭ5 в гладкой мышечной ткани были разработаны ингибиторы для лечения эректильной дисфункции наряду с легочной гипертензией . [ 1 ] [ 2 ]
Силденафил впервые был представлен для клинических испытаний в 1989 году. Это стало результатом обширных исследований химических агентов, воздействующих на ФДЭ5, которые могут быть эффективны при лечении ишемической болезни сердца . [ 22 ] Силденафил не оказался эффективным при ишемической болезни сердца, но был обнаружен интересный побочный эффект — эрекция полового члена . Этот побочный эффект вскоре стал основной областью исследований. [ 23 ] Ингибитор высокоселективен в отношении семейства ФДЭ5. [ 22 ]
Силденафил — это прототип ингибиторов ФДЭ5, который компания Pfizer выпустила под названием «Виагра» . Он был одобрен Управлением по контролю за продуктами и лекарствами (FDA) в 1998 году как первое пероральное лекарство от эректильной дисфункции. Позже, в 2005 году, он был одобрен для лечения легочной артериальной гипертензии. [ 2 ] Варденафил и тадалафил были открыты в 1990 году. Эти препараты появились в результате исследовательских программ, направленных на поиск ингибиторов ФДЭ5 для лечения сердечно-сосудистых заболеваний и эректильной дисфункции. Два ингибитора PDE5 вскоре стали использоваться для лечения этих состояний. [ 22 ] [ 23 ]
Тадалафил является наиболее универсальным ингибитором и имеет самый длительный период полураспада — 17,5 часов. Это обеспечивает более длительное терапевтическое окно и, следовательно, часто является более удобным препаратом, чем другие препараты с более коротким терапевтическим окном. Тадалафил более биодоступен (80%), чем силденафил (40%) и варденафил (15%), но всасывается медленно, или около 2 часов по сравнению с 50 минутами силденфила. Варденафил наиболее известен своей эффективностью. [ 24 ]
Из-за серьезных побочных эффектов и неудовлетворенности пациентов текущим выбором терапии недавно были одобрены для клинического использования другие ингибиторы. К этим ингибиторам относятся уденфил, аванафил, лоденафил и мироденафил. [ 25 ]
Разработка
[ редактировать ]Биологическая активность
[ редактировать ]Эрекция полового члена
[ редактировать ]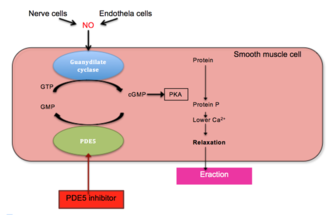
Эрекция полового члена является гемодинамическим событием в гладких мышцах кавернозного тела. [ 26 ] ФДЭ5 является основным ферментом, гидролизующим цГМФ, обнаруженным в кавернозных телах полового члена. [ 27 ] Эрекция запускается высвобождением нейромедиатора оксида азота (NO) из неадренергических и нехолинергических нейронов нервных окончаний полового члена, а также из эндотелиальных клеток . NO активирует растворимую гуанилилциклазу в гладкомышечных клетках полового члена, что приводит к увеличению выработки 3'-5'-циклического гуанозинмонофосфата из гуанозин-5'-трифосфата (GTP). [ 21 ] [ 28 ] [ 29 ] Циклический GMP связывается с цГМФ-зависимой протеинкиназой (PKG1), которая фосфорилирует несколько белков, что приводит к снижению внутриклеточного кальция. Снижение внутриклеточного кальция приводит к расслаблению гладких мышц и, в конечном итоге, к эрекции полового члена. Этот путь продемонстрирован на рисунке 1 . [ 29 ] [ 30 ]
Эректильная дисфункция
[ редактировать ]ФДЭ5 разрушает цГМФ и, следовательно, подавляет эрекцию. Как показано на рисунке 1 , ингибирование ФДЭ5 снижает деградацию цГМФ и приводит к эрекции полового члена. [ 28 ] [ 31 ] Из-за этого действия ингибиторы ФДЭ5 были разработаны для лечения эректильной дисфункции полового члена. [ 32 ]
Фермент фосфодиэстераза 5
[ редактировать ]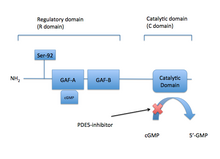
Фермент PDE5 имеет молекулярную массу 200 кДа и его активное состояние представляет собой гомодимер . [ 21 ] PDE5 состоит из мономеров , каждый из которых содержит два основных функциональных домена: регуляторный домен (R-домен), который расположен в N-концевой части белка, и каталитический домен (C-домен), расположенный в более С-концевой части белка. . [ 33 ] [ 21 ]
Домен R содержит специфический аллостерический сайт связывания цГМФ, который контролирует функцию ферментов. Этот сайт специфического связывания состоит из субдомена GAF (цГМФ-специфическая цГМФ-стимулированная ФДЭ, аденилатциклаза и FhlA), который расположен в N-концевой части специфических белков. Аллостерический сайт связывания GAF состоит из GAFa и GAFb, где GAFa имеет более высокую аффинность связывания. Важность и функциональная роль двух гомологичных сайтов связывания неизвестны. [ 34 ]
Конформационные изменения происходят, когда цГМФ связывается с аллостерическим сайтом, который экспонирует серин и обеспечивает фосфорилирование. Результаты фосфорилирования серина приводят к усилению гидролиза цГМФ в каталитическом домене. Сродство каталитического домена к цГМФ увеличивается и еще больше увеличивает активность каталитического домена PDE5. [ 33 ] Через домен C внутриклеточный цГМФ быстро разлагается под действием ФДЭ5, что сводит к минимуму активность цГМФ на его субстрате PKG1 за счет расщепления циклической фосфатной части цГМФ до ГМФ. GMP представляет собой неактивную молекулу, не имеющую активности вторичного мессенджера. [ 33 ] [ 35 ]
Фосфорилирование одного серина с помощью PKG1 и аллостерического сайта связывания цГМФ активирует каталитическую активность PDE5, и результатом является по отрицательной обратной связи регуляция передачи сигналов cGMP/NO/PKG1 . Таким образом, цГМФ взаимодействует как с аллостерическим, так и с каталитическим доменом фермента ФДЭ5, а ингибиторы ФДЭ5 конкурируют с цГМФ за связывание с каталитическим доменом, что приводит к более высоким уровням цГМФ. [ 33 ] Домены PDE5 показаны на фигуре 2 .
Ингибиторы ФДЭ5
[ редактировать ]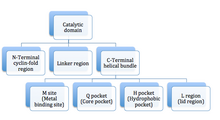
Ингибиторы ФДЭ5 силденафил, варденафил и тадалафил являются конкурентными и обратимыми ингибиторами гидролиза цГМФ каталитической стороной ФДЭ5. Структуры варденафила и силденафила схожи, они оба содержат схожее структурированное пуриновое кольцо цГМФ, что позволяет им действовать в качестве конкурентного ингибитора ФДЭ5. Различие молекулярных структур является причиной взаимодействия с каталитическим центром ФДЭ5 и повышает аффинность этих соединений по сравнению с селективностью цГМФ. [ 33 ]
Фармакофор
[ редактировать ]Фармакофорная модель ФДЭ5 обычно состоит из одного акцептора водородной связи, одной гидрофобной алифатической углеродной цепи и двух ароматических колец. Небольшой гидрофобный карман и H-петля фермента PDE5 важны для аффинности связывания ингибиторов PDE5. А также позиционные и конформационные изменения наблюдаются при связывании ингибитора во многих случаях. [ 36 ]
Активный сайт PDE5 расположен в домене спирального пучка в центре домена C (каталитический домен). Карман субстрата состоит из четырех субсайтов: сайта M (сайт связывания металла), кармана Q (карман ядра), кармана H (гидрофобный карман) и региона L (область века), как показано на фигуре 3 . [ 37 ] Карман Q вмещает пиразолопиримидиноновую группу силденафила. Это предполагает, что другие химические вещества, подобные гуанидиновым группам цГМФ, также могут связываться в этой области. Аминокислотные остатки Gln817, Phe820, Val782 и Tyr612 расположены в Q-кармане, они высококонсервативны во всех PDE. Амидный фрагмент пиразолопиримидиноновой группы образует бидентатную водородную связь с γ-амидной группой Gln817. [ 37 ] Трехмерная структура силденафила продемонстрирована на рисунке 4 .
Побочные эффекты
[ редактировать ]Ингибиторы ФДЭ5, как правило, хорошо переносятся, с побочными эффектами, включая преходящие головные боли, приливы, диспепсию, застойные явления и головокружение. [ 3 ] Также сообщалось о временных нарушениях зрения при приеме силденафила и, в меньшей степени, варденафиле, а также о болях в спине и мышцах при приеме тадалафила. [ 3 ] Эти побочные эффекты могут быть связаны с непреднамеренным действием ингибиторов ФДЭ5 на другие изоферменты ФДЭ, такие как ФДЭ1, ФДЭ6 и ФДЭ11. Предполагается, что улучшенная селективность ингибиторов ФДЭ5 может привести к меньшему количеству побочных эффектов. [ 3 ] Например, варденафил и тадалафил продемонстрировали снижение побочных эффектов, вероятно, из-за повышения селективности к ФДЭ5. [ 38 ] Однако в настоящее время не разрабатываются высокоселективные ингибиторы ФДЭ5. [ 3 ]
У пациентов, которые принимают нитраты , альфа-блокаторы или стимуляторы рГЦ в течение 24 часов после введения ингибитора ФДЭ5 (или 48 часов для тадалафила), может возникнуть симптоматическая гипотензия , поэтому одновременное применение противопоказано. [ 3 ] Ингибиторы ФДЭ5 также противопоказаны пациентам с наследственными заболеваниями глаз, такими как пигментный ретинит, из-за небольшого увеличения риска неартериальной ишемической оптической нейропатии у пациентов, принимающих лекарства. [ 3 ]
Нарушение слуха является одним из факторов риска для тех, кто использует ингибиторы ФДЭ5, и оно зарегистрировано для всех доступных на рынке лекарств. Эта проблема может быть связана с сильным воздействием цГМФ на волосковые клетки улитки. [ 33 ] Сообщалось, что ингибиторы ФДЭ5 (силденафил и варденафил) вызывают временные нарушения зрения, вероятно, из-за ингибирования ФДЭ6. [ 3 ]
В нескольких отчетах рассказывается о подходах к улучшению ингибиторов ФДЭ5, в которых химические группы были заменены для повышения эффективности и селективности, что потенциально должно привести к созданию лекарств с меньшим количеством побочных эффектов. [ 38 ] [ 39 ]
Отношения структура-деятельность (SAR)
[ редактировать ]Силденафил, первый ингибитор ФДЭ5, был открыт в рамках программы рационального проектирования лекарств. Соединение было эффективным и селективным по отношению к ФДЭ5, но не имело предпочтительных фармакологических свойств. [ 40 ]
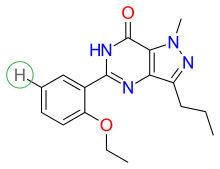
Взаимосвязь структура-активность (SAR) продемонстрирована на рисунке 5 , рисунке 6 и рисунке 7 . На рисунке 5 показаны три основные группы силденафила: R1, R2 и R3. R1 представляет собой пиразолопиримидиноновое кольцо, R2 представляет собой этоксифенильное кольцо и R3 представляет собой метилпиперазиновое кольцо. Группа R1 отвечает за связывание препарата с его активным сайтом связывания ФДЭ5. [ 27 ]

В этой подписи используются тривиальные формулировки . ( июль 2017 г. ) |
Растворимость является одним из фармакологических свойств, которое было увеличено. Атом водорода был заменен группой, как показано на фиг.6 . Сульфонамидная группа была выбрана для снижения липофильности и повышения растворимости , как показано на фигуре 7 . [ 1 ] [ 39 ]
В этой подписи используются тривиальные формулировки . ( июль 2017 г. ) |
Растворимость была дополнительно увеличена путем размещения метильной группы в положениях R, как показано на фигуре 7 . Другие ингибиторы фосфодиэстеразы-5 были разработаны на основе структуры, показанной на фигуре 7 . [ 1 ] [ 39 ]
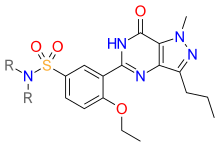
В этой подписи используются тривиальные формулировки . ( июль 2017 г. ) |
Другие исследования
[ редактировать ]Хотя ингибиторы ФДЭ5 в основном применяются при эректильной дисфункции, существует большой интерес к ингибиторам ФДЭ5 как к перспективным новым терапевтическим средствам для лечения других заболеваний, таких как болезнь Альцгеймера . Повышение уровня цГМФ за счет ингибирования ФДЭ5 позволяет улучшить память и обучение. [ 1 ] ФДЭ5 также рассматривается как потенциальное терапевтическое средство при паразитарных заболеваниях, таких как африканская сонная болезнь . В структуру силденафила были внесены стратегические изменения, чтобы молекула могла проникать в карман, специфичный для паразитов (p-карман). Аналогичный подход был использован при разработке терапевтических средств Plasmodium falciparum . [ 2 ]
Ингибиторы ФДЭ5 в клинических исследованиях
[ редактировать ]| Лекарство | Статус клинических испытаний (2005 г.) | Индикация | Продюсер |
|---|---|---|---|
| UK357903 | Фаза II | Эректильная дисфункция (ингибитор ФДЭ5 второго поколения) [ 9 ] | Пфайзер |
| Аванафил | Фаза II | Эректильная дисфункция и расстройство сексуального возбуждения у женщин [ 9 ] | Танабэ |
| Уденафил (DA-8159) | Фаза II | Эндотелиальная дисфункция, [ 9 ] эректильная дисфункция [ 9 ] и эректильная дисфункция, связанная с ожирением , [ 41 ] диабет [ 42 ] и использование СИОЗС [ 43 ] | Донг-А Фармацевтика |
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж Фиорито, Дж.; Чжан, Х.; Станишевский А.; Фэн, Ю.; Фрэнсис, Ю.И. (2013). «Синтез производных хинолина: открытие мощного и селективного ингибитора фосфодиэстеразы 5 для лечения болезни Альцгеймера» . Eur J Med Chem . 60 : 285–294. дои : 10.1016/j.ejmech.2012.12.009 . ПМЦ 3582828 . ПМИД 23313637 .
- ^ Jump up to: а б с д Ван, Г.; Лю, З.; Чен, Т.; Ван, З.; Ян, Х.; Чжэн, М.; Цзян, Х. (2012). «Разработка, синтез и фармакологическая оценка моноциклических пиримидинонов как новых ингибиторов ФДЭ5». J Med Chem . 55 (23): 10540–10550. дои : 10.1021/jm301159y . ПМИД 23137303 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х Цумас, Николаос; Фарра, Тарик Э.; Дхаун, Нирадж; Уэбб, Дэвид Дж. (12 ноября 2019 г.). «Установленные и новые терапевтические применения ингибиторов фосфодиэстеразы 5-го типа при сердечно-сосудистых заболеваниях» . Британский журнал фармакологии . 177 (24): 5467–5488. дои : 10.1111/bph.14920 . ISSN 1476-5381 . ПМК 7707100 . ПМИД 31721165 .
- ^ Jump up to: а б Бингэм, Дж.; Сударсанам С. и Шринивасан С. (2006). «Профилирование генов фосфодиэстеразы человека и изоформ сплайсинга». Коммуникации по биохимическим и биофизическим исследованиям 350, 25-32.
- ^ Jump up to: а б Цзян, WQ; и др. (2004). «Профилирование синтеза и SAR тетрациклических пирролохинолонов как ингибиторов фосфодиэстеразы 5». Биоорганическая и медицинская химия 12, 1505–1515.
- ^ Гарретт (2002). Принципы биохимии: с фокусом на человека . Форт-Уэрт: Издательство Harcourt College. ISBN 978-0-03-097369-7 .
- ^ Jump up to: а б с д и ж г Гофрани, штат Ха; Остерло, И.Х. и Гриммингер, Ф. (2006). «Силденафил: от стенокардии до эректильной дисфункции, легочной гипертензии и не только». Nature Reviews Drug Discovery 5, 689-702.
- ^ Jump up to: а б Сун, Би Джей; и др. (2003). «Структура каталитического домена фосфодиэстеразы 5 человека со связанными молекулами лекарства». Природа 425, 98-102.
- ^ Jump up to: а б с д и ж г час я дж к л Чон, Ю.Х.; и др. (2005). «Фосфодиэстераза: обзор белковых структур, потенциальное терапевтическое применение и недавний прогресс в разработке лекарств». Cmls-Клеточные и молекулярные науки о жизни 62, 1198-1220.
- ^ Jump up to: а б Лин, CS (2004). «Тканевая экспрессия, распределение и регуляция PDE5». Международный журнал исследований импотенции 16, S8-S10.
- ^ Jump up to: а б с д и Джексон, Г.; Гиллис, Х. и Остерло, И. (2005). «Прошлое, настоящее и будущее: 7-летнее обновление Виагры ((R)) (цитрат силденафила)». Международный журнал клинической практики 59, 680-691.
- ^ Блаунт, Массачусетс; и др. (2004). «Связывание тритированного силденафила, тадалафила или варденафила с каталитическим сайтом фосфодиэстеразы-5 демонстрирует эффективность, специфичность, гетерогенность и стимуляцию цГМФ». Молекулярная фармакология 66, 144–152.
- ^ Люнье, К. (2006). «Суперсемейство циклических нуклеотидных фосфодиэстераз (ФДЭ): новая мишень для разработки специфических терапевтических средств». Фармакология и терапия 109, 366-398.
- ^ Jump up to: а б с д и ж г Карта, ГЛ; и др. (2004). «Структурные основы активности препаратов, ингибирующих фосфодиэстеразу». Структура 12, 2233-2247.
- ^ Чен, Дж.; и др. (2003). «MMDB: база данных трехмерной структуры Entrez 10.1093/nar/gkg086». Нуклеиновые кислоты Рез. 31, 474–477.
- ^ Jump up to: а б МакМахон, CG; МакМахон, Китай; Леоу, LJ и Уайнсток, CG (2006). «Эффективность ингибиторов фосфодиэстеразы 5-го типа при медикаментозном лечении преждевременной эякуляции: систематический обзор». Бью Интернэшнл 98, 259-272.
- ^ Шинлапавиттаяторн, К.; Чаттипакорн С. и Чаттипакорн Н. (2005). «Влияние цитрата силденафила на сердечно-сосудистую систему». Бразильский журнал медицинских и биологических исследований 38, 1303–1311.
- ^ Чунг, К.Ф. (2006). «Ингибиторы фосфодиэстеразы при заболеваниях дыхательных путей». Европейский журнал фармакологии 533, 110-117.
- ^ Андерсон, Саймон Г.; Хатчингс, Дэвид К.; Вудворд, Марк; Рахими, Казем; Раттер, Мартин К.; Кирби, Майк; Хакетт, Джефф; Траффорд, Эндрю В.; Хилд, Адриан Х. (01 ноября 2016 г.). «Использование ингибиторов фосфодиэстеразы 5-го типа при диабете 2-го типа связано со снижением смертности от всех причин» . Сердце . 102 (21): 1750–1756. doi : 10.1136/heartjnl-2015-309223 . ISSN 1355-6037 . ПМК 5099221 . ПМИД 27465053 .
- ^ Фрэнсис, Ш.; Линкольн, ТМ; Корбин, JD (1980). «Характеристика нового белка, связывающего цГМФ, из легких крысы» . Журнал биологической химии . 255 (2): 620–626. дои : 10.1016/S0021-9258(19)86221-X . ПМИД 6153179 .
- ^ Jump up to: а б с д Ротелла, ДП (2002). «Ингибиторы фосфодиэстеразы 5: современное состояние и потенциальное применение». Обзоры природы. Открытие наркотиков . 1 (9): 674–682. дои : 10.1038/nrd893 . ПМИД 12209148 . S2CID 11807377 .
- ^ Jump up to: а б с Равипати, Г.; МакКлунг, Дж.А.; Аронов, штат Вашингтон; Петерсон, С.Дж.; Фришман, WH (2007). «Ингибиторы фосфодиэстеразы 5 типа в лечении эректильной дисфункции и сердечно-сосудистых заболеваний». Кардиол Рев . 15 (2): 76–86. дои : 10.1097/01.crd.0000233904.77128.49 . ПМИД 17303994 . S2CID 23461685 .
- ^ Jump up to: а б Реффельманн, Т.; Клонер, Р.А. (2003). «Терапевтический потенциал ингибирования фосфодиэстеразы 5 при сердечно-сосудистых заболеваниях» . Тираж . 108 (2): 239–244. дои : 10.1161/01.CIR.0000081166.87607.E2 . ПМИД 12860892 .
- ^ Киркпатрик, П; Ноймайер, К. (2004). «Тадалафил и Варденафил». Открытие натуральных референтных препаратов . 3 (4): 295–296. дои : 10.1038/nrd1362 . ПМИД 15124623 . S2CID 26423591 .
- ^ Кедия, GT; Укерт, С.; Ассади-Пур, Ф.; Кучик, Массачусетс (2013). «Аванафил для лечения эректильной дисфункции: исходные данные и ключевые клинические свойства» . Тер Адв Урол . 5 (1): 35–41. дои : 10.1177/1756287212466282 . ПМЦ 3547533 . ПМИД 23372609 .
- ^ Чен, CY; Чанг, Ю.Х.; Бау, Д.Т.; Хуанг, HJ; Цай, Ф.Дж.; Цай, CH; Чен, CY (2009). «Открытие мощных ингибиторов фосфодиэстеразы 5 путем виртуального скрининга и фармакофорного анализа» . Акта Фармакол Син . 30 (8): 1186–1194. дои : 10.1038/aps.2009.100 . ПМК 4006686 . ПМИД 19597523 .
- ^ Jump up to: а б Бир, Д.; Бхалай, Г.; Данстан, А.; Глен, А.; Хабертюэр, С.; Мозер, Х.; Цзян, Х. (2002). «Твердофазный подход к синтезу ингибиторов ФДЭ5». Bioorg Med Chem Lett . 12 (15): 1973–1976. дои : 10.1016/S0960-894X(02)00296-2 . ПМИД 12113821 .
- ^ Jump up to: а б Бернетт, Алабама (2006). «Роль оксида азота в эректильной дисфункции: значение для медикаментозной терапии» . Журнал клинической гипертонии . 8 (12): 53–62. дои : 10.1111/j.1524-6175.2006.06026.x . ПМК 8109295 . ПМИД 17170606 . S2CID 6215362 .
- ^ Jump up to: а б Корбин, JD (2004). «Механизмы действия ингибирования ФДЭ5 при эректильной дисфункции» . Int J Impot Res . 16 (1): 4–7. дои : 10.1038/sj.ijir.3901205 . ПМИД 15224127 .
- ^ Андерссон, К.Э. (2001). «Фармакология эрекции полового члена». Фармакологические обзоры . 53 (3): 417–50. ПМИД 11546836 .
- ^ Коул, Хари; Бивалаква, Тринити Дж.; Мусицки, Биляна; Сюй, Льюис Л.; Берковиц, Дэн Э.; Чемпион, Хантер К.; Бернетт, Артур Л. (2013). «Регуляция eNOS и PDE5, восстановленная цитратом силденафила, в пенисе серповидноклеточной мыши предотвращает приапизм посредством контроля окислительного / нитрозативного стресса» . ПЛОС ОДИН . 8 (7): e68028. Бибкод : 2013PLoSO...868028B . дои : 10.1371/journal.pone.0068028 . ISSN 1932-6203 . ПМЦ 3699477 . ПМИД 23844149 .
- ^ Шамлул, Р.; Ганем, Х. (2013). "Эректильная дисфункция". Ланцет . 381 (9861): 153–165. дои : 10.1016/S0140-6736(12)60520-0 . ПМИД 23040455 . S2CID 44720042 .
- ^ Jump up to: а б с д и ж Кокрилл, Бакалавр; Ваксман, AB (2013). «Ингибиторы фосфодиэстеразы-5». Фармакотерапия легочной гипертензии . Справочник по экспериментальной фармакологии. Том. 218. С. 229–255. дои : 10.1007/978-3-642-38664-0_10 . ISBN 978-3-642-38663-3 . ПМИД 24092343 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Турко, IV; Фрэнсис, Ш.; Корбин, JD (1998). «Связывание цГМФ с обоими аллостерическими сайтами цГМФ-связывающей цГМФ-специфической фосфодиэстеразы (ФДЭ5) необходимо для его фосфорилирования» . Биохимический журнал . 329 (3): 505–510. дои : 10.1042/bj3290505 . ПМК 1219070 . ПМИД 9445376 .
- ^ Окада, Д.; Асакава, С. (2002). «Аллостерическая активация цГМФ-специфической цГМФ-связывающей фосфодиэстеразы (ФДЭ5) с помощью цГМФ». Биохимия . 41 (30): 9672–9679. дои : 10.1021/bi025727+ . ПМИД 12135389 .
- ^ Томори, Т.; Хайду, И.; Лоринц, З.; Чех, С.; Дорман, Г. (2012). «Объединение 2D и 3D in silico методов для быстрого выбора потенциальных ингибиторов PDE5 из многомиллионных хранилищ соединений: биологическая оценка». Мол Дайверс . 16 (1): 59–72. дои : 10.1007/s11030-011-9335-0 . ПМИД 21947759 . S2CID 17820977 .
- ^ Jump up to: а б Сун, Би Джей; Хван, Кентукки; Чон, Ю.Х.; Ли, Джи; Привет, Ю.С.; Ким, Дж. Х. (2003). «Структура каталитического домена фосфодиэстеразы 5 человека со связанными молекулами лекарства». Природа . 425 (6953): 98–102. Бибкод : 2003Natur.425...98S . дои : 10.1038/nature01914 . ПМИД 12955149 . S2CID 4404590 .
- ^ Jump up to: а б Ю, ГХ; Мейсон, Х.; Ву, ХМ; Ван, Дж.; Чонг, Ш.; Бейер, Б. (2003). «Замещенные пиразолопиридопиридазины как перорально биодоступные мощные и селективные ингибиторы ФДЭ5: потенциальные средства для лечения эректильной дисфункции». J Med Chem . 46 (4): 457–460. дои : 10.1021/Jm0256068 . ПМИД 12570368 .
- ^ Jump up to: а б с Писсарницкий Д.А.; Асбером, Т.; Бойл, компакт-диск; Чакаламаннил, С.; Чинтала, М.; Кладер, Дж.В.; Сюй, Р. (2004). «Разработка SAR полициклических производных гуанина, направленная на открытие селективного ингибитора ФДЭ5 для лечения эректильной дисфункции». Bioorg Med Chem Lett . 14 (5): 1291–1294. дои : 10.1016/j.bmcl.2003.12.027 . ПМИД 14980684 .
- ^ Кэмпбелл, Сан-Франциско (2000). «Наука, искусство и открытие лекарств: личный взгляд». Клиническая наука . 99 (4): 255–260. дои : 10.1042/cs20000140 . ПМИД 10995589 .
- ^ Ю, JY; Канг, К.К. и Ю, М. (2006). «Эректильный потенциал нового ингибитора фосфодиэстеразы типа 5, DA-8159, у крыс с ожирением, вызванным диетой». Азиатский журнал андрологии 8, 325-329.
- ^ Ан, Дж.Дж.; и др. (2005). «Хроническое введение ингибитора фосфодиэстеразы 5 улучшает эректильную и эндотелиальную функцию на крысиной модели диабета». Международный журнал андрологии 28, 260-266.
- ^ Ан, Дж.Дж.; и др. (2005). «DA-8159 обращает вспять эректильную дисфункцию у крыс, вызванную селективным ингибитором обратного захвата серотонина». Урология 65, 202-207.