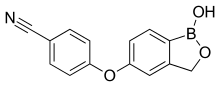
Хрисаборол
 | |
| Клинические данные | |
|---|---|
| Произношение | / j uː ˈ k r ɪ s ə / yoo- KRIS to |
| Торговые названия | Эукриса, Стакис |
| Другие имена | Ан-2728 |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а617019 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Местно ( мазь ) |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| КЭБ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.225.309 |
| Химические и физические данные | |
| Формула | С 14 Н 10 Б Н О 3 |
| Молярная масса | 251.05 g·mol −1 |
| 3D model ( JSmol ) | |
Крисаборол под торговой маркой Eucrisa , продаваемый, среди прочего, , представляет собой нестероидный препарат местного действия, (экземы) легкой и средней степени тяжести используемый для лечения атопического дерматита у взрослых и детей. [ 1 ] [ 2 ] [ 3 ] [ 4 ]
Наиболее распространенными побочными эффектами являются реакции в месте нанесения (включая жжение или покалывание). [ 3 ]
Крисаборол является ингибитором фосфодиэстеразы 4 (ФДЭ-4), хотя конкретный механизм его действия при атопическом дерматите неизвестен. [ 1 ] [ 2 ]
Побочные эффекты
[ редактировать ]В месте нанесения крисаборол может вызвать жжение или покалывание. Редко может возникнуть аллергическая реакция . [ 5 ]
Медицинское использование
[ редактировать ]В США крисаборол показан для местного лечения атопического дерматита легкой и средней степени тяжести у людей в возрасте трех месяцев и старше. [ 2 ]
В ЕС крисаборол разрешен для лечения атопического дерматита легкой и средней степени тяжести у людей в возрасте двух лет и старше с поражением ≤ 40% площади поверхности тела (ППТ). [ 3 ]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]Крисаборол — ингибитор фосфодиэстеразы-4 , в основном действующий на фосфодиэстеразу 4В (ФДЭ4В), вызывающую воспаление. [ 6 ] По химическому составу крисаборол представляет собой феноксибензоксаборол . [ 6 ] Ингибирование PDE4B, по-видимому, подавляет высвобождение фактора некроза опухоли альфа (TNFα), интерлейкина-12 (IL-12), IL-23 и других цитокинов , белков, которые, как полагают, участвуют в иммунном ответе и воспалении. [ 6 ]
Люди с атопическим дерматитом производят высокие уровни белков, называемых цитокинами, которые могут вызвать воспаление кожи, наблюдаемое при дерматите. [ 3 ] Крисаборол блокирует высвобождение некоторых цитокинов, участвующих в процессе воспаления, таких как фактор некроза опухоли альфа, интерлейкины (IL-2, IL-4, IL-5) и гамма-интерферон. [ 3 ] Ожидается, что, блокируя их высвобождение, крисаборол облегчит воспаление и, следовательно, облегчит симптомы заболевания. [ 3 ]
Химия
[ редактировать ]Крисаборол (химическое название: 4-[(1-гидрокси-1,3-дигидро-2,1-бензоксаборол-5-ил)окси]бензонитрил) представляет собой член класса бензоксаборолов, характеризующийся наличием бороновой кислоты полуэфира . с фенольным эфиром и нитрилом. [ 7 ] Крисаборол кристаллизуется в две полиморфные модификации , различающиеся конформацией оксаборольного кольца. сокристалл рентгеновской с 4,4'-бипиридином Получен и исследован методом кристаллографии . [ 8 ]
История
[ редактировать ]Крисаборол был разработан компанией Anacor Pharmaceuticals для местного лечения псориаза . [ 9 ] [ 6 ] [ 10 ] Во время доклинической и клинической разработки крисаборол назывался AN2728 и PF-06930164. [ 11 ] Когда Pfizer приобрела Anacor Pharmaceuticals, предполагалось, что препарат станет потенциальным блокбастером с оборотом в 2 миллиарда долларов в год. [ 12 ] Однако препарат не имел коммерческого успеха: объем продаж составил всего 147 миллионов долларов США в 2018 году и 138 миллионов долларов США в 2019 году. [ 13 ]
Крисаборол был одобрен для использования в США в декабре 2016 года. [ 14 ] [ 1 ] и для использования в Канаде в июне 2018 г. [ 15 ]
Безопасность и эффективность крисаборола были установлены в двух плацебо-контролируемых исследованиях с участием 1522 участников в возрасте от двух до 79 лет с атопическим дерматитом легкой и средней степени тяжести. [ 1 ] В обоих исследованиях участники получали лечение крисаборолом или плацебо два раза в день в течение 28 дней. [ 16 ] Ни участники, ни поставщики медицинских услуг не знали, какое лечение им проводилось, пока испытания не были завершены. [ 16 ] В целом, участники, получавшие крисаборол, достигли большего ответа с чистой или почти чистой кожей после 28 дней лечения. [ 1 ] [ 16 ] Испытания проводились в США. [ 16 ]
Крисаборол, одобренный для лечения атопического дерматита легкой и средней степени тяжести в Европейском Союзе, был быстро отозван с европейского рынка (март 2020 г. – февраль 2022 г.). [ 3 ]
См. также
[ редактировать ]- Таваборол - структурно родственное местное противогрибковое средство , разработанное Anacor.
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и «FDA одобряет Eucrisa для лечения экземы» (пресс-релиз). США Управление по контролю за продуктами и лекарствами (FDA). 14 декабря 2016 г.
 В данной статье использован текст из этого источника, находящегося в свободном доступе .
В данной статье использован текст из этого источника, находящегося в свободном доступе .
- ^ Jump up to: а б с «Эукриса-крисабороловая мазь» . ДейлиМед . 21 апреля 2020 г. Проверено 28 апреля 2020 г.
- ^ Jump up to: а б с д и ж г «Стакис ЭПАР» . Европейское агентство лекарственных средств (EMA) . 29 января 2020 г. Проверено 28 апреля 2020 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Хэ Ю, Лю Дж, Ван Ю, Куай В, Лю Р, Ву Дж (6 февраля 2023 г.). Пимпинелли Н (ред.). «Местное применение крисаборола при атопическом дерматите легкой и средней степени тяжести: систематический обзор и метаанализ» . Дерматологическая терапия . 2023 : 1–9. дои : 10.1155/2023/1869934 . ISSN 1529-8019 .
- ^ «ПРОДУКТ МОНОГРАФИЯ» (PDF) . Правительство Канады . 7 июня 2018 г. Архивировано (PDF) из оригинала 7 апреля 2019 г. . Проверено 7 апреля 2019 г.
- ^ Jump up to: а б с д Мустафа Ф., Фельдман С.Р. (май 2014 г.). «Обзор ингибирования фосфодиэстеразы и потенциальной роли ингибиторов фосфодиэстеразы 4 в клинической дерматологии» (PDF) . Дерматологический онлайн-журнал . 20 (5): 22608. doi : 10.5070/D3205022608 . ПМИД 24852768 .
- ^ «Информация ВОЗ о лекарствах, том 29, № 3, 2015 г. Международные непатентованные наименования фармацевтических веществ (МНН). Рекомендуемые международные непатентованные наименования: Список 74» (PDF) . Всемирная информация о здравоохранении. п. 391 . Проверено 26 апреля 2016 г.
- ^ Кампильо-Альварадо Дж., Дидден Т.Д., Оберн С.М., Свенсон Д.К., МакГилливрей Л.Р. (2018). «Исследование твердых форм крисаборола: инженерия кристаллов выявляет полиморфизм в коммерческих источниках и облегчает образование сокристаллов». Рост и дизайн кристаллов . 18 (8): 4416–4419. дои : 10.1021/acs.cgd.8b00375 . ISSN 1528-7483 .
- ^ Назарян Р., Вайнберг Дж. М. (ноябрь 2009 г.). «AN-2728, ингибитор PDE4 для потенциального местного лечения псориаза и атопического дерматита». Текущее мнение об исследуемых препаратах . 10 (11): 1236–42. ПМИД 19876791 .
- ^ Шпрейцер Х (16 августа 2016 г.). «Новые активные ингредиенты: крисаборол». Австрийская фармацевтическая газета (на немецком языке) (17/2016).
- ^ «Крисаборол» . АдисИнсайт . Проверено 24 июля 2017 г.
- ^ «Pfizer приобретает Анакор» . Pfizer (пресс-релиз). 16 мая 2016 года . Проверено 28 апреля 2020 г.
- ^ «Финансовый отчет Pfizer» (PDF) . Пфайзер . Проверено 9 апреля 2020 г.
- ^ «Эукриса (крисаборол) мазь» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 23 января 2017 года . Проверено 28 апреля 2020 г.
- ^ «Сводка нормативных решений Eucrisa» . Здоровье Канады . 23 октября 2014 г. Архивировано из оригинала 14 сентября 2019 г. . Проверено 14 сентября 2019 г.
- ^ Jump up to: а б с д «Снимок испытаний лекарств: Эвкриза» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 14 декабря 2016 года . Проверено 28 апреля 2020 г.
 В данной статье использован текст из этого источника, находящегося в свободном доступе .
В данной статье использован текст из этого источника, находящегося в свободном доступе .