Открытие и разработка триптанов
Триптаны — это слово, обычно используемое для обозначения класса против мигрени препаратов 5-гидрокситриптамина/серотонина 1B/1D (5-HT 1B/1D ) , которые представляют собой селективные агонисты . [ 1 ] Мигрень — сложное заболевание , которым страдают около 15% населения и которое может привести к тяжелой инвалидности. [ 2 ] Триптаны имеют преимущества перед эрготамином и дигидроэрготамином , такие как селективная фармакология , хорошо зарекомендовавшие себя показатели безопасности и научно обоснованные инструкции по назначению. Поэтому триптаны часто являются предпочтительным средством лечения мигрени. [ 1 ]
История
[ редактировать ]Поиск нового лекарства от мигрени начался в компании Glaxo в 1972 году. Исследования 1960-х годов показали, что вазоконстрикция под действием 5-НТ, эрготамина и норадреналина может уменьшить приступы мигрени. Исследования также показали, что уровень тромбоцитов 5-HT снижается во время мигрени. Поскольку у 5-НТ слишком много побочных эффектов для использования в качестве лекарства, ученые начали исследования рецепторов 5 -НТ, чтобы обнаружить и разработать более специфический агонист рецепторов 5-НТ. Исследования рецепторов 5-НТ и их действия привели к открытию нескольких типов и подтипов 5-НТ. AH24167 продемонстрировал эффект расширения сосудов вместо вазоконстрикции из-за агонистического действия на другой тип рецепторов 5-HT, позже получивший название 5-HT 7 . AH25086 был вторым разработанным соединением, которое продемонстрировало сосудосуживающий эффект, но не было выпущено в качестве лекарственного средства из-за низкой биодоступности при пероральном приеме . Продолжение исследований привело к открытию первого триптанового препарата, суматриптана , который обладал как вазоконстрикционным эффектом, так и лучшей биодоступностью при пероральном приеме. Суматриптан был впервые выпущен в продажу в Нидерландах в 1991 году и стал доступен в США в 1993 году. [ 3 ]
Механизм
[ редактировать ]Триптаны являются специфическими и селективными агонистами рецепторов - HT1 5 . Суматриптан [ 4 ] связывается с 5-НТ 1D- рецепторами, золмитриптаном , [ 5 ] ризатриптан , [ 6 ] наратриптан , [ 7 ] алмотриптан , [ 8 ] и фроватриптан [ 9 ] связывается с 5-HT 1B/1D и элетриптаном [ 10 ] связывается с 5-HT 1B/1D/1F- рецепторами. Считается, что триптаны оказывают свое действие через вазоконстрикцию, что приводит к снижению кровообращения в сонных артериях, не влияя на мозговой кровоток, торможение периферических нейронов или торможение передачи через нейроны второго порядка тригеминоцервикального комплекса. [ 1 ]
Рецепторы
[ редактировать ]Все рецепторы 5-HT представляют собой рецепторы, связанные с G-белком (GPCR), за исключением 5-HT 3 , который представляет собой лиганд-зависимый ионный канал . Было обнаружено, что рецепторы, участвующие в возникновении мигрени, представляют собой 5-HT 1B , 5-HT 1D и 5-HT 1F рецепторы . 5-НТ 1В обнаруживаются в менингеальных артериях, агонизм 5-НТ 1В вызывает вазоконстрикцию черепных нервов. Рецепторы 5-HT1D расположены преимущественно в тройничном нерве центральной нервной системы (ЦНС). Они также обнаруживаются в гладких мышцах сосудов , обеспечивая сокращение. Агонизм 5-НТ 1D -рецепторов подавляет высвобождение нервных стимуляторов, вызывающих воспаление. Аминокислотами , способствующими связыванию лигандов с рецептором, являются аспарагиновая кислота (Asp), фенилаланин (Phe), серин (Ser), треонин (Thr), триптофан (Trp) и тирозин (Tyr). Было показано, что рецепторы 5-HT 1B и 5-HT 1D у человека имеют очень схожие структуры аминокислот, что демонстрирует сходство свойств связывания. [ 11 ] [ 12 ] [ 13 ]
Дизайн
[ редактировать ]Все триптаны имеют индольную структуру, идентичную нейромедиатору 5-НТ. Классическая структура триптана содержит боковую цепь на индольном кольце и основной азот на таком же расстоянии от индольной структуры. Основным структурным отличием триптанов является положение сульфаниламида и присоединенной к нему боковой цепи (см. рисунок 1 и таблицу 1). Ризатриптан и золмитриптан вместо сульфаниламида содержат триазол и 2-оксазолидон соответственно. Другое исключение из классической структуры наблюдается у элетриптана, где азот-алкильная цепь, соединенная с индольным кольцом, заменена на диметилпирролидин, и у наратриптана, где азот-алкильная цепь заменена на 1-метилпиперидиновое кольцо.
Одна из боковых цепей фроватриптана образует дополнительное кольцо с индолом, в результате чего образуется карбазольная кольцевая система.
Структуры триптанов
[ редактировать ]-
Рис. 1. Индольная структура триптанов.
-
Рис 1а. Карбазольная структура фроватриптана
| Триптаны | Р 1 | Р 2 | Триптаны | Р 1 | Р 2 |
|---|---|---|---|---|---|
| Суматриптан | 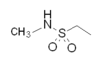
|

|
Элетриптан | 
|

|
| Ризатриптан | 
|

|
Наратриптан | 
|

|
| Алмотриптан | 
|

|
Фроватриптан | 
|

|
| Золмитриптан | 
|

|
– | – | – |
5-HT 1B/D Фармакофор
[ редактировать ]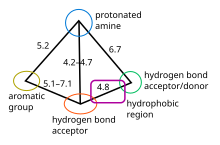

Рецепторы 5-HT 1B и 5-HT 1D считаются очень похожими, они имеют гомологию аминокислот , а их лиганды обладают схожими связывающими свойствами, поэтому они имеют схожий фармакофор . Фармакофорная модель этих лигандов рецепторов является качественной и определяет взаимное расположение важных групп. Его определяют по следующим пяти основным признакам: ароматическая группа (обычно индол), протонированный амин ( донор водородной связи ), акцептор водородной связи , дополнительный участок водородной связи (как донор, так и акцептор) и гидрофобная область, расположенная между обоими водородами. места связи , см. рисунок 2. [ 11 ] [ 14 ] Был сделан вывод, что основными точками связывания являются протонированный амин и сайт водородной связи. Было обнаружено, что область двойной связи в индоле необходима для агонизма в этом ряду соединений. На рисунке 3 показано, как различные препараты соответствуют фармакофору с C- и N-связанными аналогами 1D- агониста 5-HT. За близость отвечают отмеченные на рисунке участки. [ 14 ] [ 15 ] Фармакофор можно охарактеризовать как амфипатический , то есть в его структуре присутствуют как гидрофобные , так и гидрофильные группы. [ 16 ]
Соответствующие структурные особенности триптанов и связывание с рецептором
[ редактировать ]Структуры триптана были созданы на основе структуры 5-HT для достижения сродства к рецепторам 5-HT, следовательно, идентичной индольной структуры. Гидроксильная группа (-OH) в гексане индольного ядра и боковая цепь алкиламина в положении C 3 на 5-HT были заменены другими соединениями, такими как сульфонамиды или производные со структурой азольного кольца и различными амино-алкильными соединениями. боковые цепи. Электроотрицательная группа может образовывать водородную связь с Thr в кармане рецептора. Производные сульфаниламидов, присоединенные к гексановому кольцу индольной структуры, обладают электроотрицательными свойствами, так же как триазол и 2-оксазолидон на ризатриптане и золмитриптане соответственно. Это может повысить связывающую способность соединения и эффективность, особенно в отношении рецептора 5-HT 1D . [ 11 ]

Схематическое изображение связывания суматриптана с 5-НТ 1D- рецептором можно увидеть на рисунке 4. Одно исследование [ 11 ] показали, что суматриптан лучше вписывается в сайт связывания рецептора, когда боковая цепь с протонированным атомом азота свернута обратно по индольной структуре. Это выравнивание способствует образованию водородных связей между азотом в сульфонамине и Ser138 в сайте связывания. Это также благоприятствует образованию водородной связи между кислородом сульфонамина и Thr202 . Другое связывание в кармане сайта связывания происходит с атомом азота пентенового кольца индольной структуры триптана и аминокислотой Ser352 . Это энергетически выгодное положение агониста делает возможным дополнительное связывание лиганда с другим сером в сайте связывания, а также дополнительное закрепление между Phe в кармане сайта связывания и индолом агониста. Связывание Phe и триптана обусловлено π-стекинг-взаимодействием индола и аминокислоты, а дополнительный эффект на это взаимодействие обусловлен дисперсионным эффектом аминокислоты. лейцин (Leu; не показан на фигуре 4). Аминокислоты Trp343 и Tyr346 имеют богатые электронами π-системы в своих ароматических структурах. Своим положением в месте связывания они создают своего рода ароматическую клетку вокруг протонированного атома азота боковой цепи в положении С 3 триптанов (этот атом азота протонирован в физиологических условиях) и тем самым стабилизирует ионную связь атома азота. образовался с карбоксилатом аспарагиновой кислоты. Боковые цепи окружающих аминокислот могут оказывать влияние на связывание атома азота, преимущественно три Phe могут влиять на метильные группы, связанные с атомом азота (не показано на рисунке 4). [ 11 ] [ 12 ] [ 13 ]
Элетриптан обладает более высоким сродством к рецептору, что, вероятно, является следствием объемных заместителей в структуре. [ нужна ссылка ] Амин протонируется при физиологическом уровне pH, вызывая лучшее усвоение. [ 16 ] [ 17 ] Скорость поглощения агониста различна в зависимости от того, является ли амин в R 2 первичным, вторичным или третичным, но последний, по-видимому, дает наилучшие результаты. Для заместителя R 1 богатые электронами сульфонамидные группы и амидные группы показали лучшие результаты в связывании и активности рецептора. [ 16 ] Было замечено, что существует взаимосвязь между абсорбцией и размером молекул, поэтому более крупные гидрофильные молекулы имеют тенденцию иметь плохую абсорбцию. Небольшой заместитель R 1 необходим для поддержания быстрой пероральной биодоступности триптанов. [ 15 ]
Помещая электроноакцепторную группу или большую группу в положение C 2 индольной структуры, агонист 5-HT превращается в антагонист. Считается, что это связано с тем, что индольное кольцо не может занимать ароматическую часть сайта связывания. [ 12 ]
Триптановые препараты
[ редактировать ]Свойства составов
[ редактировать ]Суматриптан был пионером в этом классе. Вскоре стали доступны триптаны второго поколения, такие как золмитриптан, наратриптан, ризатриптан, алмотриптан, элетриптан и фроватриптан. [ 18 ] Различные триптаны доступны в разных формах и с разной эффективностью (см. таблицу 2). Они выпускаются в виде подкожных инъекций , пероральных таблеток , перорально распадающихся таблеток , назального спрея и ректальных суппозиториев . Система доставки триптанов может играть важную роль в начале действия. Выбор препарата против мигрени для пациентов зависит от их симптомов. Первый селективный агонист 5-HT 1B/1D , суматриптан, сначала был синтезирован в виде подкожных инъекций, затем в виде таблеток для перорального применения, а совсем недавно в виде назального спрея. В некоторых странах он также доступен в виде суппозиториев. Подкожная инъекция – самый быстрый способ остановить быстро прогрессирующий приступ мигрени. Назальный спрей суматриптан обеспечивает более быстрое начало действия, чем таблетки, но вызывает аналогичную головную боль через 2 часа. Некоторые пациенты предпочитают назальный спрей, поскольку он действует быстрее, чем таблетки, и не имеет такого количества побочных эффектов , как подкожная инъекция. Назальный спрей подходит не всем пациентам, поскольку у некоторых пациентов наблюдается неприятный привкус и непостоянная реакция. Золмитриптан был разработан совместно с Стратегия создания более липофильного соединения с более быстрой абсорбцией и лучшей способностью преодолевать гематоэнцефалический барьер, чем суматриптан. В некоторых странах он доступен в виде таблеток, перорально распадающихся таблеток и назального спрея. Ризатриптан доступен в виде таблеток и таблеток, распадающихся при пероральном приеме, но наратриптан, алмотриптан, элетриптан и фроватриптан пока доступны только в таблетках. [ 19 ]
| Общий | Составы [ 19 ] | Дозы (мг) [ 19 ] | Максимум суточная доза (мг) [ 19 ] |
Начало действия (мин) [ 20 ] |
Продолжительность
действия [ 20 ] |
Сродство (pKI в нМ) | Метаболизм [ 21 ] | Экскреция [ 20 ] |
|---|---|---|---|---|---|---|---|---|
| Суматриптан |
Таблетки |
25, 50, 100 |
200 |
Короткий | 7.9–8.5 | МАО-А |
Моча (57%), | |
| Золмитриптан |
Таблетки |
2.5, 5 |
10 |
45 |
Короткий | 9.2 |
CYP1A2 |
Моча (65%), |
| Наратриптан | Таблетки | 1, 2.5 |
5 |
60–180 | Длинный | 8.3 |
Кипр а |
Моча |
| Ризатриптан |
Таблетки |
5, 10 |
30 |
30–120 |
Короткий | 7.7 | МАО-А | Моча |
| Алмотриптан | Таблетки | 6.25, 12.5 | 25 | 60–180 | Короткий | 7.8 |
МАО-А |
Моча (40%), |
| Элетриптан | Таблетки | 20, 40 | 80 | <60 [ 23 ] | – | 8.9 | CYP3A4 | – |
| Фроватриптан | Таблетки | 2.5 | 7.5 | 60–120 | Длинный | 8.4 | CYP1A2 | Моча (40%) |
а Конкретный фермент пока не сообщается.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило 15 апреля 2008 года новый препарат, который представляет собой комбинацию суматриптана 85 мг и напроксена 500 мг ( НПВП ). [ 24 ] Триптаны и НПВП действуют по разным механизмам, связанным с мигренью, и поэтому при совместном применении могут обеспечить более эффективное лечение. [ 25 ]
Фармакокинетика
[ редактировать ]Фармакокинетические свойства (см. таблицу 3) важны при разработке новых лекарств. [ 26 ]
Пациенты стремятся к быстрому началу действия для облегчения головной боли. Относительно короткий tmax , хорошая биодоступность и липофильность являются фармакокинетическими свойствами , которые связаны с быстрым началом действия. Было высказано предположение, что хорошая способность преодолевать гематоэнцефалический барьер и относительно длительный период полувыведения могут привести к снижению частоты рецидивов головной боли. Суматриптан и ризатриптан подвергаются метаболизму при первом прохождении через печень , что приводит к снижению биодоступности. [ 18 ]
| Общий | Биодоступность (%) [ 26 ] | Липофильность [ 19 ] | Белок связывание (%) [ 20 ] |
т 1/2 (ч) [ 26 ] | t макс (ч) [ 22 ] | Кл Р (мл мин-1) [ 27 ] |
Log D pH7,4 [ 28 ] | В Д [ 20 ] |
|---|---|---|---|---|---|---|---|---|
| Суматриптан | 14 | Низкий | 10–21 | 2–2.5 | 2–2.5 | 260 | -1.5 | 2,4–3,3 л/кг |
| Золмитриптан | 40 | Умеренный | 25 | 3 | 2 | 193 | -1.0 | 7,0 л/кг |
| Наратриптан | 63(М) / 74(Ф) | Высокий | 28–31 | 5–6 | 2–3 | 220 | -0.2 | 2,4 л/кг |
| Ризатриптан | 47 | Умеренный | 14 | 2–2.5 | 1.3 | 414 | -0.7 | 140(М)/110(Ф)Л |
| Алмотриптан | 69 | – | 35 | 3.6 | 1.4–3.8 | – | -2.1 | 180–200 л |
| Элетриптан | 50 | Высокий | 85 [ 10 ] | 4–5 | 1–2 | 597 | 0.5 | 138 л [ 10 ] |
| Фроватриптан | 24(М) / 30(Ф) | Низкий | 20–30 | 25 [ 18 ] [ 26 ] | 2–4 | 216(М) / 132(Ф) [ 9 ] | -1.0 [ 29 ] | 4,2(М)/3,0(Ф) л/кг |
t 1/2 = период полувыведения;
t max = время достижения пиковой концентрации лекарственного средства в плазме;
Cl R = почечный клиренс;
LogD pH7,4 = показатель липофильности при pH 7,4. Увеличение числа указывает на большую растворимость;
V D = Объем распределения
М = Мужчина; Ж = Женщина
Будущие исследования
[ редактировать ]Большинство триптанов были разработаны и внедрены в 1990-е годы. Дальнейшие исследования не показали больших перспектив в отношении разработки новых триптанов с лучшей продолжительностью действия, эффективностью и профилем безопасности. Поэтому маловероятно, что будут разработаны дальнейшие вариации, и новые лекарства от мигрени, скорее всего, будут иметь другой механизм действия. [ 29 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Феррари, доктор медицины; Годсби, П.Дж.; Роон, К.И.; Липтон, Р.Б. (2002), «Триптаны (серотонин, агонисты 5-HT1B/1D) при мигрени: подробные результаты и методы метаанализа 53 исследований» , Cephalalgia , 22 (8): 633–658, doi : 10.1046 /j.1468-2982.2002.00404.x , PMID 12383060 , S2CID 2368571 , заархивировано из оригинала 17 декабря 2012 г.
- ^ Гоудсби, Питер Дж. (2006), «Последние достижения в понимании механизма, молекул и методов лечения мигрени», Trends in Molecular Medicine , 13 (1): 39–44, doi : 10.1016/j.molmed.2006.11.005 , PMID 17141570
- ^ Хамфри, Патрик П.А. (2007), «Открытие нового класса препаратов для лечения острой мигрени» , Головная боль , 47 [Приложение 1]: 10–19, doi : 10.1111/j.1526-4610.2007.00672.x , PMID 17425704 [ мертвая ссылка ]
- ^ «Имигран Таблетки 50мг Имигран Таблетки 100мг» . Архивировано из оригинала 18 декабря 2007 г. Проверено 9 ноября 2008 г.
- ^ «Зомиг Таблетки 2,5 мг» . Архивировано из оригинала 10 августа 2005 г. Проверено 9 ноября 2008 г.
- ^ «Максальт 5 мг, таблетки 10 мг, Максальт Мелт 10 мг липофилизаты для перорального применения» . Архивировано из оригинала 2 мая 2008 г. Проверено 9 ноября 2008 г.
- ^ «Нарамиг Таблетки 2,5 мг» . Архивировано из оригинала 30 апреля 2007 г. Проверено 9 ноября 2008 г.
- ^ «Аксерт» . Проверено 9 ноября 2008 г.
- ^ Перейти обратно: а б «Мигард» . Проверено 9 ноября 2008 г. [ постоянная мертвая ссылка ]
- ^ Перейти обратно: а б с «Релпакс – 20 мг и 40 мг» . Архивировано из оригинала 20 июня 2004 г. Проверено 9 ноября 2008 г.
- ^ Перейти обратно: а б с д и Бремнер, Д.Х.; Ринган, Н.С.; Уишарт, Дж. (1997), «Моделирование сайта связывания агониста серотониновых человеческих рецепторов 5-HT 1A , 5-HT Dα и 5-HT Dβ », Европейский журнал медицинской химии , 32 (1): 59–69, doi : 10.1016/S0223-5234(97)84362-0
- ^ Перейти обратно: а б с Боярский, Анджей Дж. (2006), «Фармакофорные модели для лигандов метаботропных рецепторов 5-HT», « Актуальные темы медицинской химии » , 6 (18): 2005–2026, doi : 10.2174/156802606778522186 , PMID 17017971
- ^ Перейти обратно: а б Терзиоглу, Налан; на основе рецепторов Хёлтье, Ханс-Дитер (2005), «3D QSAR-анализ агонистов рецепторов серотонина 5-HT 1D », Коллекция Чехословацкой химической связи , 70 (9): 1482–1492, doi : 10.1135/cccc20051482
- ^ Перейти обратно: а б с Бэкингем, Джанет; Глен, Роберт С.; Хилл, Алан П.; Хайд, Ричард М.; Мартин, Грэм Р.; Робертсон, Алан Д.; Вуллард, Патрик М. (1995). «Компьютерный дизайн и синтез 5-замещенных триптаминов и их фармакология на рецепторе 5-HT1D: открытие соединений с потенциальными свойствами против мигрени». Журнал медицинской химии . 38 (18): 3566–3580. дои : 10.1021/jm00018a016 . ПМИД 7658443 .
- ^ Перейти обратно: а б Джанду, Канзас; Барретт, В.; Брокуэлл, М.; Кембридж, Д.; Фаррант, ДР; Фостер, К.; Селвуд, Д.Л. (2001). «Открытие 4-[3-(транс-3-диметиламиноциклобутил)-1H-индол-5-илметил]-(4S)-оксазолидин-2-она (4991W93), частичного агониста рецептора 5HT1B/1D и мощного ингибитора Электроиндуцированная экстравазация плазмы» . Журнал медицинской химии . 44 (5): 681–693. дои : 10.1021/jm000956k . ПМИД 11262079 .
- ^ Перейти обратно: а б с Ченг, Цзыцян; Лю, Хоуфу; Ю, На; Ван, Фэй; Ан, Банда; Сюй, Ян; Айртон, Эндрю (2012). «Гидрофильные триптаны против мигрени являются субстратами для OATP1A2, переносчика, экспрессируемого через гематоэнцефалический барьер человека». Ксенобиотика . 42 (9): 880–890. дои : 10.3109/00498254.2012.675455 . ПМИД 22509823 . S2CID 6478226 .
- ^ Стрит, Лесли Дж.; Бейкер, Раймонд; Кастро, Хосе Л.; Чемберс, Марк С.; Гуиблин, Александр Р.; Хоббс, Сара С.; Пиво, Маргарет С. (1993). «Синтез и серотонинергическая активность 5-(оксадиазолил) триптаминов: мощные агонисты 5-HT1D-рецепторов». Журнал медицинской химии . 36 (11): 1529–1538. дои : 10.1021/jm00063a003 . ПМИД 8496922 .
- ^ Перейти обратно: а б с Мэтью, Нинан Т.; Лодер, Элизабет В. (2005), «Оценка триптанов», Американский медицинский журнал , 118 (12): 28–35, doi : 10.1016/j.amjmed.2005.09.014 , PMID 16356805
- ^ Перейти обратно: а б с д и Бигал, Марсело Э.; Бордини, Карлос А.; Антониацци, Ана Л.; Speciali, Хосе Дж. (2003), » (PDF) , Archivos de Neuro-Psiquiatria , 61 (2A): 313–320, : 10.1590 /s0004-282x200300020003PMID doi 28062121 «Составы триптана, критическая оценка
- ^ Перейти обратно: а б с д и «Обзор класса лекарств: пероральные 5HT 1 агонисты рецепторов » (PDF) . Министерство по делам ветеранов США. Архивировано из оригинала (PDF) 14 января 2009 г. Проверено 3 ноября 2008 г.
- ^ Армстеронг, Скотт С.; Козза, Келли Л. (2002), «Триптаны», Psychosomatics , 43 (6): 502–504, doi : 10.1176/appi.psy.43.6.502 , PMID 12444236
- ^ Перейти обратно: а б с д и Рапопорт, Алан М.; Теппер, Стюарт Дж.; Шефтелл, Фред Д.; Кунг, Эдна; Бигал, Марсело Э. (2006), «Какой триптан для какого пациента?», Neurological Sciences , 27 : 123–129, doi : 10.1007/s10072-006-0586-y , PMID 16688615 , S2CID 22223822
- ^ Ферккиля, М.; Дальлёф, К.; Стовнер, LJ; Брюгген, JP тер; Расмуссен, С.; Мюрхед, Н.; Сайкс, К.; Sikes, C (2003), «Элетриптан для лечения мигрени у пациентов с плохой реакцией или толерантностью к пероральному суматриптану», Cephalalgia , 23 (6): 463–471, doi : 10.1046/j.1468-2982.2003.00554. х , PMID 12807526
- ^ «Пресс-релиз - Таблетки Трексимет (суматриптан и напроксен натрия), одобренные FDA для лечения острой мигрени» . ГлаксоСмитКляйн. Архивировано из оригинала 4 декабря 2008 г. Проверено 9 ноября 2008 г.
- ^ Смит, Тимоти Р.; Саншайн, Авраам; Старк, Стюарт Р.; Литтлфилд, Дайан Э.; Спруилл, Сьюзен Э.; Александр, В. Джеймс (2005), «Суматриптан и напроксен натрия для лечения острой мигрени» , Головная боль , 45 (8): 983–991, doi : 10.1111/j.1526-4610.2005.05178.x , PMID 16109111 , S2CID 43314572 , заархивировано из оригинала 18 декабря 2012 г.
- ^ Перейти обратно: а б с д Джи, Стэнфорд С.; Шиовиц, Томас; Кроуфорд, А.А.рон В.; Катлер, Нил Р. (2001), «Фармакокинетика и фармакодинамика триптановых средств против мигрени», Clinical Pharmacokinetics , 40 (3): 189–205, doi : 10.2165/00003088-200140030-00004 , PMID 11327198 , S2CID 319371 63
- ^ Саксена, Прамод Р.; Тфельт-Хансен, Пер (2001), «Успехи и неудачи триптанов», Журнал головной боли и боли , 2 (1): 3–11, doi : 10.1007/s101940170040 , PMC 3611827
- ^ Паскуаль, Хулио; Муньос, Педро (2005), «Корреляция между липофильностью и результатами применения триптана» , Головная боль , 45 (1): 3–6, doi : 10.1111/j.1526-4610.2005.05003.x , PMID 15663606 , S2CID 37808880 [ мертвая ссылка ]
- ^ Перейти обратно: а б Ламберт, Джеффри А. (2005), «Доклиническая нейрофармакология наратриптана», Обзоры препаратов для ЦНС , 11 (3): 289–316, doi : 10.1111/j.1527-3458.2005.tb00048.x , PMC 6741765 , PMID 16389295 [ мертвая ссылка ]

