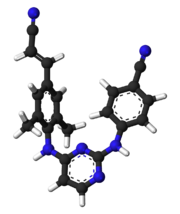
Рилпивирин
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Эдюрант, Рекамби |
| Другие имена | ТМС278 |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а611037 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Внутрь , внутримышечно |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Связывание с белками | 99.7% |
| Метаболизм | CYP3A4 |
| Период полувыведения | таблетки: 45 часов инъекция: 13–28 недель |
| Экскреция | 85% через фекалии, 6% через мочу |
| Идентификаторы | |
| Номер CAS |
|
| ПабХим CID | |
| Лекарственный Банк |
|
| ХимическийПаук | |
| НЕКОТОРЫЙ |
|
| КЕГГ | |
| КЭБ |
|
| ХЭМБЛ |
|
| НИАИД Химическая база данных | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.224.394 |
| Химические и физические данные | |
| Формула | С 22 Ч 18 Н 6 |
| Молярная масса | 366.428 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Рилпивирин , продаваемый под торговыми марками Edurant и Rekambys , представляет собой препарат , разработанный компанией Tibotec и используемый для лечения ВИЧ/СПИДа . [ 5 ] [ 6 ] Это ненуклеозидный ингибитор обратной транскриптазы (ННИОТ) второго поколения с более высокой эффективностью , более длительным периодом полувыведения и уменьшенным профилем побочных эффектов по сравнению с более старыми ННИОТ, такими как эфавиренз . [ 7 ] [ 8 ]
Медицинское использование
[ редактировать ]В США рилпивирин одобрен для пациентов, ранее не получавших лечения, с вирусной нагрузкой 100 000 копий/мл или менее в начале терапии. Его необходимо комбинировать с другими препаратами против ВИЧ. [ 9 ]
В Европейском Союзе рилпивирин одобрен в сочетании с каботегравиром для поддерживающего лечения взрослых, у которых уровень ВИЧ в крови не обнаруживается (вирусная нагрузка менее 50 копий/мл) на фоне текущего антиретровирусного лечения , а также когда вирус не развил устойчивость к определенный класс препаратов против ВИЧ, называемый ненуклеозидными ингибиторами обратной транскриптазы (ННИОТ) и ингибиторами переноса цепи интегразы (ИНИ). [ 4 ] [ 10 ]
Доступные формы
[ редактировать ]Препарат выпускается в виде таблеток (торговая марка Эдюрант пролонгированного действия, ) и в виде внутримышечных инъекций которые следует вводить один раз в месяц или два месяца ( Рекамбис ). Перед применением инъекции таблетки дают примерно на четыре недели для оценки переносимости. [ 9 ] [ 11 ]
Противопоказания и взаимодействие
[ редактировать ]Препарат противопоказан для применения с препаратами, индуцирующими фермент печени CYP3A4 , такими как карбамазепин , фенитоин , рифампицин и зверобой . Такие препараты могут ускорить расщепление рилпивирина, существенно снижая его концентрацию в плазме и потенциально приводя к потере эффективности и возможной резистентности . [ 9 ] Некоторые из этих препаратов также индуцируют фермент UGT1A1 и, таким образом, снижают концентрацию каботегравира в плазме крови, что еще больше снижает эффективность этой комбинированной терапии. [ 12 ]
Он также противопоказан в сочетании с ингибиторами протонной помпы , поскольку повышение рН желудка приводит к снижению всасывания рилпивирина из кишечника с такими же последствиями, как и при использовании индукторов CYP3A4. [ 9 ]
Побочные эффекты
[ редактировать ]Наиболее частыми побочными эффектами инъекционной формы являются реакции в месте инъекции (до 84% пациентов), такие как боль и отек, а также головная боль (до 12%) и лихорадка или ощущение жара (у 10%). . Реже (менее 10%) встречаются депрессивные расстройства , бессонница и сыпь . [ 9 ] [ 11 ] Наиболее частыми побочными эффектами таблеток также являются депрессивные расстройства (4,1%), головная боль (3,5%), бессонница (3,5%) и сыпь (2,3%). [ 13 ] Все эти побочные эффекты возникали при комбинированной терапии рилпивирином с одним или несколькими другими препаратами против ВИЧ.
Удлинение интервала QT сердечного ритма наблюдалось при применении очень высоких доз, но не имело клинического значения при применении стандартных доз препарата. [ 13 ]
Фармакология
[ редактировать ]Механизм действия
[ редактировать ]Рилпивирин является ненуклеозидным ингибитором обратной транскриптазы (ННИОТ). [ 13 ]
Фармакокинетика
[ редактировать ]При приеме внутрь рилпивирин достигает максимальной концентрации в плазме крови примерно через четыре-пять часов. Прием препарата без еды снижает его уровень в плазме на 40% по сравнению с приемом с пищей, что считается клинически значимым. Поэтому пациентам рекомендуется принимать препарат вместе с едой. [ 13 ] После инъекции в мышцу вещество достигает максимальной концентрации в плазме через три-четыре дня. [ 11 ]
Независимо от способа применения рилпивирин практически полностью связывается с белками плазмы (99,7%), преимущественно с альбумином . Метаболизируется главным образом ферментом печени CYP3A4 . Метаболиты включают несколько окисления продуктов , глюкурониды и глюкурониды окисленных метаболитов. Биологический период полувыведения составляет примерно 45 часов для таблеток и от 13 до 28 недель для инъекций. [ 11 ] [ 13 ]
Выведение изучалось только при пероральном применении: большая часть препарата выводится с калом (85%), частично в неизмененном виде (25%), частично в виде его метаболитов (60%). Незначительное количество выводится с мочой (6%), почти исключительно в виде метаболитов. [ 11 ] [ 13 ]

Комбинации с фиксированными дозами
[ редактировать ]Препарат с фиксированной дозой, сочетающий рилпивирин с эмтрицитабином и тенофовир дизопроксилом США (TDF), был одобрен Управлением по контролю за продуктами и лекарствами (FDA) в августе 2011 года под торговой маркой Complera . [ 15 ] и был одобрен для использования в Европейском Союзе под торговой маркой Eviplera в ноябре 2011 года. [ 16 ] Было показано, что эта комбинация имеет более высокие показатели вирусологической неудачи, чем эмтрицитабин/тенофовир/эфавиренц, у людей с исходной вирусной нагрузкой ВИЧ, превышающей 100 000 копий/мкл. 3 . [ 17 ] [ 18 ]
Препарат с фиксированной дозой, сочетающий рилпивирин с эмтрицитабином и тенофовира алафенамидом (TAF), был одобрен для использования в США в марте 2016 года под торговой маркой Odefsey . [ 19 ]
Долутегравир/рилпивирин , продаваемый под торговой маркой Juluca, представляет собой комбинированный антиретровирусный препарат с фиксированной дозой для лечения ВИЧ/СПИДа. Он был одобрен для использования в США в ноябре 2017 года и для использования в Европейском Союзе в мае 2018 года.
США В январе 2021 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило каботегравир/рилпивирин (торговая марка Кабенува) для лечения инфекций ВИЧ-1 у взрослых с целью замены действующего режима антиретровирусной терапии у тех, у кого вирусологическое подавление стабильным режимом антиретровирусной терапии с применением отсутствие истории неэффективности лечения и отсутствие известной или предполагаемой резистентности к каботегравиру или рилпивирину. [ 20 ] [ 21 ] Это первый полный инъекционный режим лечения, одобренный FDA, для ВИЧ-инфицированных взрослых, который вводится один раз в месяц. [ 20 ] [ 21 ] Этикетка таблеток рилпивирина была пересмотрена, чтобы отразить вводные рекомендации по пероральному применению с каботегравиром . [ 21 ]
Химия
[ редактировать ]Как и этравирин , ННИОТ второго поколения, одобренный в 2008 году, рилпивирин представляет собой диарилпиримидин (DAPY). [ 13 ]
Таблетки содержат рилпивирина гидрохлорид . [ 13 ] при этом инъекция содержит свободный рилпивирин. [ 11 ]
История
[ редактировать ]Рилпивирин вступил в III фазу клинических испытаний в апреле 2008 г. [ 22 ] [ 23 ] и был одобрен для использования в США в мае 2011 года под торговой маркой Edurant. [ 24 ] [ 25 ]
15 октября 2020 года Комитет по лекарственным препаратам для применения человеком (CHMP) Европейского агентства по лекарственным средствам (EMA) принял положительное заключение, рекомендовав выдать регистрационное удостоверение на рилпивирин под торговым названием «Рекамбис», предназначенный для лечения заболеваний человека. инфекция вируса иммунодефицита типа 1 (ВИЧ-1) в сочетании с инъекцией каботегравира . [ 26 ] Он был одобрен для медицинского использования в Европейском Союзе в декабре 2020 года. [ 4 ] Эти два препарата являются первыми антиретровирусными препаратами, выпускаемыми в форме инъекций длительного действия. [ 10 ]
Ссылки
[ редактировать ]- ^ «Эдурант 25 мг таблетки – Краткое описание характеристик препарата (ОХЛП)» . (эмс) . 21 января 2020 г. Проверено 4 января 2021 г.
- ^ «Эдурант- рилпивирина гидрохлорид таблетки, покрытые пленочной оболочкой» . ДейлиМед . Проверено 4 января 2021 г.
- ^ «Эдурант ЭПАР» . Европейское агентство лекарственных средств (EMA) . 12 декабря 2011 года . Проверено 4 января 2021 г.
- ^ Перейти обратно: а б с «Рекамбыс ЭПАР» . Европейское агентство лекарственных средств (EMA) . 13 октября 2020 г. Проверено 4 января 2021 г.
- ^ «TMC278 — новый ННИОТ» . Тиботек. Архивировано из оригинала 20 декабря 2008 г. Проверено 7 марта 2010 г.
- ^ Стеллбринк HJ (октябрь 2007 г.). «Противовирусные препараты в лечении СПИДа: что в разработке?». Европейский журнал медицинских исследований . 12 (9): 483–495. ПМИД 17933730 .
- ^ Гебель Ф., Яковлев А., Позняк А.Л., Виноградова Е., Бугертс Г., Хотельманс Р. и др. (август 2006 г.). «Кратковременная противовирусная активность TMC278 — нового ННИОТ — у субъектов, ранее не получавших лечения ВИЧ-1» . СПИД . 20 (13): 1721–1726. doi : 10.1097/01.aids.0000242818.65215.bd . ПМИД 16931936 . S2CID 26078073 .
- ^ Позняк А., Моралес-Рамирес Дж., Мохап Л. и др. «48-недельный первичный анализ исследования TMC278-C204: TMC278 демонстрирует высокую и устойчивую эффективность у пациентов, ранее не принимавших АРТ. Устный реферат 144LB» . 14-я конференция по ретровирусам и оппортунистическим инфекциям. Архивировано из оригинала 19 октября 2007 года.
- ^ Перейти обратно: а б с д и по Рилпивирину Монография . Доступ осуществлен 23 февраля 2021 г.
- ^ Перейти обратно: а б «Рекомендовано одобрение первой инъекционной антиретровирусной терапии длительного действия при ВИЧ» . Европейское агентство лекарственных средств (EMA) (пресс-релиз). 16 октября 2020 г. Проверено 16 октября 2020 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Перейти обратно: а б с д и ж «Рекамбыс: EPAR – отчет об общественной оценке» (PDF) . Европейское агентство по лекарственным средствам . 22 февраля 2021 г.
- ^ «Словарь: EPAR – Информация о продукте» (PDF) . Европейское агентство по лекарственным средствам . 05.01.2021.
- ^ Перейти обратно: а б с д и ж г час «Edurant: EPAR – отчет об общественной оценке» (PDF) . Европейское агентство по лекарственным средствам . 04.01.2021.
- ^ Лейд Дж. М., Эйвери Л. Б., Бампус Н. Н. (октябрь 2013 г.). «Человеческая биотрансформация ненуклеозидного ингибитора обратной транскриптазы рилпивирина и сравнение межвидового метаболизма» . Антимикробные средства и химиотерапия . 57 (10): 5067–5079. дои : 10.1128/AAC.01401-13 . ПМЦ 3811466 . ПМИД 23917319 .
- ^ «Одобрение препарата Комплера: комбинация фиксированных доз эмтрицитабин/рилпивирин/тенофовир DF» . США Управление по контролю за продуктами и лекарствами (FDA). 10 августа 2011 г.
- ^ «Эвиплера» . Карта СПИДа . Март 2011 года . Проверено 1 сентября 2014 г.
- ^ Хаберфельд Х, изд. Австрийский кодекс (на немецком языке). Вена: Издательство австрийского фармацевта. Таблетки, покрытые пленочной оболочкой Эвиплера.
- ^ Молина Дж.М., Кан П., Гринштейн Б., Лаззарин А., Миллс А., Сааг М. и др. (июль 2011 г.). «Рилпивирин по сравнению с эфавиренцем с тенофовиром и эмтрицитабином у взрослых, ранее не получавших лечения, инфицированных ВИЧ-1 (ECHO): рандомизированное двойное слепое исследование с активным контролем фазы 3». Ланцет . 378 (9787): 238–246. дои : 10.1016/S0140-6736(11)60936-7 . ПМИД 21763936 . S2CID 7313885 .
- ^ «Одефсей (эмтрицитабин, рилпивирин и тенофовир алафенамид) Таблетки» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 29 ноября 2016 года . Проверено 23 января 2021 г.
- ^ Перейти обратно: а б «FDA одобрило первую схему инъекционного препарата пролонгированного действия для взрослых, живущих с ВИЧ» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 21 января 2021 г. Проверено 21 января 2021 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Перейти обратно: а б с «Кабенува и Вокабрия одобрены для лечения ВИЧ-инфекции» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 27 января 2021 г. Проверено 27 января 2021 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ «Клиническое исследование пациентов с ВИЧ-1, ранее не проходивших лечение, по сравнению TMC278 с эфавиренцем в комбинации с тенофовиром + эмтрицитабином» . ClinicalTrials.gov . Национальные институты здравоохранения . 25 октября 2012 года . Проверено 1 января 2014 г.
- ^ «Клиническое исследование пациентов с ВИЧ, ранее не проходивших лечение, по сравнению TMC278 с эфавиренцем в комбинации с 2 нуклеозидными/нуклеотидными ингибиторами обратной транскриптазы» . ClinicalTrials.gov . Национальные институты здравоохранения . 14 мая 2012 года . Проверено 1 января 2014 г.
- ^ «Пакет одобрения препарата: Эдюрант (рилпивирин) NDA #202022#» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 20 августа 2013 года . Проверено 23 января 2021 г.
- ^ «FDA одобряет новое лечение ВИЧ» (пресс-релиз). США Управление по контролю за продуктами и лекарствами (FDA). Архивировано из оригинала 18 января 2017 г. Проверено 20 мая 2011 г.
- ^ «Рекамбыс: Ожидается решение ЕС» . Европейское агентство лекарственных средств (EMA) . 16 октября 2020 г. Проверено 16 октября 2020 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
Внешние ссылки
[ редактировать ]- «Рилпивирин» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Рилпивирина гидрохлорид» . Информационный портал о наркотиках . Национальная медицинская библиотека США.