селициклиб
| |
| Имена | |
|---|---|
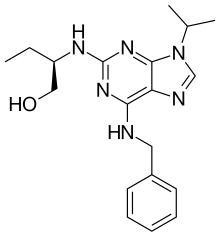
| Предпочтительное название ИЮПАК
(2 R )-2-{[6-(Бензиламино)-9-(пропан-2-ил)-9 H -пурин-2-ил]амино}бутан-1-ол | |
| Другие имена
Росковитин; CYC202
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХЭМБЛ | |
| ХимическийПаук | |
| МеШ | москвичи |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 19 Н 26 Н 6 О | |
| Молярная масса | 354.458 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Селициклиб ( росковитин или CYC202 ) является экспериментальным кандидатом на лекарственное средство из семейства фармакологических ингибиторов циклинзависимой киназы (CDK), которые преимущественно ингибируют несколько ферментов-мишеней, включая CDK2 , CDK7 и CDK9 , которые изменяют фазу роста или состояние в клеточном цикле обработанных клеток. клетки . Селициклиб разрабатывается компанией Cyclacel . Это многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование II фазы с диапазоном доз.
Целью данного исследования является оценка безопасности возрастающих доз росковитина, вводимых перорально в течение 4 циклов по 4 последовательных дня («лечение включено»), разделенных 3-дневным периодом без лечения («лечение прекращено») у взрослых пациентов с МВ с кистозной болезнью. Фиброз, несущий 2 муковисцидоза, вызывающий мутации по крайней мере с одной мутацией F508del-CFTR и хроническое инфицирование Pseudomonas aeruginosa.
В этом исследовании приняли участие 36 пациентов с муковисцидозом: 24 лечившихся и 12 контрольных. [ 1 ]
Селициклиб исследуется для лечения немелкоклеточного рака легких (НМРЛ), болезни Кушинга , лейкемии , ВИЧ-инфекции , болезни Паркинсона , инфекции простого герпеса , муковисцидоза. [ 2 ] и механизмы хронических воспалительных заболеваний.
Селициклиб – 2,6,9-замещенный аналог пурина . Его структура в комплексе с CDK2 была определена в 1996 г. [ 3 ] Селициклиб ингибирует CDK2/E, CDK2/A, CDK7 и CDK9. [ 4 ]
Клинические испытания и лабораторные испытания
[ редактировать ]Этот раздел необходимо обновить . ( январь 2014 г. ) |
Лечение рака
[ редактировать ]Было обнаружено, что селициклиб вызывает апоптоз в обработанных раковых клетках немелкоклеточного рака легких (НМРЛ) и других видов рака. Селициклиб ранее прошел клинические испытания фазы IIa на 240 пациентах с НМРЛ в комбинированной дозе с существующими препаратами первой и второй линии. [ 4 ] [ 5 ] В текущем исследовании APPRAISE исследуемый препарат проходит клинические испытания фазы IIb в качестве монотерапии НМРЛ у пациентов третьей линии. [ 6 ] Побочными эффектами, о которых сообщалось в I фазе исследований селициклиба при НМРЛ, были « тошнота , рвота, преходящее повышение сывороточного креатинина и показателей функции печени, а также преходящая гипокалиемия ». [ 5 ]
Иммунологические нарушения
[ редактировать ]Селициклиб также проходит клинические испытания при лечении В-клеточных лимфом, включая множественную миелому . Было показано, что селициклиб ингибирует РНК-полимеразы II зависимую от транскрипцию и подавляет регуляцию белка MCL1 . [ 7 ] [ 8 ]
было показано, In vitro что селициклиб индуцирует апоптоз нейтрофильных гранулоцитов . [ 9 ] Если этот механизм окажется безопасным, надежным и эффективным in vivo , препарат может улучшить лечение хронических воспалительных заболеваний, таких как муковисцидоз и артрит . Их обычно лечат глюкокортикоидами , которые часто имеют серьезные побочные эффекты.
Неврологическая терапия
[ редактировать ]Было показано, что в нервной системе селициклиб подавляет микроглии. активацию [ 10 ] и обеспечить некоторую нейропротекцию на животных моделях церебральной ишемии . [ 11 ] [ 12 ] Кроме того, он повышает противоопухолевую активность темозоломида при лечении мультиформной глиобластомы и рассматривается как возможный вариант лечения глиомы. [ 13 ]
Противовирусный эффект
[ редактировать ]Селициклиб также является возможным противовирусным средством . Вызывает гибель клеток, инфицированных ВИЧ. [ 14 ] [ 15 ] [ 16 ] и предотвращение репликации вируса простого герпеса . [ 17 ] [ 18 ]
Производство яйцеклеток
[ редактировать ]Было показано, что селициклиб вызывает партеногенетическую активацию яйцеклетки. Однако он создает аномальные вторые полярные тельца и, следовательно, возможные анеуплоидные зиготы. Активация яйцеклеток обычно включает колебания кальция, однако при применении селициклиба этого не происходит. Сециклиб вызывает активацию яйцеклеток путем ингибирования протеинкиназ, что приводит к инактивации фактора, способствующего созреванию (MPF). [ 19 ]
Гипертрофия почек
[ редактировать ]Селициклиб уменьшает гипертрофию почек на 45% после нефрэктомии 5/6. [ 20 ]
Побочные эффекты
[ редактировать ]Вызывает серьезные побочные эффекты, которые нельзя терпеть ежедневно. Побочные эффекты включают гипокалиемию и повышение активности печеночных ферментов. [ 21 ] Из-за этих побочных эффектов селициклиб не был одобрен USFDA.
Ссылки
[ редактировать ]- ^ «Фаза II, многоцентровое, двойное слепое, плацебо-контролируемое исследование по оценке безопасности и эффектов (R)-росковитина у взрослых пациентов с муковисцидозом, имеющих 2 мутации, вызывающие муковисцидоз, по крайней мере с одной мутацией F508del-CFTR и Хронически инфицированные Pseudomonas Aeruginosa: исследование с участием 36 пациентов с МВ (24 обработанных, 12 контрольных РОСКО-CF) . 11 декабря 2018 г.
- ^ Ноэль С., Фаво С., Норес С., Рожье С., Метти Ю., Бек Ф. (2006). «Открытие производных пирроло[2,3-b]пиразинов в качестве субмикромолярных активаторов сродства дикого типа, G551D и F508del, регулятора трансмембранной проводимости муковисцидоза, хлоридных каналов». J Pharmacol Exp Ther . 319 (1): 349–59. дои : 10.1124/jpet.106.104521 . ПМИД 16829626 . S2CID 1554921 .
- ^ Де Азеведо В.Ф., Леклерк С., Мейер Л., Гавличек Л., Стрнад М., Ким Ш.Х. (1997). «Ингибирование циклин-зависимых киназ аналогами пурина: кристаллическая структура человеческого cdk2 в комплексе с росковитином» . Eur J Biochem . 243 (1–2): 518–526. doi : 10.1111/j.1432-1033.1997.0518a.x . ПМИД 9030780 .
- ^ Jump up to: а б «Циклацел начинает рандомизированное исследование фазы IIb селициклиба для лечения ранее леченного немелкоклеточного рака легких» . БИОПРОВОД. 29 июня 2006 г.
- ^ Jump up to: а б «Цикласел сообщает о промежуточных данных фазы IIa селициклиба в ASCO 2005 г.» . Деловой провод. 15 мая 2005 г.
- ^ «Cyclacel Pharmaceuticals сообщает финансовые результаты за второй квартал 2006 года» . Деловой провод. 14 августа 2006 г.
- ^ МакКаллум Д.Э., Мелвилл Дж., Фрейм С., Уотт К., Андерсон С., Джанелла-Боррадори А., Лейн Д.П., Грин С.Р. (2005). «Селициклиб (CYC202, R-Росковитин) индуцирует гибель клеток в клетках множественной миеломы путем ингибирования зависимой от РНК-полимеразы II транскрипции и снижения регуляции Mcl-1». Исследования рака . 65 (12): 5399–5407. дои : 10.1158/0008-5472.CAN-05-0233 . ПМИД 15958589 .
- ^ Ноопур Радже, Шаджи Кумар, Теру Хидесима, Альдо Роккаро, Кенджи Ишицука, Хироши Ясуи, Норихико Сираиси, Дхарминдер Чаухан, Никхил С. Мунши, Саймон Р. Грин, Кеннет С. Андерсон (1 августа 2005 г.). «Селициклиб (CYC202 или R-росковитин), низкомолекулярный ингибитор циклин-зависимой киназы, опосредует активность посредством подавления Mcl-1 при множественной миеломе» . Кровь 106 (3): 1042–1047. дои : 10.1182/кровь-2005-01-0320 . ПМК 1895150 . ПМИД 15827128 .
- ^ Росси А.Г., Савацки Д.А., Уокер А., Уорд С., Шелдрейк Т.А., Райли Н.А., Калдикотт А., Мартинес-Лоса М., Уокер Т.Р., Даффин Р., Грей М., Крещенци Е., Мартин М.С., Брейди Х.Дж., Сэвилл Дж.С., Дрансфилд И., Хаслетт С. (2006). «Ингибиторы циклин-зависимой киназы усиливают разрешение воспаления, способствуя апоптозу воспалительных клеток». Природная медицина . 12 (9): 1056–1064. дои : 10.1038/nm1468 . ПМИД 16951685 . S2CID 5875865 .
- ^ Томов Н., Сурчев Л., Виденманн С., Дёбрёсси М., Никха Г. (август 2019 г.). «Росковитин, экспериментальный ингибитор CDK5, вызывает замедленное подавление микроглии, но не астроглиальное рекрутирование вокруг внутримозговых дофаминергических трансплантатов» . Экспериментальная неврология . 318 : 135–144. doi : 10.1016/j.expneurol.2019.04.013 . ПМИД 31028828 . S2CID 129946710 .
- ^ Менн Б., Бах С., Блевинс Т.Л., Кэмпбелл М., Мейер Л., Тимсит С. (12 августа 2010 г.). Манцони О.Дж. (ред.). «Отсроченное лечение системным (S)-росковитином обеспечивает нейропротекцию и ингибирует in vivo повышение активности CDK5 на моделях инсульта у животных» . ПЛОС ОДИН . 5 (8): е12117. Бибкод : 2010PLoSO...512117M . дои : 10.1371/journal.pone.0012117 . ISSN 1932-6203 . ПМК 2920814 . ПМИД 20711428 .
- ^ Руссле Э., Летондор А., Менн Б., Курбебес И., Кийе М.Л., Тимсит С. (июнь 2018 г.). «Продолжительная доставка (S)-росковитина способствует нейропротекции, связанной с функциональным восстановлением и уменьшением отека головного мозга в рандомизированном слепом исследовании очаговой церебральной ишемии» . Журнал церебрального кровотока и метаболизма . 38 (6): 1070–1084. дои : 10.1177/0271678X17712163 . ISSN 0271-678X . ПМЦ 5998998 . ПМИД 28569655 .
- ^ Пандей В., Ранджан Н., Нарн П., Бабу П.П. (21 марта 2019 г.). «Росковитин эффективно усиливает противоопухолевую активность темозоломида in vitro и in vivo, опосредованную усилением аутофагии и зависимым от каспазы-3 апоптоза» . Научные отчеты . 9 (1): 5012. Бибкод : 2019НатСР...9.5012П . дои : 10.1038/s41598-019-41380-1 . ISSN 2045-2322 . ПМК 6428853 . ПМИД 30899038 .
- ^ Садай М.Р., Мейнер Р., Донигер Дж. (январь 2004 г.). «Новый подход к разработке препаратов против ВИЧ: адаптация ненуклеозидных противораковых химиотерапевтических средств». Противовирусные исследования . 61 (1): 1–18. doi : 10.1016/j.antiviral.2003.09.004 . ПМИД 14670589 .
- ^ Памфери А., де ла Фуэнте С., Берро Р., Нехай С., Кашанчи Ф., Чао Ш. (2006). «Потенциальное использование фармакологических ингибиторов циклин-зависимой киназы в качестве средств против ВИЧ». Карр Фарм Дес . 12 (16): 1949–61. дои : 10.2174/138161206777442083 . ПМИД 16787240 .
- ^ Агботта Э, де Ла Фуэнте С, Нехай С, Барнетт А, Джанелла-Боррадори А, Памфери А, Кашанчи Ф (28 января 2005 г.). «Противовирусная активность CYC202 в клетках, инфицированных ВИЧ-1» . Ж. Биол. Хим . 280 (4): 3029–42. дои : 10.1074/jbc.M406435200 . ПМИД 15531588 .
- ^ Шанг Л.М., Розенберг А., Шаффер П.А. (2000). «Росковитин, специфический ингибитор клеточных циклин-зависимых киназ, ингибирует синтез ДНК вируса простого герпеса в присутствии ранних белков вируса» . Дж. Вирол . 74 (5): 2107–20. doi : 10.1128/JVI.74.5.2107-2120.2000 . ПМК 111691 . ПМИД 10666240 .
- ^ Диван П., Лакасс Дж.Дж., Шанг Л.М. (2004). «Росковитин ингибирует активацию промоторов в геномах вируса простого герпеса типа 1 независимо от факторов, специфичных для промотора» . Дж. Вирол . 78 (17): 9352–9365. doi : 10.1128/JVI.78.17.9352-9365.2004 . ПМК 506918 . ПМИД 15308730 .
- ^ Дори М., Галас С. (1994). «Циклинзависимые протеинкиназы и контроль клеточного деления» . ФАСЕБ Дж . 8 (14): 1114–1121. дои : 10.1096/fasebj.8.14.7958616 . ПМИД 7958616 . S2CID 3069118 .
- ^ Ю, Алан С.Л., Чертоу, Гленн М., Лайкс, Валери А., Марсден, Филип А., Скорецки, Карл, Таал, Маартен В., ред. (25 сентября 2019 г.). Почка Бреннера и ректора . Elsevier Науки о здоровье. ISBN 978-0-323-55085-7 . OCLC 1122857051 .
- ^ Ле Тюрно С., Фавр С., Лоуренс В., Дельбальдо С., Вера К., Жирре В., Чиао Дж., Армор С., Фрейм С., Грин С.Р., Джанелла-Боррари А., Диерас В., Раймонд Э. (декабрь 2010 г.). «Фаза I оценки селициклиба (R-росковитина), нового перорального ингибитора циклин-зависимой киназы, у пациентов с запущенными злокачественными новообразованиями» . Европейский журнал рака . 46 (18): 3243–3250. дои : 10.1016/j.ejca.2010.08.001 . ISSN 1879-0852 . ПМИД 20822897 .