Дициклоплатин
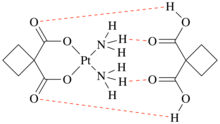 Химическая структура дициклоплатина | |
| Клинические данные | |
|---|---|
| Торговые названия | Дициклоплатин |
| Другие имена | Платины(2+) 1-карбоксициклобутанкарбоксилат аммониат (1:2:2), 1,1-циклобутандикарбоновая кислота, соединения. с (sp-4-2)-диаммин(1,1-циклобутанди(карбоксилато-каппаО)(2-))платиной (1:1) |
| Маршруты администрация | внутривенный |
| Фармакокинетические данные | |
| Биодоступность | 100% (IV) |
| Связывание с белками | < 88,7% |
| Период полувыведения | 24.49 - 108.93 часов |
| Экскреция | Реналь |
| Идентификаторы | |
| Номер CAS | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| Химические и физические данные | |
| Формула | С 12 Н 20 Н 2 О 8 Пт |
| Молярная масса | 515.382 g·mol −1 |
| 3D model ( JSmol ) |
|
Дициклоплатин — это химиотерапевтический препарат, используемый для лечения ряда видов рака, включая немелкоклеточную карциному легких и рак простаты . [ 1 ]
Некоторые побочные эффекты, которые наблюдаются при лечении дициклоплатином, включают тошноту , рвоту , тромбоцитопению , нейтропению , анемию , утомляемость , потерю аппетита , повышение уровня ферментов печени и алопецию . Препарат представляет собой противоопухолевый препарат на основе платины и действует, вызывая митохондриальную дисфункцию, которая приводит к гибели клеток . [ 2 ]
Дициклоплатин был разработан в Китае и использовался в I фазе клинических испытаний на людях в 2006 году. Препарат был одобрен FDA Китая для химиотерапии в 2012 году. [ 3 ]
Медицинское использование
[ редактировать ]Дициклоплатин может ингибировать пролиферацию опухолевых клеток посредством индукции апоптоза . Он используется для лечения ряда типов рака, включая немелкоклеточный рак легких и рак простаты . [ 2 ]
Побочные эффекты
[ редактировать ]Подобно цисплатину и карбоплатину , дициклоплатин также имеет некоторые побочные эффекты, а именно тошноту , рвоту , тромбоцитопению , нейтропению , анемию , утомляемость , потерю аппетита , повышение уровня ферментов печени и алопецию . Однако при дозах до 350 мг/м2 значительной токсичности не наблюдается; эти эффекты наблюдаются только при более высоких дозах. Кроме того, сообщается, что нефротоксичность дициклоплатина меньше, чем у цисплатина , а его миелосупрессивная эффективность аналогична таковой у карбоплатина . [ 4 ]
Химическая структура
[ редактировать ]Дициклоплатин состоит из карбоплатина и циклобутан-1,1-дикарбоновой кислоты (CBDC), связанных водородной связью . В структуре дициклоплатина существует два типа связи: OH...O — связь гидроксильной группы CBDC с карбоксильным атомом кислорода. Он создает одномерную полимерную цепь карбоплатина и CBDC. Второй - NH...O, который связывает аммиачную группу карбоплатина и кислород CBDC. Он образует двумерную полимерную цепь карбоплатина и CBDC. В водном растворе полимерная структура дициклоплатина с 2D-водородными связями разрушается. Во-первых, связь между аммиачной группой карбоплатины и кислородом CBDC разрывается, вызывая образование одномерного дициклоплатина. После этого прочная водородная связь разрывается и образуется промежуточное состояние дициклоплатина. Наконец, перегруппировка разной ориентации карбоплатины и CBDC приводит к образованию внутримолекулярной водородной связи и создается супрамолекула дициклоплатины с двумя OH...O и NH...O. [ 5 ]
Механизм действия
[ редактировать ]Подобно карбоплатину , дициклоплатин ингибирует пролиферацию раковых клеток, индуцируя апоптоз клеток . некоторые изменения свойств клеток Hep G2 При лечении дициклоплатином наблюдаются : снижение Мембранного потенциала митохондрий , высвобождение цитохрома с из митохондрий в цитозоль, активация каспазы-9 , каспазы-3 и снижение Bcl- 2 . [ 2 ] Эти явления указывают на роль митохондрий в апоптозе внутренним путем. [ 6 ] увеличение активации каспазы-8 Кроме того, также наблюдается . Это может стимулировать апоптоз за счет активации нижележащей каспазы-3. [ 7 ] или отщепляя Bid . [ 8 ] В результате расщепление Bid (tBid) передается в митохондрии и вызывает митохондриальную дисфункцию, которая способствует высвобождению цитохрома с из митохондрий в цитозоль. [ 9 ] , обработанных дициклоплатином В клетках Hep G2 избыточное количество активных форм кислорода , , было обнаружено [ 2 ] который играет важную роль в высвобождении цитохрома с . В митохондриях высвобождение гемопротеина происходит в два этапа: во-первых, происходит диссоциация цитохрома с от его связывания с кардиолипином . За счет активных форм кислорода кардиолипин окисляется, что снижает связывание цитохрома с и увеличивает концентрацию свободного цитохрома с. [ 10 ]
Примечания
[ редактировать ]- ^ Чжао Д., Чжан Ю., Сюй С., Донг С., Линь Х., Чжан Л. и др. (август 2012 г.). «Исследование фармакокинетики, распределения в тканях и связывания с белками плазмы платины, полученной из дициклоплатина, новой противоопухолевой супрамолекулы, на крысах и собаках с помощью ICP-MS». Исследование биологических микроэлементов . 148 (2): 203–8. дои : 10.1007/s12011-012-9364-2 . ПМИД 22367705 . S2CID 16035022 .
- ^ Jump up to: а б с д Ли GQ, Чен XG, Ву XP, Се JD, Лян YJ, Чжао XQ и др. (ноябрь 2012 г.). «Влияние дициклоплатина, нового платинового химиотерапевтического препарата, на ингибирование роста клеток и индукцию клеточного апоптоза» . ПЛОС ОДИН . 7 (11): e48994. Бибкод : 2012PLoSO...748994L . дои : 10.1371/journal.pone.0048994 . ПМЦ 3495782 . ПМИД 23152837 .
- ^ Ю Джей-Джей, Ян Икс, Сонг Кью, Мюллер, доктор медицинских наук, Ремик С.С. (январь 2014 г.). «Дициклоплатин, новый аналог платины в химиотерапии: синтез китайских доклинических и клинических профилей и новые исследования механизмов» . Противораковые исследования . 34 (1): 455–63. ПМИД 24403501 .
- ^ Ли С., Хуан Х., Ляо Х., Чжань Дж., Го Ю, Цзоу Б.И. и др. (февраль 2013 г.). «Фаза I клинического исследования нового платинового комплекса дициклоплатина: клинические и фармакокинетические результаты». Международный журнал клинической фармакологии и терапии . 51 (2): 96–105. дои : 10.5414/CP201761 . ПМИД 23127487 .
- ^ Ян X, Цзинь X, Сун Q, Тан К, Ян Z, Чжан X, Тан Y (июнь 2010 г.). «Структурные исследования дициклоплатина, противоопухолевой супрамолекулы». Наука Китай Химия . 53 (6): 1346–1351. дои : 10.1007/s11426-010-3184-z . S2CID 97893314 .
- ^ Кумар Р., Герберт П.Е., Уорренс А.Н. (сентябрь 2005 г.). «Введение в рецепторы смерти при апоптозе» . Международный журнал хирургии . 3 (4): 268–77. дои : 10.1016/j.ijsu.2005.05.002 . ПМИД 17462297 .
- ^ Ян Б.Ф., Сяо С., Ли Х., Ян С.Дж. (декабрь 2007 г.). «Устойчивость к Fas-опосредованному апоптозу в злокачественных опухолях восстанавливается с помощью KN-93 и цисплатина за счет снижения экспрессии и фосфорилирования c-FLIP». Клиническая и экспериментальная фармакология и физиология . 34 (12): 1245–51. дои : 10.1111/j.1440-1681.2007.04711.x . ПМИД 17973862 . S2CID 40501734 .
- ^ Бломгран Р., Чжэн Л., Стендаль О. (май 2007 г.). «Расщепляемый катепсином Bid способствует апоптозу нейтрофилов человека посредством индуцированной окислительным стрессом проницаемости лизосомальных мембран» . Журнал биологии лейкоцитов . 81 (5): 1213–23. дои : 10.1189/jlb.0506359 . ПМИД 17264306 . S2CID 13209075 .
- ^ Инь XM (март 2006 г.). «Бид, многофункциональная молекула, содержащая только BH3, находится на перекрестке жизни и смерти». Джин . 369 : 7–19. дои : 10.1016/j.gene.2005.10.038 . ПМИД 16446060 .
- ^ Отт М., Гогвадзе В., Оррениус С., Животовский Б. (май 2007 г.). «Митохондрии, окислительный стресс и гибель клеток» . Апоптоз . 12 (5): 913–22. дои : 10.1007/s10495-007-0756-2 . ПМИД 17453160 .