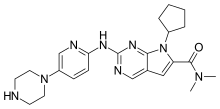
Рибоциклиб
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Кискали |
| Другие имена | ЛИ 011 |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а617008 |
| Данные лицензии |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | Неизвестный |
| Связывание с белками | ~70% |
| Метаболизм | Печень ( CYP3A4 ) |
| Период полувыведения | 32,0 (29,7–54,7) часа |
| Экскреция | 69% кала, 23% мочи |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.234.566 |
| Химические и физические данные | |
| Формула | С 23 Ч 30 Н 8 О |
| Молярная масса | 434.548 g·mol −1 |
| 3D model ( JSmol ) | |
Рибоциклиб , продаваемый под торговой маркой Кискали , представляет собой лекарство, используемое для лечения некоторых видов рака молочной железы . [6] Рибоциклиб является ингибитором киназы . [7] [8] Его разработали компании Novartis и Astex Pharmaceuticals . [9]
Наиболее распространенные побочные эффекты включают инфекции, низкий уровень лейкоцитов, головную боль, кашель, тошноту (тошнота), рвоту, диарею, запор, усталость, выпадение волос и сыпь. [5]
Рибоциклиб был одобрен Управлением по контролю за продуктами и лекарствами США (FDA) в марте 2017 года. [10] [11] Европейским агентством по лекарственным средствам (EMA) в августе 2017 г. [5] [12] и для использования в Национальной службе здравоохранения (NHS) Национальным институтом здравоохранения и передового опыта (NICE) в феврале 2021 года. [7] [13]
Медицинское использование
[ редактировать ]В США он показан для лечения взрослых с положительным по рецептору гормона (HR) и отрицательным по рецептору эпидермального фактора роста 2 человека (HER2) распространенным или метастатическим раком молочной железы в сочетании с ингибитором ароматазы в качестве начальной эндокринной терапии. ; или фулвестрант в качестве начальной эндокринной терапии или после прогрессирования заболевания на фоне эндокринной терапии у женщин в постменопаузе или у мужчин. [4] [10]
В Европейском Союзе он показан для лечения женщин с положительным по рецептору гормона (HR) и отрицательным по рецептору эпидермального фактора роста человека 2 (HER2) местно-распространенным или метастатическим раком молочной железы в сочетании с ингибитором ароматазы или фулвестрантом в качестве начальной эндокринной терапии. -основанной терапии или у женщин, ранее получавших эндокринную терапию. [5] У женщин в пре- или перименопаузе эндокринную терапию следует сочетать с агонистами рилизинг-гормона лютеинизирующего гормона (ЛГРГ). [5]
Побочные эффекты
[ редактировать ]Наиболее частыми побочными эффектами в исследованиях были снижение количества клеток крови , в основном нейтропения (у 75% пациентов по сравнению с 5% в группе плацебо), а также анемия (18% против 5%). Также часто встречались желудочно-кишечные расстройства, например, тошнота (52% против 29%) и диарея (35% против 22%), а также алопеция (33% против 16%). Препарат также увеличивает интервал QT и активность ферментов печени ( аланинтрансаминазы , аспартатаминотрансферазы ). [6] [12]
Наиболее распространенные побочные эффекты включают инфекции, низкий уровень лейкоцитов, головную боль, кашель, тошноту (плохое самочувствие), рвоту, диарею, запор, усталость, выпадение волос и сыпь. [5] К наиболее частым тяжелым побочным эффектам относятся инфекции, низкий уровень эритроцитов и лейкоцитов, рвота, отклонения в анализах крови на функцию печени и низкий уровень фосфатов в крови (гипофосфатемия). [5]
Взаимодействия
[ редактировать ]Поскольку рибоциклиб в основном метаболизируется ферментом печени CYP3A4 , ингибиторы этого фермента повышают его концентрацию в организме и могут усиливать побочные эффекты и токсичность. Примеры таких ингибиторов включают кетоконазол и аналогичные противогрибковые препараты, ритонавир , кларитромицин , а также грейпфрут . И наоборот, препараты, индуцирующие CYP3A4, такие как рифампицин и зверобой , могут снижать концентрацию рибоциклиба. [6] [12]
Рибоциклиб сам по себе является умеренным или сильным ингибитором CYP3A4 и, следовательно, может повышать концентрации других препаратов, которые разделяют этот метаболизм, как было показано в случае с мидазоламом . Он также ингибирует ряд белков-переносчиков и, таким образом, теоретически может препятствовать транспортировке других лекарств в организме. Он также может усиливать удлинение интервала QT других препаратов, таких как антиаритмические средства , кларитромицин и галоперидол . [6] [12]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]Циклин-зависимые киназы (CDK) 4 и 6 представляют собой ферменты, которые, как было показано, способствуют делению и размножению клеток как в нормальных, так и в раковых клетках. Во многих раковых клетках наблюдаются аномалии, которые повышают активность CDK, что приводит к инактивации определенных генов-супрессоров опухолей . [14] [15]
Было показано , что при использовании в сочетании с другими препаратами, такими как ингибитор АЛК или МЕК , рибоциклиб оказывает синергический эффект, что приводит к улучшению ответа. [16] [17] Опять же, это, вероятно, результат « перекрестных помех » между сигнальными путями. рака Простое блокирование одного пути онкогенеза иногда может привести к «компенсации опухоли», когда опухоль компенсирует заблокированный сигнальный путь, используя другие пути для выживания. Считается, что блокируя несколько путей одновременно, опухоль теряет способность к компенсации и часто наблюдается более сильный противоопухолевый ответ. Было показано, что использование рибоциклиба в сочетании с другими агентами снижает развитие резистентности к этим агентам. [14]
Фармакокинетика
[ редактировать ]Процент рибоциклиба, всасывающегося в кишечнике, не определен. Самые высокие уровни в плазме крови достигаются через один-четыре часа; и после повторного приема равновесная концентрация достигается примерно через восемь дней. Прием пищи не влияет на скорость всасывания. При попадании в кровоток около 70% рибоциклиба связывается с белками плазмы . [6] [12]
Вещество в основном метаболизируется CYP3A4, а затем различными ферментами фазы II , в результате чего образуется большое количество метаболитов. Те, у кого самые высокие концентрации в плазме крови у людей, называются CCI284 (неопределенный продукт N - гидроксилирования ), LEQ803 ( продукт N - деметилирования ) и M1 ( глюкуронид ). Все метаболиты обладают незначительной клинической активностью. [6] [12]
Рибоциклиб имеет небольшую тенденцию к накоплению в организме. Он выводится со средним биологическим периодом полувыведения 32 часа, в основном (69%) с калом, а также (23%) с мочой. В неизмененном виде препарат составляет 17% вещества в кале и 12% вещества в моче, остальное — метаболиты. [6] [12]
Химия
[ редактировать ]Рибоциклиб используется в форме его сукцинатной соли. Это слегка гигроскопичный кристаллический порошок желтого или коричневого цвета, растворимый в водных кислотах. [18]
История
[ редактировать ]Рибоциклиб является единственным ингибитором CDK4 / CDK6 с доказанной пользой в отношении общей выживаемости во всех трех исследованиях III фазы клинической программы MONALEESA с различными партнерами по эндокринной терапии, независимо от статуса менопаузы или линии терапии. [19] [ ненадежный медицинский источник? ] Европейское общество медицинской онкологии (ESMO) присвоило Кискали высший балл по «Шкале клинической пользы». [20] [ не удалось пройти проверку ]
В клиническом исследовании, имеющем значение для одобрения препарата, рибоциклиб значительно улучшил выживаемость без прогрессирования , то есть период времени, когда рак не ухудшался. Для участников, получавших плацебо в сочетании с летрозолом, выживаемость без прогрессирования составила в среднем 16 месяцев, тогда как в группе рибоциклиба в сочетании с летрозолом выживаемость без прогрессирования составила 25 месяцев по данным анализа в январе 2017 года. [12] Исследование продлится до сентября 2020 года. [21]
Ссылки
[ редактировать ]- ^ «Лекарства, отпускаемые по рецепту: регистрация новых химических веществ в Австралии, 2017» . Управление терапевтических товаров (TGA) . 21 июня 2022 г. Проверено 9 апреля 2023 г.
- ^ «Лекарственные средства, отпускаемые по рецепту, и биологические препараты: годовой обзор TGA за 2017 год» . Управление терапевтических товаров (TGA) . 21 июня 2022 г. Проверено 31 марта 2024 г.
- ^ «Краткое описание регулятивного решения для Кискали» . Здоровье Канады . 2 марта 2018 года . Проверено 8 июня 2024 г.
- ^ Jump up to: а б «Кискали-рибоциклиб таблетка, покрытая пленочной оболочкой» . ДейлиМед . 4 мая 2023 г. Проверено 9 июля 2023 г.
- ^ Jump up to: а б с д и ж г «Кискали ЭПАР» . Европейское агентство лекарственных средств (EMA) . 31 марта 2023 г. Проверено 9 июля 2023 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Jump up to: а б с д и ж г Профессиональная информация FDA о препаратах Кискали. По состоянию на 8 сентября 2017 г.
- ^ Jump up to: а б «Тысячи пациентов с раком молочной железы будут иметь постоянный доступ к одобренной NICE комбинации лекарств» . НИЦЦА (Пресс-релиз). Архивировано из оригинала 15 марта 2021 года . Проверено 8 марта 2021 г.
- ^ «Лечение кискали (рибоциклибом): HR+/HER2-mBC» . Новартис . Проверено 24 августа 2021 г.
- ^ «Novartis LEE011 (рибоциклиб) получил приоритетную оценку FDA для лечения первой линии HR+/HER2-распространенного рака молочной железы» (пресс-релиз). Новартис . 1 ноября 2016 г. Архивировано из оригинала 25 сентября 2018 г. Проверено 27 января 2017 г.
- ^ Jump up to: а б «Таблетки Кискали (рибоциклиб)» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 28 марта 2017 г. Проверено 9 июля 2023 г.
- ^ «FDA разрешило Novartis Kisqali использовать комбинированную терапию рака молочной железы» . Новости генной инженерии и биотехнологии . 14 марта 2017 года . Проверено 9 июля 2023 г.
- ^ Jump up to: а б с д и ж г час «Кискали: EPAR – Информация о продукте» (PDF) . Европейское агентство по лекарственным средствам . 31 августа 2017 г. Архивировано из оригинала (PDF) 18 июня 2018 г. . Проверено 8 сентября 2017 г.
- ^ «Продлевающий жизнь препарат от неизлечимого рака молочной железы одобрен для использования Национальной службой здравоохранения» . Хранитель . 26 февраля 2021 г. Проверено 8 марта 2021 г.
- ^ Jump up to: а б Самсон К (2014). «Ингибитор LEE011 CDK демонстрирует ранние перспективы в лечении лекарственно-устойчивого рака». Время онкологии . 36 (3): 39–40. дои : 10.1097/01.COT.0000444043.33304.c1 .
- ^ Ким С., Лу А., Чопра Р., Капонигро Г., Хуанг А., Вора С. и др. (2014). «Аннотация PR02: LEE011: биодоступный при пероральном приеме селективный низкомолекулярный ингибитор CDK4/6-реактивирующего Rb при раке». Молекулярная терапия рака . 12 (11_Дополнение): PR02. дои : 10.1158/1535-7163.TARG-13-PR02 .
- ^ Сосман Дж.А., Киттане М., Лолкема М.П., Постоу М.А., Шварц Г., Франклин С. и др. (2014). «Исследование фазы 1b/2 LEE011 в сочетании с биниметинибом (MEK162) у пациентов с NRAS -мутантной меланомой: ранняя обнадеживающая клиническая активность» . Журнал клинической онкологии . 32 (15 дополнений): 9009. doi : 10.1200/jco.2014.32.15_suppl.9009 . Архивировано из оригинала 7 октября 2015 года . Проверено 14 января 2017 г.
- ^ Вуд А.С., Крицка К., Райлс Х., Сано Р., Ли Н., Кинг Ф. и др. (2014). «Резюме 1000: Комбинация ингибирования CDK4/6 и ALK демонстрирует целевой синергизм против нейробластомы». Исследования рака . 74 (19 Дополнение): 1000. doi : 10.1158/1538-7445.AM2014-1000 .
- ^ «Кискали: EPAR – Отчет об общественной оценке» (PDF) . Европейское агентство по лекарственным средствам . 31 августа 2017 г. Архивировано из оригинала (PDF) 18 июня 2018 г. . Проверено 8 сентября 2017 г.
- ^ «Новартис представляет новые данные Кискали, показывающие самую длительную медиану общей выживаемости, когда-либо зарегистрированную при HR+/HER2-распространенном раке молочной железы» . Новартис (Пресс-релиз) . Проверено 19 октября 2021 г.
- ^ «ESMO-Шкала клинической пользы» . ЭСМО . Проверено 19 октября 2021 г.
- ^ Номер клинического исследования NCT01958021 «Исследование эффективности и безопасности LEE011 у женщин в постменопаузе с распространенным раком молочной железы (MONALEESA-2)» на сайте ClinicalTrials.gov .