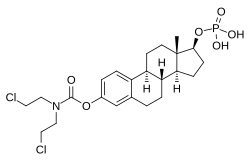
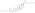Эстрамустин фосфат
Эстрамустин фосфат ( ЭМП ), также известный как эстрадиол нормустин фосфат и продаваемый под торговыми марками Emcyt и Estracyt , представляет собой двойной эстрогенный и химиотерапевтический препарат, который используется при лечении рака простаты у мужчин. [ 7 ] [ 4 ] [ 8 ] [ 9 ] [ 10 ] [ 3 ] [ 1 ] [ 11 ] [ 5 ] [ 12 ] Его принимают несколько раз в день внутрь или путем инъекции в вену . [ 7 ] [ 8 ] [ 3 ] [ 1 ] [ 5 ] [ 12 ]
Побочные эффекты ЭМИ включают тошноту , рвоту , гинекомастию , феминизацию , демаскулинизацию , сексуальную дисфункцию , образование тромбов и сердечно-сосудистые осложнения. [ 3 ] [ 9 ] [ 13 ] ЭМП является двойным цитостатическим и, следовательно, средством и гормональным противораковым средством эстрогенного химиотерапевтическим типа. [ 1 ] [ 3 ] [ 14 ] [ 5 ] Это пролекарство эстрамустина с точки зрения цитостатических эффектов и и эстромустина пролекарство эстрадиола с точки зрения его эстрогенных эффектов. [ 1 ] [ 3 ] ЭМП обладает сильным эстрогенным действием в типичных клинических дозах и, следовательно, оказывает выраженное антигонадотропное и функциональное антиандрогенное действие. [ 4 ] [ 1 ] [ 3 ] [ 14 ]
ЭМИ был использован в медицинских целях в начале 1970-х годов. [ 3 ] Он доступен в США , Канаде , Великобритании , других европейских странах и других странах мира. [ 15 ] [ 16 ]
Медицинское использование
[ редактировать ]ЭМИ показана в США для лечения метастатического паллиативного и/или прогрессирующего рака простаты. [ 6 ] тогда как в Соединенном Королевстве он показан для лечения неэффективного или рецидивирующего рака простаты. [ 17 ] [ 5 ] [ 1 ] [ 10 ] Препарат обычно предназначен для использования в гормонорезистентных случаях рака простаты, хотя он также используется в качестве монотерапии первой линии. [ 3 ] Говорят, что частота ответа на ЭМИ при раке простаты эквивалентна обычной терапии высокими дозами эстрогена . [ 18 ]
Из-за относительно серьезных побочных эффектов и токсичности ЭМИ редко используется при лечении рака простаты. [ 4 ] Это особенно актуально сегодня в западных странах . [ 4 ] В результате, а также из-за небольшого количества побочных эффектов модуляторов гонадотропин-рилизинг-гормона (модуляторов ГнРГ), таких как лейпрорелин , от ЭМИ практически отказались. [ 3 ] Однако обнадеживающие результаты клинических исследований привели к возобновлению интереса к ЭМИ для лечения рака простаты. [ 3 ]
ЭМИ использовался в дозах от 140 до 1400 мг/день перорально при лечении рака простаты. [ 19 ] Однако пероральный ЭМП чаще всего используется в дозе от 560 до 640 мг/день (280–320 мг два раза в день). [ 1 ] Рекомендуемая дозировка перорального ЭМП, указанная на этикетке Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для Эмцита, составляет 14 мг на кг массы тела (т. е. одна пероральная капсула по 140 мг на каждые 10 кг или 22 фунта массы тела), принимаемая в 3 или 4 приема. разделенные дозы в день. [ 7 ] На этикетке указано, что большинство пациентов в исследованиях перорального ЭМП в США получали от 10 до 16 мг на кг в день. [ 7 ] Это будет примерно от 900 до 1440 мг/день для мужчины весом 90 кг или 200 фунтов. [ 7 ] Было обнаружено, что более низкие дозы перорального ЭМП, такие как 280 мг/день, имеют сопоставимую эффективность с более высокими дозами, но с улучшенной переносимостью и сниженной токсичностью. [ 4 ] Дозы 140 мг/день описаны как очень низкие. [ 20 ] ЭМИ использовался в дозах от 240 до 450 мг/день внутривенно. [ 1 ]
ЭМП и другие эстрогены, такие как полиэстрадиолфосфат и этинилэстрадиол, гораздо дешевле, чем новые методы лечения, такие как модуляторы ГнРГ, абиратерона ацетат и энзалутамид . [ 4 ] [ 21 ] [ 22 ] Кроме того, эстрогены могут иметь значительные преимущества по сравнению с другими средствами андрогенной депривационной терапии , например, в отношении потери костной массы и переломов , приливов , когнитивных функций и метаболического статуса . [ 4 ] [ 22 ]
ЭМИ использовался для предотвращения повышения уровня тестостерона в начале терапии агонистами ГнРГ у мужчин с раком простаты. [ 23 ]
Доступные формы
[ редактировать ]ЭМП доступен или был доступен в форме капсул (140 мг, 280 мг) для перорального применения и водных растворов (300 мг) для внутривенных инъекций . [ 19 ] [ 24 ] [ 25 ] [ 7 ]
Противопоказания
[ редактировать ]ЭМИ противопоказан при использовании у детей, пациентов с гиперчувствительностью к эстрогенам или азотистым ипритам , людям с пептической язвой ( язвой в пищеварительном тракте ), людям с серьезно нарушенной функцией печени , людям со слабой сердечной мышцей (также известной как миокардиальная недостаточность ) и при тромбоэмболических нарушениях или осложнениях, связанных с задержкой жидкости . [ 17 ]
Побочные эффекты
[ редактировать ]Побочные эффекты ЭМИ в целом описываются как относительно серьезные. [ 3 ] Сообщается, что наиболее распространенными побочными эффектами ЭМИ являются желудочно-кишечные побочные эффекты, такие как тошнота , рвота и диарея , при этом тошнота и рвота возникают у 40% мужчин. [ 9 ] [ 1 ] Обычно они имеют легкую или умеренную степень тяжести, а тошноту и рвоту можно купировать профилактическими противорвотными препаратами. [ 9 ] Тем не менее, тяжелые случаи побочных эффектов со стороны желудочно-кишечного тракта при применении ЭМИ могут потребовать снижения дозы или прекращения терапии. [ 1 ] Хотя сообщалось, что тошнота и рвота являются наиболее распространенными побочными эффектами ЭМИ, гинекомастия (развитие мужской груди) встречается у 83% мужчин, получающих ЭМИ, а частота эректильной дисфункции , возможно, аналогична таковой у мужчин. или немного меньше, чем риск гинекомастии. [ 3 ] Как правило, феминизация , гиноидное распределение жира , демаскулинизация и импотенция наблюдаются практически или почти у 100% мужчин, получающих терапию высокими дозами эстрогенов . [ 13 ] [ 26 ] о снижении сексуальной активности у мужчин, получавших ЭМИ. Сообщалось также [ 1 ] Эти побочные эффекты обусловлены высоким уровнем эстрогена и низким уровнем тестостерона . [ 1 ] [ 3 ] Профилактическое облучение молочных желез может быть использовано для снижения частоты и тяжести гинекомастии эстрогенами. [ 13 ]
Серьезными побочными эффектами ЭМИ являются тромбоэмболические и сердечно-сосудистые осложнения, включая легочную эмболию , тромбоз глубоких вен , инсульт , тромбофлебит , ишемическую болезнь сердца (ишемическая болезнь сердца; например, инфаркт миокарда ), тромбофлебит и застойную сердечную недостаточность с задержкой жидкости . [ 9 ] [ 1 ] ЭМИ вызывает сердечно-сосудистую токсичность аналогично диэтилстильбестролу , но в меньшей степени по сравнению с низкими дозами (например, пероральный ЭМИ в дозе 280 мг/день против перорального диэтилстильбестрола в дозе 1 мг/день). [ 3 ] [ 27 ] Заболевание раком предстательной железы также увеличивает риск тромбоэмболии, а комбинация с доцетакселом также может усугубить риск тромбоэмболии. [ 9 ] Метаанализ клинических исследований показал, что общий риск тромбоэмболии при использовании ЭМП составляет от 4 до 7% по сравнению с 0,4% для схем химиотерапии без ЭМП. [ 9 ] [ 28 ] Тромбоэмболия является основной связанной с токсичностью . причиной прекращения применения ЭМП, [ 29 ] Антикоагулянтная терапия такими лекарствами, как аспирин , варфарин , нефракционированный и низкомолекулярный гепарин и антагонисты витамина К , может быть полезна для снижения риска тромбоэмболии с помощью ЭМП и других эстрогенов, таких как диэтилстильбэстрол и этинилэстрадиол . [ 9 ] [ 30 ] [ 4 ]
неблагоприятные результаты функциональных проб печени При применении ЭМП обычно наблюдаются тяжелая дисфункция печени возникает редко. , но при приеме препарата [ 1 ] Побочные эффекты со стороны центральной нервной системы редко наблюдаются при применении ЭМИ, хотя сообщалось об увеличении желудочков и нейронов пигментации у обезьян, получавших очень высокие дозы ЭМИ (20–140 мг/кг/день) в течение 3–6 месяцев. [ 1 ] ЭМИ, по-видимому, не оказывает цитостатического действия на нормальную ткань головного мозга . [ 1 ] несколько случаев незначительных гинекологических кровотечений . У женщин, получавших ЭМП в клинических исследованиях, наблюдалось [ 1 ] ЭМП описывается как относительно хорошо переносимый среди цитостатических противоопухолевых и азотисто-горчичных агентов, редко или вообще не связанный со значительной гематологической токсичностью, такой как миелосупрессия (подавление костного мозга), желудочно-кишечная токсичность или другая более выраженная токсичность, связанная с такими агентами. [ 5 ] [ 1 ] [ 31 ] В отличие от большинства других цитостатических агентов, которые часто вызывают миелосупрессию, лейкопению (снижение количества лейкоцитов ) и нейтропению (снижение количества нейтрофилов ), ЭМИ фактически вызывает лейкоцитоз (повышение количества лейкоцитов) в качестве побочного эффекта. [ 32 ] [ 33 ]
В небольшом исследовании с использованием низких доз ЭМП в дозе 280 мг/день перорально в течение 150 дней переносимость значительно улучшилась: раздражение желудочно-кишечного тракта возникло только у 15% мужчин, а случаев тяжелой сердечно-сосудистой токсичности или тромбоза глубоких вен не наблюдалось. [ 3 ] [ 4 ] Кроме того, не никаких других побочных эффектов, кроме незначительного преходящего повышения уровня ферментов печени . наблюдалось [ 3 ] Эти результаты позволяют предположить, что более низкие дозы перорального ЭМИ могут быть более безопасным вариантом лечения рака простаты, чем более высокие дозы. [ 4 ] Однако последующий метаанализ 23 исследований тромбоэмболических осложнений при применении ЭМИ в 2004 г. выявил значительную частоту тромбоэмболических событий независимо от дозировки и отсутствие связи дозы ЭМИ с риском этих осложнений. [ 28 ]
Передозировка
[ редактировать ]не было . Клинического опыта передозировки ЭМП [ 7 ] Передозировка ЭМИ может привести к выраженным проявлениям известных побочных эффектов препарата. [ 7 ] не существует . Специфического противоядия от передозировки ЭМИ [ 17 ] В случае передозировки промывание желудка при необходимости следует провести для эвакуации желудочного содержимого, а лечение должно быть симптоматическим и поддерживающим. [ 7 ] [ 17 ] В случае опасно низкого количества эритроцитов , лейкоцитов или тромбоцитов . цельную кровь при необходимости можно ввести [ 17 ] печени . При передозировке ЭМИ следует контролировать функцию [ 17 ] После передозировки ЭМП гематологических и печеночных показателей в течение как минимум 6 недель. следует продолжать контроль [ 7 ]
ЭМП использовался в высоких дозах: до 1260 мг/день при пероральном приеме и от 240 до 450 мг/день при внутривенном введении . [ 3 ] [ 1 ]
Взаимодействия
[ редактировать ]Сообщалось, что ЭМИ повышает эффективность и токсичность трициклических антидепрессантов, таких как амитриптилин и имипрамин . [ 17 ] Когда продукты, содержащие кальций , алюминий и/или магний , такие как молочные продукты , такие как молоко , различные пищевые добавки и антациды , употребляются одновременно с ЭМП, нерастворимый хелатный комплекс / фосфатная соль между ЭМП и этими металлами может образовываться , и это может заметно ухудшить абсорбцию и, следовательно, при пероральном приеме . биодоступность ЭМП [ 3 ] [ 1 ] [ 17 ] , может возникнуть повышенный риск развития ангионевротического отека У лиц, одновременно принимающих ингибиторы АПФ . [ 17 ]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]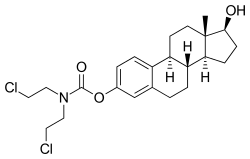
ЭМП, также известный как фосфат эстрадиола нормустин, представляет собой комбинированный эфир эстрогена и азотистого иприта эфира . [ 1 ] [ 3 ] [ 14 ] Он состоит из эстрадиола , эстрогена , связанного с эфиром фосфорной кислоты , а также эфира нормустина , азотистого иприта. [ 1 ] [ 3 ] [ 14 ] По своим фармакодинамическим эффектам ЭМП пролекарством эстрамустина и , эстромустина эстрадиола является . [ 1 ] [ 3 ] Как пролекарство эстрадиола, ЭМП является эстрогеном и, следовательно, агонистом рецепторов эстрогена . [ 1 ] [ 2 ] Сам по себе ЭМИ имеет очень слабое сродство к рецепторам эстрогена. [ 1 ] препарата примерно на 91% выше, Молекулярная масса чем у эстрадиола, из-за присутствия в нем нормустиновых эфиров C3 и фосфатных эфиров C17β. [ 35 ] [ 15 ] Поскольку ЭМП является пролекарством эстрадиола, его можно считать естественной и биоидентичной формой эстрогена. [ 14 ] хотя он обладает дополнительной цитостатической активностью за счет эстрамустин и эстромустин. [ 1 ] [ 3 ]
ЭМИ действует по двойному механизму действия : 1) прямая цитостатическая активность посредством ряда действий; и 2) как форма терапии высокими дозами эстрогенов действие , опосредованное рецепторами эстрогена , оказывающая антигонадотропное и функциональное антиандрогенное . [ 1 ] [ 3 ] [ 14 ] Антигонадотропное и функциональное антиандрогенное действие ЭМИ заключается в сильном подавлении гонадных андрогенов выработки и, следовательно, циркулирующих уровней андрогенов, таких как тестостерон ; значительно повышается уровень глобулина, связывающего половые гормоны, и, следовательно, снижается доля свободных андрогенов в кровообращении ; и прямое антиандрогенное действие на клетки простаты. [ 31 ] [ 1 ] [ 3 ] [ 4 ] [ 36 ] [ 37 ] [ 38 ] Было обнаружено, что индекс свободных андрогенов при пероральном ЭМИ в среднем в 4,6 раза ниже, чем при орхиэктомии . [ 37 ] Таким образом, ЭМИ-терапия приводит к значительно более сильной андрогенной депривации , чем орхиэктомия. [ 38 ] метаболиты ЭМП, включая эстрамустин, эстромустин, эстрадиол и эстрон Было обнаружено, что , действуют как слабые антагонисты андрогенных рецепторов ( EC 50 Tooltip = 0,5–3,1 мкМ), хотя клиническое значение этого неизвестно. . [ 39 ] [ 36 ] [ 3 ] [ 1 ]
Во время терапии ЭМИ наблюдаются чрезвычайно высокие уровни эстрадиола и эстрона. [ 3 ] [ 4 ] Эстрогенные метаболиты ЭМП ответственны за его наиболее распространенные побочные эффекты и сердечно-сосудистую токсичность . [ 1 ] В некоторых публикациях ЭМИ описывается как обладающий относительно слабым эстрогенным действием. [ 5 ] [ 31 ] Тем не менее, в клинических исследованиях он продемонстрировал по существу ту же частоту и степень эстрогенных эффектов, таких как болезненность молочных желез , гинекомастия , сердечно-сосудистая токсичность, изменения в синтезе белка в печени и подавление тестостерона, что и высокие дозы диэтилстильбестрола и этинилэстрадиола . [ 7 ] [ 4 ] [ 31 ] [ 38 ] [ 40 ] Представление о том, что ЭМИ обладает относительно слабой эстрогенной активностью, возможно, было основано на исследованиях на животных , которые показали, что ЭМИ оказывает в 100 раз меньшее утеротрофическое действие, чем эстрадиол, у крыс, и, возможно, также не принимались во внимание очень высокие дозы ЭМИ, используемые клинически в люди. [ 40 ] [ 41 ]
Механизм действия цитостатических эффектов ЭМИ сложен и изучен лишь частично. [ 1 ] Считается, что ЭМП главным образом является ингибитором митоза , ингибируя механизмы, участвующие в фазе митоза клеточного цикла . [ 1 ] [ 4 ] В частности, он связывается с белками, ассоциированными с микротрубочками , и/или с тубулином и вызывает деполимеризацию микротрубочек в (K d = 10–20 мкМ для эстрамустина), что приводит к остановке деления клеток в фазе G 2 /M (в частности, метафазе ). [ 1 ] [ 4 ] [ 42 ] Первоначально считалось, что ЭМП опосредует свои цитостатические эффекты как пролекарство нормустина , азотистого иприта , и, следовательно, считалось, что это алкилирующий противоопухолевый агент . [ 3 ] [ 10 ] [ 5 ] [ 14 ] Однако последующие исследования показали, что ЭМИ лишен алкилирующего действия и что влияние ЭМИ на микротрубочки опосредуется интактным эстрамустином и эстромустином, при этом нормустин или эстрадиол в отдельности оказывают лишь незначительные или незначительные эффекты. [ 1 ] [ 3 ] [ 43 ] Таким образом, уникальные свойства структур эстрамустин и эстромустин , содержащих карбамат - эфирную связь , по-видимому, ответственны за цитостатические эффекты ЭМИ. [ 1 ] Было обнаружено, что помимо антимитотического действия ЭМИ оказывает и другие цитостатические эффекты, включая индукцию апоптоза , вмешательство в синтез ДНК , взаимодействие ядерного матрикса , изменения клеточных мембран , индукцию активных форм кислорода (свободных кислородных радикалов) и, возможно, дополнительные механизмы. [ 1 ] [ 4 ] Было обнаружено, что ЭМИ оказывает радиосенсибилизирующее действие на клетки рака простаты и глиомы повышает чувствительность к лучевой терапии . , а также [ 1 ]
накапливаются в тканях Цитостатические метаболиты ЭМП избирательно клетках , например, в простаты рака . [ 5 ] [ 1 ] [ 4 ] Это может быть связано с наличием специфического эстрамустин-связывающего белка (EMBP) (K d = 10–35 нМ для эстрамустина), также известного как простатин или белок секреции простаты (PSP), который был обнаружен при раке предстательной железы, глиоме. , меланомы и рака молочной железы . клеток [ 1 ] [ 4 ] [ 44 ] Считается, что из-за своей тканевой селективности ЭМИ оказывает минимальное цитостатическое действие на здоровые ткани, а его тканевая селективность может быть ответственна за его терапевтическую цитостатическую эффективность против клеток рака простаты. [ 5 ] [ 4 ] [ 1 ]
Первоначально ЭМП был разработан как пролекарство с двойным эфиром эстрогена и нормустина в качестве противоопухолевого агента, алкилирующего азотистый иприт, который из-за сродства эстрогеновой части к рецепторам эстрогена будет избирательно накапливаться в тканях-мишенях эстрогена и, следовательно, в опухолях, позитивных по рецепторам эстрогена. клетки. [ 4 ] [ 14 ] [ 2 ] Следовательно, считалось, что ЭМИ будет преимущественно доставлять алкилирующую нормустиновую часть в эти ткани, позволяя снизить цитостатические эффекты в здоровых тканях и, следовательно, улучшить эффективность и переносимость . [ 4 ] эфира нормустина очень ограниченное и медленное Однако последующие исследования показали, что расщепление и что ЭМП лишен алкилирующей активности. [ 4 ] [ 1 ] [ 3 ] [ 31 ] Кроме того, оказывается, что эстрамустин и эстромустин могут преимущественно накапливаться в тканях-мишенях эстрогена не из-за сродства к рецепторам эстрогена, а вместо этого из-за сродства к отдельным EMBP. [ 1 ] [ 3 ]
Чрезвычайно высокие беременным, уровни эстрадиола, подобные могут быть ответственны за лейкоцитоз (повышение количества лейкоцитов ), который наблюдается у людей, получающих ЭМИ. [ 32 ] [ 33 ] Этот побочный эффект отличается от большинства других цитотоксических агентов, которые вместо этого вызывают миелосупрессию ( подавление костного мозга ), лейкопению (снижение количества лейкоцитов) и нейтропению (снижение количества нейтрофилов ). [ нужна ссылка ]
Антигонадотропные эффекты
[ редактировать ]Было обнаружено, что ЭМИ в дозе 280 мг/день подавляет уровень тестостерона у мужчин до кастратного уровня (до 30 нг/дл) в течение 20 дней и до низкого кастратного диапазона (до 10 нг/дл) в течение 30 дней. [ 3 ] Аналогичным образом, доза ЭМИ в 70 мг/день снижала уровень тестостерона до уровня кастрации в течение 4 недель. [ 3 ]
Фармакокинетика
[ редактировать ]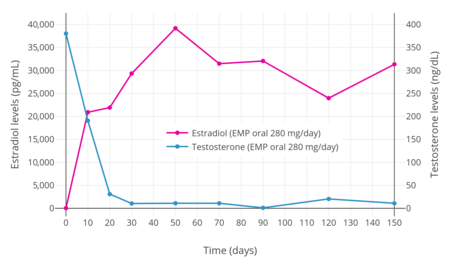
| Параметр | внутривенно 300 мг | Перорально 420 мг |
|---|---|---|
| С макс. | 506 ± 61 нг/мл | 362 ± 38 нг/мл |
| Т макс. | 2,6 ± 0,4 часа | 2,2 ± 0,2 часа |
| т 1/2 | 10,3 ± 0,95 часа | 13,6 ± 3,09 часа |
| АУК 0-32 | 4.82 ± 0.62 | 2.88 ± 0.34 |
| Биодоступность | 100.0% | 43.7% ± 4.6% |
| Источники: [ 31 ] | ||
| Метаболит | Плазма | Соотношение |
|---|---|---|
| Эстрамустин | 20 000–23 000 пг/мл | 1:9.6–9.8 |
| Эстромустин | 191 000–267 000 пг/мл | |
| Эстрадиол | 4900–9000 пг/мл | 1:9.4–11.8 |
| Эстрон | 71 000–85 000 пг/мл | |
| Источники: [ 31 ] | ||
При пероральном приеме быстро и полностью дефосфорилируется фосфатазами ЭМП в эстрамустин во время первого прохождения через желудочно-кишечный тракт. [ 1 ] [ 4 ] [ 5 ] [ 45 ] Эстрамустин также частично, но значительно окисляется в эстромустин под действием 17β-гидроксистероиддегидрогеназ во время первого прохождения. [ 5 ] [ 1 ] [ 12 ] [ 46 ] Таким образом, ЭМП попадает в кровоток в виде эстрамустин и эстромустин, а основным метаболитом ЭМП является эстромустин. [ 1 ] [ 12 ] количество (около 10–15%) эстрамустина и эстромустина далее медленно метаболизируется посредством гидролиза нормустина Ограниченное эфира в эстрадиол и эстрон соответственно. [ 1 ] [ 4 ] [ 31 ] эта реакция Считается, что катализируется карбамидазами кодирующие , хотя гены, ответственные ферменты, не охарактеризованы. [ 1 ] [ 47 ] [ 48 ] Уровни нормустина, образующегося из ЭМП, в крови незначительны. [ 43 ] [ 49 ] Высвобождение азотистого иприта из нормустина посредством расщепления карбоновой кислоты группы не было продемонстрировано и, по-видимому, не происходит. [ 42 ] [ 31 ]
Пероральная биодоступность ЭМП низкая, что обусловлено глубоким метаболизмом первого прохождения; в частности, дефосфорилирование ЭМИ. [ 1 ] Пероральная биодоступность ЭМП, особенно эстрамустина и эстромустина, составляет от 44 до 75%, что позволяет предположить, что абсорбция может быть неполной. [ 1 ] В любом случае существует линейная зависимость между пероральной дозой ЭМП и уровнями эстрамустина и эстромустина в крови. [ 1 ] Потребление кальция , алюминия или магния вместе с пероральным ЭМП может заметно ухудшить его биодоступность из-за снижения всасывания в кишечнике, и это может повлиять на его терапевтическую эффективность в низких дозах. [ 3 ] [ 17 ]
После однократного перорального приема 420 мг ЭМП у мужчин с раком простаты максимальные уровни эстромустина составляли от 310 до 475 нг/мл (475 000 пг/мл) и наблюдались через 2–3 часа. [ 1 ] Было обнаружено, что уровни эстрадиола при пероральном приеме ЭМИ в дозе 280 мг/день повышаются до очень высоких концентраций в течение одной недели терапии. [ 3 ] В одном исследовании уровни эстрадиола превысили 20 000 пг/мл через 10 дней, составили около 30 000 пг/мл через 30 дней и достигли пика около 40 000 пг/мл через 50 дней. [ 3 ] Другое исследование выявило более низкие уровни эстрадиола от 4900 до 9000 пг/мл во время хронической терапии пероральным ЭМП в дозе 560 мг/день. [ 31 ] Дополнительное исследование выявило уровни эстрадиола около 17 000 пг/мл при пероральном применении ЭМП в дозе 140 мг/день и 38 000 пг/мл при пероральном приеме ЭМП в дозе 280 мг/день. [ нужна ссылка ] Сообщалось, что циркулирующие уровни эстрадиола и эстрона во время терапии ЭМИ превышают нормальные уровни у мужчин более чем в 100 и 1000 раз соответственно. [ 4 ] [ 31 ] Уровни эстрамустина и эстрадиола в кровообращении заметно ниже, чем уровни эстромустина и эстрона соответственно, с соотношением примерно 1:10 в обоих случаях. [ 1 ] [ 31 ] Тем не менее, уровни эстрадиола во время терапии ЭМП, по-видимому, аналогичны тем, которые наблюдаются в середине и конце беременности и варьируются от 5000 до 40 000 пг/мл. [ 50 ] При пероральном приеме в кровообращении не наблюдается неизмененного ЭМП. [ 1 ]
Фармакокинетика ЭМП отличается при внутривенном введении . [ 1 ] После однократной внутривенной инъекции 300 мг ЭМП уровни ЭМП были выше, чем уровни его метаболитов в течение первых 8 часов. [ 1 ] Вероятно, это связано с обходом метаболизма первого прохождения. [ 1 ] Однако через 24 часа после введения дозы неизмененный ЭМИ уже не обнаруживался в кровообращении. [ 1 ] Клиренс . ЭМП из плазмы крови составляет 4,85±0,684 л/ч [ 1 ] Объемы распределения ЭМИ при внутривенном введении были небольшими; в модели с двумя отсеками объем распределения для центрального отсека составлял 0,043 л/кг, а для периферического отсека - 0,11 л/кг. [ 1 ] Связывание ЭМП с белками плазмы является высоким. [ 1 ] Эстрамустин накапливается в опухолевых тканях, например, раке предстательной железы и ткани глиомы , при этом уровни эстрамустина в этих тканях значительно выше, чем в плазме (например, в 6,3 и 15,9 раза соответственно). [ 1 ] И наоборот, уровни эстромустина в опухоли и плазме одинаковы (в 1,0 и 0,5 раза соответственно). [ 1 ] Эстрамустин и эстромустин накапливаются в жировой ткани . [ 1 ]
Период полувыведения эстромустина при пероральном приеме ЭМП составлял в среднем 13,6 часов с диапазоном от 8,8 до 22,7 часов. [ 1 ] И наоборот, период полувыведения эстромустина при внутривенном введении составил 10,3 часа в диапазоне от 7,36 до 12,3 часов. [ 1 ] Для сравнения, соответствующие периоды полувыведения эстрона составляли 16,5 и 14,7 часов при пероральном и внутривенном введении соответственно. [ 1 ] Эстрамустин и эстромустин в основном выводятся с желчью и, следовательно, с калом . [ 1 ] [ 31 ] Считается, что они не выводятся с мочой . [ 1 ]

Химия
[ редактировать ]ЭМП, также известный как эстрадиол-3-нормустин-17β-фосфат или эстрадиол-3-(бис(2-хлорэтил)карбамат)-17β-(дигидрофосфат), представляет синтетический эстрановый стероид и производное эстрадиола собой . [ 35 ] [ 15 ] Это сложный эфир эстрогена ; в частности, EMP представляет собой диэфир эстрадиола с нормустиновым эфиром C3 ( азотистый иприт - карбаматная группировка ) и фосфатным эфиром C17β. [ 35 ] [ 15 ] ЭМП поставляется в виде натриевой соли или меглюмина соли . [ 35 ] [ 15 ] [ 24 ] EMP по составу подобен другим эфирам эстрадиола, таким как сульфат эстрадиола и валерат эстрадиола , но отличается наличием фрагмента эфира азотистого иприта. [ 35 ] [ 15 ] Противоопухолевые средства , связанные с ЭМИ, хотя ни один из них не поступил в продажу, включают алестрамустин , атримустин , ацетат цитестрола , иприт с эстрадиолом , ICI-85966 и фенэстрол . [ 35 ] [ 15 ]
Благодаря гидрофильному фосфатноэфирному фрагменту ЭМП является легко растворимым в воде соединением. [ 51 ] [ 52 ] [ 53 ] В этом отличие от большинства других эфиров эстрадиола, которые представляют собой эфиры жирных кислот и липофильные соединения, которые не особенно растворимы в воде . [ 2 ] В отличие от ЭМП, эстрамустин высоко липофильен, практически нерастворим в воде и не ионизируется . [ 19 ] Фосфатный эфир ЭМП был включен в молекулу для увеличения его растворимости в воде и обеспечения возможности внутривенного введения . [ 7 ]
Молекулярная масса ЭМП натрия составляет 564,3 г/моль, ЭМП меглюмина – 715,6 г/моль, ЭМП – 520,4 г/моль, эстрамустина – 440,4 г/моль и эстрадиола – 272,4 г/моль. [ 54 ] В результате этих различий в молекулярной массе ЭМП содержит около 52%, ЭМП натрия - около 48%, а ЭМП меглумин - около 38% количества эстрадиола в их структурах, как и равное по массе количество эстрадиола. [ 54 ]
История
[ редактировать ]ЭМИ был впервые синтезирован в середине 1960-х годов и запатентован в 1967 году. [ 42 ] Первоначально он был разработан для лечения рака молочной железы . [ 1 ] Идея ЭМИ была вдохновлена поглощением и накоплением радиоактивно меченных эстрогенов в тканях рака молочной железы. [ 1 ] Однако первоначальные клинические результаты применения ЭМП у женщин с раком молочной железы оказались разочаровывающими. [ 1 ] Впоследствии было обнаружено, что меченый радиоактивным изотопом ЭМИ поглощается и накапливается в предстательной железе крыс , и это открытие привело к тому, что препарат был перепрофилирован для лечения рака простаты . [ 1 ] [ 3 ] ЭМИ был внедрен для медицинского использования при лечении этого заболевания в начале 1970-х годов и был одобрен в США для этого показания в 1981 году. [ 1 ] [ 3 ] [ 55 ] ЭМИ изначально был разработан для внутривенного введения. [ 31 ] Впоследствии была введена пероральная форма, а от внутривенного препарата практически отказались в пользу пероральной версии. [ 31 ]
Общество и культура
[ редактировать ]Общие имена
[ редактировать ]EMP поставляется в виде натриевой соли для перорального применения , которая имеет родовые названия эстрамустина фосфата натрия ( подсказка USAN ) и фосфат эстрамустина натрия ( утвержденное название BANM Tooltip , JAN ), а также меглюмина соль . для внутривенного введения , который имеет родовое название эстрамустин фосфат меглюмин . [ 24 ] [ 35 ] [ 15 ] [ 56 ] [ 16 ] INNM Tooltip — эстрамустин фосфат . [ 35 ] Название эстрамустинфосфат представляет собой сокращение от эстрадиола нормустинфосфата . [ 35 ] [ 16 ] ЭМИ также известен под своими бывшими кодовыми названиями Leo 299 , Ro 21-8837 и Ro 21-8837/001 . [ 35 ] [ 15 ] [ 16 ]
Названия брендов
[ редактировать ]ЭМП чаще всего продается под торговыми марками Estracyt и Emcyt, но также продается под рядом других торговых марок, включая Amsupros, Biasetyl, Cellmustin, Estramustin HEXAL, Estramustina Filaxis, Estranovag, Multosin, Multosin Injekt, Proesta, Prostamustin, и Сулопрост. [ 15 ] [ 16 ] [ 24 ]
Доступность
[ редактировать ]ЭМИ продается в США , [ 57 ] В Канаде и Мексике под торговой маркой Emcyt, тогда как препарат продается под торговой маркой Estracyt в Великобритании и других странах Европы , а также в Аргентине , Чили и Гонконге . [ 15 ] Его выпуск прекращен в ряде стран, включая Австралию , Бразилию , Ирландию и Норвегию . [ 58 ]
Исследовать
[ редактировать ]ЭМИ изучалось при лечении других видов рака, таких как глиома и рак молочной железы . [ 1 ] Было обнаружено, что он несколько улучшает качество жизни людей с глиомой в течение первых 3 месяцев терапии. [ 1 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и аль являюсь а к ап ак с как в В из хорошо топор является тот нет бб до нашей эры др. быть парень бг чб с минет БК с бм млрд быть б.п. БК бр бс БТ этот бв б бх к бз что CB копия компакт-диск Этот см. cg ч Бергенхайм А.Т., Хенрикссон Р. (февраль 1998 г.). «Фармакокинетика и фармакодинамика эстрамустина фосфата». Клиническая фармакокинетика . 34 (2): 163–172. дои : 10.2165/00003088-199834020-00004 . ПМИД 9515186 . S2CID 1943973 .
- ^ Перейти обратно: а б с д и Куль Х. (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения». Климактерический . 8 (Приложение 1): 3–63. дои : 10.1080/13697130500148875 . ПМИД 16112947 . S2CID 24616324 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и аль являюсь а к ап ак с Китамура Т. (февраль 2001 г.). «Необходимость переоценки эстрамустинфосфата натрия (ЭМП) как варианта лечения монотерапии первой линии при распространенном раке простаты». Международный журнал урологии . 8 (2): 33–36. дои : 10.1046/j.1442-2042.2001.00254.x . ПМИД 11240822 . S2CID 43384150 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С Иноуэ Т (2018). «Роль эстрамустинфосфата и других эстрогенов в лечении кастрационного рака простаты». Гормональная терапия и кастрационная резистентность рака простаты . Спрингер. стр. 249–256. дои : 10.1007/978-981-10-7013-6_26 . ISBN 978-981-10-7012-9 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м Перри CM, Мактавиш Д. (июль 1995 г.). «Эстрамустина фосфат натрия. Обзор его фармакодинамических и фармакокинетических свойств, а также терапевтической эффективности при раке простаты». Наркотики и старение . 7 (1): 49–74. дои : 10.2165/00002512-199507010-00006 . ПМИД 7579781 . S2CID 36725810 .
- ^ Перейти обратно: а б с «Дозировка Эмцита (эстрамустина), показания, взаимодействие, побочные эффекты и многое другое» . Справочник Медскейп . ВебМД . Проверено 8 февраля 2014 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л «Капсулы Emcyt эстрамустина фосфата натрия» (PDF) . FDA . Проверено 14 марта 2022 г.
- ^ Перейти обратно: а б Цинь З, Ли Х, Чжан Дж, Тан Дж, Хань П, Сюй З и др. (сентябрь 2016 г.). «Химиотерапия с эстрамустином или без него для лечения резистентного к кастрации рака простаты: систематический обзор и метаанализ» . Лекарство . 95 (39): е4801. дои : 10.1097/MD.0000000000004801 . ПМК 5265899 . ПМИД 27684806 .
- ^ Перейти обратно: а б с д и ж г час Рэвери В., Физази К., Удар С., Друэ Л., Эймар Дж.К., Кулин С. и др. (декабрь 2011 г.). «Использование эстрамустинфосфата в современном лечении распространенного рака простаты». БЖУ Интернешнл . 108 (11): 1782–1786. дои : 10.1111/j.1464-410X.2011.10201.x . ПМИД 21756277 . S2CID 33456591 .
- ^ Перейти обратно: а б с Симпсон Д., Вагстафф Эй.Дж. (2003). «Эстрамустин фосфат натрия». Американский журнал рака . 2 (5): 373–390. дои : 10.2165/00024669-200302050-00013 . S2CID 70507026 .
- ^ Худес Дж. (февраль 1997 г.). «Химиотерапия на основе эстрамустина». Семинары по урологической онкологии . 15 (1): 13–19. ПМИД 9050135 .
- ^ Перейти обратно: а б с д Крейс В. (1995). «Возвращение к Эстрамустину». Концепции, механизмы и новые мишени химиотерапии . Лечение и исследования рака. Том. 78. Спрингер. стр. 163–184. дои : 10.1007/978-1-4615-2007-8_8 . ISBN 978-1-4613-5829-9 . ПМИД 8595142 .
- ^ Перейти обратно: а б с Гэлбрейт С.М., Дюшен ГМ (апрель 1997 г.). «Андрогены и рак простаты: биология, патология и гормональная терапия». Европейский журнал рака . 33 (4): 545–554. дои : 10.1016/S0959-8049(96)00444-3 . ПМИД 9274433 .
- ^ Перейти обратно: а б с д и ж г час Эттель М., Шиллингер Э (6 декабря 2012 г.). Эстрогены и антиэстрогены II: фармакология и клиническое применение эстрогенов и антиэстрогенов . Springer Science & Business Media. стр. 540–. ISBN 978-3-642-60107-1 .
- ^ Перейти обратно: а б с д и ж г час я дж к Index Nominum 2000: Международный каталог лекарств . Тейлор и Фрэнсис. Январь 2000 г. стр. 1-1. 406–407. ISBN 978-3-88763-075-1 .
- ^ Перейти обратно: а б с д и «Использование эстрамустина, побочные эффекты и предупреждения» .
- ^ Перейти обратно: а б с д и ж г час я дж «Капсулы эстрацита – краткая характеристика продукта (SPC)» . Электронный справочник лекарственных средств . Пфайзер Лимитед. 12 августа 2013 года. Архивировано из оригинала 22 февраля 2014 года . Проверено 8 февраля 2014 г.
- ^ Лупулеску А (24 октября 1990 г.). Гормоны и витамины в лечении рака . ЦРК Пресс. стр. 40–. ISBN 978-0-8493-5973-6 .
- ^ Перейти обратно: а б с Стелла В., Борхардт Р., Хагеман М., Олияй Р., Мааг Х., Тилли Дж., ред. (12 марта 2007 г.). Пролекарства: проблемы и награды . Springer Science & Business Media. стр. 174–. ISBN 978-0-387-49782-2 .
- ^ Китамура Т., Сузуки М., Нисимацу Х., Куросаки Т., Эномото Ю., Фукухара Х. и др. (январь 2010 г.). «Окончательный отчет о монотерапии низкими дозами эстрамустинфосфата (ЭМП) и терапии ЭМП в очень низких дозах в сочетании с агонистом ЛГ-РГ при ранее не леченном распространенном раке простаты». Актуальная урология . 41 (Приложение 1): S34–S40. дои : 10.1055/s-0029-1224657 . ПМИД 20094950 . S2CID 7710924 .
- ^ Сайед Ю., Таксель П. (декабрь 2003 г.). «Применение эстрогеновой терапии у мужчин». Современное мнение в фармакологии . 3 (6): 650–654. дои : 10.1016/j.coph.2003.07.004 . ПМИД 14644018 .
- ^ Перейти обратно: а б Хедлунд П.О., Хенрикссон П. (март 2000 г.). «Парентеральная эстрогеновая абляция по сравнению с полной андрогенной абляцией при лечении распространенной карциномы простаты: влияние на общую выживаемость и сердечно-сосудистую смертность. Скандинавское исследование рака простаты (SPCG)-5». Урология . 55 (3): 328–333. дои : 10.1016/s0090-4295(99)00580-4 . ПМИД 10699602 .
- ^ Симидзу Т.С., Сибата Ю., Джинбо Х., Сато Дж., Яманака Х. (1995). «Эстрамустина фосфат для предотвращения обострений при депо-терапии аналогами рилизинг-гормона лютеинизирующего гормона». Европейская урология . 27 (3): 192–195. дои : 10.1159/000475159 . ПМИД 7541359 .
- ^ Перейти обратно: а б с д Мюллер Н.Ф., Дессинг Р.П., ред. (19 июня 1998 г.). Европейский индекс лекарств: европейские регистрации лекарств (Четвертое изд.). ЦРК Пресс. стр. 245, 454. ISBN. 978-3-7692-2114-5 .
- ^ Беккер К.Л. (2001). Принципы и практика эндокринологии и обмена веществ . Липпинкотт Уильямс и Уилкинс. стр. 2153–. ISBN 978-0-7817-1750-2 .
- ^ Таммела Т. (ноябрь 2004 г.). «Эндокринное лечение рака простаты». Журнал биохимии стероидов и молекулярной биологии . 92 (4): 287–295. дои : 10.1016/j.jsbmb.2004.10.005 . ПМИД 15663992 . S2CID 25425351 .
- ^ Кокс Р.Л., Кроуфорд Э.Д. (декабрь 1995 г.). «Эстрогены в лечении рака простаты». Журнал урологии . 154 (6): 1991–1998. дои : 10.1016/S0022-5347(01)66670-9 . ПМИД 7500443 .
- ^ Перейти обратно: а б Лубинецкий ГМ, Берлин Дж.А., Вайнштейн Р.Б., Вон DJ (декабрь 2004 г.). «Тромбоэмболические события при химиотерапии на основе эстрамустина фосфата у пациентов с гормонорефрактерной карциномой предстательной железы: результаты метаанализа». Рак . 101 (12): 2755–2759. дои : 10.1002/cncr.20673 . ПМИД 15536625 . S2CID 21465413 .
- ^ Физази К., Ле Мэтр А., Хьюд Дж., Берри В.Р., Келли В.К., Эймард Дж.К. и др. (ноябрь 2007 г.). «Добавление эстрамустина к химиотерапии и выживаемость пациентов с кастрационно-резистентным раком простаты: метаанализ индивидуальных данных пациентов». «Ланцет». Онкология . 8 (11): 994–1000. дои : 10.1016/S1470-2045(07)70284-X . ПМИД 17942366 .
- ^ Петриоли Р., Ровиелло Г., Фиаски А.И., Лаэра Л., Бьянко В., Понкьетти Р. и др. (октябрь 2015 г.). «Низкие дозы эстрамустина фосфата и сопутствующие низкие дозы ацетилсалициловой кислоты у пациентов с распространенным кастрационно-резистентным раком простаты, прошедших интенсивное предварительное лечение». Клинический рак мочеполовой системы . 13 (5): 441–446. дои : 10.1016/j.clgc.2015.03.004 . ПМИД 25920994 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п Гуннарссон П.О., GP Forshell (июнь 1984 г.). «Клиническая фармакокинетика эстрамустинфосфата». Урология . 23 (6 дополнений): 22–27. дои : 10.1016/S0090-4295(84)80093-X . ПМИД 6375076 .
- ^ Перейти обратно: а б Александр Н.К., Хэнкок А.К., Масуд М.Б., Пит Б.Г., Прайс Дж.Дж., Тернер Р.Л. и др. (март 1979 г.). «Эстрацит при распространенной карциноме молочной железы: исследование II фазы». Клиническая радиология . 30 (2): 139–147. дои : 10.1016/S0009-9260(79)80133-6 . ПМИД 86404 .
- ^ Перейти обратно: а б Дапонте Д., Сильвестр Р., Де Пау М., Фришман А., Смит Р.М., Смит П.Х. (август 1983 г.). «Изменение количества лейкоцитов во время лечения распространенного рака простаты эстрамустинфосфатом и стильбоэстролом». Британский журнал урологии . 55 (4): 408–412. дои : 10.1111/j.1464-410X.1983.tb03333.x . ПМИД 6349745 .
- ^ «Капсулы Emcyt эстрамустина фосфата натрия» (PDF) . FDA . Проверено 14 марта 2022 г.
- ^ Перейти обратно: а б с д и ж г час я дж Элкс Дж. (14 ноября 2014 г.). Словарь лекарств: Химические данные: Химические данные, структуры и библиография . Спрингер. стр. 502–503. ISBN 978-1-4757-2085-3 .
- ^ Перейти обратно: а б Ван Л.Г., Лю К.М., Крейс В., Будман Д.Р. (май 1998 г.). «Андрогенантагонистический эффект метаболитов эстрамустинфосфата (EMP) на дикий тип и мутировавшие рецепторы андрогенов» . Биохимическая фармакология . 55 (9): 1427–1433. дои : 10.1016/S0006-2952(97)00657-6 . ПМИД 10076535 .
- ^ Перейти обратно: а б Ван Поппель Х., Вербрук П.В., Баерт Л. (1990). «Влияние эстрамустинфосфата на свободные андрогены. Сравнительное исследование влияния орхиэктомии и эстрамустинфосфата на свободные андрогены у больных раком предстательной железы». Acta Urologica Belgica . 58 (4): 89–95. ПМИД 2093302 .
- ^ Перейти обратно: а б с Карр Дж.П., Вайсман З., Кирдани Р.Ю., Мерфи Г.П., Сандберг А.А. (август 1980 г.). «Влияние диэтилстильбестрола и эстрамустинфосфата на уровни глобулина, связывающего половые гормоны, и тестостерона в сыворотке крови у пациентов с раком простаты». Журнал урологии . 124 (2): 232–236. дои : 10.1016/S0022-5347(17)55383-5 . ПМИД 7190620 .
- ^ Олсон К.Б., Пиента К.Дж. (май 2000 г.). «Последние достижения в химиотерапии распространенного рака простаты». Текущие отчеты по урологии . 1 (1): 48–56. дои : 10.1007/s11934-000-0035-z . ПМИД 12084341 . S2CID 31084737 .
- ^ Перейти обратно: а б Даэлин Л., Дамбер Дж. Э., фон Шульц Б., Бергман Б. (август 1986 г.). «Эстрогенные эффекты этинилэстрадиола/полиоэстрадиолфосфата и эстрамустинфосфата у пациентов с карциномой предстательной железы. Сравнительное исследование эстроген-чувствительных белков печени, гонадотропинов и пролактина». Британский журнал урологии . 58 (4): 412–416. дои : 10.1111/j.1464-410X.1986.tb09095.x . ПМИД 3092893 .
- ^ Фредхольм Б., Дженсен Г., Линдског М. и Мунцинг Дж. (1974, январь). Влияние эстрамустинфосфата (эстрацита) на рост опухолей молочной железы, вызванных ДМБА, у крыс. В Acta Pharmacologica et Toxicologica (том 35, стр. 28-28). 35 Норре Согаде, а/я 2148, DK-1016 Копенгаген, Дания: Munksgaard Int Publ Ltd.
- ^ Перейти обратно: а б с Пунци Дж.С., Дуакс В.Л., Стронг П., Гриффин Дж.Ф., Флокко М.М., Захариас Д.Е. и др. (март 1992 г.). «Молекулярная конформация эстрамустина и двух аналогов» . Молекулярная фармакология . 41 (3): 569–576. ПМИД 1545778 .
- ^ Перейти обратно: а б Хаузер А.Р., Мерриман Р. (май 1984 г.). «Эстрамустина фосфат натрия». Разведка по наркотикам и клиническая фармация . 18 (5): 368–374. дои : 10.1177/106002808401800502 . ПМИД 6373212 . S2CID 25303747 .
- ^ Тью К.Д., Стернс МЭ (1989). «Эстрамустин - азотистый иприт/стероид с антимикротрубочковой активностью». Фармакология и терапия . 43 (3): 299–319. дои : 10.1016/0163-7258(89)90012-0 . ПМИД 2682681 .
- ^ Кавалли Ф., Кэй С.Б., Хансен Х.Х., Армитидж Дж.О., Пиккарт-Гебхарт М., ред. (12 сентября 2009 г.). Учебник медицинской онкологии (Четвертое изд.). ЦРК Пресс. стр. 442–. ISBN 978-0-203-09289-7 .
- ^ Гуннарссон О, Андерссон СБ, Йоханссон С.А. (1983). «Гидролиз эстрамустинфосфата; исследования in vitro». Европейский журнал метаболизма лекарств и фармакокинетики . 8 (4): 395–402. дои : 10.1007/BF03188772 . ПМИД 6673977 . S2CID 22105700 .
- ^ Перейти обратно: а б Озэки Т., Такеучи М., Сузуки М., Китамура Т., Такаянаги Р., Ёкояма Х., Ямада Ю. (октябрь 2009 г.). «Однонуклеотидные полиморфизмы гена 17бета-гидроксистероиддегидрогеназы типа 7: механизм побочных реакций, связанных с эстрамустином?». Международный журнал урологии . 16 (10): 836–841. дои : 10.1111/j.1442-2042.2009.02374.x . ПМИД 19735314 . S2CID 38350076 .
- ^ Перейти обратно: а б Сузуки М., Муто С., Хара К., Озеки Т., Ямада Ю., Кадоваки Т. и др. (февраль 2005 г.). «Однонуклеотидные полиморфизмы в генах 17-бета-гидроксистероиддегидрогеназы могут предсказать риск побочных эффектов эстрамустина фосфата натрия у пациентов с раком простаты». Международный журнал урологии . 12 (2): 166–172. дои : 10.1111/j.1442-2042.2005.01004.x . ПМИД 15733111 . S2CID 71166897 .
- ^ Ворота L, Тью К.Д. (2011). «Алкилирующие агенты». Лечение рака у человека: химиотерапия, биологическая терапия, гипертермия и вспомогательные меры . Рост и прогрессирование рака. Спрингер. стр. 61–85. дои : 10.1007/978-90-481-9704-0_4 . ISBN 978-90-481-9703-3 .
- ^ «Эстрадиол» (PDF) . Лаборатории Эбботт . Ноябрь 2009 года.
- ^ Лофтссон Т. (25 января 2014 г.). Стабильность лекарств для ученых-фармацевтов . Академическая пресса. стр. 77–. ISBN 978-0-12-411562-0 .
- ^ Бернал С. (21 августа 1997 г.). Лекарственная устойчивость в онкологии . ЦРК Пресс. стр. 287–. ISBN 978-1-4200-0209-6 .
- ^ Мерфф SJ (20 февраля 2012 г.). Справочник по безопасности и гигиене цитотоксических препаратов . Государственные институты. стр. 89–. ISBN 978-1-60590-705-5 .
- ^ Перейти обратно: а б «Эстрамустин фосфат» . ПабХим . Национальная медицинская библиотека США.
- ^ Фигг В.Д., Чау Ч.С., Смолл Э.Дж. (14 сентября 2010 г.). Лекарственное управление при раке простаты . Springer Science & Business Media. стр. 402–. ISBN 978-1-60327-829-4 .
- ^ Мортон И.К., Холл Дж.М. (6 декабря 2012 г.). Краткий словарь фармакологических средств: свойства и синонимы . Springer Science & Business Media. стр. 114–. ISBN 978-94-011-4439-1 .
- ^ «Drugs@FDA: Лекарственные препараты, одобренные FDA» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США . Проверено 29 января 2017 г.
- ^ Свитман, С., изд. (12 февраля 2013 г.). «Эстрамустина натрия фосфат». Мартиндейл: Полный справочник лекарств . Лондон, Великобритания: Фармацевтическая пресса . Проверено 8 февраля 2014 г.
Дальнейшее чтение
[ редактировать ]- Тью К.Д. (сентябрь 1983 г.). «Механизм действия эстрамустина». Семинары по онкологии . 10 (3 Приложение 3): 21–26. ПМИД 6364362 .
- Хойсаетер П.А., Бакке А. (сентябрь 1983 г.). «Эстрамустинфосфат (Эстрацит): экспериментальные и клинические исследования в Европе». Семинары по онкологии . 10 (3 Приложение 3): 27–33. ПМИД 6364363 .
- Сандберг А.А. (сентябрь 1983 г.). «Метаболические аспекты и действия, уникальные для Эстрацита». Семинары по онкологии . 10 (3 Приложение 3): 3–15. ПМИД 6364364 .
- Хаукаас С.А. (1984). «Иммунологические эффекты диэтилстильбестрола и эстрамустинфосфата». Скандинавский журнал урологии и нефрологии. Дополнение . 83 : 1–32. ПМИД 6387896 .
- Хаузер А.Р., Мерриман Р. (май 1984 г.). «Эстрамустина фосфат натрия». Разведка по наркотикам и клиническая фармация . 18 (5): 368–374. дои : 10.1177/106002808401800502 . ПМИД 6373212 . S2CID 25303747 .
- Сандберг А.А. (июнь 1984 г.). «Метаболические параметры эстрацита, имеющие отношение к его эффекту при раке предстательной железы». Урология . 23 (6 дополнений): 11–21. дои : 10.1016/S0090-4295(84)80092-8 . ПМИД 6375075 .
- Гуннарссон П.О., GP Forshell (июнь 1984 г.). «Клиническая фармакокинетика эстрамустинфосфата». Урология . 23 (6 дополнений): 22–27. дои : 10.1016/S0090-4295(84)80093-X . ПМИД 6375076 .
- Форсгрен Б., Бьорк П. (июнь 1984 г.). «Специфическое связывание эстрамустина с белками простаты». Урология . 23 (6 дополнений): 34–38. дои : 10.1016/S0090-4295(84)80095-3 . ПМИД 6375077 .
- Калланд Т., Хаукаас С.А. (июнь 1984 г.). «Иммунологические эффекты эстрамустинфосфата». Урология . 23 (6 дополнений): 39–45. дои : 10.1016/S0090-4295(84)80096-5 . ПМИД 6375078 .
- Хойзаетер П.А. (июнь 1984 г.). «Способ действия Эмцита». Урология . 23 (6 дополнений): 46–48. дои : 10.1016/S0090-4295(84)80097-7 . ПМИД 6375079 .
- Мюнцинг Дж., Гуннарссон К. (июнь 1984 г.). «Доклиническая фармакология и токсикология эстрамустинфосфата». Урология . 23 (6 доп.): 6–10. дои : 10.1016/S0090-4295(84)80091-6 . ПМИД 6375082 .
- Slack NH, GP Мерфи (июнь 1984 г.). «Клиническая токсичность и отдаленные результаты терапии Emcyt при раке простаты». Урология . 23 (6 дополнений): 73–77. дои : 10.1016/S0090-4295(84)80103-X . ПМИД 6375085 .
- Хедлунд П.О. (1985). «Способ действия эстрамустина фосфата при гормонозависимом и гормонозависимом раке предстательной железы». Прогресс клинических и биологических исследований . 185А : 197–202. ПМИД 3898129 .
- Хедлунд П.О. (1987). «Эстрацит - способ действия и клинический опыт». Прогресс клинических и биологических исследований . 243Б : 215–219. ПМИД 3309981 .
- Гран-при Мерфи (1987). «Текущий обзор клинического опыта применения эстрацита». Прогресс клинических и биологических исследований . 243Б : 221–225. ПМИД 3309982 .
- Форсгрен Б. (1988). «Эстрамустин-связывающий белок в простате крысы и человека». Скандинавский журнал урологии и нефрологии. Дополнение . 107 : 56–58. ПМИД 3287598 .
- Тью К.Д., Стернс МЭ (1989). «Внутриклеточные эффекты эстрамустина (Estracyt/Emcyt)». Прогресс клинических и биологических исследований . 303 : 169–175. ПМИД 2674983 .
- Тью К.Д., Стернс МЭ (1989). «Эстрамустин - азотистый иприт/стероид с антимикротрубочковой активностью». Фармакология и терапия . 43 (3): 299–319. дои : 10.1016/0163-7258(89)90012-0 . ПМИД 2682681 .
- Кёнивес I (1989). «Эстрамустинфосфат (Эстрацит) в лечении рака предстательной железы». Международная урология и нефрология . 21 (4): 393–397. дои : 10.1007/BF02559635 . ПМИД 2693392 . S2CID 9727646 .
- Бенсон Р., Хартли-Асп Б (1990). «Механизмы действия и клиническое применение эстрамустина». Исследование рака . 8 (3–4): 375–380. дои : 10.3109/07357909009012056 . ПМИД 2207764 .
- Ван Поппель Х., Баерт Л. (1991). «Современная роль эстрамустинфосфата при распространенном раке простаты». Прогресс клинических и биологических исследований . 370 : 323–341. ПМИД 1924466 .
- Янкнегт Р.А. (1992). «Эстрамустинфосфат и другие цитотоксические препараты в лечении распространенного рака предстательной железы с плохим прогнозом». Простата. Добавка . 4 : 105–110. дои : 10.1002/pros.2990210516 . ПМИД 1574449 . S2CID 40562112 .
- Тью К.Д., Глускер Дж.П., Хартли-Асп Б., Худес Г., Спейчер Л.А. (декабрь 1992 г.). «Доклинические и клинические перспективы использования эстрамустина в качестве антимитотического препарата». Фармакология и терапия . 56 (3): 323–339. дои : 10.1016/0163-7258(92)90023-S . ПМИД 1301594 .
- Крейс В. (1995). «Возвращение к Эстрамустину». Концепции, механизмы и новые мишени химиотерапии . Лечение и исследования рака. Том. 78. Спрингер. стр. 163–184. дои : 10.1007/978-1-4615-2007-8_8 . ISBN 978-1-4613-5829-9 . ПМИД 8595142 .
- Перри CM, Мактавиш Д. (июль 1995 г.). «Эстрамустина фосфат натрия. Обзор его фармакодинамических и фармакокинетических свойств, а также терапевтической эффективности при раке простаты». Наркотики и старение . 7 (1): 49–74. дои : 10.2165/00002512-199507010-00006 . ПМИД 7579781 . S2CID 36725810 .
- Худес Дж. (февраль 1997 г.). «Химиотерапия на основе эстрамустина». Семинары по урологической онкологии . 15 (1): 13–19. ПМИД 9050135 .
- Бергенхайм А.Т., Хенрикссон Р. (февраль 1998 г.). «Фармакокинетика и фармакодинамика эстрамустина фосфата». Клиническая фармакокинетика . 34 (2): 163–172. дои : 10.2165/00003088-199834020-00004 . ПМИД 9515186 . S2CID 1943973 .
- Китамура Т. (февраль 2001 г.). «Необходимость переоценки эстрамустинфосфата натрия (ЭМП) как варианта лечения монотерапии первой линии при распространенном раке простаты». Международный журнал урологии . 8 (2): 33–36. дои : 10.1046/j.1442-2042.2001.00254.x . ПМИД 11240822 . S2CID 43384150 .
- Рэвери В., Физази К., Удар С., Друэ Л., Эймар Дж.К., Кулин С. и др. (декабрь 2011 г.). «Использование эстрамустинфосфата в современном лечении распространенного рака простаты». БЖУ Интернешнл . 108 (11): 1782–1786. дои : 10.1111/j.1464-410X.2011.10201.x . ПМИД 21756277 . S2CID 33456591 .
- Цинь З, Ли Х, Чжан Дж, Тан Дж, Хань П, Сюй З и др. (сентябрь 2016 г.). «Химиотерапия с эстрамустином или без него для лечения резистентного к кастрации рака простаты: систематический обзор и метаанализ» . Лекарство . 95 (39): е4801. дои : 10.1097/MD.0000000000004801 . ПМК 5265899 . ПМИД 27684806 .