Ингибитор протеасом
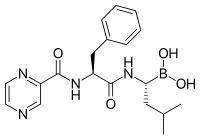
Ингибиторы протеасом ( стебель МНН –зомиб) [ 1 ] — препараты, блокирующие действие протеасом — клеточных комплексов, расщепляющих белки . Их изучают при лечении рака ; три из них одобрены для лечения множественной миеломы .
Механизм
[ редактировать ]Вероятно, задействовано множество механизмов, но ингибирование протеасом может предотвратить деградацию проапоптотических факторов, таких как белок p53 , позволяя активировать запрограммированную гибель клеток в неопластических клетках, зависящую от подавления проапоптотических путей. Например, бортезомиб вызывает быстрое и резкое изменение уровня внутриклеточных пептидов. [ 2 ]
Примеры
[ редактировать ]- Первым обнаруженным непептидным ингибитором протеасом был натуральный продукт лактацистин . [ 3 ]
- Дисульфирам был предложен в качестве еще одного ингибитора протеасом. [ 4 ] [ 5 ] [ 6 ]
- эпигаллокатехин-3-галлат . Также был предложен [ 7 ]
- Маризомиб (салиноспорамид А) начал клинические испытания при лечении множественной миеломы .
- Опрозомиб (ONX-0912), деланзомиб (CEP-18770) также начали клинические испытания. [ 8 ]
- Эпоксомицин является природным селективным ингибитором. [ 9 ]
- MG132 представляет собой синтезированный пептид, обычно используемый для in vitro . исследований
- Бета-гидрокси-бета-метилбутират является ингибитором протеасом в скелетных мышцах человека. [ 10 ] [ 11 ] живой . [ 12 ]
Разрешенные лекарства
[ редактировать ]- Бортезомиб ( Велкейд ) был одобрен в 2003 году. Это был первый ингибитор протеасом, одобренный для использования в США. Его атом бора связывает каталитический сайт 26S протеасомы . [ 13 ]
- Карфилзомиб ( Кипролис ) был одобрен FDA для лечения рецидивирующей и рефрактерной множественной миеломы в 2012 году. [ 14 ] Он необратимо связывается и ингибирует химотрипсиноподобную активность 20S протеасомы .
- Иксазомиб ( Нинларо ) был одобрен FDA в 2015 году для использования в сочетании с леналидомидом и дексаметазоном для лечения множественной миеломы после как минимум одной предшествующей терапии. Это первый перорально доступный ингибитор протеасом. [ 15 ]
Ссылки
[ редактировать ]- ^ «Использование стеблей при выборе международных непатентованных названий (МНН) фармацевтических веществ» (PDF) . Всемирная организация здравоохранения . Проверено 5 ноября 2016 г.
- ^ Гельман Дж.С., Сирони Дж., Березнюк И., Дасгупта С., Кастро Л.М., Гоццо ФК, Ферро Э.С., Фрикер Л.Д. (2013). «Изменения внутриклеточного пептидома в ответ на ингибитор протеасом бортезомиб» . ПЛОС ОДИН . 8 (1): e53263. Бибкод : 2013PLoSO...853263G . дои : 10.1371/journal.pone.0053263 . ПМЦ 3538785 . ПМИД 23308178 .
- ^ Фентеани Г., Стандарт Р.Ф., Лейн В.С., Чой С., Кори Э.Дж., Шрайбер С.Л. (1995). «Ингибирование активности протеасом и субъединично-специфической модификации аминоконцевого треонина лактацистином». Наука . 268 (5211): 726–31. Бибкод : 1995Sci...268..726F . дои : 10.1126/science.7732382 . ПМИД 7732382 . S2CID 37779687 .
- ^ Лёвборг Х., Оберг Ф., Рикардсон Л., Гуллбо Дж., Нюгрен П., Ларссон Р. (март 2006 г.). «Ингибирование активности протеасом, транслокации ядерного фактора-КаппаВ и выживания клеток антиалкогольным препаратом дисульфирамом» . Международный журнал рака . 118 (6): 1577–80. дои : 10.1002/ijc.21534 . ПМИД 16206267 .
- ^ Викстрем М., Дэниелссон К., Рикардсон Л. и др. (январь 2007 г.). «Фармакологическое профилирование дисульфирама с использованием линий опухолевых клеток человека и опухолевых клеток человека, полученных от пациентов». Биохимическая фармакология . 73 (1): 25–33. дои : 10.1016/j.bcp.2006.08.016 . ПМИД 17026967 .
- ^ Цвек Б., Дворжак З. (август 2008 г.). «Значение ингибирования протеасом при раке. Может ли старый препарат дисульфирам иметь блестящее новое будущее в качестве нового ингибитора протеасом?». Открытие наркотиков сегодня . 13 (15–16): 716–22. дои : 10.1016/j.drudis.2008.05.003 . ПМИД 18579431 .
- ^ Осанаи К., Лэндис-Пивовар К.Р., Доу К.П., Чан Т.Х. (август 2007 г.). «Парааминозаместитель в D-кольце полифенола эпигаллокатехин-3-галлата зеленого чая как новый ингибитор протеасом и индуктор апоптоза раковых клеток» . Биоорг. Мед. Хим . 15 (15): 5076–82. дои : 10.1016/j.bmc.2007.05.041 . ПМЦ 2963865 . ПМИД 17544279 .
- ^ «Современные достижения в новых подходах к лечению рецидивирующей / рефрактерной множественной миеломы на основе ингибиторов протеасом» . 2011.
- ^ Мэн, Л.; и др. (1999). «Эпоксомицин, мощный и селективный ингибитор протеасом, проявляет противовоспалительную активность in vivo» . Учеб. Натл. акад. наук. США . 96 (18): 10403–10408. Бибкод : 1999PNAS...9610403M . дои : 10.1073/pnas.96.18.10403 . ЧВК 17900 . ПМИД 10468620 .
- ^ Уилсон Дж.М., Фитшен П.Дж., Кэмпбелл Б., Уилсон Дж.Дж., Занчи Н., Тейлор Л., Уилборн С., Калман Д.С., Стаут Дж.Р., Хоффман Дж.Р., Зигенфусс Т.Н., Лопес Х.Л., Крайдер Р.Б., Смит-Райан А.Е., Антонио Дж. (февраль 2013 г.) . «Позиция Международного общества спортивного питания: бета-гидрокси-бета-метилбутират (HMB)» . Дж. Межд. Соц. Спортивный Нутр . 10 (1): 6. дои : 10.1186/1550-2783-10-6 . ПМК 3568064 . ПМИД 23374455 .
Протеолиз скелетных мышц усиливается в катаболических состояниях, таких как голодание, иммобилизация, старение и болезни [77]. Было показано, что HMB уменьшает деградацию белков скелетных мышц как in vitro[72,73], так и in vivo[78]. ... Действительно, было показано, что HMB снижает экспрессию протеасом [72] и активность [72,78-80] во время катаболических состояний, тем самым ослабляя деградацию белков скелетных мышц по пути убиквитин-протеасома.
- ^ Лукозе Ф., Пандей М.К., Радхакришна К. (2015). «Влияние производных аминокислот на физическую, умственную и физиологическую деятельность». Крит. Преподобный Food Sci. Нутр . 55 (13): 1793–1807. дои : 10.1080/10408398.2012.708368 . ПМИД 24279396 . S2CID 22657268 .
HMB, производное лейцина, предотвращает повреждение мышц и увеличивает мышечную силу за счет уменьшения протеолиза в мышцах, вызванного физической нагрузкой, а также помогает увеличить мышечную массу тела.
- ^ Уилкинсон DJ, Хоссейн Т., Хилл Д.С., Филлипс Б.Е., Кроссленд Х., Уильямс Дж., Лафна П., Черчворд-Венн Т.А., Брин Л., Филлипс С.М., Этеридж Т., Ратмахер Дж.А., Смит К., Шевчик Н.Дж., Атертон П.Дж. (июнь 2013 г.) . «Влияние лейцина и его метаболита β-гидрокси-β-метилбутирата на метаболизм белков скелетных мышц человека» . Дж. Физиол . 591 (11): 2911–2923. дои : 10.1113/jphysicalol.2013.253203 . ПМК 3690694 . ПМИД 23551944 .
хотя пероральный прием HMB не вызывал увеличения уровня инсулина в плазме, он вызывал депрессию MPB (-57%). Обычно постпрандиальное снижение МПБ (около 50%) объясняется азотсберегающим действием инсулина, поскольку фиксация инсулина в постабсорбционных концентрациях (5 мкЕ/мл) при непрерывном введении АК (18 гх-1) не подавляла MPB (Greenhaff et al., 2008), поэтому мы решили не измерять MPB в группе Leu из-за ожидаемой гиперинсулинемии (рис. 3C). Таким образом, HMB снижает MPB аналогично инсулину, но независимо от него. Эти данные согласуются с сообщениями об антикатаболических эффектах HMB, подавляющих MPB в доклинических моделях, посредством ослабления протеасомно-опосредованного протеолиза в ответ на LPS (Eley et al. 2008).
- ^ Бонвини П., Зорзи Э., Бассо Г., Розолен А. (2007). «Ингибирование 26S-протеасом, опосредованное бортезомибом, вызывает остановку клеточного цикла и индуцирует апоптоз при анапластической крупноклеточной лимфоме CD-30+» . Лейкемия . 21 (4): 838–42. дои : 10.1038/sj.leu.2404528 . PMID 17268529 .
- ^ «Сообщения для прессы — FDA одобрило Кипролис для лечения некоторых пациентов с множественной миеломой» . Управление по контролю за продуктами и лекарствами США. 20 июля 2012 года . Проверено 24 апреля 2016 г.
- ^ «Сообщения для прессы — FDA одобряет Нинларо, новый пероральный препарат для лечения множественной миеломы» . Управление по контролю за продуктами и лекарствами США . Проверено 24 апреля 2016 г.