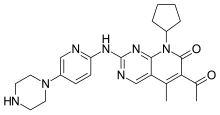
Палбоциклиб
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Ибранс и другие |
| Другие имена | ПД-0332991 |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а615013 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 46% |
| Связывание с белками | 85% |
| Метаболизм | Печень ( CYP3A , SULT2A1 , глюкуронидация ) |
| Период полувыведения | 29 (±5) часов |
| Экскреция | 74% кала, 18% мочи |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| КЭБ | |
| ХЭМБЛ | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.238.221 |
| Химические и физические данные | |
| Формула | С 24 Н 29 Н 7 О 2 |
| Молярная масса | 447.543 g·mol −1 |
| 3D model ( JSmol ) | |
Палбоциклиб под торговой маркой Ibrance , продаваемый, среди прочего, , представляет собой препарат, разработанный компанией Pfizer для лечения HR-положительного и HER2-негативного рака молочной железы . Это селективный ингибитор циклинзависимых киназ CDK4 и CDK6 . [5] [6] Палбоциклиб был первым ингибитором CDK4/6, одобренным для лечения рака. [7]
Механизм действия
[ редактировать ]Это селективный ингибитор циклинзависимых киназ CDK4 и CDK6 . [5] [6]
В фазе G1 клеточного клетки цикла млекопитающих должны пройти контрольную точку, известную как точка ограничения «R», чтобы завершить клеточный цикл и поделиться. Комплекс CDK4 и CDK6 с циклином D запускает фосфорилирование белка ретинобластомы Rb, что позволяет клетке проходить R и переходить к делению . [8] Регуляция одного или нескольких белков, участвующих в этой контрольной точке, теряется при многих видах рака. Однако, ингибируя CDK4/6, палбоциклиб гарантирует, что комплекс циклин D-CDK4/6 не сможет способствовать фосфорилированию Rb. Это не позволяет ячейке пройти R и выйти из G1 и, в свою очередь, продолжить клеточный цикл. [8]
Администрация
[ редактировать ]Палбоциклиб принимают ежедневно перорально во время еды в цикле из 21 дня активного приема препарата, а затем 7 дней без него. В настоящее время палбоциклиб назначают в виде комбинированной терапии с летрозолом или фулвестрантом . [9] Пациентам также не следует принимать ингибиторы или индукторы CYP3A во время приема палбоциклиба. Информация FDA также предостерегает от употребления продуктов из грейпфрута во время приема палбоциклиба. [9]
Допуски и показания
[ редактировать ]HR+ рак молочной железы
[ редактировать ]Препарат был рассмотрен и одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) 3 февраля 2015 года в рамках программы ускоренного рассмотрения приоритетов и прорывной терапии в качестве лечения (в сочетании с летрозолом) для пациентов с положительными рецепторами эстрогена (ER+). рак молочной железы. [10] Это было ускоренное одобрение . [11]
В марте 2017 года FDA предоставило регулярное одобрение палбоциклибу при распространенном или метастатическом раке молочной железы с положительным по рецептору гормона (HR) и отрицательным по рецептору эпидермального фактора роста 2 человека (HER2) в сочетании с ингибитором ароматазы. [12]
Исследование III фазы PALOMA-2 было полностью включено к февралю 2015 года, а положительные результаты были получены в апреле 2016 года. [13] Результаты исследования PALOMA-2 (опубликованы в ноябре 2016 г.) показали значительно более длительную выживаемость без прогрессирования у пациентов, принимавших палбоциклиб в сочетании с летрозолом, по сравнению с пациентами, принимавшими летрозол и плацебо. Выживаемость без прогрессирования оценивалась по рентгенологически подтвержденному прогрессированию заболевания по критериям RECIST или смерти во время исследования. На момент публикации данных об общей выживаемости было недостаточно, и окончательный анализ планируется провести после того, как в общей сложности произойдет 390 смертей по протоколу и по согласованию с регулирующими органами. Следует отметить, что добавление палбоциклиба вызывало более высокий уровень миелотоксических явлений. в исследовании [14]
Препарат был одобрен для использования в Европейском Союзе в ноябре 2016 года для лечения местно-распространенного или метастатического рака молочной железы, положительного по рецептору гормона (HR), отрицательного по рецептору эпидермального фактора роста 2 человека (HER2) либо в сочетании с ингибитором ароматазы , либо для лечения рака молочной железы. женщинам, ранее получавшим эндокринную терапию, в сочетании с фулвестрантом. Женщинам в пре- или перименопаузе рилизинг-гормона лютеинизирующего гормона . агонисты следует также назначать [15]
В декабре 2017 года палбоциклиб был принят к использованию Национальной службой здравоохранения после прохождения процедуры Шотландского медицинского консорциума в отношении лекарств, используемых для лечения очень редкого рака молочной железы, находящегося в конце жизни. [16]
Побочные эффекты
[ редактировать ]У большинства пациентов, принимающих палбоциклиб, наблюдается нейтропения – состояние, при котором у пациента наблюдается аномально низкое количество нейтрофилов . Этот побочный эффект влияет на иммунную систему и, таким образом, вероятно, является причиной второго наиболее распространенного побочного эффекта — инфекции . [17] лейкопения и анемия . Среди пациентов, принимающих палбоциклиб, также часто наблюдаются [17] Более 10% пациентов также испытывают побочные эффекты, такие как усталость , тошнота , диарея , респираторные инфекции , головная боль , тромбоцитопения , рвота и снижение аппетита. [18] [17] FDA также указывает, что пациенты должны проявлять бдительность и следить за любыми признаками тромбоэмболии легочной артерии . FDA также предупреждает, что женщины должны знать, что препарат может оказать вредное воздействие на плод , и поэтому его не следует принимать во время беременности. [9]
Механизмы сопротивления
[ редактировать ]Резистентность к палбоциклибу
[ редактировать ]Одобрение FDA и EMA палбоциклиба зависит от результатов клинических испытаний относительно выживаемости без прогрессирования заболевания (ВБП). Однако, хотя данные оказались многообещающими (одно исследование [19] имели значения p, очень близкие к порогу значимости, который при дальнейших клинических испытаниях может продемонстрировать статистическую значимость), по состоянию на 2019 г. [update] не наблюдалось значительного улучшения общей выживаемости (ОВ) при приеме палбоциклиба. Например, в исследовании PALOMA-2 у более чем 70% пациентов, принимавших палбоциклиб и летрозол, прогрессирование заболевания наблюдалось к 40 месяцам. [20] Это препятствовало всемирному признанию препарата, поскольку экономический анализ не показал, что палбоциклиб экономически эффективен.
снова Сопротивление
[ редактировать ]Устойчивость de novo к палбоциклибу затрагивает множество мишеней как выше, так и ниже пути CDK4/6 к Rb. Сверхэкспрессия транскрипционного фактора E2F2 способна способствовать устойчивости к ингибированию CDK4/6, а не просто потере Rb (прямой нижестоящей мишени CDK4/6). [21] Палбоциклиб менее эффективен у пациентов, у которых клетки рака молочной железы сверхэкспрессируют циклин E1 или E2 и Brk (киназу, связанную с опухолью молочной железы). Brk представляет собой внутриклеточную киназу, которая сверхэкспрессируется в 60% случаев рака молочной железы и чья амплификация приводит к усилению фосфорилирования Y88 белка p27, а также к увеличению активности циклина D и CDK4, тем самым делая раковые клетки более устойчивыми к палбоциклибу. [21]
Исследование 2018 года показало, что мутации в пути, совершенно не связанном с осью CDK4/6-Rb, также участвуют в устойчивости к палбоциклибу. Потеря супрессора опухоли FAT1 способствовала устойчивости к ингибиторам CDK4/6 через путь Hippo , сигнальный путь, который, как известно, действует как супрессор опухоли. [22] Ранее предполагалось, что FAT1 является супрессором опухолей и онкогеном, хотя никогда ранее не было явно связано с резистентностью. Команда обнаружила, что клеткам, подавляющим FAT1, требуются значительно более высокие дозы ингибиторов CDK4/6, чтобы блокировать пролиферацию клеток рака молочной железы in vivo . [22]
Резистентность вследствие эндокринной терапии
[ редактировать ]Палбоциклиб показан при метастатических клетках рака молочной железы HR+, HER2-. Поскольку ингибирование CDK4/6 действует непосредственно после целей эндокринной терапии, возможно развитие резистентности к перекрестной терапии в результате прогрессирования заболевания на гормональной терапии. Однако в целом эндокринно-резистентные опухоли способны сохранять чувствительность к ингибированию CDK4/6, причем особый успех наблюдался у пациентов, получавших комбинированную терапию палбоциклибом с эндокринной терапией. [20] Например, исследование PALOMA-3, в котором изучалась польза палбоциклиба и фулвестранта по сравнению с одним фулвестрантом, показало, что комбинированный режим лечения улучшает ВБП как у пациентов с мутацией ESR1 , так и у пациентов с ктДНК дикого типа ESR1 . Такие результаты показывают, что ингибиторы CDK4/6 эффективны независимо от статуса мутации ESR1 , маркера, который в противном случае показал бы у пациента эндокринную резистентность. [23]
Определенные проявления резистентности к эндокринной терапии могут еще больше повысить чувствительность рака молочной железы к ингибиторам CDK4/6. Например, нарушения репарации ошибочного спаривания, вызванные мутацией MutL при ER+ раке молочной железы, ускользают от CHK2-опосредованного ингибирования CDK4, тем самым приводя к эндокринной резистентности. [20] Однако было продемонстрировано, что ингибиторы CDK4/6 высокоэффективны в MutL-дефектных ER+ клетках рака молочной железы, а MutL потенциально может выступать в качестве биомаркера для выявления пациентов, наиболее подходящих для лечения ингибиторами CDK4/6.
Другие механизмы сопротивления
[ редактировать ]Исследователи из Института Даны Фарбер обнаружили, что клетки рака молочной железы, у которых развилась устойчивость к палбоциклибу, снова стали чувствительными к препарату после семидневного «лечебного отпуска». [24] Ученые связали первоначальное развитие резистентности с увеличением экспрессии CDK6 (но не CDK4, другой мишени палбоциклиба) со специфическим механизмом активации CDK6, возникающим в результате подавления пути TGF-β через miR-432-5p. микроРНК . Ученые сделали это открытие после того, как заметили, что в лаборатории все клетки рака молочной железы в чашке приобретали устойчивость в одно и то же время - явление, противоположное классическим моделям приобретения устойчивости, в которых одна или две клетки становятся устойчивыми, а затем расширяются до охватывают большую часть опухоли по мере деления. Эти клетки, устойчивые к палбоциклибу, также не содержали конкретной мутации, а скорее стали устойчивыми и продолжали распространять эту устойчивость на соседние клетки через экзосомы. Хотя механизм этой устойчивости еще не выяснен, он открывает возможности для дальнейших исследований совершенно нового метода, с помощью которого раковые клетки приобретают устойчивость. С другой стороны, это говорит о том, что пациенты, у которых, по-видимому, прогрессирует на палбоциклибе, могут получить пользу от более длительного лечения после отпуска, во время которого их опухоли «сбрасываются».
Существует множество способов, с помощью которых раковые клетки становятся устойчивыми к палбоциклибу, причем механизмы резистентности включают множество мишеней и процессов на протяжении всего пути действия палбоциклиба. По оценкам предыдущих исследований, клетки рака молочной железы демонстрируют адаптацию к палбоциклибу уже через 72 часа после лечения. [21] Было показано, что доказательства этого «опосредованы неканонической активацией комплексов циклин D1/CDK2, что, в свою очередь, вызывает восстановление экспрессии циклина E2 и [последующий] вход в S-фазу, несмотря на ингибирование CDK4/6» выше этих двух мишеней. . [21] Кроме того, по оценкам, примерно 10% пациентов имеют первичную резистентность к ингибиторам CDK4/6 (резистентность до лекарственной терапии). [25] Например, пациенты, у которых на исходном уровне наблюдаются признаки функциональной потери Rb, вряд ли получат пользу от ингибирования CDK4/6, равно как и пациенты, у которых на исходном уровне наблюдаются признаки повышенной экспрессии циклина E1 или высокого соотношения CCNE1/RB. [25]
Клинические испытания
[ редактировать ]HR+ рак молочной железы
[ редактировать ]В апреле 2015 года в исследовании PALOMA-3 было объявлено, что добавление палбоциклиба превосходит монотерапию фулвестрантом по выживаемости без прогрессирования заболевания . [26]
В исследовании фазы II PALOMA-1, о котором сообщалось на ежегодном собрании Американской ассоциации исследований рака в апреле 2014 года, было показано, что добавление палбоциклиба к летрозолу значительно замедляет прогрессирование распространенного рака (медиана выживаемости без прогрессирования увеличилась с 10,2 месяцев до 20,2 месяца), но не было показано, что он оказывает статистически значимое влияние на увеличение общей продолжительности выживаемости пациентов. [27] [28] [29]
31 мая 2020 г. компания Pfizer объявит результаты запланированного анализа эффективности и бесполезности. Результаты показывают, что при использовании в сочетании с послеоперационной эндокринной терапией «маловероятно, что будет продемонстрировано статистически значимое улучшение первичной конечной точки — инвазивной безрецидивной выживаемости (iDFS)». [30] Исследование проводилось на пациентах мужского и женского пола с HR-положительным и HER2-отрицательным раком молочной железы на ранних стадиях.
Активные клинические исследования
[ редактировать ]По данным NIH, Национального института рака в настоящее время проводится 39 активных клинических испытаний палбоциклиба отдельно или в сочетании с другими препаратами. В то время как большинство из них изучают дальнейшее использование палбоциклиба для лечения рака молочной железы, другие исследования изучают потенциальное применение палбоциклиба при раке головы и шеи, немелкоклеточном раке легких , рецидивирующих метастазах в головной мозг, плоскоклеточном раке, центральной нервной системе. опухоли и другие типы солидных опухолей. [31]
В декабре 2017 года компания Pfizer объявила, что исследование PALOMA-2, продолжающееся исследование фазы III, сочетающее палбоциклиб с летрозолом, показало снижение риска прогрессирования заболевания среди участников исследования на 44%. Исследование также продемонстрировало более чем годовое улучшение медианы выживаемости без прогрессирования у пациентов, получающих комбинированную терапию (по сравнению с летрозолом в отдельности). Медианное время наблюдения за пациентами PALOMA-2 в настоящее время превышает три года, что делает это самыми продолжительными отслеживаемыми данными для III фазы исследования ингибитора CDK4/6. [7]
Палбоциклиб в настоящее время находится на второй фазе клинических испытаний в качестве комбинированного лечения с пероральными SERD при раке молочной железы ER+ / HER2- . Исследования включают палбоциклиб плюс G1 Therapeutic. ринтодестрант [32] и Zn-c5 компании Zentalis. [33]
Препараты со схожим механизмом действия
[ редактировать ]У Палбоциклиба есть несколько прямых конкурентов, которые в настоящее время присутствуют на рынке или проходят клинические испытания. В сентябре 2017 года абемациклиб , еще один селективный ингибитор CDK4/6, принадлежащий и производимый компанией Eli Lilly , был одобрен для лечения HR-положительного и HER2-негативного распространенного метастатического рака молочной железы как в сочетании с фулвестрантом, так и в качестве монотерапии . В марте 2017 года FDA также одобрило рибоциклиб , принадлежащий Novartis , в качестве комбинированной терапии с ингибиторами ароматазы по показаниям, аналогичным показаниям палбоциклиба и рибоциклиба. Примечательно, что рибоциклиб, по-видимому, также оказывает ингибирующее действие на активность циклина D3 /CDK6. [34] G1 Терапия [35] также имеется ингибитор CDK4/6, трилациклиб , который подлежит одобрению FDA (плановая дата принятия решения — 15 февраля 2021 г.) для использования при мелкоклеточном раке легких. [36]
Общество и культура
[ редактировать ]Экономика
[ редактировать ]Ибранс «можно заказать в избранных» специализированных аптеках , и он «продается по цене 9850 долларов США на 30 дней или 118 200 долларов США за годовой запас без учета скидок». [37] Согласно заявлению нью-йоркской компании Pfizer, цена «не является стоимостью, которую платит большинство пациентов или плательщиков», поскольку большинство рецептов выдаются через планы медицинского страхования, которые договариваются о скидках на лекарства или получают установленные правительством ценовые уступки. [37] В специализированных аптеках США выписывают рецепты на лекарства, которые обычно стоят дорого. [38] [39]
Сопротивление стоимости
[ редактировать ]В феврале 2017 года Национальный институт здравоохранения и совершенствования медицинской помощи (NICE) в Соединенном Королевстве опубликовал заявление, в котором говорилось, что стоимость Ибранса (приблизительно 3700 долларов США за 28 дней) не оправдывает дополнительных преимуществ для здоровья. [40] Было заявлено, что, учитывая побочные эффекты, вызванные Ибрансом, NICE не может одобрить это лекарство с точки зрения затрат. [41] В то время годовое лечение палбоциклибом и таким препаратом, как фулвестрант, стоило 106 105 долларов США (79 650 фунтов стерлингов). [41] В ноябре 2017 года NICE объявила, что после переговоров с Pfizer цена будет снижена, и препарат будет рекомендован к применению. [42]
Ссылки
[ редактировать ]- ^ «Лекарства, отпускаемые по рецепту: регистрация новых химических веществ в Австралии, 2017» . Управление терапевтических товаров (TGA) . 21 июня 2022 года. Архивировано из оригинала 10 апреля 2023 года . Проверено 9 апреля 2023 г.
- ^ «Лекарственные средства, отпускаемые по рецепту, и биологические препараты: годовой обзор TGA за 2017 год» . Управление терапевтических товаров (TGA) . 21 июня 2022 г. Проверено 31 марта 2024 г.
- ^ «Разрешения на новые лекарства Министерства здравоохранения Канады: основные события 2016 г.» . Здоровье Канады . 14 марта 2017 года . Проверено 7 апреля 2024 г.
- ^ «Ибранс ЭПАР» . Европейское агентство по лекарственным средствам . 9 ноября 2016 года . Проверено 16 мая 2024 г.
- ^ Jump up to: а б Финн Р.С., Деринг Дж., Конклин Д., Калус О., Коэн Д.Д., Десаи А.Дж. и др. (2009). «PD 0332991, селективный ингибитор циклин-D-киназы 4/6, преимущественно ингибирует пролиферацию люминальных эстроген-положительных клеточных линий рака молочной железы человека in vitro» . Исследование рака молочной железы . 11 (5): R77. дои : 10.1186/bcr2419 . ПМЦ 2790859 . ПМИД 19874578 .
- ^ Jump up to: а б Рокка А., Фарольфи А., Браваччини С., Широне А., Амадори Д. (февраль 2014 г.). «Палбоциклиб (PD 0332991): воздействие на механизм клеточного цикла при раке молочной железы». Экспертное заключение по фармакотерапии . 15 (3): 407–420. дои : 10.1517/14656566.2014.870555 . ПМИД 24369047 . S2CID 23229580 .
- ^ Jump up to: а б «Обновленные данные фазы 3 исследования Ибранса (палбоциклиб) плюс летрозол при HR+, HER2-метастатическом раке молочной железы подтверждают улучшение выживаемости без прогрессирования» (пресс-релиз). Пфайзер. Архивировано из оригинала 22 июня 2021 года . Проверено 16 декабря 2017 г.
- ^ Jump up to: а б Сюй Х, Ю С, Лю Q, Юань X, Мани С, Пестель Р.Г. и др. (апрель 2017 г.). «Последние достижения в области высокоселективных ингибиторов CDK4/6 при раке молочной железы» . Журнал гематологии и онкологии . 10 (1): 97. дои : 10.1186/s13045-017-0467-2 . ПМК 5404666 . ПМИД 28438180 .
- ^ Jump up to: а б с «Этикетка препарата IBRANCE FDA» (PDF) . Архивировано (PDF) из оригинала 1 апреля 2021 года . Проверено 15 декабря 2017 г.
- ^ «FDA одобрило палбоциклиб для лечения метастатического рака молочной железы» . ОнкЛайв. 3 февраля 2015 года. Архивировано из оригинала 31 октября 2018 года . Проверено 4 февраля 2015 г.
- ^ «Pfizer получила ускоренное одобрение FDA США на IBRANCE (палбоциклиб)» . Пфайзер. 3 февраля 2015 г. Архивировано из оригинала 18 января 2021 г. Проверено 4 февраля 2015 г.
- ^ «Палбоциклиб (Ибранс)» . FDA. 31 марта 2017 года. Архивировано из оригинала 23 апреля 2019 года . Проверено 7 июля 2017 г.
- ^ «Исследование на поздней стадии расширенного использования Ibrance от Pfizer прошло успешно; последуют глобальные нормативные заявки. Апрель 2016 г.» . 19 апреля 2016 г. Архивировано из оригинала 25 апреля 2020 г. . Проверено 20 апреля 2016 г.
- ^ Финн Р.С., Мартин М., Руго Х.С., Джонс С., Им С.А., Гельмон К. и др. (ноябрь 2016 г.). «Палбоциклиб и летрозол при распространенном раке молочной железы» . Медицинский журнал Новой Англии . 375 (20): 1925–1936. дои : 10.1056/NEJMoa1607303 . ПМИД 27959613 .
- ^ «Отчет об общественной оценке ибранса (палбоциклиба) в Европе» . Архивировано из оригинала 29 мая 2017 года . Проверено 6 мая 2017 г.
- ^ «Препарат от рака молочной железы одобрен для использования Национальной службой здравоохранения» . Новости Би-би-си . 11 декабря 2017 года. Архивировано из оригинала 25 апреля 2020 года . Проверено 11 декабря 2017 г.
- ^ Jump up to: а б с «Разрешенные лекарственные средства – Палбоциклиб (ИБРАНС)» . Центр оценки и исследования лекарственных средств . Управление по контролю за продуктами и лекарствами США. Архивировано из оригинала 23 апреля 2019 года . Проверено 16 декабря 2017 г.
- ^ Тернер Н.К., Ро Дж., Андре Ф., Лой С., Верма С., Ивата Х. и др. (июль 2015 г.). «Палбоциклиб при распространенном раке молочной железы с положительным статусом гормонов» . Медицинский журнал Новой Англии . 373 (3): 209–219. дои : 10.1056/NEJMoa1505270 . ПМИД 26030518 . Архивировано из оригинала 23 сентября 2021 года . Проверено 10 декабря 2019 г.
- ^ Тернер Н.К., Сламон Д.Д., Ро Дж., Бондаренко И., Им С.А., Масуда Н. и др. (ноябрь 2018 г.). «Общая выживаемость при применении палбоциклиба и фулвестранта при распространенном раке молочной железы» . Медицинский журнал Новой Англии . 379 (20): 1926–1936. дои : 10.1056/nejmoa1810527 . ПМИД 30345905 .
- ^ Jump up to: а б с Портман Н., Александру С., Карсон Э., Ван С., Лим Э., Калдон С.Э. (январь 2019 г.). «Преодоление резистентности к ингибиторам CDK4/6 при ER-положительном раке молочной железы» . Эндокринный рак . 26 (1): С15–С30. дои : 10.1530/erc-18-0317 . ПМИД 30389903 .
- ^ Jump up to: а б с д Гуардуччи С., Бонечи М., Боккалини Дж., Бенелли М., Ризи Э., Ди Лео А. и др. (октябрь 2017 г.). «Механизмы устойчивости к ингибиторам CDK4/6 при раке молочной железы и потенциальные биомаркеры ответа» . Уход за грудью . 12 (5): 304–308. дои : 10.1159/000484167 . ПМК 5704709 . ПМИД 29234249 .
- ^ Jump up to: а б Ли З, Разави П, Ли Кью, Той В, Лю Б, Пинг С и др. (декабрь 2018 г.). «Потеря супрессора опухоли FAT1 способствует устойчивости к ингибиторам CDK4/6 через путь гиппопотама» . Раковая клетка . 34 (6): 893–905.e8. дои : 10.1016/j.ccell.2018.11.006 . ПМК 6294301 . ПМИД 30537512 .
- ^ Тернер Н.К., Ро Дж., Андре Ф., Лой С. , Верма С., Ивата Х. и др. (июль 2015 г.). «Палбоциклиб при распространенном раке молочной железы с положительным статусом гормонов» . Медицинский журнал Новой Англии . 373 (3): 209–219. дои : 10.1056/nejmoa1505270 . ПМИД 26030518 . Архивировано из оригинала 23 сентября 2021 года . Проверено 10 декабря 2019 г.
- ^ Корнелл Л., Вандер С.А., Визал Т., Вагл Н., Шапиро Г.И. (март 2019 г.). «Опосредованное микроРНК подавление пути TGF-β обеспечивает трансмиссивную и обратимую резистентность к ингибитору CDK4/6» . Отчеты по ячейкам . 26 (10): 2667–2680.e7. дои : 10.1016/j.celrep.2019.02.023 . ПМК 6449498 . ПМИД 30840889 .
- ^ Jump up to: а б Маккартни А., Мильяччо И., Бонечи М., Бьяджони С., Романьоли Д., Де Лука Ф. и др. (23 июля 2019 г.). «Механизмы устойчивости к ингибиторам CDK4/6: потенциальные последствия и биомаркеры для клинической практики» . Границы онкологии . 9 : 666. doi : 10.3389/fonc.2019.00666 . ПМК 6664013 . ПМИД 31396487 .
- ^ «Pfizer объявляет о досрочном прекращении исследования PALOMA-3 для IBRANCE (палбоциклиба) из-за эффективности, наблюдаемой у пациентов с HR +, HER2-метастатическим раком молочной железы, у которых заболевание прогрессировало после эндокринной терапии» . 15 апреля 2015 г. Архивировано из оригинала 25 апреля 2020 г. . Проверено 3 мая 2015 г.
- ^ Поллак А (6 апреля 2014 г.). «Лекарство от рака молочной железы показывает «революционные» результаты» . Нью-Йорк Таймс . Архивировано из оригинала 9 июня 2021 года.
- ^ Бизли Д. (6 апреля 2014 г.). «Испытание препарата Pfizer удваивает время роста опухоли рака молочной железы» . Yahoo! Новости . Рейтер . Архивировано из оригинала 6 апреля 2014 года . Проверено 7 апреля 2014 г.
- ^ «Палбоциклиб показывает многообещающие результаты у пациентов с метастатическим раком молочной железы, положительным по рецепторам гормонов» . AACR в новостях . 6 апреля 2014 г. Архивировано из оригинала 8 апреля 2014 г.
- ^ «Pfizer предоставляет обновленную информацию о 3-й фазе исследования PALLAS препарата IBRANCE® (палбоциклиб) плюс эндокринная терапия при HR+, HER2-раннем раке молочной железы» (пресс-релиз). 29 мая 2020 года. Архивировано из оригинала 8 августа 2020 года . Проверено 2 июня 2020 г.
- ^ «Страница со списком динамических испытаний вмешательств» . Национальный институт рака . Архивировано из оригинала 23 января 2018 года . Проверено 16 декабря 2017 г.
- ^ Номер клинического исследования NCT03455270 «Открытое многоцентровое исследование фазы 1 для оценки безопасности, переносимости, фармакокинетики и предварительной противоопухолевой активности возрастающих доз G1T48 отдельно и в комбинации с палбоциклибом у женщин с положительным рецептором эстрогена, HER2». -Отрицательный результат на распространенный рак молочной железы» на сайте ClinicalTrials.gov.
- ^ Номер клинического исследования NCT03560531 для «Открытого многоцентрового исследования фазы 1/2 для оценки безопасности, переносимости, фармакокинетики и противоопухолевой активности ZN-c5 отдельно и в комбинации с палбоциклибом у субъектов с положительными рецепторами эстрогена, у людей». Отрицательный результат на рецептор эпидермального фактора роста-2 при распространенном раке молочной железы» на сайте ClinicalTrials.gov
- ^ «Словарь лекарств NCI» . Национальный институт рака . 2 февраля 2011 г. Архивировано из оригинала 10 августа 2019 г. . Проверено 16 декабря 2017 г.
- ^ «G1 Therapeutics, Inc. | Оптимизация химиотерапии, повышение выживаемости» . Архивировано из оригинала 4 августа 2021 года . Проверено 16 декабря 2017 г.
- ^ «FDA предоставляет приоритетный обзор трилациклиба для лечения мелкоклеточного рака легких» . www.uspharmacist.com . Архивировано из оригинала 20 января 2021 года . Проверено 2 января 2021 г.
- ^ Jump up to: а б «Препарат Pfizer от рака молочной железы получил раннее одобрение FDA» . Бизнес-стандарт . Ассошиэйтед Пресс. 3 февраля 2015 года. Архивировано из оригинала 25 октября 2015 года . Проверено 2 ноября 2015 г.
- ^ Герпер М. (19 февраля 2010 г.), «Самые дорогие лекарства в мире» , Forbes , заархивировано из оригинала 28 апреля 2021 г. , получено 25 июня 2015 г.
- ^ Томас К., Поллак А. (15 июля 2015 г.). «Специализированные аптеки множатся вместе с вопросами» . Нью-Йорк Таймс . Синкинг-Спринг, Пенсильвания. Архивировано из оригинала 25 февраля 2019 года . Проверено 5 октября 2015 г.
- ^ «Британское агентство считает, что лекарство Pfizer от рака молочной железы слишком дорогое» . Рейтер . 3 февраля 2017 года. Архивировано из оригинала 12 апреля 2019 года . Проверено 16 декабря 2017 г.
- ^ Jump up to: а б «Стоимость лекарств от рака молочной железы слишком высока по сравнению с обычным финансированием Национальной службы здравоохранения» . ХОРОШИЙ . Архивировано из оригинала 25 апреля 2020 года . Проверено 16 декабря 2017 г.
- ^ «После нового соглашения пациенты с раком молочной железы будут иметь постоянный доступ к двум лекарствам, продлевающим жизнь», - говорится в проекте руководства NICE . ХОРОШИЙ . Архивировано из оригинала 25 апреля 2020 года . Проверено 16 декабря 2017 г.